В I клинической группе (рис. 3) преобладали субдуральные гематомы – 152 больных (76%), в 6 раз реже встретились эпидуральные – 27 больных (13,5%) и в 30 раз реже – внутримозговые – 5 больных (4,5%). Сочетанные гематомы встретились у 13 больных (6%), из них преобладали сочетания эпидуральной и субдуральной (7 больных, 3,5%). Объем гематом колебался от 30 до 200 мл (в среднем – 68,9 ± 9,3 мл).
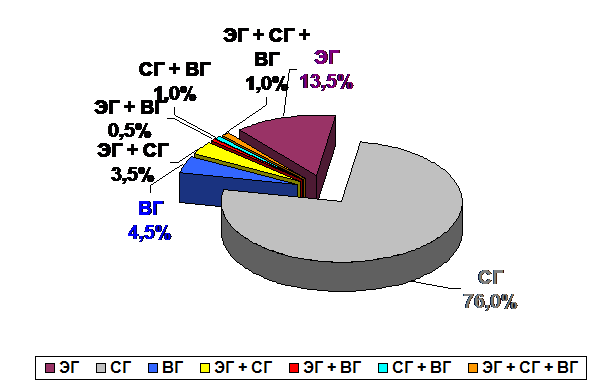
Рис. 3. Распределение больных I клинической группы с ОТВГ по виду гематом (группа сравнения, 200 наблюдений).
Преобладали крупноочаговые гематомы (142 случая, 71%), встретились также гематомы малого (50 мл и менее) объема и пластинчатые, объемом до 60 мл (последние два вида гематом составили 58 наблюдений – 29% от общего числа). В этой группе умерло 74 больных (летальность – 37%).
В послеоперационном периоде интенсивная терапия включала в себя следующие компоненты.
1. Проведение оптимальной нейровегетативной защиты с использованием бензодиазепинов в дозе 0,1-0,2 мг/кг и наркотических анальгетиков в дозе 2-3 мг в сутки.
2. Цереброперфузионное давление в пределах Раср 95-110 мм рт. ст. достигали инфузионной терапией, включавшей солевые кристаллоидные растворы, препараты гидроэтилкрахмала в дозе 25-40 мл/кг веса больного. При сохраняющейся гипотензии добавляли вазоконстрикторные препараты в дозах, необходимых для поддержания оптимального цереброперфузионного давления.
3. Для снижения перекисного окисления: Витамин С в дозе до 3 г в сутки, флуимуцил до 1200 мг/сут.
4. Для инактивации протеолиза применяли препараты группы ингибиторов протеаз, в частности, Гордокс до 1000000 ед/сут.
5. С целью профилактики гнойных осложнений проводилась антибактериальная терапия. Начинали с назначения карбепенемов (Меронем, тиенам, имипенем и др.) в дозе 3 г в сутки. При возникновении гнойных осложнений ее меняли в соответствии с результатами посевов биологических сред. При возникновении интракраниальных гнойных осложнений антибактериальную терапию дополняли люмбальными пункциями с введением в субарахноидальное пространство антибиотиков (меронем, амикацин, натриевая соль пенициллина и др.).
6. Респираторная поддержка в режимах принудительной вентиляции со строгим контролем газового состава крови PaСО2 35 мм рт. ст., с регулярным применением протокола «рекрутирования альвеол» в комплексе с небулайзерной терапией Будесонит в дозе до 1000 мг/сут, Флуимуцил до1200 мг/сут.
7. Нутритивную поддержку рассчитывали, исходя из метаболической характеристики: увеличенная энергопотребность, гиперкатаболизм, повышенные потери азота (до 30 г в сутки или 750 г мышечной массы), гипергликемия, как проявление феномена инсулинорезистентности.
С целью обеспечения энергообмена энтеральное введение аминокислотных смесей для парэнтерального питания с привлечением препаратов: N(2)-L-аланин-L-глютамин аминокислот и глюкозо-калиевой смеси в объёме до 2500 мл на протяжении первых двух суток с переходом на полуэлементарные смеси для энтерального питания в объёме до 2500 мл в комплексе с противоязвенными препаратами (Лосек в/в до 120 мг/сут).
Нутритивную поддержку проводили в условиях мониторирования гликемического профиля и при необходимости присоединяли инсулины короткого действия.
8. Метаболическую церебральную терапию начинали с 4-6 суток при достоверных критериях регресса посттравматического отека ГМ. Назначали препараты, активизирующие межнейрональную передачу и выполняющие ноотропную функцию.
II группа (основная клиническая группа) – 60 больных с ОТВГ (см. табл.1), которым стандартную терапию дополняли регионарной иммуномодулирующей терапией тактивином. Больным проводили интраоперационное орошение ложа удаленной гематомы тактивином (100 мкг). В твердую оболочку головного мозга вводили 100 мкг тактивина. В 1-3, 5-7, 9 сутки после операции через поверхностную височную артерию по интраоперационно установленному катетеру инъецировали 200 мкг тактивина.
Основная клиническая группа отличалась от группы сравнения числом больных в возрасте менее 30 лет (преобладали лица в возрасте 31-40 лет, средний возраст – 39,5 ± 10,2 лет) и преобладанием мужчин (соотношение мужчин и женщин – 7,5 : 1).
Сроки поступления пострадавших в стационар были следующими: ,5%) больных группы сравнения и,3%) – основной клинической группы поступили в стационар до 6 часов с момента получения ЧМТ.,5%) больных группы сравнения и,7%) основной группы поступили в стационар в сроки от 6 до 24 часов с момента травмы. 6 (3%) больных группы сравнения и 3 (5%) основной группы поступили в стационар позднее 24 часов.
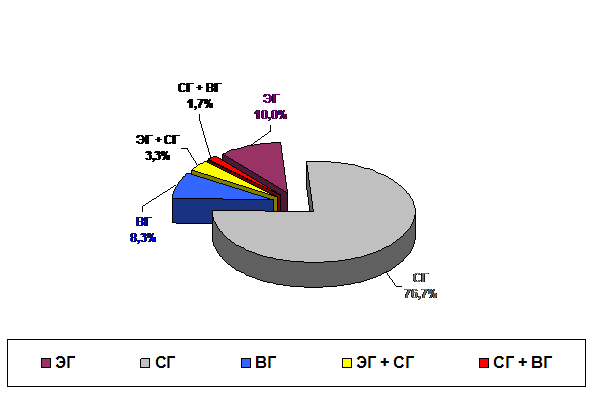 Во II группе, также как и в I клинической группе сравнения, преобладали субдуральные – 46 больных (76,7%) и эпидуральные гематомы – 6 больных (10%). 5 больных было с внутримозговыми (8,3%) и 3 – с сочетанными гематомами (5%) /рис. 4/. Встретились сочетания эпидуральных и субдуральных гематом (2 больных, 3,3%) и субдуральной и внутримозговой (1 больной, 1,7%). Объем гематом колебался от 20 до 150 мл (в среднем – 61,3 ± 10,7 мл).
Во II группе, также как и в I клинической группе сравнения, преобладали субдуральные – 46 больных (76,7%) и эпидуральные гематомы – 6 больных (10%). 5 больных было с внутримозговыми (8,3%) и 3 – с сочетанными гематомами (5%) /рис. 4/. Встретились сочетания эпидуральных и субдуральных гематом (2 больных, 3,3%) и субдуральной и внутримозговой (1 больной, 1,7%). Объем гематом колебался от 20 до 150 мл (в среднем – 61,3 ± 10,7 мл).
Рис. 4. Распределение больных II клинической группы с ОТВГ (основной группы) по виду гематом (60 наблюдений).
I и II клинические группы были также сопоставлены по уровню нарушения сознания (табл. 2) и сопутствующей патологии.
Таблица 2
Распределение больных по уровню нарушения сознания
(по шкале ком Глазго) при поступлении
Показатель | Ясное созна-ние | Умерен-ное оглу-шение | Глубо-кое оглу-шение | Сопор | Поверх-ностная кома | Умерен-ная кома | Глубо-кая кома | Число больных |
Группа сравнения (I группа) | 6 (3%) | 40 (20%) | 52 (26%) | 28 (14%) | 24 (12%) | 36 (18%) | 14 (7%) | 200 (100%) |
Основная группа (II группа) | 1 (1,7) | 13 (21,6%) | 16 (26,7%) | 16 (26,7%) | 5 (8,3%) | 5 (8,3%) | 4 (6,7%) | 60 (100%) |
Как видно из табл. 2, в обеих клинических группах все больные были относительно равномерно распределены по глубине нарушения сознания. В большей части больные поступали в состоянии глубокого оглушения – умеренной комы.
Все больные в обеих клинических группах были оперированы в среднем в течение 1,5-2 часов после поступления.
У %) больных группы сравнения и у%) – основной группы была диагностирована хроническая алкогольная интоксикация. Значительно преобладали мужчины - 123 б-х (88%).
Другие экзогенные интоксикации у больных обеих клинических групп выявлены не были, отсутствовали также инфекционные, инфекционно-аллергические или аутоиммунные заболевания, которые могли бы влиять на их иммунный статус.
Как видно из табл. 3, обе клинические группы были сопоставимы по указанным в ней показателям, что позволило провести сравнительное исследование клинического эффекта от введения в стандартную схему лечения больных с ОТВГ из основной группы местной интраоперационной иммуномодулирующей терапии тактивином.
Таблица 3
Сравнительная характеристика основных
показателей I и II клинических групп.
Показатель | I группа | II группа | Достоверность разницы |
Вид гематомы (число больных в %): СГ | 76,0% | 76,7% | р < 0,05 |
ЭГ | 13,5% | 10,0% | р < 0,05 |
ВГ | 4,5% | 8,3% | р > 0,05 |
Сочетанные | 6% | 5% | р < 0,05 |
Возраст больных (лет) | 31,3 ± 11,7 | 39,5 ± 10,2 | р < 0,05 |
Соотношение мужчин и женщин | 3,3 : 1 | 7,5 : 1 | р > 0,05 |
Гематомы большого объема (в %) | 71% | 75% | р < 0,05 |
Гематомы малого объема (50 мл и менее) и пластинчатые (в %) | 29% | 25% | р < 0,05 |
Число часов от момента получения травмы до поступления в стационар (число больных в %): Менее 6 часов | 64,5 | 58,3% | р < 0,05 |
6-24 часа | 31,5% | 36,7% | р < 0,05 |
Более 24 часов | 3% | 5% | р < 0,05 |
Время до операции после поступления в стационар (число больных в %): 1,5 – 2 часа | 100% | 100% | р < 0,05 |
Средний обьем гематомы (мл) | 68,0 ± 9,3 | 61,3 ± 10,7 | р < 0,05 |
Наличие хронического алкоголизма (число больных в %) | 54% | 53% | р < 0,05 |
В основной группе из 60 больных умерло 18. Послеоперационная летальность составила 30%.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Медико-статистический анализ 400 аутопсийных наблюдений ОТВГ у больных, оперированных и леченых по стандартной схеме (при изолированных ЧМТ со сходными повреждениями головного мозга), показал, что частота экстракраниальных гнойно-воспалительных осложнений (пневмоний) составила 56%. Это оказалось в средней зоне показателей, которые приводятся в литературе. Так, по данным большинства авторов, частота пневмоний при острых травматических внутричерепных гематомах колеблется по клиническим данным от 20 до 80% (в зависимости от тяжести ЧМТ), а по данным аутопсий достигает 95-97%.
Первое место (54-67%) по частоте пневмоний занимали эпидуральные гематомы и сочетанные гематомы (эпидуральные + субдуральные гематомы, эпидуральные + субдуральные + внутримозговые гематомы, субдуральные + внутримозговые гематомы). Второе место принадлежало СГ (54%), третье – ВГ (50%). Разница по частоте пневмоний была достоверна (в 1,3 раза, р<0,05) только между ЭГ, СГ + ВГ с одной стороны и ВГ – с другой. Было бы логичнее ожидать более высокую частоту пневмоний у больных с ВГ и СГ, а не с ЭГ, когда травма ГМ обычно выражена меньше. Кроме того, не отмечалась достоверная зависимость частоты пневмоний от пола и возраста больных.
По-видимому, возникновение пневмоний, которые являются ярким проявлением тяжелых иммунных нарушений, в большей мере связано не с видом гематомы, а с другими особенностями ЧМТ, в частности, с тяжестью поражения ткани ГМ, влиянием сопутствующей патологии и других факторов, определяющих глубину ВИДС у конкретного больного. На это обращают внимание и другие авторы (, 1990; и соавт., 1998; и соавт, 1997, 1999; и соавт., 2000; Goodpasture С., 1976; Van Woerkom T. H. et al., 1997).
Доказательством этого положения явилось то, что пневмонии, как и интракраниальные осложнения, возникали значительно чаще (первые – в 6 раз, последние – в 1,4 раза) у больных, страдающих хроническим алкоголизмом. Кроме того, пневмонии были выявлены практически у всех больных с ОТВГ, страдавших хроническими обструктивными заболеваниями легких.
Частота интракраниальных гнойно-воспалительных осложнений (гнойные менингит, менингоэнцефалит, вентрикулит, пахименингит, субдуральная эмпиема) составила 14%. Полученные результаты соответствуют данным других исследователей. Большинство авторов указывают на частоту развития интракраниальных гнойно-воспалительных осложнений у 2-18% больных.
Внутримозговые и сочетанные гематомы среди причин развития интракраниальных гнойно-воспалительных осложнений статистически достоверно лидировали (30-46% против 7-15%, р<0,05), что, по-видимому, обусловлено более тяжелым поражением ткани ГМ. Интракраниальные осложнения, независимо от пола, в 2-3 раза чаще встречались у больных старше 30 лет (р<0,05). Более 50% интракраниальных осложнений развивалось на 4-10 сутки после получения травмы. Эти данные не отличаются от известных из литературы, в соответствии с которыми посттравматический менингит возникает, в основном, независимо от особенностей нейрохирургического вмешательства, в течение первых 14 суток после ЧМТ.
Среди интракраниальных осложнений превалировал гнойный менингит (50% наблюдений). По данным литературы он также является одним из наиболее тяжелых и частых гнойных интракраниальных осложнений.
Результаты исследования интракраниальных гнойно-воспалительных осложнений согласуются с данными литературы о том, что они могут возникнуть как при открытой, так и при закрытой ЧМТ. При целостности костей черепа основную роль в их возникновении играют гематогенный и метастатический пути проникновения инфекции в область гематомы, а также оперативное вмешательство и активация аутоинфекции.
Отмеченные выше причины экстра - и интракраниальных гнойно-воспалительных осложнений (микробные ассоциации с преобладанием условно патогенной флоры и резистентность к проводимой терапии) характерны также для больных с ВИДС (вторичный иммуно-дефицитный синдром). Особенностью гнойно-воспалительных осложнений у больных с ЧМТ, протекающих на фоне иммунных нарушений, являются резистентность к терапии и низкая чувствительность микрофлоры к антибиотикам.
Важное значение для прогнозирования развития гнойно-воспалительных осложнений у больных с ОТВГ и своевременной организации профилактических и лечебных мероприятий имеет факт обнаружения достоверной разницы частоты и структуры гнойно-воспалительных осложнений в зависимости от латерализации гематомы – локализации ОТВГ в левом или правом полушариях ГМ.
Ранее, в отдельных исследованиях, было отмечено более частое развитие гнойно-воспалительных осложнений и выраженный ВИДС при поражении различными патологическими процессами левого (доминантного у большинства людей) полушария ГМ. На ограниченном числе наблюдений ЧМТ было показано, что пневмонии также преобладают при травмах левого полушария.
Проведенное исследование показало, что при двустороннем поражении ГМ как пневмонии, так и интракраниальные гнойно-воспалительные осложнения, наблюдались достоверно чаще (разница в 1,3 – 2 раза, р<0,05), чем при одностороннем, особенно по сравнению с локализацией ОТВГ в правом полушарии. Отмечалась также тенденция, хотя и статистически недостоверная, к более частому (в 1,2 раза) развитию пневмоний при поражении левого полушария ГМ, по сравнению с правым. Для интракраниальных осложнений существовала обратная зависимость, они развивались в 1,2 раза чаще при поражении правого полушария ГМ.
При изучении только монолатеральных гематом малого объема (50 мл и менее) и пластинчатых, объемом до 80 мл, обнаруженная тенденция зависимости вида и частоты гнойно-воспалительных осложнений от латерализации ОТВГ, становилась статистически достоверной. По сравнению с другими, такие ОТВГ объединяет менее выраженная тяжесть поражения ткани ГМ противоположенного полушария, где локализована гематома. Это позволило уточнить зависимость развития гнойно-воспалительных осложнений от травмы левого или правого больших полушарий ГМ.
Частота экстракраниальных гнойно-воспалительных осложнений (пневмоний) при малых и пластинчатых ОТВГ составляла 38% (в 1,5 раза меньше, чем при анализе всех 400 наблюдений – 56%). Также ниже, в 1,7 раза, была частота интракраниальных осложнений (8 против 14%). Эти различия частоты гнойно-воспалительных осложнений от объема ОТВГ были статистически достоверны (р<0,05).
При наличии ОТВГ малого объема в области левого полушария ГМ частота экстракраниальных гнойно-воспалительных осложнений (пневмоний) оказалась в 2,2 раз выше, чем при травме правого (58 против 27%). Частота интракраниальных гнойно-воспалительных осложнений (гнойных менингита и менингоэнцефалита), напротив, была в 2 раза выше при локализации гематомы в области правого полушария ГМ (10 против 5%).
Таким образом, результаты медико-статистического исследования показали, что лечение гнойно-воспалительных осложнений у больных с ОТВГ, по-прежнему, представляют собой нерешенную проблему. Полученные данные об их частоте несколько ниже приводимых в литературе. По нашим данным пневмонии развились у 46-56% больных, а гнойные менингиты и другие интракраниальные гнойно-воспалительные осложнения – у 7-14%. Достоверно, в 1,2 раза, снизилась частота пневмоний у больных в 2004 г., леченых по стандартной схеме, по сравнению с наблюдениями предыдущих 5-ти лет. Это обусловлено включением в лечение таких больных небулайзерной терапии и других современных методов, которые позволили снизить показатели бронхолегочных осложнений у оперированных больных. Особенности этих осложнений подтверждают общепринятое мнение о ведущей роли ВИДС в их патогенезе. Следовательно, целесообразность включения иммуномодуляторов в комплексное лечение ВИДС и гнойно-воспалительных осложнений ОТВГ следует считать обоснованной.
Полученные данные о гетерогенности частоты и структуры гнойно-воспалительных осложнений при ОТВГ в зависимости от латерализации гематомы, позволяют прогнозировать большую или меньшую вероятность развития этих осложнений. С другой стороны, получено еще одно доказательство ведущей роли центральной регуляции функций иммунной системы доминантным полушарием ГМ (у правшей – левого). При его поражении общая частота гнойно-инфекционных осложнений и, особенно, пневмоний достоверно выше. Известно, что именно развитие пневмонии ярко отражает наличие тимус-зависимого ВИДС. Следовательно, тяжесть ВИДС при левосторонних ОТВГ выражена больше, чем при травме правого полушария ГМ.
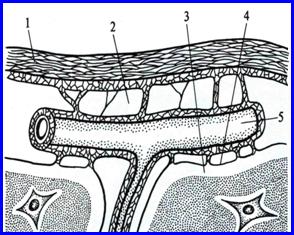
Морфологическое исследование оболочек ГМ в наблюдениях контрольной группы и при ОТВГ, а также анализ литературных источников, позволили выяснить и описать структурную основу их уникальной местной системы иммунитета (рис.5).
Особенностями системы местного иммунитета оболочек ГМ являются:
- одновременное участие ликвора, тканевой жидкости дурально-арахноидального слоя и крови в афферентных и эфферентных путях местной системы иммунитета. Ликвор выполняет роль лимфы для ткани ГМ и его мягких оболочек (сосудистой и паутинной), а тканевая жидкость дурально-арахноидального слоя – для паутинной и, частично, твердой оболочек. Кровоснабжение оболочек ГМ осуществляется из двух артериальных систем (интра - и экстракраниальных), объединенных множественными анастомозами, особенно в бассейнах средней оболочечной и наружной сонной артерий. Венозный отток осуществляется в синусы и вены твердой мозговой оболочки, в вены мягкой оболочки и ткани ГМ;
- немногочисленные популяции иммунокомпетентных клеток (Т - и В-лимфоцитов, макрофагов) в оболочках ГМ, но большое число резидентных макрофагов (микроглии и астроглии) в его ткани;
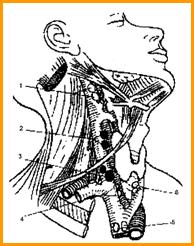
- значение средних и нижних яремных лимфатических узлов как регионарных лимфоидных органов местной иммунной системы мозговых оболочек. В этих лимфатических узлах происходят антигензависимые пролиферация и дифференцировка лимфоцитов, ассоциированных с оболочками ГМ. Оттекает лимфа от этих лимфатических узлов в яремный лимфатический ствол, далее – в правый лимфатический проток (слева – непосредственно в грудной проток). Грудной проток открывается в левую подключичную вену. Таким образом, эфферентный путь от регионарной системы иммунитета мозговых оболочек прямо или косвенно приводит к верхней полой вене.
|
|
|
|
![]()
|
|

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |


