![]() отток лимфы
отток лимфы
|
![]()
лимфатическую
систему шеи
1 – твердая оболочка, 1, 2 - средние и нижние
2 – паутинная оболочка, яремные лимфатические
3 –сосудистая оболочка (5) узлы
4 – ткань головного мозга
Рис. 5. Схема структурной основы местной (регионарной) системы иммунитета оболочек головного.
Важнейшим структурно-функциональным компонентом регионарного иммунитета оболочек ГМ являются местные клеточные кооперации, которые в твердой оболочке представлены немногочисленными Т - и В-лимфоцитами, лаброцитами и клетками системы мононуклеарных фагоцитов (гистиоцитами, моноцитами, макрофагами). Лимфоциты не формируют каких-либо структур, а присутствуют в виде диффузно рассеянных клеток. По-видимому, большое значение в местных иммунных реакциях принадлежит лаброцитам и эндотелиоцитам сосудов. Внутренний листок твердой оболочки покрыт изнутри слоем пограничных уплощенных отростчатых клеток. Роль этого мезотелиоподобного эпителия оболочек в иммунных реакциях остается неясной. Эти клетки связаны десмосомальными контактами с такими же клетками дурально-арахноидального промежуточного слоя – бессосудистого клеточного синцития, образующего сотовую структуру между твердой и паутинной оболочками ГМ. В ее ячейках циркулирует не ликвор, а межклеточная (тканевая) жидкость дурально-арахноидального слоя. При патологии, например, развитии субдуральной гематомы, в клеточном синцитии дурально-арахноидального промежуточного слоя формируется субдуральное пространство.
Изнутри дурально-арахноидальный клеточный синцитий контактирует с наружным слоем клеток (арахноэндотелием) паутинной оболочки, ячейки которой в субарахноидальном пространстве заполнены ликвором. При анализе особенностей местного иммунитета оболочек ГМ важно учитывать то, что они участвуют в фильтрации и резорбции ликвора. Из ГМ часть ликвора (в норме около 70%) через арахноидальные ворсины (грануляции), выступающие в просвет венозных синусов твердой оболочки, поступает непосредственно в кровь. Другая часть (около 30%, при патологии – до 70-80%) фильтруется через клеточный синцитий паутинной оболочки и, уже в виде межклеточной жидкости дурально-арахноидального слоя попадает в лимфатические и кровеносные сосуды твердой оболочки.
Субарахноидальное пространство ограничено мягкой оболочкой, содержащей множество сосудов и покрытой эпителиоподобными клетками. В мягкой оболочке, как и в ткани ГМ, лимфатические сосуды отсутствуют, а клетки омываются ликвором (Haines D., 1991. Frederickson R., 1991). Клетки иммунной системы представлены единичными Т - и В-лимфоцитами, моноцитами и макрофагами гематогенного происхождения и мигрировавшими из ликвора. Мягкая оболочка тесно прилежит к ткани ГМ и, при развертывании в ней иммунных реакций, в них принимают участие, прежде всего, микроглия и расположенные в периваскулярных пространствах сосудов ГМ лимфоциты и клетки системы мононуклеарных фагоцитов.
Другим структурно-функциональным компонентом регионарного иммунитета оболочек ГМ являются хорошо развитые сети лимфатических сосудов твердой оболочки, лимфатическая сеть слизистой оболочки носовой полости, адвентиции крупных сосудов головы и шеи, глубокая лимфатическая сеть шеи и регионарные лимфатические узлы. Лимфа из сосудов твердой оболочки (и, после фильтрации ликвора в области обонятельных луковиц, через лимфатическую сеть слизистой оболочки носовой полости) поступает, главным образом, в глубокую лимфатическую систему шеи. Другой путь лимфы идет по лимфатическим сосудам адвентиции крупных сосудов головы и шеи. Большая часть лимфы, в итоге, поступает в группу глубоких шейных лимфатических узлов, главным образом, средние и нижние яремные. Сходные данные получили и (1998, 1999). Именно эти группы лимфатических узлов являются регионарными для всей лимфатической системы оболочек ГМ. Их особенностью является сложная обратная связь с тканью ГМ и ликвором из-за наличия гемато-энцефалического барьера и прямая связь с артериальной системой мозговых оболочек.
Таким образом, структурной основой уникальной системы местного (регионарного) иммунитета оболочек ГМ являются: артериальные сосуды оболочек и ГМ, оболочечные и внутримозговые пути циркуляции ликвора, оболочечные пути циркуляции дурально-арахноидальной тканевой жидкости (афферентные пути); клеточные кооперации оболочек и ткани ГМ; сеть лимфатических сосудов твердой оболочки, адвентиции крупных кровеносных сосудов шеи и глубокая лимфатическая сеть шеи (эфферентные пути); нижние и средние яремные лимфатические узлы (регионарные лимфатические узлы).
Изучение структурно-функциональных особенностей регионарного иммунитета при ОТВГ показало, что первыми реакциями оболочек ГМ являются микроциркуляторные: миграция и дегрануляция лаброцитов, миграция полиморфноядерных лейкоцитов, а в ткани ГМ – микроциркуляторные (приводящие к его отеку) и активация микроглии. Уже в первые сутки большое число эритроцитов из гематомы, следовательно, и различные биологически активные вещества из поврежденных тканей, поступают в лимфатические сети твердой оболочки, адвентиции крупных сосудов шеи, глубокую лимфатическую сеть шеи и синусы регионарных для оболочек ГМ глубоких шейных лимфатических узлов. Таким образом «запускается» уникальный регионарный иммунный ответ, который включает в себя реакцию ткани ГМ и изменения ликвора, активацию клеточных коопераций мягкой, паутинной и твердой оболочек ГМ, лимфоидной ткани средних и нижних яремных лимфатических узлов. По-видимому, важную роль играет эритрофагия макрофагами в синусах этих лимфатических узлов. Умеренная активация В-системы иммунитета отражает, вероятно, в том числе и т. н. «санитарные» аутоиммунные реакции в ответ на нарушение целостности гематоэнцефалического барьера и поступления в лимфу и кровоток антигенов ткани ГМ и разрушенных эритроцитов. В отдельных случаях трансформация гомеостатических санитарных аутоиммунных реакций в патологические может приводить к прогрессирующему аутоиммунному посттравматическому поражению ГМ.
Включение в комбинированное лечение ОТВГ местной иммунотерапии тактивином активирует как регионарные иммунные реакции, так и репаративные процессы в оболочках ГМ. В отличие от традиционно леченых больных, после введения тактивина заметно усиливаются пролиферативные процессы (фибробластов, эндотелия) и рост грануляционной ткани со стороны твердой оболочки, лимфо-макрофагальная инфильтрация оболочек и, напротив, уменьшаются микроциркуляторные нарушения и лейкоцитарная инфильтрация, особенно эозинофильными лейкоцитами (что указывает на быструю нормализацию функции лаброцитов). В регионарных лимфатических узлах фаза опустошения лимфоидной ткани сменяется на гиперпластическую с выраженным усилением пролиферации лимфоцитов, активацией Т - и В-звеньев иммунитета. Однако выраженной активации В-звена не происходит, что указывает на отсутствие риска прогрессирования аутоиммунных реакций. Специально проведенные иммунологические исследования показали, что проведенная местная иммуномодулирующая терапия тактивином не сопровождается повышением активности аутоиммунных реакций. Уменьшение выраженности асептического реактивного воспаления в области гематомы и снижение частоты его трансформации в гнойное воспаление, приводит к формированию меньшего объема посттравматических рубцовых изменений мозговых оболочек.
Исследование анатомо-функциональных особенностей поверхностной височной артерии проводили двумя методами: 1) окрашиванием сосудистого бассейна наружной сонной артерии, в частности, поверхностной височной артерии и 2) проведением серии посмертных селективных ангиографий наружной сонной артерии.
При введении красителя в ретроградном направлении мы получили его поступление в сосуды твердой мозговой оболочки через сеть анастомозов, в частности, через верхнюю челюстную артерию, от которой и отходит средняя оболочечная артерия.
При введении красящего вещества в антероградном направлении отмечено интенсивное прокрашивание сосудистой сети мягких покровов мозгового отдела головы: кожи, подкожной жировой клетчатки, апоневроза, как на стороне введения, так и на противоположенной стороне, надкостницы, височной мышцы, и костей свода черепа вдоль швов. После проведения циркулярной трепанации черепа обнаружено наличие красителя в сосудах твердой мозговой оболочки, в основном в ветвях средней оболочечной артерии. При этом отмечено незначительное окрашивание самой твердой мозговой оболочки, в основном вдоль сагиттальной линии. Полученные данные свидетельствуют о наличии развитой артериальной анастоматической сети между ветвями поверхностной височной артерии и средней оболочечной артерии.
После прокрашивания сосудов твердой мозговой оболочки производили забор участка твердой мозговой оболочки для гистологического исследования. При данном исследовании находили краситель в просвете и на внутренней поверхности стенок как основных, так и мелких ветвей средней менингиальной артерии. Красящим веществом заполнялись так же мелкие интратекальные артерии и артериолы. Вблизи артериол отмечалось небольшое накопление красителя в капиллярах. Следует заметить, что вены, расположенные рядом с артериями, не содержали красителя.
Полученные данные позволяют судить о возможности применения регионарной иммунотерапии через поверхностную височную артерию у больных с внутричерепными травматическими кровоизлияниями.
Для изучения диаметра исследуемых сосудов в секционной, по описанной ранее методике, произведен забор сегментов поверхностной височной артерии (ПВА) и её ветвей: основного ствола до его деления, теменной и лобной ветвей.
Иссеченные участки сосудов были направлены на патогистологическое исследование и измерение диаметра сосудов.
Нами установлено, что диаметр основного ствола ПВА, колеблющийся в пределах от 1,3 до 1,57 мм. При этом после деления диаметр его ветвей чаще всего не уменьшался менее 0,65 мм. Следует отметить, что чаще лобная ветвь ПВА по диаметру немного превосходит теменную. Однако лобная ветвь отходит от основного ствола под углом, в отличие от теменной ветви, которая чаще является продолжением основного ствола ПВА.
Эти анатомические особенности предопределили преимущественную интраоперационную катетеризацию либо основного ствола ПВА при ее высоком делении, или теменной ветви при низком делении ПВА.
При проведении посмертной ангиографии были получены ангиографические снимки сосудистого русла наружной сонной артерии при введении контраста в ретроградном направлении через катетер, установленный в поверхностную височную артерию. Это дает основание предполагать возможность введения лекарственных средств через регионарное сосудистое русло.
Следует учесть, что на всех произведенных ангиограммах отсутствует ангиографическая капиллярная фаза, так как сосуды диаметром 0,5-1 мм контрастом не заполняются (рис. 6).
![]()
![]()
![]()
![]()
![]()
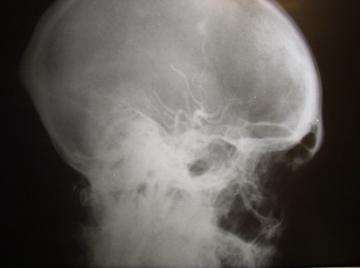
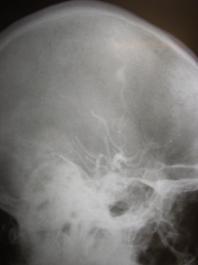 Рис. 6. Ангиограммы наружной сонной артерии (стрелками указана контрастированная средняя оболочечная артерия).
Рис. 6. Ангиограммы наружной сонной артерии (стрелками указана контрастированная средняя оболочечная артерия).
Необходимо отметить, что в ряде случаев контрастное вещество частично попадало во внутреннюю сонную артерию, контрастируя её основные ветви (рис. 7).
|

|

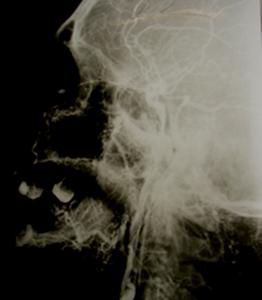
Рис. 7. Ангиограмма наружной сонной артерии. Катетер (указан белой стрелкой) введен в ретроградном направлении через поверхностную височную артерию. Отмечается контрастирование средней оболочечной (стрелка А) артерии. Частичное попадание контраста в бассейн внутренней сонной артерии (стрелка Б).
Исходя из вышеизложенного, можно сделать вывод о возможности подведения лекарственных препаратов и, в частности, иммуномодуляторов в регионарное сосудистое русло методом катетеризации поверхностной височной артерии. В условиях кровотока вероятность поступления препарата в сосуды твердой мозговой оболочки при антероградном введении катетера в поверхностную височную артерию в настоящее время мы можем рассматривать лишь теоретически. Напротив, при ретроградном введении катетера в ПВА проведенные исследования подтверждают достоверное поступление лекарственных веществ в артериальные сосуды твердой мозговой оболочки.
Таким образом, нами были определены два основных способа введения иммуномодулирующих препаратов (тактивина) в область оперативного вмешательства для регионарной терапии: 1. интраоперационное орошение операционной раны или введение его между листками твердой мозговой оболочки,
2. интраоперационная катетеризация поверхностной височной артерии для проведения регионарной иммунотерапии в послеоперационном периоде.
Результаты лечения в клинических группах оценивались по шкале исходов Глазго (табл. 4). Как видно из табл., у больных основной клинической группы послеоперационный период протекал более благоприятно. Летальность в группе сравнения составила 37%, а в основной группе – 30% (меньше в 1,23 раза, р<0,05), что видно из табл. 5.
Таблица 4
Распределение больных в клинических группах
при оценке состояния по шкале исходов Глазго
Группа | БАЛЛЫ | Всего больных | ||||
I | II | III | IV | V | ||
Группа сравнения | 38 (19%) | 64 (32%) | 10 (5%) | 14 (7%) | 74 (37%) | %) |
Основная группа | 10 (16,6%) | 19 (31,7%) | 12 (20%) | 1 (1,7%) | 18 (30%) | 60 (100%) |
Приводим основные показатели результатов лечения больных в основной группе и в группе сравнения.
Таблица 5
Результаты лечения больных в клинических группах
Показатель | Группа сравнения | Основная группа | Достоверность разницы |
Число больных | 200 | 60 | - |
Средний койко-день | 24,4±1,3 | 23,5±2,0 | р<0,05 |
Летальность | 74 (37%) | 18 (30%) | р<0,05 |
Число экстракраниаль-ных гнойно-воспали-тельных осложнений | 92 (46%) | 19 (32%) | р<0,05 |
Число интракраниаль-ных гнойно-воспали-тельных осложнений | 31 (15,5%) | 4 (6,7%) | р<0,05 |
Наиболее частыми гнойно-воспалительными осложнениями в обеих клинических группах явились бронхолегочные – очаговые и сливные пневмонии (46% в группе сравнения и 32% - в основной группе).
Достоверно, в 1,2 раза, снизилась частота пневмоний у больных в 2004 г. в том числе и леченых по стандартной схеме, по сравнению с наблюдениями за гг. Это обусловлено, в частности, включением в лечение таких больных небулайзерной терапии и других современных методов профилактики и лечения, которые позволили снизить показатели бронхолегочных осложнений у оперированных больных.
На втором месте (табл. 6) в I и II клинических группах были гнойный менингит (18 и 3 набл., соответственно) и менингоэнцефалит (8 и 1 набл., соответственно). Только в I клинической группе (группе сравнения), где проводилась стандартная терапия, выявлено развитие таких осложнений, как гнойный пахименингит (3 больных) и вентрикулит (2 больных).
Таблица 6
Интракраниальные гнойно-воспалительные осложнения у больных группы сравнения (С) и основной клинической группы (О)
Вид гемато-мы | ГМ* | ГМЭ | ГМ+В | ГМ+ГПМ | ГМ+СЭ | ГМЭ+ГПМ | Число больных | ВСЕГО | |||||||
С | О | С | О | С | О | С | О | С | О | С | О | С | О | ||
ЭГ | 4 | 1 | 1 | - | - | - | 1 | - | - | - | - | - | 6 | 1 | 7 |
СГ | 11 | - | 3 | - | - | - | 2 | - | - | - | - | - | 16 | - | 16 |
ВГ | 1 | - | 3 | 1 | 1 | - | - | - | - | - | - | - | 5 | 1 | 6 |
ЭГ + СГ | 2 | 1 | 1 | - | - | - | - | - | - | - | - | - | 3 | 1 | 4 |
ЭГ + ВГ | - | - | - | - | - | - | - | - | - | - | - | - | - | - | |
СГ + ВГ | - | 1 | - | - | - | - | - | - | - | - | - | - | 1 | 1 | |
ЭГ + СГ + ВГ | - | - | - | - | 1 | - | - | - | - | - | - | - | 1 | 1 | |
Итого | 18 | 3 | 8 | 1 | 2 | - | 3 | - | - | - | - | - | 31 | 4 | 35 |
Примечания: *сокращения: ЭГ – эпидуральная гематома, СГ – субдуральная гематома, ВГ – внутримозговая гематома; ГМ – гнойный менингит, В – вентрикулит, ГМЭ – гнойный менингоэнцефалит, ГПМ – гнойный пахименингит, СЭ – субдуральная эмпиема.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |


