Предлагаемые условия оптимизированы по хроматографическим параметрам (табл. 3). Значения коэффициента емкости k¢ находятся в диапазоне от 0,532 для ДГК до 2,902 для кверцетина. Оптимальными являются значения параметров селективности a и разрешающей способности RS, служащие мерой качества разделения.
Эффективность хроматографической колонки (N), рассчитанная для пика ДГК, составила от 4325 до 5100 теоретических тарелок, коэффициент ассиметрии пика (AS) от 0,94 до 1,05. Относительное стандартное отклонение площади пика ДГК (S) составило 1,0%. Хроматографические параметры свидетельствуют о пригодности хроматографической системы. Методика валидирована по соответствующим параметрам, подтверждающим ее специфичность, точность и воспроизводимость, линейную зависимость в аналитической области, что позволяет использовать ее для достоверной оценки качества субстанции и препарата диквертин.
Таблица 3. Параметры хроматографического разделения компонентов диквертина (среднее из 5 определений)
Соединение | Эффективность N, т. т. | Коэффициент емкости, k¢ | Селективность, a | Разрешающая способность, RS |
Дигидрокверцетин | 5050 | 0,532 | ||
1,859 | 1,86 | |||
Дигидрокемферол | 3210 | 0,989 | ||
2,612 | 15,4 | |||
Нарингенин | 4420 | 2,585 | ||
1,124 | 1,89 | |||
Кверцетин | 5320 | 2,902 |
При разработке методики анализа большое внимание уделялось унификации условий анализа с целью возможности сквозной стандартизации диквертина от растительного сырья до лекарственной формы по фармакопейным тестам (схема 3).
Схема 3. Унификация ВЭЖХ методики анализа диквертина
Анализ ДКВ методом ВЭЖХ | ||||
| ||||
Стандартизуемые показатели | ||||
|
|
|
|
|
ПОДЛИННОСТЬ | ПОСТОРОННИЕ ПРИМЕСИ | РОДСТВЕННЫЕ СОЕДИНЕНИЯ | ОДНОРОДНОСТЬ ДОЗИРОВАНИЯ | КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ |
растительное сырье субстанция таблетки | субстанция таблетки | субстанция таблетки | субстанция таблетки | растительное сырье субстанция таблетки |
Подтверждение подлинности ДКВ производится путем сопоставления хроматограмм образцов субстанции или таблеток с хроматограммой СО ДГК. Наряду с пиком ДГК в образцах ДКВ содержатся пики, соответствующие дигидрокемпферолу и нарингенину с временами удерживания относительно СО ДГК 1,3 ± 0,1 и 2,4 ± 0,1 соответственно. Возможно наличие пика, соответствующего кверцетину с относительным временем удерживания 2,7 ± 0,1.
Содержание родственных соединений и ДГК в образцах ДКВ в процентах рассчитывается на основании площадей соответствующих пиков и пика ГСО ДГК. Суммарное содержание дигидрокемпферола, нарингенина и кверцетина в образце должно быть не более 10,0%, содержание ДГК – не менее 90,0%.
Стандартизация растительного сырья, содержащего ДКВ. В целях сквозной стандартизации ДКВ от растительного сырья до препарата разработанная методика адаптирована для анализа содержания ДГК в цельном и измельченном ЛРС – древесине лиственницы.
С этой целью разработана специальная процедура пробоподготовки, направленная на освобождение исследуемой пробы от ряда примесей, способных не только помешать анализу, но и опасных с позиции сохранности сорбента колонки и хроматографического оборудования. В методику пробоподготовки к анализу была введена стадия твердофазной экстракции (ТФЭ). Выявлено, что оптимальным сорбентом для проведения ТФЭ явились патроны Nexus 60 mg (Varian). Путем последовательного промывания патрона с нанесенной пробой растворителями различной полярности производилось удаление примесей – неполярных (элюированием хлороформом и бензолом) и полярных (элюированием 2% водным раствором уксусной кислоты). Подбор экспериментальных условий элюирования примесей без десорбции ДГК проводили под контролем чувствительной цианидиновой пробы и с помощью ВЭЖХ.
Для элюирования ДГК с патрона достаточно 1 мл ацетонитрила. Анализ содержания ДГК в древесине лиственницы проводили по вышеописанной методике.
Установлено, что содержание ДГК в древесине лиственницы варьирует в широком интервале от 0,5% до 3,0 – 3,5% (редко до 4,0 – 4,5%). Это связано с разными географическими зонами произрастания. Важно отметить, что по количественному содержанию ДГК в древесине нет принципиального различия между двумя ботаническими видами лиственницы – сибирской и даурской.
5. Анализ и стандартизация комбинированных препаратов на базе диквертина
5.1. Способы анализа многокомпонентных препаратов на основе диквертина с использованием метода твердофазной экстракции
Для стандартизации асковертина, саливертина и каровертина необходимо было решить задачи пробоподготовки и анализа действующих веществ - ДГК и аскорбиновой кислоты (АК), ДГК и ацетилсалициловой кислоты (АСК), ДГК и АК и β-каротина соответственно.
Непосредственное одновременное спектрофотометрическое определение всех компонентов комбинированных препаратов в одной пробе затруднено тем, что получаемая при их совместном присутствии кривая УФ-спектра представляет собой спектр наложения, в котором невозможно выделить области индивидуального поглощения каждого из компонентов. Кроме того, спектры действующих веществ в неионизированном и ионизированном состоянии значительно различаются и необходимо было выбрать интервал рН, в котором воспроизводимость спектра наибольшая. Так, анализ водных и водно-метанольных растворов АК методом УФ-спектроскопии показал, что в течение короткого промежутка времени происходит изменение интенсивности оптического поглощения. В водных растворах кислот – 0,1% H3PO4 или 0,03% CF3COOH – с pH 2,5–2,7 (степень ионизации, вычисленная по данным pKa АК = 4,04 и pH составляет не более 2%), а также при добавлении к растворам кислот до 30% метанола по объему оптическая плотность АК не изменяется в течение 2 ч, что достаточно для анализа. Стабильность действующих веществ в той или иной среде учитывалась при выборе экстрагентов и элюентов.
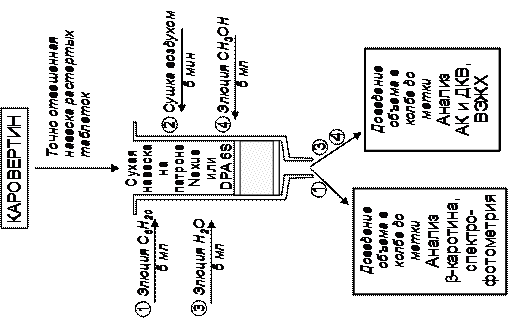
Для каждого из перечисленных препаратов предложены варианты анализа, основанные на предварительном разделении компонентов методом ТФЭ (рис. 3). Анализируемые смеси пропускали через колонку, заполненную соответствующим адсорбентом, на которой сорбировались отдельные компоненты. В наибольшей степени данной цели отвечали универсальные патроны для ТФЭ Nexus (Varian) и патроны с полиамидным сорбентом DPA-6S (Supelco). Разделение компонентов достигалось элюированием подходящим растворителем.
|
Достоинством способа анализа, основанного на разделении компонентов методом ТФЭ и их спектрофотометрическом определении, является экспресность и применение доступного, недорогого оборудования. Вместе с тем, очевидны и недостатки метода. Не учитывается вклад в поглощение ДГК родственных соединений – дигидрокемпферола и нарингенина, имеющих аналогичные спектральные характеристики. Таким образом, можно проводить анализ только совокупности флавоноидных компонентов ДКВ, а не ДГК. При анализе АСК не учитывается и не анализируется примесь СК, а ее содержание в препаратах АСК регламентируется. В случае асковертина оценка эффективности ТФЭ показала, что не происходит полного разделения АК и флавоноидов, до 3–4% флавоноидов от их общего содержания в таблетке не сорбируется на патроне ТФЭ и находится в водном растворе. Поэтому данный подход не является оптимальным для стандартизации асковертина и саливертина и для этих препаратов безусловный интерес представляла разработка универсальной методики одновременного определения действующих веществ, родственных соединений и примесей с использованием метода ВЭЖХ.
В то же время для стандартизации каровертина данный вариант анализа является оптимальным, так как в альтернативном случае пришлось бы разрабатывать два способа ВЭЖХ анализа – один для АК и флавоноидов и другой для β-каротина, учитывая, что их анализ требует различного сочетания подвижных и неподвижных фаз. Использование ТФЭ (рис. 3в) позволяет отделить АК и проанализировать ее спектрофотометрически, выделить и проанализировать методом ВЭЖХ компоненты ДКВ. β-Каротин экстрагируется из исследуемого образца гексаном и анализируется спектрофотометрически при длине волны 465±4 нм с использованием удельного показателя поглощения равного 2335. Предлагаемый вариант анализа с использованием ТФЭ характеризуется высокой селективностью, чувствительностью и воспроизводимостью.
![]()
![]()
![]()
![]()
![]()

![]()
![]()


5.2. Разработка унифицированной методики одновременного определения компонентов препарата Асковертин методом ВЭЖХ
В результате исследования различных вариантов пробоподготовки к анализу методом ВЭЖХ выбран простой, эффективный способ жидкостной экстракции. Компоненты ДКВ полностью извлекаются метанолом, при последующем добавлении к пробе 0,03% раствора ТФУ происходит полное растворение АК. Определяемые компоненты АК и ДГК устойчивы в растворах ТФУ и ПФ в течение 2 ч и более.
Поиск лучшего варианта хроматографических условий показал, что оптимальное разделение высокополярной АК и менее полярных и гидрофильных флавоноидов ДКВ достигается на сорбентах с привитой циано–фазой в режиме обращенно-фазного элюирования (сорбент Zorbax CN, 5 мкм; ПФ метанол – 0,03% трифтороуксусная кислота 21 : 79 об.%). При данной кислотности ПФ (pH среды 2,7) все компоненты асковертина находятся в неионизированной форме и наряду с неспецифическими взаимодействиями «сорбат-сорбент» появляются специфические – водородные связи между сорбатом и нитрильной группой сорбента. Таким образом, селективность данной хроматографической системы отличается от селективности традиционных обращенно-фазных алкильных сорбентов, при разгонке на которых АК элюируется практически с мертвым объемом.
Методика одновременного анализа АК и флавоноидов ДКВ оптимизирована по хроматографическим параметрам. Пики родственных ДГК соединений, входящих в состав субстанции ДКВ, четко различаются от пиков действующих веществ и имеют следующие показатели времени удерживания относительно СО ДГК: дигидрокемпферол 1,3 ± 0,1 и нарингенин 1,9 ± 0,1. Эффективность хроматографической колонки (N) варьирует по пику АК от 1554 до 1577 и по пику ДГК от 1354 до 1370 т. т. Разрешающая способность R для пары АК–ДГК составляет 1,3, для пары ДГК–дигидрокемпферол 1,1, для пары дигирокемпферол–нарингенин 2,5. Коэффициент асимметрии пика варьирует от 0,8 до 0,9 для пика АК и от 0,85 до 1,08 для пика ДГК. Относительное стандартное отклонение площади пика (S) составило 2,49% ± (n = 5) для площади пика АК и 1,32% ± (n = 5) для площади пика ДГК. Все приведённые параметры характеризуют пригодность хроматографической системы для анализа асковертина. Для проведения количественного анализа компонентов асковертина АК и ДГК методика валидирована по линейности, воспроизводимости, правильности.
Унификация методики ВЭЖХ анализа осуществлена таким образом, чтобы она служила единой аналитической базой для испытаний на подлинность, родственные соединения, растворение, однородность дозирования и для количественного определения АК и ДГК в таблетках. Подлинность: на хроматограмме полученной методом ВЭЖХ в предложенных условиях, должны содержаться пики ДГК и АК, совпадающие по времени удерживания с пиками ГСО ДГК и РСО АК, а также должны обнаруживаться родственные соединения – дигидрокемпферол и нарингенин.
На рисунке 4 приведены результаты теста «растворение», который введен только для ДГК как наименее растворимого из двух действующих веществ. Определение проводили в соответствии с требованиями ОФС 42‑0003‑00. По данным анализа 5 серий препарата через 20 мин количество ДГК в растворе достигало максимума и составляло не менее 80% от его номинального содержания в таблетке.
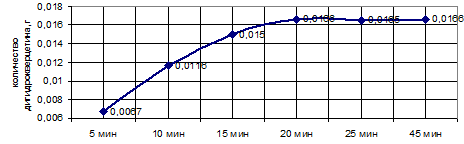
Рис. 4. Профиль высвобождения ДГК из таблеток асковертина
По результатам теста «однородность дозирования» отклонение содержания ДГК в одной таблетке составило от + 7 до – 6,5% от среднего содержания; отклонение содержания АК одной таблетке составило от + 7,2 до – 6,0% от среднего содержания, что удовлетворяет требованиям ГФ XI.
Результаты количественного определения АК и ДГК 5 опытно-промышленных партий таблеток «Асковертин», выработанных , приведены в табл. 4.
Таблица 4. Результаты анализов образцов таблеток Асковертина, изготовленных
Серия | Количественное определение в таблетке (ВЭЖХ): | |
дигидрокверцетина, от 0,0185 г до 0,0215 г | аскорбиновой кислоты от 0,0462 г до 0,0537 г | |
010503 | 0,0194 | 0,0485 |
020603 | 0,0196 | 0,0510 |
030703 | 0,0200 | 0,0492 |
040803 | 0,0201 | 0,0515 |
050903 | 0,0187 | 0,0490 |
Таким образом, разработанная методика анализа действующих веществ асковертина методом ВЭЖХ является универсальной и может быть использована для определения фармакопейных показателей, лежащих в основе оценки качества препарата.
5.3. Разработка унифицированной методики анализа компонентов саливертина методом ВЭЖХ
Основная цель в создании такой методики заключалась в разработке оптимальных условий одновременного определения действующих веществ саливертина – ДГК и АСК, родственных соединений биофлавоноидного комплекса ДКВ и посторонней примеси СК.
Хорошее разделение всех компонентов композиции ДКВ и АСК удалось реализовать в обращенно-фазном варианте в ПФ метанол-водный раствор кислоты в условиях градиентного элюирования. В качестве аналитической выбрана длина волны 280 нм, при которой АСК, СК и компоненты ДКВ имеют интенсивное поглощение.
Разработка состава ПФ включала выбор органического компонента и водного раствора кислоты. Для данной многокомпонентной смеси преимущество, по сравнению с ацетонитрилом, имеет метанол, как более «мягкий» элюент, имеющий более низкую элюирующую способность. Для выбора лучших параметров удерживания изучено влияние величины ПФ и типа кислоты на эффективность, разрешающую способность и размывание хроматографической зоны.
В таблице 5 представлены параметры пиков ДГК и АСК, полученные при использовании ПФ метанол-водный раствор кислоты в изократическом режиме 45 : 55 об.%. Оптимальное значение коэффициента ёмкости k¢ реализуется только для ПФ с 1% уксусной кислотой или 0,01% фосфорной кислотой. Наиболее высокая симметрия пиков ДГК и АСК достигается при использовании ПФ с ортофосфорной кислотой или трифтороуксусной кислотой (коэффициент ассиметрии пиков ДГК и АСК составляет в ПФ с H3PO4 0,93–0,94 и 0,91–1,05, соответственно, тогда как при использовании 1% CH3COOH 0,89 и 0,84). Критерий разделения пиков RS ДГК/АСК и селективность aДГК/АСК при использовании ортофосфорной кислоты находится в оптимальном диапазоне значений, что предопределило включение данной кислоты в состав ПФ.
Таблица 5. Выбор оптимального кислотного модификатора ПФ
Состав ПФ | CH3OH : 5% CH3COOH pH 3,51 | CH3OH : 2% CH3COOH pH 3,68 | CH3OH : 1% CH3COOH pH 3,68 | CH3OH : 0,01% H3PO4 pH 3,25 | CH3OH : 0,03% CF3COOH pH 2,88 |
k¢ДГК | 0,682 | 0,902 | 0,964 | 1,020 | 0,890 |
k¢АСК | 1,07 | 1,27 | 1,27 | 1,32 | 1,21 |
aДГК/АСК | 1,57 | 1,39 | 1,30 | 1,29 | 1,39 |
NДГК | 5202 | 4842 | 5305 | 5202 | 4389 |
NАСК | 7698 | 7025 | 7844 | 7516 | 6505 |
RS ДГК/АСК | 3,73 | 3,10 | 2,71 | 2,9 | 2,9 |
ASДГК | 0,77 | 1,13 | 0,89 | 0,93 | 0,91 |
ASАСК | 0,94 | 0,95 | 0,84 | 0,94 | 1,05 |
Для оптимизации хроматографического процесса по каждому компоненту саливертина предпочтительным является градиентный режим разгонки: фаза А – CH3OH, фаза Б – 0,01% H3PO4; в начальный момент соотношение А : Б – 45 : 55 об.%, к седьмой минуте разгонки 48 : 52 об.%, к 15 минуте 80 : 20 об.%. Хроматограмма образца таблетки саливертина представлена на рис. 5, а параметры разделения компонентов в табл. 6. Как видно из представленных данных все параметры находятся в оптимальном диапазоне.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



