На правах рукописи
САВВАТЕЕВ АЛЕКСЕЙ МИХАЙЛОВИЧ
ОЦЕНКА КАЧЕСТВА И СТАНДАРТИЗАЦИЯ
КОМПОЗИЦИЙ НА БАЗЕ ДИКВЕРТИНА
15.00.02 – фармацевтическая химия, фармакогнозия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата фармацевтических наук
МОСКВА – 2007
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования Московская медицинская академия имени Федерального агентства по здравоохранению и социальному развитию
Научный руководитель:
доктор фармацевтических наук
Официальные оппоненты:
профессор, доктор химических наук
профессор, доктор фармацевтических наук
Ведущая организация:
Институт стандартизации и контроля лекарственных средств ФГУ «Научный центр экспертизы средств медицинского применения» Росздравнадзора
Защита состоится «____»_______________2007 г. в _____ часов на заседании диссертационного совета Д.208.040.09 при Московской медицинской академии имени г. Москва, Никитский бульвар, 13.
С диссертацией можно ознакомиться в библиотеке Московской медицинской академии имени г. Москва, Нахимовский проспект, 49.
Автореферат разослан «____» __________2007 г.
Ученый секретарь
диссертационного совета Д.208.040.09
доктор фармацевтических наук, профессор Садчикова Наталья
Петровна
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Для России с ее богатейшими растительными ресурсами характерен широкий масштаб производства фитопрепаратов. В состав многих из них входят флавоноидные соединения.
Относительно недавно этот список пополнился препаратом Диквертин®, обладающим антиоксидантными и капилляропротекторными свойствами. Растительным источником диквертина служит древесина лиственницы. Состав его представлен тремя флавоноидными соединениями при подавляющем количестве (90% и выше) одного из них – дигидрокверцетина.
Банк присущих диквертину фундаментальных фармакологических свойств обеспечивает ему базисный статус для создания на его основе препаратов, комбинированных с другими лекарственными средствами с целью оптимизации отдельных видов фармакологического действия. В последние годы проведены совместные исследования сотрудниками НИИ фармакологии ТНЦ СО РАМН и кафедры органической химии ММА им. по разработке принципиально новой группы гемореологических лекарственных препаратов. Известно, что гемореологические нарушения осложняют течение таких заболеваний, как ишемическая болезнь сердца, артериальная гипертензия и др.
Препарат, сочетающий диквертин и аскорбиновую кислоту, зарегистрирован как ангиопротекторное лекарственное средство Асковертин®. Препарат, сочетающий диквертин и ацетилсалициловую кислоту (под рабочим названием Саливертин), прошел стадию доклинического изучения с выявлением антитромбоцитарного и гемореологического действия. Cочетание диквертина с двумя компонентами – аскорбиновой кислотой и β-каротином – используется как биологически активная добавка к пище «Каровертин».
Появление новых комбинированных препаратов в силу усложнения состава действующих веществ, существенно различающихся по свойствам, ставит задачу поиска оптимальных путей их фармацевтического анализа.
Актуальность настоящей работы определяется необходимостью совершенствования на современном физико-химическом уровне стандартизации базового фитопрепарата диквертина, а также создания системы стандартизации новых комбинированных препаратов.
Цель и задачи исследования. Целью настоящего исследования являлась разработка методологического подхода к оптимизации хроматографического анализа в качестве сквозного унифицированного метода стандартизации как базового препарата диквертина, так и комбинированных препаратов на его основе.
Для достижения поставленной цели решались следующие задачи:
· модификация и унификация методик анализа диквертина – от растительного сырья, субстанции, стандартного образца до лекарственной формы;
· совершенствование методик спектрального (УФ, ИК, ЯМР) анализа стандартного образца дигидрокверцетина;
· разработка методик хроматографического анализа с учетом специфичности состава комбинированных препаратов – асковертина, саливертина и БАД – каровертина;
· валидация предлагаемых методик на основе изучения соответствующих валидационных характеристик;
· включение разработанных методик в фармакопейную документацию.
Научная новизна. Предложен единый методический подход к стандартизации комбинированных препаратов на базе диквертина путем сквозного использования метода ВЭЖХ в сочетании со специфичностью пробоподготовки.
Определены оптимальные хроматографические условия эффективного разделения флавоноидных компонентов диквертина и аскорбиновой кислоты, компонентов диквертина и ацетилсалициловой и салициловой кислот в составе комбинированных препаратов – асковертина и саливертина соответственно. Разработаны селективные и воспроизводимые методики качественного и количественного анализа действующих веществ комбинированных препаратов.
Предложены спектральные (УФ-, ИК-, ЯМР 1Н, ЯМР 13С) и хроматографические критерии подлинности и оценки качества стандартного образца дигидрокверцетина.
Разработан оригинальный комбинированный способ использования в определенной последовательности методов твердофазной экстракции, ВЭЖХ и спектрофотометрии для анализа разнополярных компонентов каровертина.
Впервые разработана система стандартизации лекарственного растительного сырья – древесины лиственницы цельной и измельченной.
Практическая значимость. Методики анализа действующих веществ препаратов диквертина, асковертина и саливертина валидированы и унифицированы с целью определения таких фармакопейных показателей, как подлинность, родственные соединения, посторонние примеси, растворение, однородность дозирования, количественное определение. Разработанные аналитические методики включены в зарегистрированные фармакопейные статьи: Лиственницы древесина цельная, измельченная «ангро»; Дигидрокверцетин–стандартный образец; Диквертин субстанция; Диквертин таблетки; Асковертин таблетки; в проект фармакопейной статьи Саливертин таблетки; в Технические условия на БАД «Каровертин».
Предложенные методики апробированы на производственных сериях таблеток диквертина, асковертина и саливертина.
Основные положения, выносимые на защиту.
· Результаты изучения хроматографических характеристик флавоноидных компонентов диквертина. Усовершенствованная методика стандартизации и оценки качества диквертина методом ВЭЖХ.
· Спектральная (УФ-, ИК-, ЯМР 1Н и ЯМР 13С) и хроматографическая характеристика дигидрокверцетина как стандартного образца и оценка его индивидуальности и степени чистоты.
· Оптимальные хроматографические параметры ВЭЖХ для одновременного качественного и количественного анализа аскорбиновой кислоты и флавоноидов диквертина. Валидированная и унифицированная для определения ряда фармакопейных показателей методика стандартизации препарата асковертина методом ВЭЖХ.
· Оптимальные хроматографические параметры ВЭЖХ для одновременного качественного и количественного анализа ацетилсалициловой кислоты, примеси салициловой кислоты и флавоноидов диквертина. Валидированная и унифицированная для определения фармакопейных показателей методика стандартизации желудочно-резистентных таблеток саливертина методом ВЭЖХ.
· Комплексный аналитический подход (твердофазная экстракция, ВЭЖХ, спектрофотометрия) к анализу компонентов каровертина (аскорбиновая кислота, диквертин, b-каротин).
· Стандартизация лекарственного растительного сырья – древесины лиственницы цельной, измельченной «ангро».
· Результаты изучения возможности использования разработанных методик в анализе опытно-промышленных серий асковертина и лабораторных серий саливертина.
Апробация работы. Основные положения работы доложены на IV, VI, IX и X международных съездах «Актуальные проблемы создания новых лекарственных препаратов природного происхождения» (Великий Новгород 2001, С-Пб 2002, 2005 и 2006), на VI Симпозиуме по фенольным соединениям (Москва 2004) на XII Российском национальном конгрессе «Человек и лекарство» (Москва 2005).
Публикации. По теме диссертации опубликовано 9 печатных работ
Связь задач исследования с проблемным планом фармацевтических наук. Диссертационная работа выполнена в рамках комплексной темы кафедры органической химии ММА им. : «Физико-химические основы стандартизации и биотрансформации лекарственных средств и биологически активных добавок к пище». Номер госрегистрации .
Объем и структура диссертации. Диссертация изложена на 0000 страницах машинописного текста и состоит из введения, обзора литературы, двух глав, отражающих собственные экспериментальные исследования, выводов, списка литературы и приложения. Работа иллюстрирована 000 таблицами, 000 рисунками и 000 схемами. Библиографический список включает 124 отечественных и 64 зарубежных источников.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
1. Характеристика основных объектов и методов исследования
Объектами настоящего исследования являлись образцы древесины лиственницы сибирской и л. даурской; дигидрокверцетин – стандартный образец; биофлавоноидный комплекс диквертин и одноименный препарат «Диквертин»; композиции на базе диквертина, лежащие в основе создаваемых оригинальных комбинированных препаратов. Доминирующий компонент диквертина (90% и более) – дигидрокверцетин. В состав диквертина входят также родственные флавоноиды дигидрокемпферол и нарингенин.
Препарат «Асковертин» является комбинацией диквертина и аскорбиновой кислоты (таблетки, содержащие 0,02 г диквертина в пересчете на 100% содержание дигидрокверцетина и 0,05 г аскорбиновой кислоты). Композиция диквертина и ацетилсалициловой кислоты лежит в основе разрабатываемого препарата «Саливертин» (таблетки покрытые желудочно-резистентной оболочкой, содержащие 0,01 г диквертина в пересчете на 100% содержание дигидрокверцетина и 0,05 г ацетилсалициловой кислоты). Композиция диквертина, аскорбиновой кислоты и b‑каротина является основой БАД «Каровертин» (таблетки, содержащие 0,01 г диквертина в пересчете на 100% содержание дигидрокверцетина, 0,05 г аскорбиновой кислоты и 0,001 г b‑каротина). В исследование включались модельные смеси, субстанции и таблетки одноименных препаратов.
Основным аналитическим методом, используемым в работе, являлся метод ВЭЖХ. Для идентификации и анализа объектов исследования привлекались методы УФ-, ИК-, ЯМР 1Н и ЯМР 13С спектроскопии. Для фракционирования многокомпонентных смесей на стадии пробоподготовки применялась твердофазная экстракция в ее современном техническом исполнении.
2. Методический подход к анализу многокомпонентных смесей на базе диквертина
В состав биофлавоноидного комплекса и вышеуказанных композиций входят разнохарактерные с химической точки зрения соединения: от наиболее полярной и гидрофильной аскорбиновой кислоты, полярных и менее гидрофильных флавоноидов до неполярного и гидрофобного b‑каротина. Эффективное разделение компонентов смеси является основой для их аналитического определения.
Многокомпонентность состава комбинированных препаратов обусловила поиск оптимальных способов анализа и стандартизации их действующих веществ. Методические пути анализа многокомпонентных смесей, использованные в настоящей работе, представлены на схеме 1.
Схема 1. Алгоритм разработки методик анализа смесей на базе диквертина
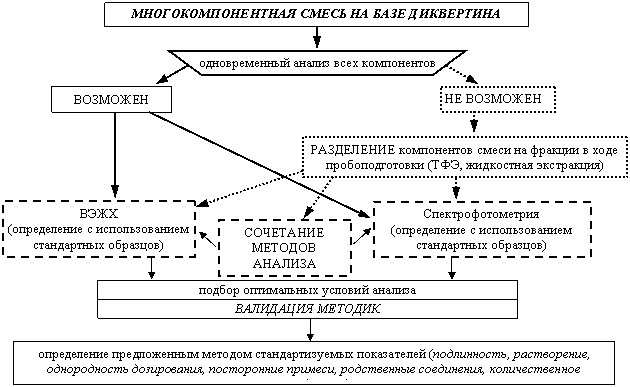

Унификация методик качественного и количественного анализа композиций осуществлялась таким образом, чтобы они служили единой аналитической основой для определения фармакопейных показателей качества препарата: подлинность, посторонние примеси, растворение, однородность дозирования, количественное определение. Большое значение уделено валидации методик, дающей высокую степень уверенности в том, что разработанная методика приводит к результатам, отвечающим установленным критериям приемлемости.
3. Физико-химическая характеристика дигидрокверцетина как стандартного образца
В фармацевтическом анализе для получения точных (правильных) и воспроизводимых результатов анализа ЛС решающее значение имеет применение высокоочищенных и хорошо охарактеризованных стандартных образцов.
Стандартный образец дигидрокверцетина (СО ДГК), получаемый из древесины лиственницы сибирской (Larix sibirica Ledeb.) и л. гмелина, или л. даурской (Larix gmelinii (Rupr.) Rupr., синоним Larix dahurica Turcz.), был разработан в 1996 г. совместно кафедрой органической химии ММА им. и г. Иркутск. За прошедший период проведена работа по совершенствованию способа выделения ДГК из экстракта древесины с использованием ВЭЖХ в полупрепаративном варианте. Экспериментальная работа по получению СО ДГК проведена в , г. Иркутск.
Одна из целей настоящей работы заключалась во всесторонней характеристике физико-химических свойств СО ДГК, доказательстве его строения и степени чистоты.
Индивидуальность и стереохимическое строение ДГК доказывалось с помощью хроматографических (ВЭЖХ) и спектральных (УФ-, ИК-, ЯМР 1Н и ЯМР 13С) методов.
Хроматографический анализ проводили с использованием двух типов сорбентов – октадецилсилановых и цианопропилсилановых – как в изократическом, так и в градиетном режимах элюирования. Подвижной фазой (ПФ) служили смеси ацетонитрила или метанола с водными растворами кислоты (фосфорной, трифтороуксусной или уксусной) с рН 3,0 – 3,5. Создание такой кислотности среды необходимо для подавления диссоциации фенольных гидроксильных групп. Детектирование осуществляли на аналитических длинах волн: при 230 нм для обнаружения соединений с короткой хромофорной системой; при 290 нм – ДГК и флаванонов с близкой структурой и при 370 нм – возможных примесей флавонов. Широкое варьирование условий производили с целью выявления возможных примесей. В качестве оптимальных нами предложены следующие условия ВЭЖХ анализа ДГК: колонка LiChrosper RP-18 5 мкм (250 х 4,6 мм); ПФ: А – ацетонитрил, Б – 2% уксусная кислота. Градиентное элюирование А : Б: 0–4 мин 35 : 65 об.%; 4,1–10 мин 70 : 30 об.%. Скорость потока – 1 мл/мин, аналитическая длина волны 290 нм. В данных условиях эффективность колонки по пику ДГК составляет 5450 т. т.; коэффициент емкости k¢ – 1,6; фактор симметрии пика As – 0,9–1,05; относительное стандартное отклонение площади пика S 0,98%. На всех хроматограммах образцов ДГК содержался единственный пик практически со 100% степенью чистоты.
Степень чистоты ДГК подтверждалась также методом ЯМР. Спектры ЯМР 1Н и ЯМР 13С регистрировали в дейтерированных растворителях – метаноле и диметилсульфоксиде. Отнесение сигналов, их мультиплетность и константы спин-спинового взаимодействия спектра ЯМР 1Н ДГК в ДМСО-D6 в области от 0,5 до 12 м. д. представлены в табл. 1. Суммарная интенсивность всех указанных сигналов соответствует 12 протонам молекулы ДГК С15Н12О7.
Наряду с сигналами протонов, представленных в табл. 1, наблюдаются сигналы растворителя: ДМСО-D6 (квинтет остаточных протонов дейтерированных метильных групп при 2,50 м. д.) и уширенный сигнал воды при 3,34 м. д.; а также незначительные примесные сигналы – уширенный синглет при 1,25 м. д. (0,03 массовых%) и синглет при 2,07 м. д. (0,007 массовых%), который можно отнести к ацетону, используемому в технологическом цикле. В целом, на основании анализа методами ВЭЖХ и ЯМР можно оценить степень чистоты образцов ДГК не ниже 99,96%.
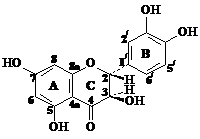 Также проведено отнесение всех сигналов в спектре ЯМР 13С. Химические сдвиги ядер 13С ДГК в ДМСО-D6 (δ, м. д.): 71,62 (С-3), 83,10 (С-2), 95,02 (С-8), 96, 03 (С-6), 100,53 (С-4а), 115,17 (С-5/), 115,40 (С-2/), 119,41 (С-6/), 128,08 (С-1/), 144,98 (С-3/), 145,81 (С-4/), 162,6 (С-8а), 163,37 (С-5), 166,83 (С-7), 197,78 (С-4).
Также проведено отнесение всех сигналов в спектре ЯМР 13С. Химические сдвиги ядер 13С ДГК в ДМСО-D6 (δ, м. д.): 71,62 (С-3), 83,10 (С-2), 95,02 (С-8), 96, 03 (С-6), 100,53 (С-4а), 115,17 (С-5/), 115,40 (С-2/), 119,41 (С-6/), 128,08 (С-1/), 144,98 (С-3/), 145,81 (С-4/), 162,6 (С-8а), 163,37 (С-5), 166,83 (С-7), 197,78 (С-4).
Таблица 1. Химические сдвиги (d) и константы спин-спинового взаимодействия (J) в ЯМР 1Н спектре СО ДГК в ДМСО-D6 *
(д, д – дублет дублетов, д – дублет, с – синглет, АВ – АВ-система)
Данные спектра | Кольцо С | Кольцо А | Кольцо В | Протоны ОН групп при: | |||||||
Н-2 | Н-3 | Н-6 | Н-8 | Н-2/ | Н-5/ и Н-6/ | С-5 | С-3 | С-7 | С-3/ | С-4/ | |
d, м. д. | 4,973 | 4,483 | 5,898 | 5,848 | 6,868 | 6,72 – 6,76 | 11,87 | 5,712 | 10,78 | 8,98 | 8,93 |
J, Гц | 11,1 | 6,1 и 11,1 | 2,0 | 2,0 | – | 8,2 | – | 6,1 | – | – | – |
Сигнал | д | д, д | д | д | с | АВ | с | д | с | с | с |
* Спектры ЯМР получены и обсуждены старшим научным сотрудником химического факультета МГУ им. , д. хим. н.
Индивидуальность структуры ДГК наиболее полно подтверждена методом ЯМР. Для отнесения сигналов в спектрах ЯМР 1Н и ЯМР 13С наряду с мультиплетностью, интегральной интенсивностью и положением сигналов использовалась информация двумерных экспериментов HSQC и HMBC. Особенно важную информацию дают кросс-пики двумерного эксперимента НМВС, которые позволяют устанавливать корреляцию сигналов 1Н и 13С, находящихся друг от друга через две–три связи. Использование современного подхода позволило впервые разделить и сделать надежное отнесение сигналов протонов всех гидроксильных групп. Ранее не удавалось идентифицировать сигналы протонов гидроксильных групп при С-7, С-3/ и С-4/ сигналы которых перекрывались и наблюдались в виде уширенного пика. В наиболее слабом поле расположен неуширенный сигнал гидроксильной группы 5‑ОН (11,87 м. д.), что свидетельствует об образовании внутримолекулярной водородной связи между 5‑ОН и карбонильной группой. Протон 5‑ОН группы дает отчетливые кросс-пики, соответствующие константам 13С–Н через две, три и четыре связи с атомами углерода С‑5, С‑4а, С‑6, и С‑7. Относительно мало уширен также сигнал протона группы 4¢‑ОН, который имеет кросс‑пики с С‑3¢, С‑4¢, С‑5¢ (рис. 1).
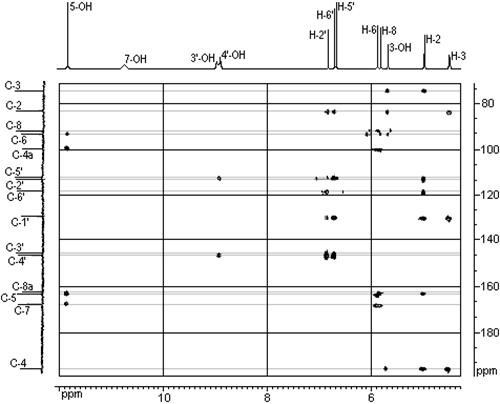
Рис. 1. Двумерный спектр ЯМР дигидрокверцетина: – по оси абсцисс сигналы протонов и их отнесение;– по оси ординат сигналы ядер 13С и их отнесение
Молекулярной специфичностью (за исключением отнесения стероизомеров) обладает и метод ИК-спектроскопии. Для подтверждения индивидуальности исследованного СО ДГК нами предложен ИК‑спектр в виде суспензии в вазелиновом масле (рис. 2).
В высокочастотной области хорошо разрешаются полосы поглощения, обусловленные валентными колебаниями ОН-связей: свободных (3550 см-1); связанных внутримолекулярной (3406 см-1) и межмолекулярной (широкая полоса с максимумом при 3250 см-1) водородными связями.
Валентные колебания связей С–Н в ароматическом кольце проявляются при 3080 см-1, валентные колебания ароматического кольца – при 1615, 1588 см-1. Положение интенсивной полосы валентного колебания карбонильной группы (1644 см-1) свидетельствует об ее участии в водородном связывании. Высокое разрешение полос поглощения в области «отпечатков пальцев» (1300–600 см-1) позволяет использовать ИК-спектр в суспензии в вазелиновом масле для надежной идентификации ДГК (рис. 2).
УФ-спектр СО ДГК в подкисленном этаноле в области длин волн от 230 нм до 380 нм характеризуется наличием полосы поглощения с минимумом при 247±2 нм и максимумом при 290±2 нм, имеющей плечо при 320–327 нм. Концентрации испытуемых растворов (0,001%) отвечала оптическая плотность от 0,590 до 0,640. Для количественной характеристики СО предложен удельный показатель поглощения Е1см1% при длине волны 290,0 нм. Проведено 9 независимых определений удельного показателя трех образцов ДГК. Величина удельного поглощения для этих растворов составила в среднем 623 ± 19.
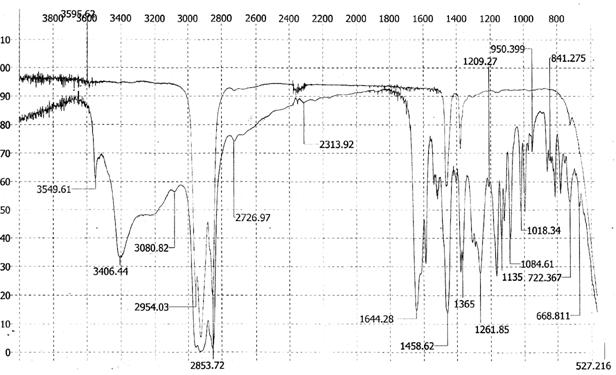
Рис. 2. ИК-спектр дигидрокверцетина в вазелиновом масле
Молекула ДГК содержит два центра хиральности и является оптически активным веществом. Для решения вопроса об относительной конфигурации стереоцентров в молекуле исследуемого дигидрокверцетина ключевую роль играет величина константы спин-спинового взаимодействия (J) протонов Н-2 и Н-3. По данным ЯМР 1Н спектра эта константа равна 11,1 Гц, что свидетельствует об их транс-расположении. Такую относительную конфигурацию имеют два стереоизомера дигидрокверцетина – 2R,3R-изомер и его энантиомер – 2S,3S-изомер. Учитывая сумму установленных в настоящее время физико-химических характеристик для всех четырех стереоизомерных форм ДГК, можно воспользоваться сравнением со специфическим сочетанием для каждого стереоизомера двух характеристик: величины константы J и направления угла оптического вращения.
Исследуемый в нашей работе ДГК имеет положительное значение удельного вращения, что в сочетании со значением константы J 11,1 Гц позволяет считать его изомером с 2R,3R-конфигурацией.
С помощью комплекса физико-химических методов установлено, что СО ДГК представляет собой индивидуальное соединение высокой степени чистоты, отвечающее структуре (2R,3R)-2,3-дигидро-3,5,7-тригидрокси-2-(3,4-дигидроксифенил)-4Н-1-бензопиран-4-она.
На базе высокоразрешающей аппаратуры усовершенствованы спектральные и хроматографические методики анализа, обеспечивающие достоверность проверки подлинности и чистоты ДГК, которые легли в основу соответствующей ФС для регистрации ДГК в качестве государственного стандартного образца.
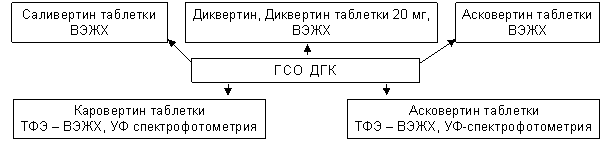
ГСО ДГК использовался в нашей работе для количественного определения модельных смесей, субстанций и лекарственных форм исследуемых объектов (схема 2).
Схема 2. Использование ГСО ДГК для количественного определения препаратов на базе диквертина

4. Анализ и стандартизация диквертина в субстанции, таблетках и растительном сырье
В состав субстанции диквертина (ДКВ) входят ДГК (90% и более), родственные соединения флаванонового ряда – дигидрокемпферол и нарингенин, допускается наличие флавонола кверцетина. Суммарное содержание дигидрокемпферола, нарингенина и кверцетина в субстанции должно быть не более 10%. В древесине листвинницы в незначительных количествах присутствуют пиностробин, пиноцембрин и пинобаксин.
Учитывая многокомпонентный состав ДКВ, оптимальным для его анализа является метод ВЭЖХ. Общим в структуре флавоноидных компонентов ДКВ является наличие малополярной ароматической углеродной и гетероуглеродной основы, несущей более полярные гидроксильные заместители. Такой тип структуры предопределяет использование обращенно-фазного варианта ВЭЖХ.
Пробоподготовка субстанции и таблеток ДКВ заключалась в непосредственном растворении образцов в ацетонитриле, фильтрации и дальнейшем разбавлении смесью растворителей, используемой в качестве ПФ. Нерастворимые в ацетонитриле вспомогательные вещества удалялись фильтрованием. Установлено, что вспомогательные вещества, растворимые в ацетонитриле, не мешают определению компонентов ДКВ.
При выборе аналитической длины волны изучены УФ-спектры ДКВ в ацетонитриле с добавлением водного раствора кислоты или щелочи в интервале pH от 2 до 8. В интервале pH от 2 до 4 спектр ДКВ, как и спектр ДГК, характеризуется максимумом полосы поглощения при 290±2 нм, имеющий плечо при 320–327 нм. При увеличении pH от 4 до 8 наблюдается уменьшение интенсивности поглощения при 290 нм и увеличение при 325 нм, что обусловлено ионизацией фенольных гидроксильных групп. Наилучшая воспроизводимость спектров достигается в интервале pH 2–3, когда ДГК находится в неионизированном состоянии. Это обстоятельство учитывалось при выборе состава ПФ. Дигидрокемпферол и нарингенин имеют сходную с ДГК хромофорную систему и, соответственно, подобный УФ-спектр. Кверцетин (флавонол) имеет максимум поглощения при 370 нм. Современные детекторы позволяют проводить обсчет результатов сразу для нескольких длин волн. В то же время чувствительность УФ детекторов такова, что, даже используя в качестве аналитической только длину волны 290 нм, можно обнаружить кверцетин (если он имеется) в образце ДКВ вплоть до его содержания 0,01% по массе.
Выбор обращенно-фазного сорбента осуществлен на основе анализа эффективности разделения компонентов ДКВ на этил-, октил - и октадецилсилановых сорбентах с использованием модельных смесей, содержащих ванилин в качестве внутреннего стандарта. В составе ПФ использовали метанол или ацетонитрил и 2% уксусную кислоту. Расчет хроматографических параметров показывает преимущество октадецилсиланового сорбента по эффективности, симметрии пика и воспроизводимости площади пика (табл. 2).
Таблица 2. Сравнение некоторых хроматографических параметров анализа ДКВ (при 5 повторных определениях)
Определяемый показатель | Колонки | ||
LiChrosorb 100 RP-2 250 мм х 4,6 мм; 5 мкм | LiChrosorb 100 RP-8 250 мм х 4,6 мм; 5 мкм | LiChrosorb 100 RP мм х 4,6 мм; 5 мкм | |
N по пику ДГК, т. т. | 815, 860, 900, 840, 810 | 3900, 3850, 3800, 3600, 3700 | 4300, 4400, 4500,4800,4900 |
RS пиков ДГК и ванилина | 2,1; 2,0; 2,1; 2,0; 2,1 | 2,0;2,2; 2,0; 2,1; 2,1 | 2,7; 2,6; 2,5; 2,5; 2,5 |
S площади пика ДГК, % | 1,8 ± 0,2 | 1,5 ± 0,2 | 1,1 ± 0,1 |
AS пика ДГК | 0,9; 1,5; 2,0; 0,7; 1,2 | 0,8; 1,2; 1,5; 1,2; 1,1 | 1,0; 1,1; 0,8; 0,9; 1,0 |
Изократический режим элюирования не позволяет оптимизировать хроматографический процесс для каждого компонента ДКВ. В ПФ ацетонитрил – 2% уксусная кислота (30 : 70 об.%) оптимизированы условия для ДГК и дигидрокемпферола, но на хроматограммах наблюдается асимметрия пиков нарингенина и кверцетина, имеющих большую величину коэффициетна емкости k¢. При резком увеличении органического модификатора ПФ (ацетонитрил – 2% уксусная кислота 70 : 30 об.%), ДГК элюируется практически с мертвым временем колонки, но для пиков нарингенина и кверцетина это соотношение оптимально. Поэтому, для оптимизации хроматографического процесса подобран градиентный режим элюирования: колонка 250 мм х 4,6 мм; сорбент LiChrospher 100, RP-18, 5 мкм; аналитическая длина волны 290 нм; ПФ– ацетонитрил (А), кислота уксусная 2,0% (Б); условия градиента (время/отношение А к Б (об.%)): 0 – 4,0 мин / 35 : 65, 4,1 – 10,0 мин / 70 : 30; скорость потока ПФ 1 мл/мин; температура колонки 20 °С

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



