Лекарственной формой саливертина являются таблетки покрытые кишечно-растворимой оболочкой. Наряду со вспомогательными веществами ядра (мелкокристаллическая целлюлоза, лактоза, картофельный крахмал и стеарат кальция) они содержат вспомогательные вещества оболочки (колликут МАЕ-100Р, полиэтиленоксид 400, диоксид титана). Процесс пробоподготовки оптимизирован таким образом, чтобы вспомогательные вещества ядра и оболочки не извлекались в анализируемый раствор. Поиск подходящего экстрагента привел к выбору в качестве такового ацетонитрила. Установлено, что в нем плохо растворимы компоненты оболочки таблетки, которые удаляют фильтрованием, но хорошо растворимы действующие вещества. Полученный раствор разбавляют ПФ А до удобного для анализа уровня концентраций действующих веществ.
|
|
|
|
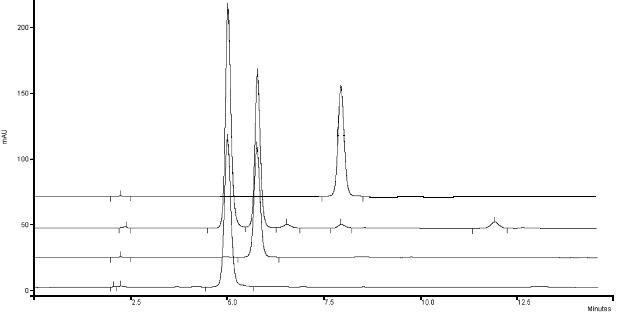
Рис. 5. Хроматограммы, иллюстрирующие селективность определения дигидрокверцетина, ацетилсалициловой кислоты и салициловой кислоты в таблетках саливертина
а – ГСО ДГК; б – РСО АСК; в – таблетки саливертина, порядок выхода веществ: ДГК (5,3); АСК (6,1); дигидрокемпферол (7,3); СК (8,5); нарингенин (12,8); г – РСО СК.
Таблица 6. Хроматографические параметры разделения компонентов смеси АСК и ДКВ (среднее из n=9)
Соединение | N | k¢ | a | RS |
ДГК | 5000 | 1,020 | ||
1,29 | 2,9 | |||
АСК | 7000 | 1,32 | ||
1,49 | 2,52 | |||
Дигидрокемпферол | 4800 | 2,12 | ||
1,11 | 1,32 | |||
Салициловая кислота | 7900 | 2,53 | ||
1,82 | 11,24 | |||
Нарингенин | 6510 | 4,27 |
Разработанная методика позволяет проводить качественный и количественный анализ саливертина с использованием внешних стандартов образцов – ГСО ДГК, РСО АСК и СК. Относительное стандартное отклонение площади пика ДГК составляет 2,37%, АСК 1,22% .Универсальность методики ВЭЖХ анализа саливерина позволяет использовать её в фармакопейных тестах «подлинность», «количественное определение», «растворение», «однородность дозирования», «посторонние примеси».
Поскольку саливертин относится ко 2-й группе ГЛФ – желудочно-резистентные таблетки, то в соответствии с фармакопейными требованиями тест «растворение» проводится в две стадии – в кислой, а затем нейтральной среде. Тест «растворение» может быть введен только для ДГК, как наименее растворимого из двух действующих веществ. Количество перешедшего в раствор ДГК определяли методом ВЭЖХ по представленной методике, в сравнении с раствором ГСО ДГК в подвижной фазе. Таким образом, для тестов «растворение» и «количественное определение» предложена единая методика ВЭЖХ, а в качестве стандарта один и тот же раствор ГСО ДГК. По данным анализа 5 серий препарата на 1-й стадии (кислотной) в раствор через 60 мин переходило не более 10% ДГК, на 2-й стадии (буферной) в растворе через 45 мин определялось не менее 70% ДГК, что соответствует требованиям ГФ XI.
Количественный анализ ДГК и АСК с использованием стандартных образцов по данной единой методике ВЭЖХ лежит и в основе теста «однородность дозирования».
В препаратах, содержащих АСК в качестве посторонней примеси может присутствовать СК. Она образуется в результате гидролиза АСК на технологических стадиях производства и при нарушении условий хранения. В различных фармакопеях допустимые уровни нормирования примеси СК в лекарственных формах АСК несколько различаются. По Европейской Фармакопее содержание СК в таблетках АСК должно быть не более 0,15%, а по Фармакопее США – не более 0,3%. В таблетках аспирина покрытых оболочкой в Фармакопее США нормируется допустимая примесь СК не более 3%.
Обнаружение примеси СК в препарате осуществляется на основании совпадения на хроматограммах времен удерживания пика в образцах с таковым для РСО СК. Методика позволяет анализировать СК в таблетках без оболочки и в таблетках покрытых оболочкой. Для таблеток покрытых оболочкой анализ СК рекомендуется проводить, используя разбавленный раствор, одновременно с анализом действующих компонентов препарата, а не покрытых желудочно-резистентной оболочкой более концентрированный раствор.
По результатам анализа таблеток 5 серий препарата саливертина установлено, что содержание СК изменялось в интервале 0,0009 – 0,0014 г. Ни в одной из анализируемых серий содержание примеси СК не превышало допустимое значение (не более 3%).
Разработанная методика оценки качества саливертина с использованием ВЭЖХ испытана в анализе модельных смесей и таблеток двух лабораторных партий. Методика нашла отражение в подготавливаемой фармакопейной документации для регистрации препарата саливертина «подлинность», «однородность дозирования», «растворение», «посторонние примеси», «количественное определение».
6. Валидация методик анализа диквертина, асковертина и саливертина
Важнейшим критерием оценки аналитической методики служит доказательство её валидности, включающей взаимосвязанную систему характеристик – специфичность, пригодность хроматографической системы, линейность, правильность и воспроизводимость.
С этой целью выполнено экспериментальное исследование по изучению комплекса валидационных характеристик разработанных методик определения действующих веществ указанных препаратов методом ВЭЖХ. Пригодность хроматографической системы для анализа каждого препарата подтверждена оптимальными значениями хроматографических параметров, представленными выше.
Специфичность методики основана на возможности достоверно определять количественное содержание действующих веществ в таблетке в присутствии вспомогательных веществ и родственных соединений. Процесс пробоподготовки оптимизирован таким образом, что вспомогательные вещества ядра и оболочки не извлекаются в анализируемый раствор. На хроматограммах модельной смеси, содержащей вспомогательные вещества без действующих веществ (плацебо), отсутствуют пики, мешающие определению действующих веществ. Тождественность действующих веществ препаратов ДГК, АК, АСК и СК подтверждалась совпадением времен удерживания анализируемых компонентов таблетки и стандартных образцов. Пики родственных соединений, входящих в состав субстанции диквертин, хорошо разделяются с пиками действующих веществ.
Линейная зависимость методики отражает пропорциональность возрастания площади пика на хроматограмме при возрастании количества анализируемых веществ в испытуемых образцах. Данная валидационная характеристика исследовалась на модельных смесях в интервале 70–130% от заявленного содержания действующих компонентов в таблетках. Зависимость аналитического сигнала (условных единиц площади пика) от содержания анализируемых веществ (в г) описаны уравнением регрессии y = bx + a (табл. 7). Согласно полученным результатам все линейные зависимости характеризуются высоким коэффициентом корреляции в интервале 70–130% декларируемой величины. Этот интервал можно определить как аналитическую область методики.
Правильность (точность) методики показывает систематические погрешности метода и выражается как процент регенерации точно взвешенного количества анализируемого образца. Правильность разработанных методик установлена по результатам анализа модельных смесей с использованием СО для трех повторностей определений семи аналитических концентраций. В таблице 8 продемонстрированы результаты данной характеристики валидности на примере саливертина. Как видно из представленных данных, методика обладает удовлетворительной точностью. Полученные аналогичным образом результаты для препарата асковертина показали, что средний процент регенерации составляет для АК 99,1%, для ДГК – 99,2%. Результаты оценки правильности, полученные для всех методик, находятся в интервале 97–103%.
Таблица 7. Параметры линейной регрессии зависимостей площадей пиков от содержания анализируемых веществ в модельных смесях
Действующее вещество | Отрезок а | Наклон b | Коэффициент корреляции |
ДИКВЕРТИН | |||
ДГК | 127000 | 8,647 | 0,9993 |
АСКОВЕРТИН | |||
ДГК | 7257,3571 | 7,0212 | 0.9984 |
АК | 6554,3571 | 3,8295 | 0,9998 |
САЛИВЕРТИН | |||
ДГК | 11310 | 6,16 | 0,9989 |
АСК | 340660 | 8,88 | 0,9993 |
СК | 1050 | 9,63 | 0,9886 |
Таблица 8. Оценка правильности методики определения действующих компонентов саливертина
Действующих веществ от заявленного в таблетке, % | Состав в модельной смеси, г | Найдено*,г | Регенерация*,% | |||
ДГК | АСК | ДГК | АСК | ДГК | АСК | |
70 | 0,0072 | 0,0358 | 0,0071 | 0,0357 | 98,6 | 99,7 |
80 | 0,0080 | 0,0407 | 0,0082 | 0,0405 | 102,5 | 99,5 |
90 | 0,0091 | 0,0455 | 0,0090 | 0,0454 | 98,9 | 99,7 |
100 | 0,0101 | 0,0506 | 0,0100 | 0,0507 | 99,0 | 100,2 |
110 | 0,0112 | 0,0555 | 0,0112 | 0,0558 | 101,8 | 100,5 |
120 | 0,0121 | 0,0602 | 0,0121 | 0,0600 | 100,0 | 99,7 |
130 | 0,0134 | 0,0653 | 0,0133 | 0,0652 | 99,3 | 99,8 |
* - среднее из 3 определений
Воспроизводимость аналитической методики характеризовалась степенью совпадения результатов индивидуальных определений при многократном использовании. По представленным в таблице 9 параметрам (величины стандартного отклонения, доверительный интервал) можно сделать заключение о хорошей воспроизводимости методик анализа асковертина и саливертина. Относительная ошибка среднего результата определения ДГК составляет 2,73 и 1,97% соответственно, АК 1,70%, АСК – 1,74% и СК 2,9%.
Таблица 9. Оценка воспроизводимости методик анализа асковертина и саливертина
хi, мг | n | хср±Dхср | S | eср | Р, f | хi, мг | n | хср±Dхср | S | eср | |
АСКОВЕРТИН | |||||||||||
по ДГК | по АК | ||||||||||
18,90; 19,27; 19,54; 19,58; 19,84; 20,20; 20,45; 20,85; 21,04 | 9 | 19,96±0,5452 | 0,724 | 2,73 | 2,26 | 48,50; 48,85; 48,93; 49,00; 49,20; 50,10; 50,75; 51,23; 51,47 | 9 | 49,78±0,85 | 1,3 | 1,70 | |
САЛИВЕРТИН | |||||||||||
по ДГК | по АСК | ||||||||||
10,1; 10,2; 9,8; 9,7; 10,3; 9,5; 9,9; 9,8; 10,1 | 9 | 9,93±0,1959 | 0,260 | 1,97 | 2,26 | 48,51; 48,96; 51,33; 48,80; 50,10; 50,85; 49,01; 49,23; 51,47 | 9 | 49,8±0,87 | 1,15 | 1,74 | |
По валидационным характеристикам разработанные методики являются специфичными для определения содержания действующих веществ, характеризуются корректной точностью и воспроизводимостью, линейной зависимостью в аналитической области ± 30% по отношению к заявленному содержанию действующих веществ в таблетках, что позволяет использовать их для достоверной оценки качества препаратов.
ВЫВОДЫ
1. Разработан единый аналитический подход к стандартизации и оценке качества в цепи объектов: древесина лиственницы – биофлавоноидный комплекс диквертин – комбинированные препараты на базе диквертина: асковертин (с аскорбиновой кислотой), саливертин (с ацетилсалициловой кислотой), БАД каровертин (с аскорбиновой кислотой и b-каротином). Аналитический подход, включающий этапы соответствующей пробоподготовки и анализа методом ВЭЖХ, применим для определения фармакопейных показателей как субстанций, так и лекарственных форм.
2. С помощью комплекса физико-химических методов установлено, что стандартный образец дигидрокверцетина (производства , г. Иркутск) представляет собой индивидуальное соединение высокой степени чистоты, отвечающее структуре (2R,3R)-2,3-дигидро-3,5,7-тригидрокси-2-(3,4-дигидроксифенил)-4Н-1-бензопиран-4-она. Предложены спектральные и хроматографические методики анализа, обеспечивающие достоверность подлинности (ИК-, ЯМР 1Н и ЯМР 13С спектры) и чистоты (ВЭЖХ, ЯМР 1Н и УФ-спектроскопия) дигидрокверцетина. Исследованные образцы дигидрокверцетина соответствуют фармакопейным требованиям, предъявляемым к государственным стандартным образцам, и могут быть использованы для анализа лекарственных средств и лекарственного растительного сырья.
3. Определены оптимальные условия разделения и анализа флавоноидных компонентов диквертина с использованием обращенно-фазного варианта ВЭЖХ на октадецилсилановых сорбентах в градиентном режиме элюирования. Предложена усовершенствованная методика стандартизации субстанции и таблеток диквертина с применением стандартного образца дигидрокверцетина и обосновано ее применение для анализа основного компонента дигидрокверцетина и родственных соединений – дигидрокемпферола и нарингенина.
4. Установлено, что оптимальное разделение полярной и гидрофильной аскорбиновой кислоты и менее полярных и более гидрофобных флавоноидных компонентов диквертина достигается на сорбентах с привитой циано-фазой в режиме обращенно-фазного элюирования. На основе изученных хроматографических характеристик композиции диквертина и аскорбиновой кислоты предложена унифицированная методика стандартизации субстанции и таблеток препарата асковертина.
5. Разработаны эффективные способы пробоподготовки и одновременного анализа методом ВЭЖХ ацетилсалициловой кислоты, флавоноидных компонентов диквертина и салициловой кислоты (как возможной примеси) в таблетках саливертина, покрытых желудочно-резистентной оболочкой. В предлагаемых хроматографических условиях эффективность колонки по пику дигидрокверцетина составила не менее 5000 т. т., по пику ацетилсалициловой кислоты не менее 7000 т. т., степень разделения всех пиков не ниже 2,5, фактор симметрии близок к единице. Относительное стандартное отклонение площади пика дигидрокверцетина 2,4%, ацетилсалициловой кислоты 1,2%. Все хроматографические параметры соответствуют современным фармакопейным требованиям.
6. Предложен селективный и воспроизводимый способ анализа композиции диквертина, аскорбиновой кислоты и b-каротина, как основы БАД каровертин и одноименного разрабатываемого препарата. Способ основан на предварительном фракционировании компонентов смеси методом твердофазной экстракции и последующем анализе фракций методом ВЭЖХ (аскорбиновая кислота и компоненты диквертина) и УФ-спектрофотометрии (b-каротин).
7. Изучен комплекс валидационных характеристик предложенных методов анализа и стандартизации препаратов диквертин, асковертин и саливертин в субстанции и лек. формах. По результатам валидации установлено, что все разработанные методики являются специфичными для определения содержания действующих веществ, характеризуются корректной точностью (правильностью) и воспроизводимостью, линейной зависимостью в аналитической области ± 30% по отношению к заявленному содержанию действующих веществ в препарате, что позволяет использовать их для достоверной оценки качества препаратов.
8. Показано, что унифицированные методики анализа препаратов диквертин, асковертин и саливертин можно использовать для сквозной стандартизации препаратов по фармакопейным показателям подлинность, родственные соединения, посторонние примеси, растворение, однородность дозирования, количественное определение. Методики включены в нормативную документацию по стандартизации и контролю качества вышеперечисленных препаратов.
Список работ опубликованных по теме диссертации
1. , , и др. Разработка новой биологически активной добавки к пище «Антоксид». // Материалы IV международного съезда «Актуальные проблемы создания новых лекарственных препаратов природного происхождения». Великий Новгород. – 2001. – С. 210–216.
2. , , и др. Разработка методов анализа смеси диквертина и ацетилсалициловой кислоты – действующей основы нового комплексного препарата // Материалы VI международного съезда «Актуальные проблемы создания новых лекарственных препаратов природного происхождения». Санкт-Петербург. – 2002. – С. 184–186.
3. , , Тюкавкина анализ композиции диквертина и аскорбиновой кислоты. // Материалы VI Симпозиума по фенольным соединениям. М., 2004. – С. 106.
4. , , и др. Валидация методики анализа препарата «Асковертин» // Фармация№ 3. - С. 11-14.
5. , , и др. Валидность методики определения компонентов препарата «Саливертин» // Фармация№ 3. - С. 11-14.
6. , , и др. Стандартизация композиции аскорбиновой кислоты, диквертина и b-каротина // Материалы XII Российского нац. конгр. «Человек и лекарство». М., 2005. – С. 702.
7. , , и др. Разработка фармакопейного хроматографического метода анализа нового отечественного препарата саливертин // Материалы IX междунар. съезда «Актуальные проблемы создания новых лекарственных препаратов природного происхождения». Санкт-Петербург, 2005. – С. 556–559.
8. , , Тюкавкина примеси салициловой кислоты в новом препарате «Саливертин» методом ВЭЖХ // Микроэлементы в медицине. – 2005. – Т. 6. Вып. 3. – С. 90–93.
9. , , и др. Физико-химическая характеристика дигидрокверцетина как стандартного образца // Материалы Х междунар. съезда «Актуальные проблемы создания новых лекарственных препаратов природного происхождения». Санкт-Петербург, 2006. – С. 338–342.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



