Из таблицы видно, что у больных в основной подгруппе уменьшение вегетативных и астенических проявлений в структуре абстинентного синдрома заметно выражена уже на 6-8 день, несмотря на то, что в этой подгруппе наблюдалось значительно большее количество сопутствующей соматической патологии (вирусный и токсический гепатит в основной подгруппе выявлялся у 13,75% больных, в контрольной - у 8,6%; сочетание различной соматической патологии (гепатиты, хронические заболевания желудочно-кишечного тракта, токсическое поражение ретикулоэндотелиальной и иммунной систем и др. в основной подгруппе выявлялись у 72,5% больных, в контрольной подгруппе - 71,4%). В то время как у больных контрольной подгруппы эта симптоматика редуцировалась только ко второй неделе лечения. Причем во всех случаях показатели статистически достоверны - р<0,05.
Такие признаки как подавленное настроение, ранняя и поздняя бессонница, работоспособность, заторможенность, тревога, внутреннее напряжение, обидчивость, чувство неудовлетворенности собой у больных основной подгруппы уменьшались значительно раньше, и, как видно из таблицы, эти данные статистически достоверны - р<0,05.(Табл. 2)
Аффективные, вегетативные и соматические расстройства в основной подгруппе уменьшались синхронно и в короткое время без назначения антидепрессантов.
В контрольной подгруппе аффективные расстройства были более устойчивы. Практически всем больным этой подгруппы начиная с третьих суток лечения оказалось необходимы назначение антидепрессантов (леривон 30 мг/сут; людиамил до 150 мг/сут.). Использование именно этих антидепрессантов определялось отсутствием у них холинолитических побочных эффектов. Выбор антидепрессанта определялся выраженностью депрессивной симптоматики.
Табл. №2
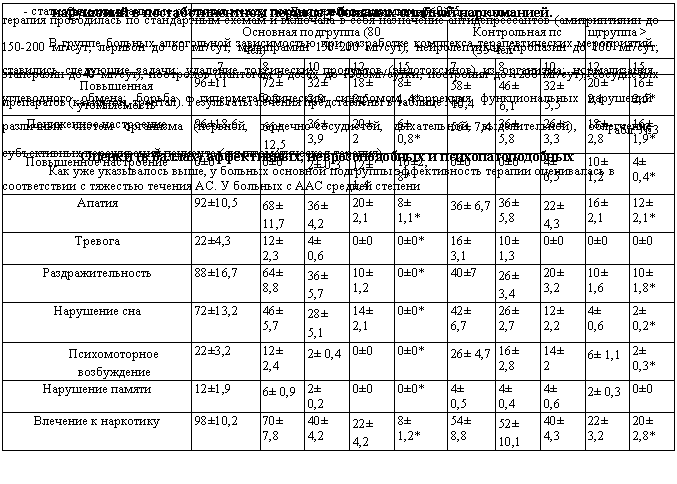
Динамика психопатологических проявлений в структуре опийного абстинентного синдрома во время лечения (количество больных с данным признаком в % по отношению ко всей подгруппе)
Симптомы | Основная подгруппа | Контрольная подгруппа | ||||||
1 день | 7 день | 1 день | 7 день | |||||
Абс | % | Абс | % | Абс | % | Абс | % | |
Влечение к наркотику | 80 | 100 | 30* | 37,5 | 34 | 97,1 | 25* | 71,4 |
Нарушение сна | 80 | 100 | 27* | 33,8 | 33 | 94,3 | 28 | 80 |
Пониженное настроение | 76 | 95 | 23* | 28,7 | 34 | 97,1 | 32 | 91,4 |
Тревога | 79 | 98,8 | 24* | 30 | 35 | 100 | 15* | 42,9 |
Страх | 80 | 100 | 0* | 0 | 35 | 100 | 7* | 20 |
Раздражительность | 77 | 96,3 | 16* | 20 | 33 | 94,3 | 31 | 88,6 |
Психомоторное возбуждение | 70 | 87,5 | 0* | 0 | 33 | 94,3 | 10* | 28,6 |
- статистически значимые различия между показателями в динамике, р<0,05
Из таблицы видно, что к 10 дню лечения в основной подгруппе такие показатели, как влечение к наркотику, нарушение сна, пониженное настроение, тревога снизились втрое. В контрольной же подгруппе эти показатели к десятым суткам лечения не уменьшились даже вдвое.
Критериями завершения острого абстинентного синдрома, который длился до 5-7 суток пребывания в стационаре, считалось снижение компульсивного влечения к наркотику, отсутствие выраженных расстройств настроения и сна. В это время у больных устанавливалось состояние неустойчивого равновесия в первую очередь характеризующееся нестабильным гомеостазом, когда любая нагрузка вызывает возвращение отдельных абстинентных признаков. Кроме того, в постабстинентный период продолжают выявляться отдельные психопатологические феномены, проявляющиеся, прежде всего эмоциональными расстройствами - депрессией, сопровождающейся дисфорией или апатией. Этот период может длиться от 3 недель до 2 месяцев. В данном исследовании изучалось влияние терапии на симптоматику в наиболее рискованном для рецидива раннем постабстинентном периоде.
Аффективные расстройства у больных опийной наркоманией являются наиболее существенным компонентом не только синдрома отмены, но и синдрома патологического влечения к наркотику в постабстинентный период. Клинические проявления аффективных нарушений вариабельны. Наиболее характерными являются апатический (13-16,25%) и истерический (19-23,75%) варианты депрессий, формирующиеся в постабстинентный период. Дисфорический (12-15%) и тревожный (12-15%) варианты депрессий абстинентного периода имеют тенденцию к трансформации в астенические (11-13,75%) и ипохондрические( 19-23,75%) депрессивные расстройства в постабстинентный период.
В задачи исследования входила разработка терапии с использованием ксенона и при ранних проявлениях постабстинентного синдрома. Такое состояние и характеризует постабстинентный период, проявляясь возникающим время от времени компульсивным влечением к наркотику, транзиторными вегетативными расстройствами, подавленным настроением, неустойчивым ритмом сна, нарушением аппетита и астеническим симптомокомп лексом.
Показаниями для назначения ксенона в раннем постабстинентном периоде при лечении опийной наркомании мы считали следующие состояния:
1. Психические и поведенческие расстройства: астено-депрессивные состояния (пониженный фон настроения, снижение волевых качеств, пессимистическая окраска эмоций, быстрая истощаемость, истероидные и ипохондрические симптомы). Аддиктивное поведение (повышенная раздражительность вплоть до брутальности, демонстративное упрямство, тенденция к антисоциальным поступкам, назойливость, резонерство, сверхценные идеи, в особенности, объясняющие причину и «необходимость» употребления наркотика).
2. Соматические, неврологические расстройства: полинейропатии и энцефалопатии смешанного генеза (токсические и сосудистые), сопровождающиеся двигательными и вегетативными нарушениями, расстройствами памяти, невралгиями и цефалгиями; кардиомиопатии с колебаниями артериального давления и нарушениями сердечного ритма; нейролептический синдром; страх приступа бронхиальной астмы.
Ксенон вводился ингаляционно ежедневно в течение 5 дней один раз в сутки. Отказов от терапии не было, все больные дали письменное согласие на проведение сеансов ингаляции ксенона. Терапия ксеноном в раннем постабстинентном периоде в основной подгруппе сочеталась с назначением нормотимиков (финлепсин в дозе до 400 мг в сутки). Нейролептики и антидепрессанты этим больным не назначались. В контрольной подгруппе
тяжести - 63 больных (57,3 %) - соматовегетативные, гемодинамические и поведенческие расстройства были умеренно выражены. Гемодинамические и биохимические параметры, как правило, выходили за рамки нормальных, не создавая при этом ситуаций опасных для жизни. Такие больные находились в ОРИТ до трех суток. Медикаментозная терапия ААС у этих больных была минимальна - назначались внутривенные капельные инфузии глюкозо-электролитных изотонических растворов до 1000 мл. в сутки и витаминотерапия. Общее количество ингаляций ксеноно-кислородной смеси равнялось 5: в первые сутки проводилось 2-3 сеанса ксеноновой терапии в зависимости от выраженности сомато-вегетативных проявлений ААС; во вторые и третьи сутки - по одному сеансу ксеноновой терапии в вечернее время.
У 47 больных - 42,7% от общего числа исследуемых и у них было диагностировано
тяжелое течение ААС. У 6 человек (5,4%) тяжелым течением ААС развились острые
алкогольные психозы (алкогольный делирий - 4 человека и острый алкогольный галлюциноз
- 2 человека). У остальных больных с тяжелым течением ААС в 65,9% случаев (27 чел.)
абстинентное состояние протекало с преимущественными гемодинамическими и
вегетативными расстройствами (нестабильной гемодинамикой, нарушениями сердечного
ритма, профузным потоотделением, значительными ишемическими изменениями миокарда).
Эти расстройства, как правило, сопровождались психомоторным возбуждением, страхом
смерти. В 34,1% случаев (14 чел.) тяжелый ААС протекал с преимущественными
неврологическими расстройствами (грубой диэнцефальной и мозжечковой симптоматикой,
атаксиями, полинейропатиями, интеллектуально-мнестическими нарушениями,
эписиндромом). Больные с тяжелым ААС находились в ОРИТ от 3-х до 5-ти суток, где им проводилась терапия ксеноном 3 раза в первые и вторые сутки лечения и по два раза в сутки в остальные дни пребывания в отделении реанимации.
Течение сеансов терапии ксеноном у всех больных с ААС средней степени выраженности протекало без возбуждения. Среднее время достижения желаемого уровня анестезии в этой группе больных составляло 5,5±2,5 мин. Через 30-60 секунд после начала ингаляции происходила нормализация ЧСС на цифрах 68-80 сокращения в 1 мин., артериальное давление стабилизировалось на цифрах 120/6/70 мм. рт. ст., насыщение артериальной крови кислородом по данным пульсоксиметрии (Sat О2) не снижалось ни в одном случае и составляло 96-100%. Угнетения дыхания так же не наблюдалось, оно было глубоким, ровным, частота дыхания составляла 10-14 вдохов/мин. Через 45-60 секунд после окончания ингаляций ксеноном сознание больных становилось ясным. Объективно и субъективно отмечалась редукция сомато-вегетативных нарушений - исчезали гипергидроз, тремор, головокружение, головные боли. Субъективно больные отмечали чувство облегчения, исчезновение влечения к алкоголю. После сеанса больные, как правило, засыпали. Сон продолжался 1,5-3 часа, а при вечернем назначении сеанса - 6-7 часов. Причем было отмечено, что чем тяжелее было состояние пациента, тем продолжительнее был сон. Из этой подгруппы 22 человека (34,9%) уже на следующие сутки были переведены в наркологические отделения и не нуждались в дополнительных назначениях корректоров поведения и снотворных препаратов.
Сеансы анестезии у большинства больных с тяжелым ААС также протекали без возбуждения. Время достижения желаемого уровня анестезии колебалось от 15 до 3-х минут (в среднем) и снижалось при повторном проведении сеансов. У трех больных в состоянии алкогольного психоза наблюдались кратковременные (10-15 сек.) периоды психомоторного возбуждения. У двух больных возбуждение прошло самостоятельно, и лишь в одном случае для его купирования потребовалось внутривенное введение мидазолама 0,1 мг/кг веса.
У всех больных с тяжелой формой ААС при проведении сеансов терапии ксеноном был отмечен эффект стабилизации гемодинамики: при гипотонии - АД повышалось, а при гипертензии - снижалось и стабилизировалось на цифрах 120/7/80 мм. рт. ст.; уменьшалась частота экстрасистол при аритмиях (34,1%), а в отдельных случаях (19,5%) -пароксизмы острых нарушений ритма купировались полностью; улучшались показатели метаболизма миокарда по данным ЭКГ. По всей видимости, такие результаты связаны с подавлением ксеноном симпатической и, в меньшей степени, парасимпатической периферической нейротрансмиссии, что позволяет считать ксенон относительным ваготоником ( с соавт., 1999; Ishiguro et al., 2000).
Симптомы | До лечения | На фоне лечения препаратом | ||||||
Через 1 час | Через 3 часа | В конце дня | 2 | 3 | 4 | 5 | ||
Влечение к алкоголю | 91±13,7 | 83±9,2 | 83±16, 6 | 79±10, 7 | 67±9, 5 | 60±9, 7 | 51±6, 6 | 37±6,9 * |
Нарушение сна | 82±13,2 | 67±9,8 | 61±7,6 | 61±10, 8 | 54±9, 5 | 40±7 | 35±5, 1 | 24±3,4 |
Пониженное настроение | 77±12,2 | 65±9,3 | 59±8,6 | 55±7,9 | 52±6, 6 | 50±6, 3 | 47±5 | 37±4,9 * |
Тревога | 51±8,8 | 38±6,8 | 36±5,7 | 30±4,1 | 30±3, 9 | 21 ±2, 4 | 11±1, 6 | 6±1,2* |
Страх | 24±3,7 | 17±2,2 | 17±2,6 | 15±2,6 | 13±1, 4 | 9±1 | 3±0,3 | 2±0,3* |
Раздражительность | 73±12,5 | 73±13, 7 | 64±8,8 | 64±9,5 | 63±8, 9 | 52±7, 6 | 48±5, 5 | 31±3,5 * |
Психомоторное возбуждение | 26±4,6 | 20±3,9 | 19±3 | 14±1,4 | 9±1 | 8±1,6 | 6±0,9 | 0±0* |
Таким образом, после проведенного курса комплексной терапии с использованием ингаляций ксенона у всех пациентов основной подгруппы отмечалась редукция сомато-вегетативных расстройств, и положительная динамика в выраженности психопатологических симптомов (Табл.№4). Наиболее отчетливо реагировали на это лечение диссомнические расстройства: трудности засыпания, пробуждения среди ночи, ранние пробуждения. У всех больных уже после первого сеанса ингаляции ксенона отмечалось улучшение засыпания и продолжительности ночного сна. На вторые-третьи сутки лечения среднетяжелого течения ААС и на третьи-четвертые сутки - при тяжелом течении ААС больные отмечали появление ощущения бодрости, чувства полноценного отдыха после сна, резко снижалась частота кошмарных сновидений.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |


