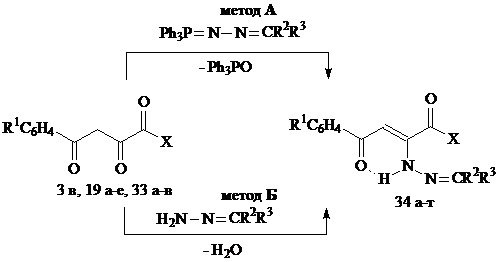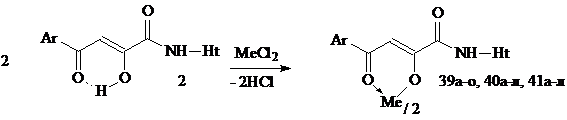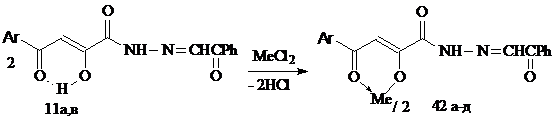Установлено, что N-(5-R-2-тиазолил)амиды 2 внутримолекулярно циклизуются в производные имидазо[2,1-b]тиазолов 27,28 только под действием диазометана и диазоэтана. При взаимодействии N-(2-тиазолил)амида 2у с диазоэтаном был также выделен N-(2-тиазолил)амид 4-оксо-4-фенил-2-этокси-2-бутеновой кислоты (29). При проведении реакции N-(2-тиазолил)амида 2ф с диазоэтаном в аналогичных условиях получен продукт 1,3-диполярного циклоприсоединения – N-(2-тиазолил)амид 3-(4-хлорбензоил)-5-метилпиразол-4-карбоновой кислоты (30).
Взаимодействие эквимолярных количеств гетериламида 2у с дифенилдиазометаном при кипячении реакционной смеси приводит к образованию продукта β-С-алкилирования исходного амида – соединению 31, что вероятно, можно объяснить [1,3]-сигматропной перегруппировкой первоначально образующихся продуктов С2-О-дифенилметилирования исходного амида в реакционных условиях (110оС), вследствие большей термодинамической устойчивости соединения 31:

27: R1=H, Ar=C6H5 (а), 4-ClC6H4 (б); R1=NO2, Ar=C6H5 (в)
Реакция бензоилметиленгидразидов АрПК 11 с диазометаном региоселективна и приводит к α-О-метильным производным 32а, б. Их спектральные характеристики хорошо согласуются с данными аналогичных производных N-гетериламидов 24, 29.
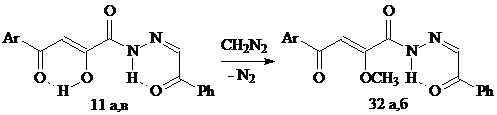
32: Ar=4-СH3C6H4 (а), Ar=4-СlC6H4 (б)
В продолжение исследования реакции Штаудингера, позволяющей вводить в карбонильный субстрат потенциально биологически активные азофрагменты, нами изучены реакции АрПК 19, метилового эфира АрПК 3 и анилидов АрПК 33 с трифенилфосфазинами различного строения. Установлено, что вне зависимости от структуры карбонильного соединения, образуются продукты по α-карбонильной группе его дикетоформы - соответственно замещенные 2-метиленгидразино-4-арил-4-оксо-2-бутеновые кислоты (34а-з), анилиды 34о-с и метиловый эфир 34т (метод А). Производные 34и-н получены методом Б – реакцией кислот 19 с моногидразоном бензила. Полученные спектральные характеристики соединений 34 свидетельствуют о существовании их в кристаллическом состоянии и в растворе ДМСО-d6 в енгидразинной форме с ВВС Н-хелатного типа с локализацией атома водорода при атоме азота, т. е. в форме Z-изомера.
3: Х=СН3О, R1=Br (в). 33: Х=NHC6H5, R1=H (а), CH3 (б), Cl (в)
34: Х=ОН, R2=R3=C6H5; R2=H, R3=C6H5СО; R2=C6H5, R3=C6H5СО; Х=NHC6H5, R2=R3=H; R2=Н, R3=C6H5СО; Х=CH3О, R2=R3= C6H5
При проведении реакции кислоты 19а, эфира 3а и анилида 33а с трифенилфосфазином, полученным на основе этоксикарбонилдиазометана, в аналогичных условиях из реакционной смеси удается выделить лишь ТФО и известные производные 3-фенил-5-пиразолкарбоновой кислоты (35а-в).
Нами установлено, что N-гетериламиды АрПК 2 взаимодействуют с гидразонами бензофенона, фенил(4-бромфенил)кетона и 9-флуоренона с образованием соответственно N-гетериламидов 4-арил-2-диарилметиленгидразино - и 4-арил-2-флуоренилиденгидразино-4-оксо-2-бутеновых кислот (36,37):
R=Н, Br. 36: Ht=2-С5Н4N, С6Н6N, 3-С5Н4N, С3Н2NS, С2Н1N2S, С3Н3N2S, С4Н5N2S, С11Н11N2O, С7Н5N2.
37: Ht=2-С5Н4N, 3-С5Н4N, С3Н2NS, С2Н1N2S, С3Н3N2S, С4Н5N2S, С11Н11N2O.
Изучение спектров ЯМР1Н соединений 36 и 37, снятых в ДМСО-d6 и CDCl3, показало наличие Z-кетоенгидразинной (Z-KEГ), Е-кетоенгидразинной (Е-КЕГ) и b-кетогидразонной (b-КГ) форм в растворе этих соединений. Нами установлено, что состав таутомерных форм в растворе определяется, в первую очередь, природой растворителя, а также строением гетероциклического и гидразинного фрагментов. Так, в растворе ДМСО-d6 соединений 36,37 форма Z-КЕГ наблюдается у всех изученных веществ, составляет 32-100% для соединений 36 и 15-80% для соединений 37.
Содержание минорной формы Е-КЕГ в растворе ДМСО-d6 составляет 25-48% для производных 36 и 15-28% для производных 37. Она характеризуется сдвигом сигнала протона NH-группы, вовлеченного во ВВС, в более слабое поле до 8.45-11.22 м. д., а также небольшим сдвигом сигналов протонов NH-N= и –СН= групп в сильное поле, где они наблюдаются, соответственно, при 9.55-13.35 и 6.12-6.67 м. д..

Для формы β-КГ характерен синглет двух протонов метиленовой группы при 4.42-4.62 м. д. и отсутствие сигнала протона –NH-N= группы. При этом её содержание для производных 36 составляет 15-50%, а для производных 37 – 50-100%. В целом, форма Е-КЕГ присутствует в таутомерном равновесии трех форм только в растворе ДМСО-d6, а в растворе CDCl3 – только в равновесии с Z-КЕГ со значительным преобладанием последней. Введение электроноакцепторного заместителя в ароильный фрагмент соединений 36,37 приводит к сдвигу таутомерного равновесия в сторону большего содержания формы Z-КЕГ только в растворах ДМСО-d6.
Нами установлено, что при взаимодействии N-гетериламидов АрПК 2 с этиловым эфиром гидразинэтановой кислоты направление реакции не меняется, но осуществляется дальнейшее замыкание в цикл с образованием N-гетериламидов 5-арил-1-этоксикарбонилметил-1Н-пиразол-3-карбоновых кислот (38).
При изучении спектров ЯМР1Н производных N-[2-(5-R-1,3,4-тиадиазолил)]амидов 38б-з в ДМСО-d6 и СDCl3, нами обнаружена прототропная амино-иминная таутомерия - наличие соответствующих таутомерных форм И и К. Таутомерное равновесие этих форм зависит от природы растворителя, а также от характера заместителя в Ar и Ht. Так, при снятии спектров ЯМР1Н соединений 38г, д в разных растворителях установлено, что при введении заместителя в арильный фрагмент наблюдаются обе формы с преобладанием формы К в ДМСО-d6 и формы И в СDCl3, в то время как отсутствие заместителя способствует их 100% содержанию в соответствующем растворителе. При анализе спектров амидов 38в-з, снятых в ДМСО-d6, выявлено, что соединения 38г, е существуют в форме К (100%), в то время как их замещенные аналоги 38в, д,ж, з существуют в виде равновесных форм К:И (43-62% : 38-57%), количественное содержание которых определяется, в свою очередь, строением гетериламидного фрагмента.
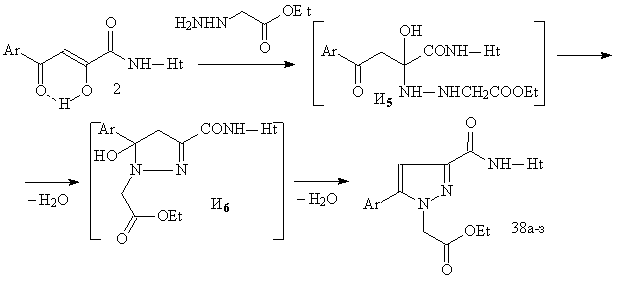

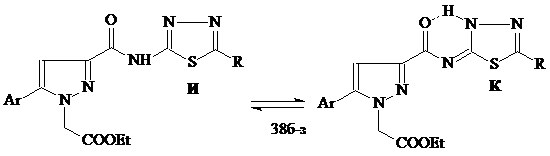
38: Ht=3-С5Н4N, С2Н1N2S, С3Н3N2S, С4Н5N2S
Механизм образования соединений 38, по-видимому, включает первоначальную атаку первичной аминогруппы замещенного гидразина на карбонильную группу С2=О субстрата. Образующийся при этом интермедиат И5 элиминирует воду и циклизуется в производное пиразола И6 за счет внутримолекулярной атаки вторичной аминогруппы гидразина на карбонильную группу С4=О субстрата, а последующее отщепление молекулы воды приводит к соответствующим соединениям 38.
Реакция N-гетериламидов АрПК 2 с катионами переходных металлов ранее не исследована. Эти соединения могут быть использованы в качестве лигандов, благодаря наличию нескольких потенциально активных комплексообразующих групп β-дикарбонильного, амидного и гетероциклического фрагментов. Нами установлено, что амиды 2 взаимодействуют с дихлоридами меди, цинка, кадмия в соотношении 2:1, в мягких условиях в среде спирта этилового с образованием бис[3-арил-1-(N-гетерил)карбоксамидо-1,3-пропандионато] меди (39а-о), цинка (40а-л), кадмия (41а-л):
39: Me=Сu, Ht=2-С5Н4N, С5Н3BrN, 3-С5Н4N, С3Н2NS, С2Н1N2S, С3Н3N2S, С4Н5N2S, С11Н11N2О 40: Ме=Zn, Ht=2-С5Н4N, С5Н3BrN, 3-С5Н4N, С3Н2NS, С2Н1N2S, С3Н3N2S, С7Н5N. 41: Ме=Сd, Ht=2-С5Н4N, 3-С5Н4N, С3Н2NS, С3Н3N2S, С4Н5N2S, С7Н5N2
Полученные результаты атомно-абсорбционного анализа комплексных соединений свидетельствуют о том, что металл в составе комплекса связан с двумя лигандами, а отрицательная проба Бельштейна показывает также отсутствие атомов хлора. По-видимому, хлор элиминируется из зоны реакции в составе молекулы HСl.
На наш взгляд, для соединений 39-41 наиболее вероятными структурами продуктов реакции являются Л, М, Н. Кроме того, не исключаются структуры с возможными координационными связями с гетероатомами в цикле.
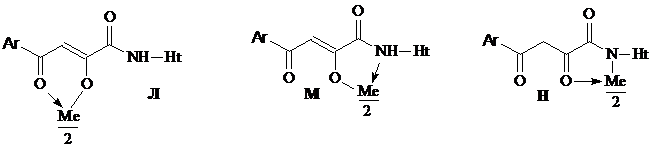
В пользу структуры Л свидетельствует наличие полос поглощения NH-групп в ИК-спектрах соединений 39-41, а также наличие сигнала протонов NH-групп в спектрах ЯМР1Н. Кроме того, в ИК-спектрах полоса поглощения С4=О смещена в область низших частот на 10-15 см-1, по сравнению с исходными амидами, что свидетельствует об её участии в образовании более прочной координационной связи.

Для подтверждения структуры хелатов нами выполнены квантово-химические расчеты неэмпирическим методом в базисе G6 31* в приближении АМ1 у соединения 40а для четырех комплексов цинка, ковалентно связанного с двумя лигандами через атомы кислорода О2 енолизованных карбонильных групп и имеющего соответствующие координационные связи (структуры О, П, Р, С). Согласно выполненным расчетам и вычисленным значениям теплот образования комплексов (ΔНf), наиболее стабильной является форма комплекса П. Таким образом, N-гетериламиды 2 в реакции комплексообразования координируются металлами как бидентатные О-О лиганды и образуют с ними продукты со структурой типа П с делокализованными кратными связями в шестичленных хелатных циклах.
Нами установлено, что направление реакции комплексообразования не меняется при использовании в качестве исходных соединений N2-замещенных метиленгидразидов 11а, в и дихлоридов меди, цинка, кадмия при соотношении реагентов 2:1. Взаимодействие протекает в аналогичных вышеописанным условиях с образованием бис {3-арил-1-[N2-(бензоилметилен)карбоксгидразидо]-1,3-пропандионато}меди, цинка, кадмия (42а-д):
42: Me=Cu, R=CH3 (а), Сl (б); Me=Zn, R=Cl (в); Me=Сd, R=CH3 (г), Сl (д)
Спектральные характеристики соединений 42 согласуются с данными, полученными для хелатов 39-41.
3.2. Синтезы на основе производных 2-(2-гидроксифенил)-2-оксоэтановой кислоты
В продолжение изучения химического поведения гетериламинов в реакциях с α-оксокислотами и с целью синтеза БАВ нами исследовано взаимодействие 2-(2-гидроксифенил)-2-оксоэтановой кислоты (4) с 2-, 4-аминопиридинами, 2-аминотиазолом и 2-амино-(5-R-1,3,4-тиадиазолом). Реакция протекает в условиях, аналогичных получению бутеноатов 20, с образованием соответствующих 2-(2-гидроксифенил)-2-оксоэтаноатов гетериламмония (43а-д):

43: Ht=2-С5Н4N (а),4-С5Н4N (б),С3Н2NS (в),С2Н1N2S (г),С3Н3N2S (д)
Реакция кислоты 4 с гидразонами бензофенонов и 9-флуоренона в среде безводного толуола и соотношении реагентов 1:1 или 2:1 приводит к 2-(2-гидроксифенил)-2-[(2-гидроксифенил)карбоксиметилен] гидразоноэтановой кислоте (46) (метод А) и азинам 47 а-в.

47: R1=C6H5, R2=C6H5(а), 4-BrC6H4(б); СR1R2=C13H8(в), C9H7NO (г)
Предполагаемый механизм реакции включает, по-видимому, промежуточное образование азинов (интермедиат И7), которые в процессе реакции взаимодействуют со второй молекулой кислоты 4, давая азин 46.
Взаимодействие кислоты 4 с соответствующими фосфазинами также завершается получением азина 46, симметричных азинов 47а-г и ТФО (метод Б). Соединение 46 при нагревании в уксусном ангидриде циклизуется с высоким выходом в 3-(2,3-дигидро-2-оксо-3-бензо[b]фуранилиден)гидразоно-2,3-дигидро-2-оксобензо[b]-фуран (48).
Нами установлено, что взаимодействие гидразонов бензофенона или 9-флуо-ренона с 2-тиазолиламидом 6г протекает по кетонной карбонильной группе последнего с образованием соответственно N-(2-тиазолил)амидов 2-(2-гидроксифенил)-2-дифенилметилен - и 2-флуоренилиденгидразоноэтановой кислоты (49а, б): 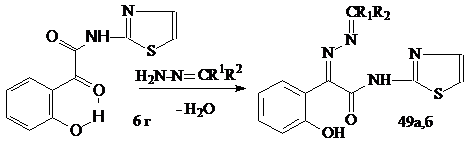
R1=R2=C6H5; CR1R2=C13H8
С целью получения водорастворимых БАВ нами изучена реакция N-гетериламидов о-ГФГК 6а, б,д, ж с натрия карбонатом при эквимолярном соотношении реагентов, в результате чего выделены 2-[2-(N-гетериламино)-2-оксоацетил]феноляты натрия (50а-г). При взаимодействии амидов 6г, е-з с дихлоридами цинка и кадмия при соотношении 2:1 в среде спирта этилового, образуются бис{2-[2-(N-гетериламино)-2-оксоацетил]феноляты} цинка и кадмия (51а-д):
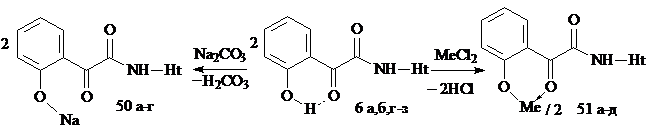
50: Ht=С5Н3BrN, 3-С5Н4N, С2Н1N2S, С4Н5N2S
51: Ме=Zn, Ht=С4Н5N2S; Ме=Сd, Ht=С3Н2NS, С3Н3N2S, С4Н5N2S, С7Н5N2
В спектрах ЯМР1Н полученных соединений отсутствует сигнал протона ОН-группы, что свидетельствует о депротонизации лиганда. Кроме того, в ИК-спектрах соединений 51а-д наблюдается сдвиг полос поглощения группы С2=О и С=С, С=N связей в область низших частот, по сравнению с таковыми исходных амидов 6, вследствие образования более прочной координационной связи, что также согласуется с данными для комплексных соединений 39-41.
3.3. Синтезы на основе N-замещенных 2-метиленгидразоно-2,3-дигидро-3-бензо[b]фуранонов
С целью поиска альтернативных путей синтеза производных N2-замещенных гидразидов α-оксокарбоновых кислот и введения в структуру исходных соединений биологически активных фрагментов нами изучены превращения бензо[b]фуранонов 17 с ароилкетеном, ариламинами, о-фенилендиамином (о-ФДА).
Установлено, что при взаимодействии эквимолярных количеств 3-бензо[b]фуранона 17в с п-метоксибензоилкетеном, генерируемым при термолизе 2,2-диметил-6-(4-метоксифенил)-1,3-диоксин-4-она, образуется 3'-бензоил-метиленамино-6'-(4-метоксифенил)-спиро[бензо[b]фуран-2(3Н),2'-[2H][1,3]-оксазин] -3,4'-(3'Н)-дион (52):
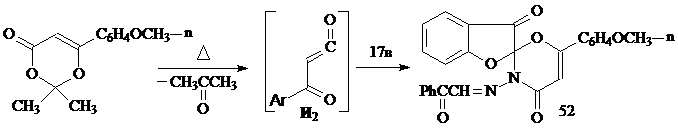
Спектральные характеристики спиросоединения 52 доказывают его структуру и свидетельствуют о протекании [4π+2π] циклоприсоединения ароилкетена по С=N связи исходного фуранона 17в, выступающего в роли диенофила. Продуктов циклоприсоединения по карбонильной группе и СН=N связи боковой цепи не выделено, что свидетельствует о региоселективности протекающего процесса.
Реакция бензо[b]фуранона 17в с анилином в среде четыреххлористого углерода при температуре 20-25°С приводит к образованию 2-[(2-оксо-2-фенил-1-фениламино)этил]гидразоно-2,3-дигидро-3-бензо[b]фуранона (53). Однако, при взаимодействии соединения 17в с п-анизидином в аналогичных условиях, вместо ожидаемого продукта, нами был выделен 2-гидразоно-2,3-дигидро-3-бензо[b]фуранон (54) (метод А). Очевидно, при взаимодействии бензофуранона 17в и амина с более высокой нуклеофильностью, чем образующийся гидразон 54, реакция не останавливается на стадии присоединения амина по активированной СН=N связи исходного соединения, а происходит вытеснение гидразона 54 более нуклеофильным реагентом с образованием продуктов переиминирования. Соединение 54 было также получено при взаимодействии фуранона 17в с о-ФДА (метод Б):
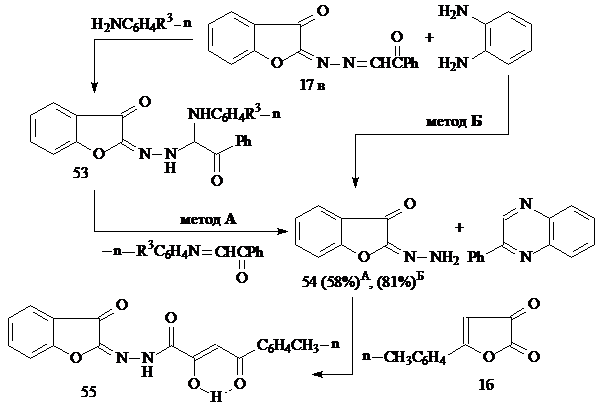
Необходимо отметить, что неустойчивость бензофуранового цикла препятствует получению его 2-гидразонопроизводного прямым взаимодействием с гидразинами, поэтому взаимодействие фуранонов 17 с о-ФДА или n-анизидином является удобным в препаративном отношении методом синтеза незамещенного гидразона 54.
Для подтверждения структуры соединения 54 проведена его реакция с фурандионом 1б с образованием N2-(3-оксобензо[b]фуран-2-илиден)гидразида 2-гидрокси-4-(4-метилфенил)-4-оксо-2-бутеновой кислоты (55). Таким образом, путем ароилацетилирования гидразона 54 можно получать различные представители нового типа N2-замещенных метиленгидразидов АрПК, содержащие сохраненный биологически активный бензо[b]фурановый цикл.
4. Биологическая активность синтезированных соединений
Производные α-оксокарбоновых кислот и продукты их химических превращений были подвергнуты биологическим испытаниям с целью поиска БАВ с противовоспалительной, анальгетической, жаропонижающей, антигипоксической, гипогликемической, антикоагулянтной, гемостатической и противомикробной активностью. Также изучена острая токсичность отдельных представителей в синтезированных рядах соединений. Испытания проводились в ГОУ ВПО ПГФА Росздрава на кафедрах: фармакологии, клинической фармакологии под руководством зав. каф., проф. и зав. каф., проф. , микробиологии под руководством зав. каф., доц. и зав. каф., проф. , физиологии с основами анатомии под руководством зав. каф., проф. , а также в лаборатории Пермского НПО «Биомед» и в лаборатории БАВ ЕНИ ПерГУ доц. Махмудовым выражает глубокую благодарность за проведенные исследования.
Результаты биологических испытаний обработаны статистически с определением критерия Стьюдента с помощью статистических программ Windows XP (Excel).
Исследование острой токсичности показало, что изученные соединения в рядах 2, 11-14, 17, 20, 27, 36-43, 51, 53 являются малотоксичными веществами по классификации , а производные 6ж, 16а, ф, 18в, 21б, 34е, ж,к, л,с относятся к практически нетоксичным соединениям и имеют значительные преимущества перед известными препаратами сравнения. Обнаружено, что соединения 9а и 20 е являются умеренно токсичными.
4.1. Противовоспалительная активность
Противовоспалительную активность (ПВА) изучали на модели острого воспалительного отека, вызванного субплантарным введением 0,1 мл 1% водного раствора каррагенина белым беспородным крысам обоего пола. О выраженности воспалительной реакции в динамике судили по изменению объема стопы, регистрируемой онкометрически. Исследуемые вещества в дозе 50 мг/кг вводили внутрибрюшинно (в/б) или перорально (п/о) в виде взвеси в 2% крахмальном растворе. Препаратом сравнения служил диклофенак в дозе 10 мг/кг, вводимый аналогично.
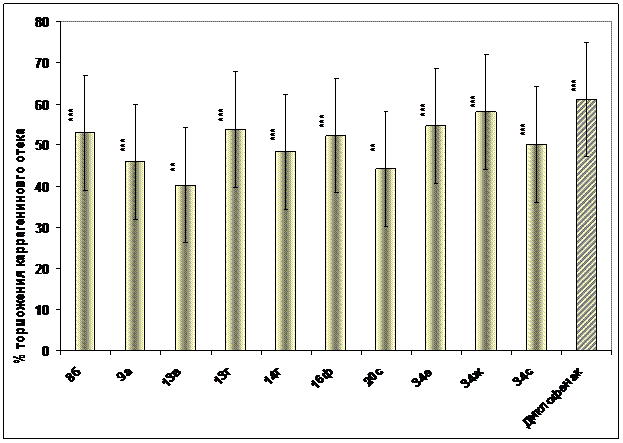
Примечание: по сравнению с контролем **= р<0,01 *** р<0,001
Рис. 1. Сравнительная характеристика наиболее активных соединений и диклофенака, проявивших противовоспалительную активность при внутрибрюшинном введении.
Проведенные исследования показали, что из 60 соединений, вводимых в/б, ПВА оказали 26 веществ, о чем свидетельствует достоверное торможение воспалительного отека на пике воспаления. Среди них 10 соединений тормозили воспалительную реакцию в такой же мере, что и препарат сравнения, однако его значение не превысили. С учетом данных по токсичности, следует выделить 4 активных соединения (пиридазин 16ф, 2-гидразинопроизводные АрПК 34 е, ж,с) (рис. 1).
Изучение ПВА у соединений, вводимых п/о, показало, что более 50 веществ проявили действие с различной степенью выраженности, из них 24 соединения тормозили воспалительный отек у животных во все сроки наблюдения. Сравнительная характеристика 5 наиболее активных изученных веществ (гетериламида 6ж, гидразида 11а, фуранона 12г, 2-гидразинопроизводного 34л и хелата 51б) представлена на рис. 2. Все они значительно превосходили по действию диклофенак на 1 ч. развития воспаления, а на 3 и 5 ч. опыта они действовали в такой же степени, что и препарат сравнения. Однако, с учетом данных по токсичности, более выигрышную позицию здесь занимают соединения 6ж и 34л.
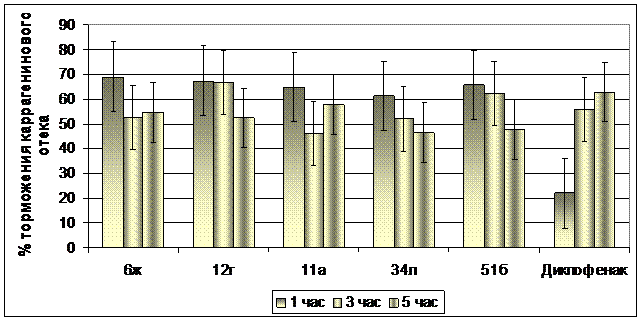
Рис. 2. Сравнительная характеристика наиболее активных соединений и диклофенака, проявивших противовоспалительную активность при пероральном введении.
На рис. 3 дана сравнительная оценка 19 изученных соединений, проявивших ПВА при п/о введении, но уступающих по действию вышеуказанным соединениям.
В целом, полученные данные позволили определить некоторые закономерности структуры веществ с действием в отдельных рядах. Так, в ряду N-[2-(5-R-1,3,4-тиадиазолил)]амидов 2 при увеличении алкильной цепи в 5 положении гетероцикла значительно уменьшается ПВА, вплоть до ее потери. Существенный вклад в изучаемое действие у гетериламидов 2 вносят электронодонорные заместители в ароильном фрагменте. N-Гетериламиды о-ГФГК 6, по сравнению с N-гетериламидами АрПК 2, проявляют более выраженную активность, и в первый 1 ч. воспаления все исследуемые вещества превышают активность диклофенака. У них отмечается прямая зависимость влияния заместителя в 5 положении 1,3,4-тиадиазолила на ПВА, которая увеличивается при увеличении алкильной цепи у соединений 6д-ж, в отличие от аналогичных производных 2ш-ав. Лидирующую позицию занимает гетериламид 6ж, не уступающий на пике воспаления диклофенаку, но в 20 раз менее токсичный. Таким образом, наряду с гетерилом, у производных 6 фармакофором – носителем ПВА является 2-(2-гидроксифенил)-2-оксоэтановый фрагмент.
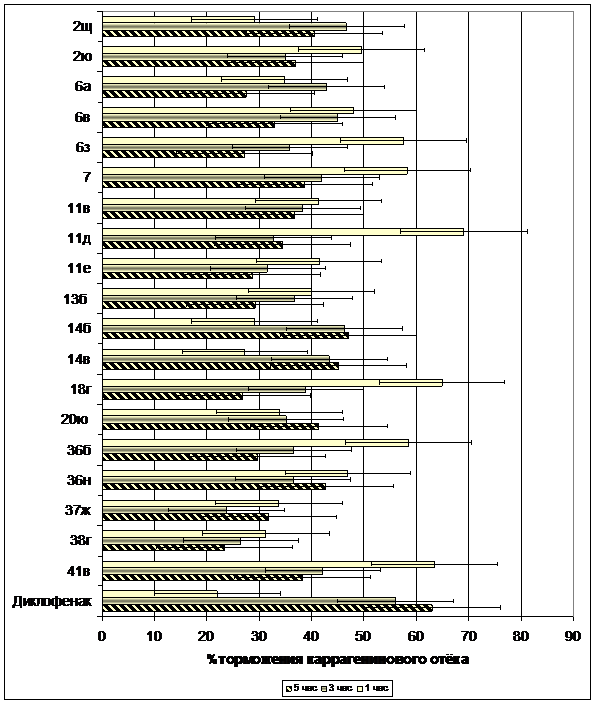
Рис. 3. Сравнительная характеристика противоспалительной активности некоторых изученных соединений и диклофенака при пероральном введении.
В ряду N2-замещенных гидразидов АрПК 11 высокую активность проявили бензоилметиленгидразиды 11а, в и адамантаноилгидразид 11д. Введение гетероциклического заместителя в гидразидный фрагмент у соединений 11з-к не привело к увеличению ПВА. В целом, в ряду гидразидов 11, не зависимо от строения гидразидного фрагмента, установлен наибольший вклад в ПВА электронодонорных заместителей. В то же время, в рядах гидразонов 13 и пиридазинонов 14 выраженность действия ПВА возрастает при введении электроноакцепторных заместителей.
Установлено, что пентантрионы 15 ПВА не обладают, а их модификация в пиридазины 16 приводит к различной активности. Наиболее существенное значение для ПВА оказывают электронодонорные заместители в арильном кольце в положении 6 гетероцикла. Выявлено, что кислотный гидролиз бензофуранона 17д до гидразида 18в приводит к увеличению его ПВА, а введение в молекулу гидразида 18г фуранового фрагмента также способствует флоголитическому действию. Невысокую активность показали бутеноаты 20. Однако, ввиду их низкой токсичности и водорастворимости, поиск БАВ в этом ряду является целесообразным.
В ряду замещенных 2-метиленгидразинопроизводных АрПК 34 обнаружены высокоактивные соединения. Установлено, что наибольшее действие проявляют производные АрПК, а замена кислотного фрагмента на ариламидную или сложноэфирную группы снижают его. В этом ряду наибольший вклад в ПВА вносят 1,2-дифенил-2-оксоэтилиденгидразиновый фрагмент и электронодонорный заместитель в арильном радикале. Введение в положение 2 исходных N-гетериламидов АрПК дифенилметиленгидразинового фрагмента приводит, как правило, к увеличению ПВА соединений 36. Меньшее влияние на этот вид активности оказывает введение флуоренилиденгидразинового заместителя у соединений 37. У соединений 38 отмечено повышение ПВА с увеличением алкильной цепи в положении 5 фрагмента 1,3,4-тиадиазола.
При переходе от N-гетериламидов 2 и 6 к их комплексным соединениям 39-41, 51 происходит усиление активности, при этом, в большей степени, влияет характер металла и строение гетероцикла.
Таким образом, обобщая результаты проведенных испытаний на противовоспалительное действие и с учетом данных по токсичности, наиболее перспективными для дальнейших исследований являются ряды соединений 6, 11, 12, 16, 34.
4.2. Анальгетическая активность
Анальгетическую активность (АА) изучали на белых беспородных мышах на моделях термического («горячая пластинка») и химического раздражения («уксусные корчи»). Исследуемые вещества в дозе 50 мг/кг вводили в/б или п/о в виде взвеси в 2% крахмальном растворе. Препараты сравнения – метамизол натрия (50 мг/кг) и диклофенак (10 мг/кг). Для анализа связи АА со строением скринингу были подвергнуты около 100 соединений.
Изучение АА у 35 соединений из трех рядов при в/б введении показало, что 15 веществ обладают анальгетическим действием, достоверно увеличивая порог болевой чувствительности у животных при термическом воздействии (рис. 4). Выявлено, что среди них пиридазины 16д, с и бутеноаты 20ж, ч не уступают по активности метамизолу натрия, но действуют слабее диклофенака.
При изучении АА некоторых производных α- оксокарбоновых кислот при п/о введении оказалось, что более 30 соединений достоверно проявили обезболивающее действие на модели термического раздражения (рис.5,6). Анализ степени выраженности эффекта показал, что соединения 11б, д,ж; 12а, в,г; 14б, г; 18г, 20я, 34б, г,е, ж,т; 36б, е,о; 37г, 39л, 41в проявили такой же обезболивающий эффект, что и метамизол натрия, но вместе с тем, они уступали диклофенаку. Производное 27а превышает действие метамизола натрия, но также уступает диклофенаку. Соединения 6ж, 11а, 18в, 27б, 36н, 40в проявили такое же действие, что и диклофенак. Производные 34к и 34л по АА превысили действие диклофенака, при этом лидирующую позицию заняло соединение 34л (рис.5).
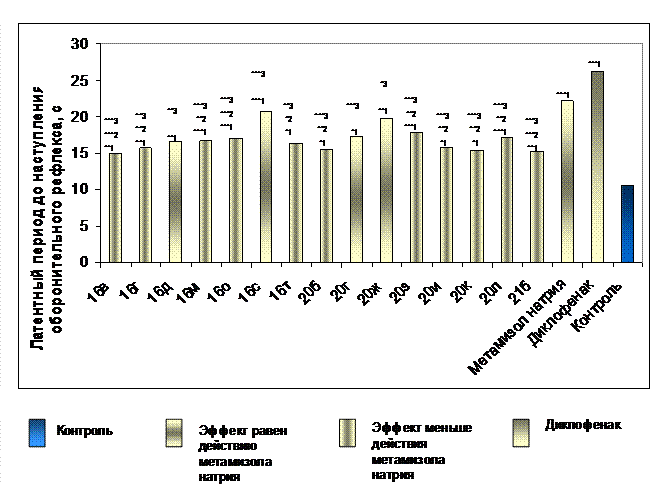
Примечание: * = p < 0,05, ** = p < 0,01, *** = p < 0,001;1 –по сравнению с контролем;
2- по сравнению с метамизолом натрия; 3 – по сравнению с диклофенаком
Рис. 4. Сравнительная характеристика анальгетической активности некоторых изученных соединений по методике «горячая пластинка» при внутрибрюшинном введении.
При изучении связи действия со строением в ряду амидов 2 установлено, что, как и в случае с ПВА, у N-[2-(5-R-1,3,4-тиадиазолил)] амидов 2 АА уменьшается с увеличением алкильной цепи в 5 положении гетероцикла. Среди N-гетериламидов о-ГФГК 6 наибольшей активностью также обладает соединение 6ж. В ряду гидразидов АрПК 11 наиболее активны, как и при изучении ПВА, бензоилметиленгидразид 11а и адамантаноилгидразид 11д (рис. 5, 6). В ряду фуранонов 12 лидирует соединение 12г, содержащее электроноакцепторный заместитель. В ряду пиридазинонов 14 введение электронодонорных заместителей незначительно увеличивают действие веществ. Среди пиридазинов 16 наибольшая АА отмечается у соединения 16с, содержащего в ароматическом кольце в положении 6 гетероцикла атом брома, а также у 16д, не имеющего заместителя. В ряду бутеноатов 20 наибольшую активность на уровне митамизола натрия проявили соединения с 3-, 4-пиридильным и 5-меркапто-1,3,4-тиадиазолильным заместителем.
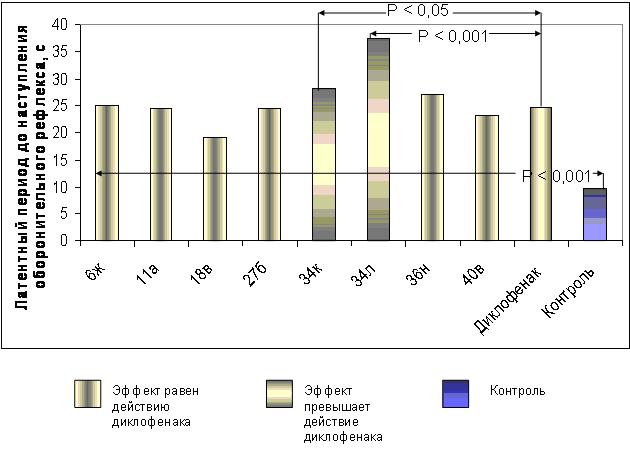
Рис. 5. Сравнительная характеристика анальгетической активности некоторых изученных соединений и диклофенака по методике «горячая пластинка» при пероральном введении.
Выявлено, что имидазо[2,1-b]тиазолы 27а, б проявляют выраженную АА, однако более активно производное 27б с электроноакцепторным заместителем. В ряду производных АрПК 34 соединение 34л значительно активнее диклофенака, но при этом оно в 20 раз менее токсично, чем препарат сравнения и также обладает высокой ПВА. Введение во второе положение исходных амидов 2 дифенилметиленгидразинового фрагмента, а также наличие электронодонорных заместителей в арильном радикале приводит к увеличению АА. Среди комплексных соединений 39-41 наиболее активен цинковый хелат 40в (рис. 5, 6).
Исследование АА на модели «уксусные корчи» показало, что из 7 изученных веществ производные 9а, 13в, 14а и 14г тормозили их развитие на уровне метамизола натрия, о чем свидетельствуют достоверные отличия в количестве корчей опытных и контрольных мышей. Установлено, что введение электронодонорных заместителей в структуру производных 13, 14 увеличивает их активность.
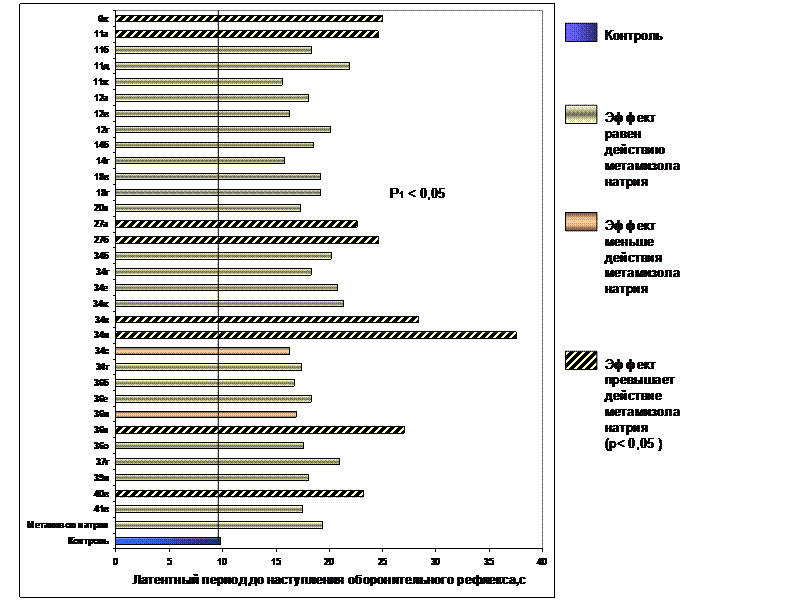 Примечание: 1 – по сравнению с контролем
Примечание: 1 – по сравнению с контролем
Рис. 6. Сравнительная характеристика анальгетической активности некоторых изученных соединений и метамизола натрия по методике «горячая пластинка» при пероральном введении.
Таким образом, поиск БАВ с анальгетическим действием целесообразно продолжить в рядах соединений 6, 11, 18, 27, 34, 36, 40, а соединения 6ж и 34л требуют дальнейшего изучения, поскольку они обладают также и высокой ПВА.
Жаропонижающая активность
Жаропонижающее действие было изучено у соединений 6ж, 34к, л, показавших высокую ПВА и АА, а также бутеноатов 20ю, аг. Лихорадочную реакцию у белых беспородных крыс вызывали внутривенным введением пирогенала. Изменение температуры тела животных регистрировали ректально. Активность веществ оценивали по уменьшению гипотермии через 1 и 2 ч. после введения пирогенала. Изучаемые соединения в дозе 50 мг/кг вводили п/о в виде взвеси в 2% крахмальном растворе. Препарат сравнения – диклофенак в дозе 10 мг/кг.
Выявлено, что производные 20ю и 34к не проявили достоверного эффекта в исследуемой дозе. Соединения 6ж, 20аг и 34л во все сроки наблюдения оказали жаропонижающую активность, при этом гетериламид 6ж тормозил лихорадочную реакцию у животных на уровне диклофенака.
В целом, проведенные исследования показали, что соединения 6ж и 34л по выраженности и направленности эффектов относятся к потенциальным НПВС, при этом они превосходят препараты сравнения (табл. 1).
Таблица 1
Сравнительная характеристика наиболее перспективных соединений 6ж и 34л
Соеди-нение | ЛД50, в/б | Доза от ЛД50 | Противово-спалительная активность | Анальгетическая активность | Жаропонижающая активность | |
1ч | 2ч | |||||
6ж | 1500 | 0,03 | 52,4±3,8***1 | 25,0±1,7***1*2 | 1,7***1 | 1,7***1 |
34л | 1500 | 0,03 | 52,0±2,5***1 **2 | 37,5±1,4***1 ***2***3 | 0,7***1 | 0,9***1 |
дикло-фенак | 74 | 0,14 | 56,0±7,3***1 | 24,7±0,4***1 | 1,7***1 | 2,0***1 |
мета- мизол натрия | 350 | 0,14 | 19,4±0,8***1 |
Примечание: = p < 0,05, ** = p< 0,01, *** = p < 0,001

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |