1 - ознакомительный (узнавание ранее изученных объектов, свойств);
2 - репродуктивный (выполнение деятельности по образцу, инструкции или под руководством);
3 – продуктивный (планирование и самостоятельное выполнение деятельности, решение проблемных задач).
2.3. условия реализации УЧЕБНОЙ дисциплины
2.3.1. Требования к минимальному материально-техническому обеспечению
Реализация учебной дисциплины требует наличия учебного кабинета химических дисциплин; лаборатории аналитической химии.
Оборудование учебного кабинета: Периодическая таблица , справочник физико-химических величин
Технические средства обучения: мультимедиа-проектор, ноутбук, колонки, набор цифровых образовательных ресурсов по дисциплине (презентации к лекциям, видеоопыты, анимационные схемы и модели химических процессов)
Оборудование лаборатории и рабочих мест лаборатории:
доска для сушки лабораторной посуды, вытяжной шкаф, столы лабораторные, штативы для пробирок, набор вспомогательных принадлежностей для хозяйственной деятельности и техники безопасности. Приборы: весы технические электронные, весы аналитические, плитка электрическая с закрытой спиралью, шкаф сушильный, муфельная печь, дистиллятор электрический, рефрактометр, лабораторное многоканальное устройство Unipractic с набором датчиков физико-химических величин с программным обеспечением, спектрофотометр. Комплекты: химической посуды и реактивов для выполнения лабораторных опытов.
2.3.2. Информационное обеспечение обучения
Перечень учебных изданий, Интернет-ресурсов, дополнительной литературы
Основные источники:
1. Цитович аналитической химии. М.; 2007.
2. Глубоков химия. М.; 2011.
3. , , и др.
Под ред. Аналитическая химия. М.; 2011.
4. Основы качественного и количественного анализа. М.; 2007.
Дополнительные источники:
1. Золотов химия. М.; 2009.
2. Саенко химия. Ростов-на-Дону; 2011.
Интернет-ресурсы:
1. Портал фундаментального химического образования
http://www. *****
2. Каталог образовательных Интернет-ресурсов http://www. *****
3. Мир химии http://chem. *****
4. Электронная библиотека по химии и технике http://*****
2.4. Контроль и оценка результатов освоения УЧЕБНОЙ Дисциплины
Контроль и оценка результатов освоения учебной дисциплины осуществляется преподавателем в процессе проведения практических занятий и лабораторных работ, тестирования, а также выполнения обучающимися индивидуальных заданий, проектов, исследований.
Результаты обучения (освоенные умения, усвоенные знания) | Формы и методы контроля и оценки результатов обучения |
умение: · описывать механизм химических реакций количественного и качественного анализа · обосновывать выбор методики анализа, реактивов и химической аппаратуры по конкретному заданию; · готовить растворы заданной концентрации; · проводить количественный и качественный анализ с соблюдением правил техники безопасности; · анализировать смеси катионов и анионов; · контролировать и оценивать протекание химических процессов; · проводить расчеты по химическим формулам и уравнениям реакций; · производить расчеты результатов анализа и оценивать достоверность результатов. знание: · агрегатнго состояния вещества; · аналитической классификации ионов; · аппаратуры и техники выполнения анализов; · значения химического анализа, методов качественного и количественного анализа химических соединений; · периодичности свойств элементов; · способов выражения концентрации веществ; · теоретических основ методов анализа; · теоретических основ химических и физико-химических процессов; · техники выполнения анализов; · типов ошибок в анализе; · устройства основного лабораторного оборудования и правила его эксплуатации. | Письменная проверочная работа Устный опрос Выполнение химического эксперимента на лабораторных работах Выполнение химического эксперимента на лабораторных работах Выполнение химического эксперимента на лабораторных работах Выполнение химического эксперимента на лабораторных работах Письменная самостоятельная работа Письменная самостоятельная работа Стандартизированный контроль Стандартизированный контроль Устный опрос Устный опрос Стандартизированный контроль Письменная проверочная работа Устный опрос Письменная проверочная работа Выполнение химического эксперимента на лабораторных работах Письменная проверочная работа Устный опрос |
3. Методические указания по изучению учебного материала
по теме Введение
При изучении данной темы необходимо обратить внимание на методы исследования химического состава веществ, их классификации по различным критериям. Требования, предъявляемые к анализу. Качественный и количественный анализ. Аналитические реакции и реактивы, требования к ним. Значение аналитического контроля технологических процессов. Правила техники безопасности работы в лаборатории.
Вопросы для самоконтроля
1. Понятие «аналитическая химия» и «химический анализ».
2. Задачи аналитической химии.
3. Значение аналитической химии.
Литература [3], с.68-73, 80-93,113-118
Методические указания по теме 1.1. Тема 1.1. классификация катионов и анионов
При изучении данной темы необходимо обратить внимание на сущность качественного химического анализа веществ, качественные реакции и требования к ним, методы выполнения качественных реакций. Следует уяснить, что является дробным, а что систематическим методом качественного анализа, виды классификации ионов, положительные стороны метода кислотно-основной классификации катионов и анионов на аналитические группы.
Вопросы для самоконтроля
1. Какие реакции называются аналитическими? Признаки аналитических реакций.
2. Что такое реактив?
3. В чем сущность анализа, проводимого сухим и мокрым путем?
4. Что такое систематический ход анализа?
5. В чем разница между макро-, микро - и полумикрометодами? Назовите преимущества полумикроанализа.
6. Что такое специфические реакции и реактивы? Приведите примеры специфических реакций. Объясните значение специфических реакций и реактивов в анализе смеси катионов.
7. Что такое чувствительная реакция? Приведите примеры.
8. Перечислите условия выполнения химических реакций.
9. Что такое аналитическая группа и групповой реактив?
10. Что положено в основу кислотно-основной классификации катионов на группы?
11. На какие аналитической группы делятся кантоны?
12. Что положено в основу классификации анионов на аналитические группы?
13. На какие аналитической группы делятся анионы?
Литература [ 3 ], с.22-38
Методические указания по теме 2.1. Техника подготовки к проведению анализа
При изучении данной темы необходимо обратить внимание на:
· технику безопасности при работе с химической посудой;
· технику работы с аналитическими весами;
· методы разделения веществ и их очистки от примесей.
Вопросы для самоконтроля
1. Как можно очистить от примесей неорганические вещества?
2. Как можно очистить от примесей органические вещества?
3. Какие моющие средства можно использовать для удаления неорганических загрязнений?
4. Какие моющие средства можно использовать для удаления неорганических загрязнений?
Литература [3], с. 215-227
Методические указания по теме 2.1. Гравиметрический (весовой) метод анализа
При изучении данной темы необходимо обратить внимание на:
· вычисление результатов по данным анализа;
· вычисление погрешности анализа.
Гравиметрические (весовые) определения разнообразны, но их можно разделить на три типа.
Первый тип – когда определяемая составная часть количественно выделяется из анализируемого вещества в свободном виде и взвешивается.
По этому типу делают анализы на определение зольности, CaO в кальците, МgО в магнезите, нерастворимых веществ, сухого остатка.
Формула расчета по этому типу имеет вид:
w (%)=m(остатка) · 100%/m(навески),
где m(остатка) – масса остатка после прокаливания до постоянной массы;
m(н) – масса навески, взятая для анализа.
Второй тип – когда определяемая составная часть полностью удаляется из анализируемого вещества, а остаток взвешивается.
Расчет массовой доли ведут по формуле:
w (%)=m(остатка) · 100 %/ m(навески),
где m(остатка) – разность между массой навески до и после высушивания;
m(н) – масса навески вещества, взятая для анализа.
По этому типу анализируют сырье на содержание гигроскопической воды (влажность), также определяют кристаллизационную воду в кристаллогидратах (типа BaCI2·2H2O), СО2 в кальците и магнезите.
Во влажном или воздушно-сухом состоянии в веществе присутствует внешняя или гигроскопическая вода. Сухое или (абсолютно сухое) вещество получают высушиванием при 105-110°С. При этом удаляется гигроскопическая и внешняя влага. Для вычисления содержания компонента в сухом веществе массу определяемого компонента относят к массе сухой пробы. Для расчета используют формулу:
w (в-ва) × 100 %
w (абсолютно сухого вещества) = ¾¾¾¾¾¾¾
100 % – w (H2O)
где: ω (в-ва) массовая доля вещества;
ω (Н2О) – массовая доля воды в определяемом веществе.
Третий тип – когда определяемую составную часть связывают в химическое соединение, в виде которого она будет выделена и взвешена. Образовавшийся при этом осадок в большинстве случаев прокаливают. При этом аморфные осадки изменяют свой химический состав, теряя воду, а кристаллические – нет. Вследствие этого различают две формы анализируемого вещества: осаждаемую и весовую. Например, при анализе сплава на содержание AI его осаждают в виде AI(OH)3.
AI3+ + 3OH - = ¯ AI(OH)3
при прокаливании AI(OH)3 разлагается
2AI(OH)3 ¾¾¾® AI2O3 + 3H2O
AI(OH)3 – осаждаемая форма;
AI2O3 – весовая форма.
Иногда химический состав осаждаемой и весовой форм одинаков. Например, при определении бария осаждаемая и весовая форма – BaSO4.
Расчет массовой доли ведут по формуле:
mосадка × 100 % × F
w (о. в.) = ¾¾¾¾¾¾¾¾
m (н)
где: m(O) - масса осадка, получаемого в результате прокаливания до
постоянной массы;
m(н) - масса навески анализируемого вещества, взятая для анализа;
F - фактор пересчета, равный отношению молярной массы экви-
валента определяемого вещества к молярной массе эквива-
лента весовой формы.
По этому типу, в основном, делают все анализы. Когда нужно определить составную часть смеси (сплава).
Кроме расчета массовой доли компонента часто приходится рассчитывать массу навески анализируемого вещества. Масса навески пробы для анализа должна быть такой, чтобы массу взвешиваемой (весовой, гравиметрической) формы осадка можно было бы определить на аналитических весах с погрешностью не превышающей допустимого значения.
Обычно по техническим условиям допустимая погрешность анализа составляет десятые доли процента. Для соблюдения такого требования масса весовой формы осадка должна быть не менее 100 мг. При очень большой массе осадка возрастает количество реактивов и объем растворов, что затрудняет работу. Поэтому массу весовой формы осадка ограничивают в пределах нескольких десятых долей грамма путем выбора соответствующей исходной навески анализируемого вещества.
При этом нужно учесть, что если не известна масса остатка для первого и второго типа весовых определений, то ее принимаем равной от 0,01– 0,1 г.
Для третьего типа весовых определений массу осадка принимаем (если она не известна) в зависимости от формы осадка:
для кристаллических 0,3 – 0,5 г.;
для аморфных 0,1 – 0,3 г.
Часто для анализа веществ по третьему типу весовых определений необходимо рассчитать объем растворителя (осадителя), необходимый для проведения анализа. Теоретической основой этих расчетов является закон эквивалентов: все вещества реагируют друг с другом нацело в количествах, пропорциональных их эквивалентам.
Причем, если растворитель (осадитель) вещество летучее, его берут в два-три раза больше рассчитанного, если нелетучее – в полтора раза больше рассчитанного.
Расчет начальной навески или объема осадителя (растворителя) носит приближенный характер и рассчитывается до второго знака.
Например: Навеска каменного угля массой 1,9982г. после удаления влаги стала весить 1,8612г. Определить массовую долю гигроскопической влаги в угле.
Дано: Решение:
 Это определение относится ко второму типу, поэтому применяем формулу:
Это определение относится ко второму типу, поэтому применяем формулу:
m(нав.) = 1,9982г 1.1 ω (Н2О) = 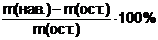
 m (ост.) = 1,8612г ω (Н2О) =
m (ост.) = 1,8612г ω (Н2О) = 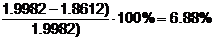
ω (Н2О) - ?
Ответ: ω (Н2О) = 6,88%
Вопросы для самоконтроля
1. Какие количественные определения можно проводить при помощи гравиметрии-ческого метода анализа?
2. Как рассчитывается навеска вещества, необходимая для анализа, например, золы?
3. Какой объём растворителя (осадителя) эквивалентный или избыточный используют при осаждении и почему?
4. Что такое весовая, осаждаемая форма вещества?
5. Каковы условия осаждения кристаллических осадков?
Литература [3], с.11-35
Методические указания по теме 2.3. Титриметрический анализ
При изучении данной темы необходимо обратить внимание на:
· сходство и различие между гравиметрическим и титриметрическим методами анализа;
· способы выражения концентраций растворов в титриметрии;
· расчеты, производимые в титириметричсеском анализе.
Для решения задач в титриметрическом методе следует повторить из курса “Химия” понятие эквивалента для всех классов неорганических соединений, т. к. основным законом в количественном методе анализа является закон эквивалентов. Кроме того, из этого же курса нужно повторить тему “Различные способы выражения концентрации растворов”.
Кроме рассмотренных ранее способов выражения концентрации растворов, в титриметрическом методе используется такое понятие как титр.
Титр раствора – масса вещества Х, содержащаяся в одном кубическом сантиметре раствора.
Т = ![]() (г/см3) (1)
(г/см3) (1)
где: m(Х) – масса вещества (Х), г;
V – объем раствора, см3;
Т – титр раствора, г ⁄см-3.
Титр рабочего вещества:
Т(р. в.) = (2)
где: С(р. в.) – молярная концентрация эквивалента рабочего вещества, (моль/ дм3);
М(f экв(р. в.) р. в.) – молярная масса эквивалента рабочего вещества, (г/моль).
Титр рабочего вещества по определяемому веществу равен:
Т( р. в./ о. в.) = (3)
где: С(р. в.) – молярная концентрация эквивалента рабочего вещества, (моль/дм3);
М(f экв(о. в.) о. в.) – молярная масса эквивалента определяемого вещества, (г/моль).
Если речь идет об одном веществе, то используют титр рабочего вещества, если одно вещество используют для определения второго, то для расчета пользуются титром по определяемому веществу. Титр расчитывается с точностью до седьмого знака ± 0,0000002.
Для приготовления раствора заданного титра (Т) в объеме (V) рассчитывается масса навески химически чистого растворенного вещества.
mнав. ═ Т × V (г) (4)
Если в условии задачи по результатам титрования даны объемы реагирующих веществ и молярная концентрация эквивалента одного из реагирующих веществ, тогда из отношения
С1• V1 = С2 • V2 (5)
можно определить молярную концентрацию эквивалента другого вещества.
C1 = 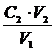
Приготовить раствор строго заданной концентрации не всегда удается, поэтому пользуются поправочными коэффициентом «К».
К = 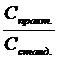 (6)
(6)
где: Спрак. – практически полученная молярная концентрация эквивалента рабочего вещества (моль / дм3);
Сстанд. – стандартная молярная концентрация эквивалента рабочего вещества, (моль ⁄ дм3)
С целью стандартизации расчетных формул в заводских химических лабораториях пользуются краткими величинами молярных концентраций эквивалента рабочих растворов. Чаще всего 0,1 моль / дм3; 0,01 моль / дм3; 0,5 моль /дм3; 0.05 моль/дм3; 0,2 моль /. Поправочный коэффициент величина всегда близкая к единице.
Заключительным моментом в проведении анализа является расчет массы определяемого вещества.
В основу расчета массы положена формула:
m (о. в.) = Т (р. в./о. в.) × V (р. р. ) (7)
Например: Для установления точной концентрации пипеткой отобрали 25,00 см3 раствора NaOH, на титрование которого затратили 23,61 см3 раствора соляной кислоты с титром 0,0040230 г/см3. Вычислить титр раствора щелочи и его титр по соляной кислоте.
Дано: Решение:
 |
V(NaOH) = 25,00 cм3 1.1 Определяем молярную концентрацию эквивалента вещества соляной
V(HCl) = 23,61 см3 кислоты:
 Т(HCl) = 0,0040230 г/см3 Т(HCl) =
Т(HCl) = 0,0040230 г/см3 Т(HCl) =![]()
Т(NaOH) − ? С(HCl)=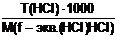 =
=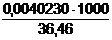 = 0,11034 моль/дм3
= 0,11034 моль/дм3
Т(NaOH/HCl) − ? 1.2 Определяем молярную концентрацию эквивалента вещества щелочи:
С(NaOH) = ![]() =
= ![]() = 0,1043 моль/см3
= 0,1043 моль/см3
1.3 Определяем титр раствора щелочи:
Т(NaOH) =![]() =
=![]() = 0,0041720 г/см3
= 0,0041720 г/см3
1.4 Определяем титр раствора щелочи по соляной кислоте:
Т(NaOH/HCl) =![]() =
=![]() = 0,0038028 г/см3
= 0,0038028 г/см3
Ответ: Т(NaOH) = 0,0041720 г/см3 , Т(NaOH/HCl) = 0,0038028 г/см3
Вопросы для самоконтроля
1. В чём сходство и различие между гравиметрическим и титриметрическим методами анализа?
2. Как определяется молярная масса эквивалента вещества в реакциях ионного обмена?
3. Что такое титрованный раствор?
4. Что такое поправочный коэффициент?
5. Что такое титр рабочего раствора? Что такое титр рабочего раствора по определяему веществу?
6. Что такое точка эквивалентности и как она устанавливается при титровании?
7. Как готовят титрованные растворы?
8. В чём заключается сущность титрований:
8.1. прямого;
8.2. по остатку;
8.3. методом замещения?
Литература [3], с.92-114.
Методические указания по теме 2.3.1. Метод кислотно-основного титрования
При изучении данной темы необходимо обратить внимание на определение молярной массы эквивалента.
При определении молярной массы эквивалента в методе нейтрализации возникают определенные трудности. Поэтому нужно обязательно записывать уравнения химических реакций.
Так в реакции: Na2CO3 + HCI ® NaHCO3 + NaCI
M(f экв.(Na2CO3)Na2CO3) = M(Nа2CO3) г/моль
а в реакции: Na2CO3 + 2HCI ®2NaCI + H2CO3
M(f экв.(Na2CO3)Na2CO3) = ½ M(Na2CO3) = 106/2 = 53 г ⁄ моль
Вопросы для самоконтроля
Какие исходные вещества применяются для определения концентрации соляной кислоты? Их преимущества и недостатки. Химизм процесса.
1. Расчёт рН в точке эквивалентности при определении концентрации соляной кислоты тетраборатом натрия.
2. Обоснуйте выбор индикатора при титровании раствора соляной кислоты раствором тетрабората натрия.
3. В каких случаях проводят анализ смеси NаОН и Nа2СО3?
4. Какое значение при титровании NаОН с примесью Nа2СО3 имеет температура?
Литература [3], с. 116-124
Методические указания по теме 2.3.2. Метод оксидиметрии
При изучении данной темы необходимо обратить внимание на определение молярной массы эквивалента окислителя и восстановителя.
При изучении окислительно-восстановительных реакций необходимо понять, что такое окисление и восстановление с электронной точки зрения.
Необходимо овладеть методикой составления окислительно-восстановительных реакций.
Подбирая коэффициенты для окислителя и восстановителя, а следовательно и для продуктов реакций, руководствуются правилом электронного баланса, согласно которого число электронов, отданных восстановителем, должно равняться числу электронов, принятых окислителем.
Например:
2FeCI2 + CI2 ® 2FeCI3
 Fe+2 –1e ® Fe+3 2
Fe+2 –1e ® Fe+3 2
CI20 + 2e ® 2CI - 1
В этой реакции (железо +2) отдает один электрон (восстановитель), а хлор принимает один электрон (окислитель).
При составлении окислительно – восстановительных реакций обратите внимание на зависимость процессов от характера среды.
Например: а) в кислой среде:
5Na2SO3 + 2KMnO4 + 3H2SO4 = 5Na2SO4 + K2SO4 + 2MnSO4 + 3H2O
 SO32-+ H2O – 2e ® SO42-+ 2H+ 5
SO32-+ H2O – 2e ® SO42-+ 2H+ 5
MnO4– + 8H++ 5e ® Mn2+ + 4H2O 2
M(f экв(KMnO4) KMnO4) = 1/5 M(KMnO4)
б) в щелочной среде:
Na2SO3 + 2KMnO4 + 2KOH = Na2SO4 + 2K2MnO4 + H2O
 SO32-+ 2OН - – 2e ® SO42-+ H2O 1
SO32-+ 2OН - – 2e ® SO42-+ H2O 1
MnO4- + 1e ® MnO42- 2
M(f экв.(KMnO4)KMnO4) = M(KMnO4)
в) в нейтральной среде:
3Na2SO3 + 2KMnO4 + H2O = 3Na2SO4 + 2MnO2 + 2KOH
![]() SO32-+ H2O – 2e ® SO42-+ 2H+ 3
SO32-+ H2O – 2e ® SO42-+ 2H+ 3
MnO4- + 2H2O + 3e ® MnO2 + 4ОН - 2
M(f (KMnO4)KMnO4) = 1/3 M(KMnO4)
В методе йодометрии могут иметь место такие реакции:
2I - - 2e = I20
I2 + 2e = 2I-
М(fэкв. (I2)I2) = ½ M(I2) = 127 г/моль
Кроме иода в идометрии стандартным может быть раствор Na2S2O3 · 5H2O
2Na2S2O3 + I2 = 2NaI + Na2S4O6
 2S2Oe = S4O62- 2
2S2Oe = S4O62- 2
I2 + 2e = 2I - 2
Так как два иона S2O32– теряют два электрона (по одному на каждый ион), то:
M(f экв.(Na2S2O3·5H2O) Na2S2O3·5H2O) = M(Na2S2O3·5H2O) =248,18 г/моль
Вопросы для самоконтроля
1. Чем отличается течение реакций окисления перманганата калия в кислой и щелочной средах?
2. Как фиксируют точку эквивалентности в перманганатометрии?
3. Как готовят раствор перманганата калия? Каковы условия его хранения?
4. Как проводят перманганатометрическое определение восстановителей, окислителей, инертных ионов? Привести примеры.
5. Почему Nа2S2О3 не отвечает требованиям, предъявляемым к исходным веществам?
6. Каковы условия приготовления титрованного раствора Nа2S2О3?
Литература [3], с.132-160
Методические указания по теме 2.3.3.Метод комплексонометрии
При изучении данной темы необходимо обратить внимание на особенности метода комплексонометрии и практическое применение данного метода.
Вопросы для самоконтроля
1. Сущность трилонометрического определения сульфата магния.
2. Влияние среды на трилонометрическое определение.
3. Механизм действия индикатора.
4. Расчёт содержания МgSО4 по данным титрования.
Литература [3], с.237-243, [5], с.
Методические указания по темеМетод осаждения
При изучении данной темы необходимо обратить внимание на методы расчёта результатов анализа.
Например:
Для титрования KCI необходим раствор AgNO3 молярная концентрация эквивалента которого 0,0036 моль/дм3. Определите титр AgNO3 по KCI.
Дано:
С(AgNO3) = 0,0036 моль/дм3
Т - (AgNO3/KCI) - ?
Решение:
Для решения воспользуемся формулой (3)
Т(AgNO3/KCI) = 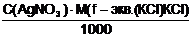 =
=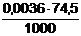 = 0,000268 г/см3
= 0,000268 г/см3
Вопросы для самоконтроля
1. Cущность метода Мора
2. Биологическое действие раствора нитрата серебра на живые организмы
3. Какие вещества можно анализировать методом аргентометрии?
4. В каких случаях содержание хлорида нельзя определять методом аргентометрии?
5. Как установить титр стандартного раствора нитрата серебра?
Литература [3], с.224-236
Методические указания по теме 3.1. Фотометрические методы анализа. Колориметрия
При изучении данной темы необходимо обратить внимание на расчёты результатов анализа.
Колориметрические, фотоколориметрические методы анализа основаны на измерении интенсивности светового потока, прошедшего через окрашенный раствор. Зависимость между интенсивностью окраски раствора и содержанием в нем окрашенного вещества выражается законом светопоглощения Бугера-Ламберта-Бера:
Ii=I0 × 10- e c i
Если уравнение закона пролагорифмировать, то оно примет вид:
Ii
Ig ¾¾ = - e c i
I0
где : Ii – интенсивность светового потока, прошедшего через раствор;
I0 – интенсивность падающего на раствор светового потока;
e– коэффициент поглощения света – постоянная величина;
c – молярная концентрация окрашенного вещества в растворе;
i толщина слоя раствора, см.
Величину lg (I0/ Ii) называют оптической плотностью раствора D:
I0
D = Ig ¾¾ = e c i
Ii
Оптическая плотность раствора прямо пропорциональна концентрации окрашенного раствора и толщине слоя раствора.
При С = 1моль/дм3 и i =1см D = e. Коэффициент e, таким образом, означает оптичес-кую плотность окрашенного раствора с концентрацией С = 1моль/ дм3 и i =1см
Например: Определите содержание Fe3+(мг/ дм3), если оптическое поглощение его раствора с сульфосалициловой кислотой равно 0,45 в кювете, толщиной 2 см,
а e = 4 ×10-3.
Решение:
По формуле 1.1. рассчитываем концентрацию раствора по Fe3+ в (моль/ дм3).
D 0,45
С = ¾¾¾ = ¾¾¾¾¾ = 5,6 ×10-5 моль/ дм3
e × i 4 ×10-3 ×2
Тогда содержание Fe3+ (мг/ дм3) составит:
56г - 1 моль/ дм3
С(Fe3+ ) - 5,6 ×10-5 моль/ дм3
5,6 ×10-5×56
С = ¾¾¾¾¾¾¾ = 3,13 10-3 г / дм3 = 3,13 мг/ дм3
1
Вопросы для самоконтроля
1. В чём сущность метода колориметрии?
2. На каком законе основаны колориметрические определения?
3. Какими преимуществами обладает метод колориметрии по сравнению с другими методами количественного анализа?
Литература [3], с.266-277
Методические указания по темеРефрактометрия
При изучении данной темы необходимо обратить внимание на сущность рефрактометрического метода анализа, зависимость показателя преломления от различных факторов, способы измерение показателя преломления, типы рефрактометров, область применения метода.
Рефрактометрия основана на измерении угла преломления светового луча при переходе его из одной среды в другую. Преломление света веществами характеризует относительным показателем преломления.
sin a
nотн = ¾¾¾¾
sin b
Рефрактометрическое определение проводят методом калибровочных графиков, по таблицам показателей преломления и рефрактометрическому фактору F.
n2 – n1 n
F = ¾¾¾¾¾ = ¾¾¾
C2 – C1 C (8)
nx = n0 + FCx (9)
(nx - n0 )
Cx = –––––––
F (10)
n2 – показатель преломления раствора с большей (известной) концентрацией С2;
n1 – показатель преломления анализируемого раствора с меньшей (известной)
концентрацией С1;
n(x) – показатель преломления анализируемого раствора концентрацией Сх;
n0 – показатель преломления растворителя.
Вопросы для самоконтроля
1. Что такое показатель преломления и от чего он зависит?
2. В чём заключается правило аддитивности мольной рефракции?
3. Приведите примеры использования этого метода в Вашей лаборатории.
Литература [3], с.381-389
Методические указания по темеПотенциометрия
При изучении данной темы необходимо обратить внимание на:
· сущность метода потенциометрического титрования;
· технику работы с pН – метром.
Вопросы для самоконтроля
1. Существующие формы кривых потенциометрического титрования.
2. Зависимость потенциала индикаторного электрода от концентрации раствора.
Литература [2], с.262-264
4. Задания для выполнения контрольной работы
Указание по выбору варианта и определение вопросов и заданий для контрольной работы
Выбор вопросов и заданий к контрольной работе определяется по фамилии, имени и отчеству студента, которые записываются в виде таблички, где номер буквы в ФИО определяет номер задачи, а буква, по нижеприведенной таблице, номер вопроса.
Если фамилии студентов одинаковые, то отсчёт номеров вопросов у одного из них, того кто имеет больший порядковый номер в журнале, производится в обратном порядке.
Например:
С | И | Д | О | Р | О | В |
1 | 2 | 3 | 4 | 5 | 6 | 7 |
9 | 19 | 33 | 52 | 68 | 82 | 92 |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



