Таким образом, у пациенток с гиперплазией коры надпочечников с поздним началом нами отмечены достаточно высокие показатели овариального резерва. Они оказались выше таковых у пациенток с трубно-перитонеальным фактором бесплодия и вполне сопоставимыми с показателями у пациенток с СПКЯ.
Гиперпролактинемия как причина бесплодия имела место у 65 больных. Исходные концентрации пролактина колебались в пределах 900‑1850 МЕ/л (1480±271 МЕ/л), а перед началом протокола КСС, т. е. на фоне лечения снижались до 300-600 МЕ/л (437±126 МЕ/л). Всем пациенткам после исключения пролактинсекретирующей аденомы гипофиза проводили терапию бромокриптином в дозе 2,5 мг в сутки в течение 2-х месяцев. Cравнение показателей эффективности протоколов стимуляции суперовуляции с использованием агонистов и антагонистов ГнРГ не выявило достоверной разницы в результатах, хотя отмечена тенденция к улучшению исходов на протоколах с агонистами ГнРГ. Так, ЧНБсц и ЧНБпэ была выше у пациенток на протоколах с агонистами ГнРГ (соответственно 38,8±8,1% и 42,4±8,6%) по сравнению с ЧНБсц и ЧНБпэ у пациенток на протоколах с антагонистами ГнРГ (соответственно, 37,9±9,0% и 40,7±9,1%).
У больных гиперпролактинемией оказался также достаточно сохранным овариальный резерв. Анализ результатов контролируемой стимуляции суперовуляции и исходов ВРТ выявил ту же закономерность, что и в других группах. Так, наименьшее число ооцитов (3,8±0,5) и самое низкое число беременностей на перенос эмбриона (33,3±15,7%) были отмечены у пациенток, где концентрация АМГ не превышала 0,75±0,4 нг/мл (Табл. 1).
Наилучшие результаты получены при концентрации АМГ более 2,5 нг/мл: число ооцитов составило 12,1±0,8, а ЧНБпэ 41,6±14,6% или почти на 10% более по сравнению с пациентками, у которых концентрация АМГ была самой низкой.
В то же время выбор протокола стимуляции суперовуляции (предпочтение агонистов или антагонистов ГнРГ) не оказывал существенного влияния на результаты КСС. Иными словами в группе пациенток с гиперпролактинемией еще раз продемонстрирована четкая зависимость результатов контролируемой стимуляции от концентрации АМГ и числа антральных фолликулов. У всех пациенток на 3‑5 сутки менструального цикла концентрация базального ФСГ находилась в пределах референтных значений, но была достоверно выше (9,2±1,2 МЕ/л) у больных со сниженным овариальным резервом. Концентрация эстрадиола у пациенток не различалась.
Наружный генитальный эндометриоз I-II степени распространения как причина бесплодия отмечен у 73 пациенток.
У 48 из них выполнены «длинный» и «супердлинный» протоколы КСС с применением агонистов ГнРГ. У 25 остальных пациенток использованы антагонисты ГнРГ. Показатели фолликуло - и эмбриогенеза у больных, которым были применены агонисты ГнРГ в «длинных» и «супердлинных» протоколах оказались лучше, чем в случаях использования антагонистов ГнРГ. На фоне протоколов с агонистами было получено большее количество фолликулов >14 см, зрелых ооцитов и эмбрионов хорошего качества, чем в случаях применения антагонистов ГнРГ.
Полученные результаты совпадают с данными литературы (, 2004; Смольникова В. Ю., 2005). Преимуществом «длинных» и «супердлинных» протоколов с агонистами ГнРГ является их эффект подавления биосинтеза эндогенных гонадотропинов. В результате улучшаются «стартовые» условия для фолликулогенеза. Поэтому при последующем назначении препаратов рекомбинантного ФСГ в фазу активного роста вступают фолликулы на одной и той же стадии развития, что является предпосылкой для получения большего количества «зрелых» ооцитов и, как следствие, эмбрионов более высокого качества.
Применению «длинных» и «супердлинных» протоколов с агонистами ГнРГ соответствовало уменьшение частоты «бедного ответа» по сравнению с таковой на фоне антагонистов ГнРГ у пациенток с НГЭ I-II степени распространения, у которых сохранен овариальный резерв. А у больных с НГЭ III-IV степени распространения «бедный» ответ был самым высоким во всех подгруппах и практически одинаковым как на фоне агонистов, так и антагонистов ГнРГ. Следует подчеркнуть, что оценка показателей овариального резерва имеет первостепенное значение при выборе протокола КСС.
Число ооцитов и эмбрионов высокого качества также имело тенденцию к увеличению на протоколах с агонистами ГнРГ (соответственно, 10,4±1,2 и 5,8±1,1 по сравнению с 8,6±0,9 и 3,9±0,7 на фоне антагонистов ГнРГ). Та же тенденция прослеживалась по числу беременностей на перенос эмбриона, которое было несколько выше на фоне агонистов ГнРГ, особенно в «супердлинном» протоколе. В то же время нельзя не отметить, что на фоне протоколов с использованием антагонистов было меньшее число самопроизвольных абортов (14,2±13,1 против 22,2±13,8% на агонистах ГнРГ), и несколько выше оказалось число родов (ЧРсц и ЧРпэ соответствовали 20,0±8,0% и 21,7±10,2% против 17,8±7,2 и 18,5±7,4% на агонистах ГнРГ в «длинном» протоколе). Кроме того, применение антагонистов ГнРГ не сопровождалось риском развития СГЯ.
Анализ показал, что у больных НГЭ I-II степени имеется относительно сохранный овариальный резерв. Концентрация АМГ равнялась 1,8±0,6 нг/мл у пациенток, получивших протокол с агонистами ГнРГ и 2,3±0,9 нг/мл у пациенток, получивших протокол с антагонистами ГнРГ.
При концентрации АМГ 0,64±0,3 нг/мл число антральных фолликулов было наименьшим (4,3±0,8), базальная концентрация ФСГ была несколько выше по сравнению с другими подгруппами и составила 9,6±1,8 МЕ/л, а концентрация эстрадиола – 510,1±87,2 пмоль/л. Стартовая доза рекомбинантного ФСГ оказалась самой высокой (266,1±16,2 МЕ), число полученных ооцитов (3,9±0,7) и ЧНБпэ (28,5±12,0%) были значительно ниже, чем в других подгруппах (Табл. 2).
При концентрации АМГ от 1 до 2,5 нг/мл число антральных фолликулов соответствовало 8,1±1,1, базальная концентрация ФСГ составила 7,3±1,5 МЕ/л, эстрадиола – 435,4±30,7 пмоль/л. Стартовые дозы рекомбинантного ФСГ у пациенток были средними (196,6±12,3 МЕ).
При концентрации АМГ >2,5 нг/мл число антральных фолликулов оказалось наиболее высоким (11,3±2,5), базальная концентрация ФСГ составила 6,9±1,3 МЕ/л, концентрация эстрадиола – достоверно не отличалась от таковой в других подгруппах (488,5±124,1 пмоль/л), а стартовая доза рекомбинантного ФСГ была меньше, чем в других подгруппах (128,5±11,9 МЕ). У этих пациенток получено наибольшее число ооцитов (10,2±1,8). ЧНБпэ составила 42,8±18,7% (Табл. 2).
Таким образом, применение агонистов ГнРГ в протоколах КСС у пациенток с НГЭ I-II степени обеспечивает более высокие результаты. В то же время большее значение для прогнозирования исходов стимуляции суперовуляции имеет оценка показателей овариального резерва и особенно, АМГ, как наиболее информативного из них.
Наружный генитальный эндометриоз III-IV степени имел место у 55 пациенток. Тяжесть заболевания оказала влияние на длительность стимуляции в протоколах и с агонистами и с антагонистами ГнРГ, и суммарную дозу препаратов рекомбинантного ФСГ. Последняя у больных этой группы была достоверно выше, чем в случаях эндометриоза I-II степени
(р<0,05).
Как и у пациенток с НГЭ I-II ст., у больных данной группы несколько лучший эффект лечения получен при использовании «длинных» и «супердлинных» протоколов с агонистами ГнРГ.
Так, число ооцитов, число эмбрионов высокого качества, было несколько больше, чем в протоколах с антагонистами ГнРГ, а частота «бедного ответа», которая оказалась высокой во всех протоколах, на агонистах ГнРГ составила 38,1±10,5 в «длинном» протоколе, 47,6±10,8% – в «супердлинном» протоколе против 26,1±9,1% на антагонистах ГнРГ.
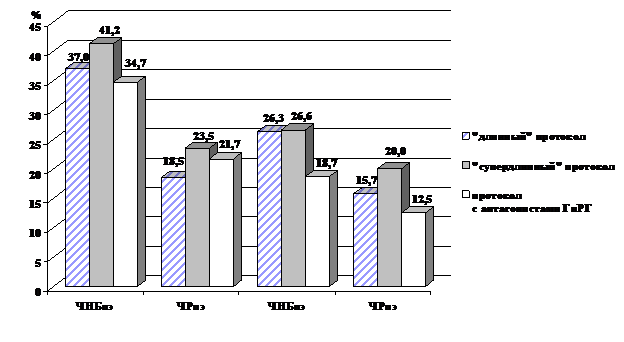
При использовании протоколов с агонистами ГнРГ получены несколько лучшие показатели ЧНБпэ и ЧРпэ по сравнению с применением протоколов, включающих антагонисты ГнРГ (рис. 2).
Полученные данные подтверждают результаты других авторов (, , 2005). Они свидетельствуют, что протоколы с агонистами ГнРГ у пациенток данной группы позволяют добиться повышения эффективности ВРТ по важнейшим показателям – ЧНБ на ПЭ и ЧР на ПЭ в сравнении с другими схемами стимуляции.
Принципиальным отличием группы больных НГЭ III-IV ст. был значительно сниженный овариальный резерв, о чём свидетельствовали не только самые низкие результаты контролируемой стимуляции суперовуляции по сравнению со всеми другими группами пациенток, но и клинические данные, и оценочные показатели овариального резерва.
![]()
![]()
Рис. 2. Эффективность программ ВРТ у пациенток с эндометриозом
Так, клиническим подтверждением недостаточной функции яичников являлась чрезвычайная частота «бедного ответа» на стимуляцию. Отмена циклов в связи с отсутствием ответа на стимуляцию оказалась самой высокой в данной подгруппе, поэтому полагаем, что препаратами выбора при таком сниженном овариальном резерве являются антагонисты ГнРГ. Следует также отметить, что в данной подгруппе не наблюдалось случаев развития СГЯ.
Мало удовлетворительными в этой группе были показатели фолликуло - и эмбриогенеза.
Оценка показателей овариального резерва выполнена у 49 больных. При этом достаточная сохранность овариального резерва выявлена лишь у шести больных. Концентрация АМГ в сыворотке крови у них превышала 2,5 нг/мл, число антральных фолликулов составляло 7,3±2,4. У всех остальных пациенток концентрация АМГ была или менее 1 нг/мл (28 больных) или составляла 1,2±0,6 нг/мл (15 больных). Анализ показателей овариального резерва подтвердил ту же закономерность, а именно, зависимость результатов протоколов стимуляции суперовуляции от функционального состояния яичников. При концентрации АМГ менее 1 нг/мл число антральных фолликулов составляло лишь 3,2±1,1, соответственно этому получено лишь 2,4±0,8 ооцита и ЧНБпэ составила 14,2±6,5% (Табл. 2). При концентрации АМГ 1,2±0,6 нг/мл и числе антральных фолликулов 4,8±2,3 выполнение протокола КСС закончилось извлечением 4,3±1,2 ооцитов на фоне стартовой дозы рекомбинантного ФСГ, равной 228,3±10,5 МЕ. Частота наступления беременностей на один перенос эмбриона составила 26,6±11,4%, т. е. оказалась также достаточно низкой, хотя этот показатель почти в 2 раза превысил таковой в группе женщин с концентрацией АМГ менее 1 нг/мл (Табл. 2).
У пациенток с концентрацией АМГ >2,5 нг/мл и наибольшим числом антральных фолликулов (7,3±2,4) получено наибольшее число ооцитов (6,5±1,4) и беременностей на один перенос эмбриона (33,3±19,2%).
Сравнение показателей овариального резерва в разных группах пациенток позволяет выявить чёткую и закономерную тенденцию, свидетельствующую о тесной зависимости результатов протоколов контролируемой стимуляции суперовуляции (как с использованием агонистов, так и с использованием антагонистов ГнРГ) от исходной концентрации АМГ в сыворотке крови и числа антральных фолликулов. Достоверность такой зависимости, несомненно, будет подтверждаться с увеличением числа наблюдений.
Анализ оценочных показателей овариального резерва позволяет составить определённый рейтинг их информативности. Согласно полученным данным, он выглядит следующим образом: наиболее информативным показателем является определение концентрации АМГ в сыворотке крови. Так как источником биосинтеза АМГ являются преантральные и малые антральные фолликулы диаметром менее 4 мм, то очевидна связь показателя с другим информативным критерием – пулом антральных фолликулов. Если ФСГ и эстрадиол являются зависимыми по принципу отрицательной обратной связи, то продукция АМГ не меняется в течение менструального цикла, что позволяет исследовать гормон в любой удобный период.
Таблица 2
Зависимость стартовой дозы гонадотропинов от уровня АМГ
и других показателей овариального резерва
у пациенток с наружным генитальным эндометриозом
НГЭ I-II ст. | Показатель | АМГ<1 нг/мл | АМГ 1-2.5 нг/мл | АМГ >2,5 нг/мл | р |
n=14 | n=37 | n=7 | |||
Возраст | 35,1±3,2 | 33,8±2,9 | 32,4±3,5 | >0,05 | |
Базальный уровень ФСГ, МЕ/л | 9,6±1,8 | 7,3±1,5 | 6,9±1,3 | >0,05 | |
Базальная концентрация Е2 пмоль/л | 510,1±87,2 | 465,4±30,7 | 488,5±124,1 | >0,05 | |
Число антральных фолликулов | 4,3±0,8* | 8,1±1,1 | 11,3±2,5* | *<0,01 | |
АМГ, нг/мл | 0,64±0,3* | 1,5±0,4 | 3,9±1,2* | *<0,01 | |
Стартовая доза ФСГ, МЕ | 266,1 ± 16,2 | 196,6 ± 12,3 | 128,5 ± 11,9 | <0,01 | |
Число ооцитов | 3,9±0,7* | 7,8±0,9 | 10,2±1,8* | *<0,01 | |
Число берем./(ЧНБпэ | 4 /28,5±12,0% | 13 /35,1±7,8% | 3/42,8±18,7% | >0,05 | |
СГЯ | 0 | 1 (2,7±2,6%) | 0 | – | |
НГЭ III-IV ст | n=28 | n=15 | n=6 | ||
Возраст | 37,1±3,4 | 34,4±3,1 | 31,8±2,9 | >0,05 | |
Базальный уровень ФСГ, МЕ/л | 12,4±2,1* | 7,6±1,8 | 3,8±1,7* | *<0,01 | |
Базальная концентрация Е2 пмоль/л | 815,8±59,8 | 711±91,8 | 723,6±226,4 | >0,05 | |
Число антральных фолликулов | 3,2±1,1 | 4,8±2,3 | 7,3±2,4 | >0,05 | |
АМГ, нг/мл | 0,52±0,1* | 1,2±0,6 | 2,6±0,8* | *<0,01 | |
Стартовая доза ФСГ, МЕ | 276,8±15,6 | 228,3±10,5 | 212,5±10,1 | <0,01 | |
Число ооцитов | 2,4±0,8* | 4,3±1,2 | 6,5±1,4* | *<0,05 | |
Число берем. /ЧНБпэ | 4/14,2±6,5%* | 4 /26,6±11,4% | 2/33,3±19,2%* | >0,05 | |
СГЯ | 0 | 0 | 0 |
В то же время настоящее исследование позволяет сделать вывод о недостаточной пригодности для оценки овариального резерва и прогноза исходов КСС, результатов определения базальной концентрации эстрадиола. Известно, что референтные пределы норм эстрадиола на 3-5-й дни менструального цикла отличаются большими колебаниями (90-715 пмоль/л). Такие вариации норм характерны и для многих других гормонов, в том числе – для ФСГ (2,5‑10,2 МЕ/л) и являются лишь свидетельством сохранной эндокринной функции яичников, но не отражают истинное состояние овариального резерва. Полагают, что базальная концентрация ФСГ 3-8 МЕ/л прогнозирует хороший ответ на стимуляцию, тогда как при базальной концентрации ФСГ 10-12 МЕ/л можно ожидать плохой ответ на КСС (Назаренко Т. А., 2008). Согласно собственным данным концентрация ФСГ в группах наблюдения находилась в пределах 1,8-15,0 МЕ/л. Отмечена обратная корреляция нижних и верхних значений «норм» ФСГ и АМГ. В то же время широкие колебания «норм» ФСГ в отличие от очень четких, конкретных значений АМГ заставляет отдать безусловное предпочтение последнему как фактору, влияющему на подбор стартовой дозы гонадотропинов и фактору прогноза исхода КСС.
Программы криоконсервации использованы у 279 пациенток в 321 цикле размораживания эмбрионов.
Всего подверглись криоконсервации 889 эмбрионов, из них 463 на стадии раннего дробления (3 сутки развития, т. е. на стадии 6-8 бластомеров) и 426 на стадии бластоцисты. После размораживания всего 450 эмбрионов были перенесены в полость матки.
При криоконсервации на 3 сутки развития (123 случая) в,6±3,8%) после размораживания получены эмбрионы «хорошего» качества и произведен их перенос в матку (среднее количество перенесенных эмбрионов составило 1,6±0,1). При криоконсервации на стадии бластоцисты (198 циклов) перенос эмбрионов в полость матки произведен в 147 случаях
(74,2±3,1%). Среднее количество перенесенных было эмбрионов 1,8±0,2.
Показатель выживаемости эмбрионов оказался достоверно ниже в подгруппе пациенток, где криоконсервация проводилась на стадии раннего дробления (39,4±2,3%) по сравнению с эмбрионами, замороженными на стадии бластоцисты, где выживаемость составила 63,8±2,3% (р<0,01).
Из 463 эмбрионов, криоконсервированых на 3 сутки развития, 281 оказался с дегенерацией (60,7±2,3%). Этот показатель был достоверно выше (р<0,01) по сравнению с таковым при размораживании бластоцист (37,1±2,3% или 158 эмбрионов с дегенерацией из 426 размороженных).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |




