Всего было получено 68 беременностей, включая два случая эктопической беременности, что составило 28,3±2,9%. При этом 20 из них наступили в результате переноса эмбрионов, криоконсервированных на стадии раннего дробления (ЧНБпэ составила 21,5±4,2%) и 48 беременностей – после переноса эмбрионов, криоконсервированных на стадии бластоцисты (ЧНБпэ 32,6±3,9%).
Существуют разные мнения о возможном влиянии применяемого протокола КСС в циклах, когда производилась криоконсервация невостребованных эмбрионов и стадии развития эмбриона, на эффективность последующих программ переноса размороженных эмбрионов. По данным A. Salumets, 2003; P. J. Stokes, 2008 криоконсервация эмбрионов человека может быть осуществлена на различных стадиях развития (стадии пронуклеусов, раннего дробления или бластоцисты). В связи с этим возникает вопрос определения наиболее подходящей для криоконсервации стадии развития эмбрионов.
В нашем исследовании в 171 случае эмбрионы были криоконсервированы в программах, где стимуляция суперовуляции проводилась на фоне агонистов ГнРГ. Из них в 68 циклах эмбрионы были заморожены на 3 сутки развития, в 103 – на стадии бластоцисты.
В 150 программах ВРТ криоконсервация эмбрионов осуществлялась в циклах, где стимуляция суперовуляции проводилась с использованием антагонистов ГНРГ: в 55 случаях эмбрионы были криоконсервированы на стадии 6-8 бластомер и 95 – на стадии бластоцисты.
Наибольшая частота наступления беременности была получена при использовании эмбрионов, где КСС проводилась на фоне агонистов ГнРГ: ЧНБпэ составила 24,5±6,1% при переносе эмбрионов на 3 сутки и в 35,5±5,4% при переносе эмбрионов на 5 сутки по сравнению с аналогичными показателями на фоне КСС с антагонистами ГнРГ (соответственно 18,2±5,8% и 29,5±5,4%).
Таким образом, эффективность программ переноса криоконсервированных эмбрионов достоверно выше при криоконсервации бластоцист по сравнению с таковыми при криоконсервации эмбрионов ранней стадии дробления (Табл. 3). Вероятно, это связано с возможностью отбора эмбрионов лучшего качества при культивировании их до стадии бластоцисты. Кроме того, использование агонистов ГнРГ позволило получить больше эмбрионов хорошего качества, по сравнению с использованием антагонистов ГнРГ.
Повышение эффективности программ переноса криоконсервированных эмбрионов достигается применением бесконтактного инфракрасного лазера с длиной волны 1,48 мкм с целью воздействия на оболочку эмбриона после
оттаивания и перфорации зоны пелюцида, как метода вспомогательного хетчинга с целью улучшения условий для имплантации (B. Balaban, 2006).
Таблица 3
Эффективность переноса эмбрионов в случаях применения
вспомогательного хетчинга
Параметры | ЛВХ | МВХ | Без ВХ | |||
3 сутки | 5 сутки | 3 сутки | 5 сутки | 3 сутки | 5 сутки | |
Число циклов с ПЭ | 29 | 52 | 33 | 49 | 31 | 46 |
Число перенесенных эмбрионов | 59 | 93 | 65 | 91 | 58 | 84 |
Число беременностей | 7 | 20 | 7 | 16 | 6 | 12 |
ЧНБпэ, (%±m%) | 24,1±7,9 | 38,5±6,7 | 21,2±7,1 | 32,6±6,7 | 19,3±7,1 | 26,1±6,4 |
Одноплодные/ | 5/2 | 16/4 | 6/1 | 14/2 | 5/1 | 10/2 |
Частота имплантаций, (%±m%) | 15,2±4,6 | 25,8±4,5* | 12,3±4,1* | 19,8±4,2 | 12,1±4,3* | 16,6±4,1 |
Примечание: * – р<0,05
С целью исследования влияния вспомогательного хетчинга на эффективность программ переноса эмбрионов после криоконсервации выполняли вспомогательный хетчинг непосредственно перед переносом эмбрионов. При этом эмбрионы, криоконсервированные на 3 сутки размораживали накануне, а эмбрионы, криоконсервированные на стадии бластоцисты – в день планируемого переноса. Вспомогательный хетчинг производили несколькими способами: с помощью бесконтактного инфракрасного лазера – лазерный вспомогательный хетчинг (ЛВХ) и с помощью механического воздействия на зону пелюцида с целью ее перфорации – механический вспомогательный хетчинг (МВХ).
Лазерный вспомогательный хетчинг выполнен в 81 случае, при криоконсервации эмбрионов на третьи сутки – у 59 эмбрионов (38,8%) и при криоконсервации на стадии бластоцисты – у 93-х (61,2%). В данной группе частота наступления беременности на перенос эмбриона оказалась самой высокой: 24,1±7,9% при переносе эмбрионов, криоконсервированных на третьи сутки, и 38,5±6,7%, при переносе эмбрионов, криоконсервированных на стадии бластоцисты. Частота имплантаций так же была достаточно высокой и соответственно составила 15,2±4,6 и 25,8±4,5% (Табл. 3). Всего в данной группе получено 20 беременностей: 16 из них одноплодные и 4 двойни.
Механический вспомогательный хетчинг выполнен в 82 случаях, у 65 эмбрионов (41,6±3,9%) – при криоконсервации на третьи сутки и у,1±3,9%) – при криоконсервации эмбрионов на стадии бластоцисты. ЧНБпэ при использовании МВХ была несколько меньше: 21,2±7,1% при переносе эмбрионов, криоконсервированных на третьи сутки, и 32,6±6,7%, при переносе эмбрионов, криоконсервированных на стадии бластоцисты.
Частота имплантаций оказалась ниже, чем в случаях применения вспомогательного лазерного хетчинга и соответственно составила 12,3±4,1% при переносе эмбрионов, криоконсервированных на третьи сутки, и 19,8±4,2% при переносе эмбрионов, криоконсервированных на стадии бластоцисты (Табл. 3).
В группе, где вспомогательный хетчинг не был использован, осуществлён перенос 58 эмбрионов, криоконсервированных на третьи сутки развития, и 84 эмбриона, криоконсервированных на стадии бластоцисты. Результаты оказались значительно хуже, чем в случаях применения хетчинга. Так, при криоконсервации эмбрионов на третьи сутки частота наступления беременности и частота имплантаций соответственно составили 19,3±7,1% и 12,1±4,3%. Всего в группе получено шесть беременностей.
В случаях переноса эмбрионов, криоконсервированных на стадии бластоцисты, частота наступления беременности на перенос эмбриона и частота имплантаций соответственно составили 26,1±6,4% и 16,6±4,1%. Получено всего 12 беременностей (Табл. 3).
Таким образом, очевидно значение метода вспомогательного хетчинга как фактора, значимо повышающего частоту имплантации эмбрионов в программах ВРТ. Безусловное предпочтение следует отдать методу вспомогательного хетчинга с помощью лазера.
Исходы беременностей, наступивших в программах ВРТ
Выше отмечено, что всего было получено 210 беременностей, в том числе 198 маточных и 12 эктопических (трубные). После переноса нативных эмбрионов наступили 142 беременности (67±3,2%), после переноса криоконсервированных эмбрионов – 68 (32,4±3,2%). Многоплодных беременностей в группе оказалось 12 (17,6±4,6%). Меньшее число многоплодных беременностей получено в программах переноса криоконсервированных эмбрионов.
Родами закончились 148 беременностей (74,7±3,1%). В 50 случаях произошел аборт в первом – втором триместрах беременности (25,3±3,1%).
В 96 случаях беременность и роды были после переноса нативных эмбрионов и в 52 – после переноса криоконсервированных эмбрионов.
Самыми частыми осложнениями беременности были угроза невынашивания и гестоз. В первом триместре беременности угроза аборта отмечена в 30,3±7,9% случаев, в том числе даже чаще на фоне одноплодной беременности.
Во втором и третьем триместрах угроза невынашивания беременности оставалась такой же высокой (31,2±4,7%), была значительно выше в случаях многоплодия (40,9±10,4%).
В целом высокой оказалась частота гестоза: при беременности на фоне переноса нативных эмбрионов – в 34,4±4,8% случаев, при переносе криоконсервированных эмбрионов – в 30,8±6,4% случаев. Значительно чаще, чем в популяции беременных женщин в целом (данные по Санкт-Петербургу), т. е. фактически у каждой 4-5-й пациентки с гестозом отмечены его тяжёлые формы. Это было особенно характерно для случаев беременности, наступившей при переносе нативных эмбрионов.
Независимо от протокола ВРТ, переноса нативных или криоконсервированных эмбрионов, достаточно часто наблюдалась задержка развития плода. Этот диагноз отмечен соответственно в 18,7±3,9 и 19,2±5,4% случаев переноса нативных и криоконсервированных эмбрионов. В то же время средний показатель частоты задержки развития плода по отчётам родовспоможения Санкт-Петербурга составляет 14,8%.
Сравнение особенностей течения беременности у пациенток при переносе нативных или криоконсервированных эмбрионов показало меньшее число осложнений во второй группе. Так, беременность при переносе эмбрионов после криоконсервации реже осложнялась гестозом, включая его тяжёлые формы, реже – нарушением функции печени по типу холестатического гепатоза и реже – анемическим синдромом. Полагаем, что такое различие связано с некоторым «отдыхом» пациентки после протокола контролируемой стимуляции суперовуляции в случаях переноса криоконсервированных эмбрионов. Напротив, перенос нативных эмбрионов и, следовательно, течение беременности на фоне проведенной стимуляции суперовуляции, нередко – с явлениями синдрома гиперстимуляции, затрудняет адаптацию к беременности. Это, возможно, в определённой степени способствует осложненному течению беременности.
В то же время нельзя исключить влияние фоновой патологии на частоту осложненного течения беременности, так как пациентки, попадающие в программы ВРТ, как правило, отягощены не только гинекологической, но и соматической патологией.
Показатель преждевременных родов в популяции беременных женщин Санкт-Петербурга в течение последних 10 лет () устойчиво удерживается в пределах 5,0-5,5-6,0%. В нашем исследовании этот показатель оказался в 4-5 раз выше: при переносе нативных эмбрионов 31,6±4,3%, при переносе эмбрионов после криоконсервации – 23,1±5,8%.
Полагаем, что все репродуктивные потери, отмеченные выше осложнения беременности, а также высокая частота преждевременных родов, полученная в настоящем исследовании, преимущественно объясняются состоянием здоровья пациенток. Помимо отмеченных выше гинекологических и соматических заболеваний у большинства негативное влияние на течение беременности оказывали отягощённый акушерский анамнез, хронические инфекции урогенитальной системы, поздний репродуктивный возраст женщин. На увеличение числа преждевременных родов могла влиять большая, чем при естественном наступлении беременности, частота многоплодия.
Роды в срок наступили у 75,7±3,5% женщин, чаще – на фоне одноплодной беременности (85,4±3,2%), реже – при многоплодной (38,7±8,7%). Показатели частоты срочных родов при беременности после переноса нативных и криоконсервированных эмбрионов существенно не различались и составляли соответственно при одноплодной и многоплодной беременности 85,1±4,1 и 40,9±10,4% и 86,0±5,2 и 33,3±15,7%.
Всего родилось 179 детей: 117 родов одним плодом и 31 роды двойней. Доношенных детей родилось ,5±3,6%), недоношенных,4±3,6%).
Основным методом родоразрешения оказалась операция кесарева сечения, которая выполнена в 82,9±3,3% случаев. В случаях многоплодной беременности производилось только оперативное родоразрешение.
Не получено достоверных различий в массе тела и оценке по шкале Апгар детей, родившихся вследствие программ с переносом нативных и криоконсервированных эмбрионов. Это касается новорожденных, рожденных как в одноплодных, так и в многоплодных беременностях.
Так, например, число детей с массой тела более 2500 грамм, родившихся от многоплодной беременности при переносе нативных и криоконсервированных эмбрионов соответственно составило 25,0±6,5% и 27,7±10,5%.
В случаях одноплодных беременностей несколько выше оказалась частота рождения детей с массой рамм при переносе криоконсервированных по сравнению с переносом нативных эмбрионов. Частота рождения крупных детей (масса более 4-х килограмм) оказалась ниже, чем в популяции беременных женщин по Санкт-Петербургу за указанные выше годы.
Анализируя здоровье рожденных детей следует подчеркнуть высокий риск рождения детей с различной патологией при многоплодных беременностях (рис. 3).
![]()
![]()
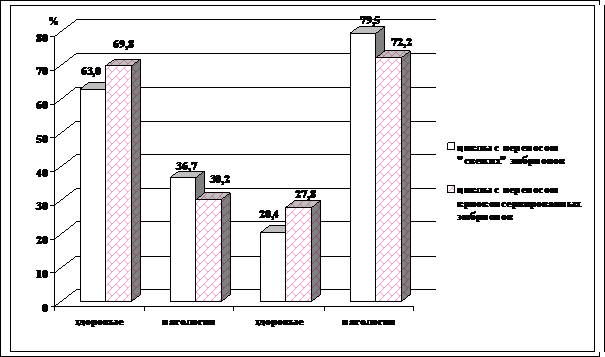
Рис. 3. Состояние здоровья детей в исследуемых группах.
Высокая частота задержки развития плода при беременности подтверждена данными неонатологов: гипотрофия плода диагностирована у 10,6±2,3% новорожденных (при переносе нативных и криоконсервированных эмбрионов соответственно в 11,0±8,3 и 9,8±3,8% в сравнении с 4,2% в популяции новорожденных по Санкт-Петербургу).
Частота “take home baby” при переносе нативных и криоконсервированных эмбрионов соответственно составила 31,9±2,4 и 25,0±2,8%.
Перинатальная смертность в группе в целом составила 11,17‰ в сравнении с 5,89 – 6,01‰ по Санкт-Петербургу за гг. Врождённые пороки выявлены у двух новорожденных или в 1,1% случаев, что сопоставимо с популяционными данными (1,8-3,6%).
Таким образом, течение беременности, индуцированной с помощью программ ВРТ, является более осложнённым, чему способствует совокупный комплекс факторов, включая более высокую частоту многоплодной беременности, возраст и отягощённый анамнез женщин и особенности выбранного протокола ВРТ.
ВЫВОДЫ
1. Дифференцированный выбор протокола контролируемой стимуляции суперовуляции с учётом фоновой гинекологической патологии, использованных ранее методов лечения и показателей овариального резерва существенно повышает эффективность программ ВРТ.
2. У пациенток с трубно-перитонеальным фактором бесплодия получен наибольший эффект от программ ВРТ (ЧНБпэ 44,0±5,7%), отмечена тенденция к улучшению показателей при использовании агонистов ГнРГ (ЧНБпэ 45,0±7,8%).
3. Предшествующие оперативные вмешательства на яичниках у женщин с СПКЯ неблагоприятно влияют на исходы ВРТ, особенно в случаях проведения протоколов с антагонистами ГнРГ (ЧНБпэ, соответственно 35,3±11,5% против 41,2±11,9%).
4. В связи с уменьшением фолликулярного запаса, качественными изменениями ооцитов наиболее низкая эффективность программ ВРТ отмечена у больных НГЭ III-IV степени, где частота «бедного ответа» на КСС оказалась самой высокой, независимо от использования агонистов или антагонистов ГнРГ.
5. При гиперплазии коры надпочечников с поздним началом одинаково эффективно использование стандартных протоколов с агонистами и антагонистами ГнРг (ЧНБпэ соответственно 42,8±10,8% и 43,4±10,3%).
6. Выбор программы ВРТ и стартовой дозы должен быть основан на совокупности данных, включающих фоновое состояние пациентки, причину бесплодия и овариальный резерв. В совокупной оценке последнего целесообразно определение антимюллерового гормона как наиболее информативного показателя функционального состояния яичников.
7. Метод криоконсервации невостребованных жизнеспособных эмбрионов, способствуя повышению кумулятивной частоты наступления беременностей в циклах ВРТ, является высокоэффективным способом лечения бесплодия.
8. Эффективность метода криоконсервации повышается при замораживании эмбрионов на стадии бластоцисты и проведении лазерного хетчинга перед переносом эмбриона в полость матки.
9. ЧНБпэ после криоконсервации оказалась выше в случаях, где были применены протоколы КСС с агонистами ГнРГ (36,1±7,0%) по сравнению с антагонистами ГнРГ (31,3±6,4%).
10. Развитие синдрома гиперстимуляции яичников достоверно выше в группах женщин, у которых были использованы агонисты, а не антагонисты ГнРГ. Отмечена зависимость частоты развития синдрома гиперстимуляции от фоновой гинекологической патологии с самым высоким процентом у больных СПКЯ (30,9±7,1%) и отсутствием такового у пациенток с НГЭ III-IV ст.
11. Беременности, наступившие в результате переноса размороженных эмбрионов по течению не отличаются от беременностей, полученных в стимулированных циклах и относятся к группе высокого риска в отношении развития угрозы прерывания, гестоза, ВЗРП, преждевременных родов. Особенно осложненным является течение многоплодной беременности.
12. Риск перинатальных потерь и врожденных пороков развития у новорожденных от матерей, которым проводился перенос нативных или размороженных эмбрионов, не превышает этот показатель в общей популяции.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Выбор программы ВРТ должен быть индивидуальным, зависеть от совокупной оценки фоновых факторов, явившихся причиной бесплодия, предшествующего лечения бесплодия (ВРТ, операции на яичниках) и овариального резерва.
2. В комплексе показателей овариального резерва особое значение приобретает антимюллеровый гормон, являющийся высокоинформативным критерием функции яичников и критерием для подбора стартовой дозы препаратов гонадотропинов в протоколе контролируемой суперовуляции.
3. Выбор протокола контролируемой стимуляции суперовуляции у пациенток с СПКЯ зависит от исходного состояния яичников: оперативные вмешательства в анамнезе решают выбор в пользу длинного протокола с агонистами ГнРГ; в остальных случаях предпочтительнее протокол с антагонистами, снижающий риски развития тяжёлых степеней синдрома гиперстимуляции яичников.
4. НГЭ является основанием для выбора протоколов с агонистами ГнРГ, а при НГЭ III-IV cтепени распространения и значительном снижении овариального резерва препаратами выбора являются антагонисты ГнРГ, так как высока вероятность отсутствия ответа на стимуляцию суперовуляции при использовании агонистов ГнРГ. Также целесообразна рекомендация как можно более раннего использования программ ВРТ у пациенток с НГЭ.
5. Выбор протокола (агонисты или антагонисты ГнРГ) у пациенток с трубно-перитонеальным фактором бесплодия и гиперплазией коры надпочечников должен зависеть не столько от указанной патологии, сколько от овариального резерва, связанного с возрастом и другими факторами.
6. Использование протоколов с агонистами ГнРГ обеспечивает получение большего числа эмбрионов хорошего качества, что позволяет их сохранять, используя метод криоконсервации, хотя протоколы с агонистами ГнРГ не являются универсальными, так как имеют высокий процент осложнений.
7. Метод криоконсервации позволяет избегать повторных протоколов конролируемой суперовуляции, исключает риск развития синдрома гиперстимуляции яичников, повышает совокупную частоту наступления беременностей.
8. Криоконсервацию эмбрионов целесообразно проводить на стадии бластоцисты (5-е сутки), рекомендуется проведение лазерного хетчинга перед переносом размороженного эмбриона в полость матки.
9. Течение беременностей, полученных с помощью ВРТ, сопряжено с высокой частотой осложнений (невынашивание на разных сроках, гестоз, нарушения функции печени, задержка развития плода). Выбор метода родоразрешения зависит от совокупных факторов, при показаниях к кесареву сечению, его лучше выполнять в плановом порядке.
СПИСОК ОПУБЛИКОВАННЫХ РАБОТ
1. Беременность и роды после переноса криоконсервированных эмбрионов: течение, перинатальные исходы, период новорожденности / Калугина А. С., , //Акушерство и гинекология. – 2006. – № 1. – С. 21-24.
2. ВРТ в лечении бесплодия / , , Корнилов Н. В., Чежина М. В. // 3-й Международный научный конгресс «Новые технологии в акушерстве и гинекологии». – СПб., 2007. – С.63-64.
3. Зиневич, глюкокортикоидами и эффективность ЭКО и ПЭ у больных с функциональной гиперандрогенией яичникового, надпочечникового и смешанного происхождения / Зиневич Я. Л., Калугина А. С., Краснопольская К. В. //Акушерство и гинекология. – 2002. – № 4. – С.33-38.
4. Кабанова, ингибитора ароматазы анастрозола при терапии бесплодия у кломифенрезистентных пациенток с синдромом поликистозных яичников / Кабанова Д. И., Калугина А. С., Краснопольская К. В. // Вопросы гинекологии, акушерства и перинатологии. – 2003. ―Т.2, № 5-6. – С.35-38.
5. Калугина, агонистов и антагонистов ГнРГ в программах ВРТ у пациенток с трубно-перитонеальным фактором и СПКЯ / // Тезисы докладов научно-практической конференции, посвященной 10‑летию клиники «АВА-ПЕТЕР». – СПб., 2006.
6. Калугина, агонистов и антагонистов ГнРГ в циклах ВРТ у пациенток с эндометриозом / // 3-й Международный научный конгресс «Новые технологии в акушерстве и гинекологии». – СПб., 2007. – С.64-65.
7. Калугина, программы ЭКО у пациенток с предшествующими оперативными вмешательствами на яичниках / Калугина А. С., Краснопольская К. В. //Акушерство и гинекология. – 2000. – № 6. – С.35-39.
8. Клинические аспекты преимплантационной генетической диагностики / Калугина А. С., Каменецкий Б. А., Логинова Ю. А., Шлыкова С. А. // VI Московская ассамблея «Здоровье столицы». – М., 2007. – С.95.
9. Краснопольская, лютеинизирующего гормона при контролируемой суперовуляции гонадотропинами в программах экстракорпорального оплодотворения / Краснопольская К. В., Калугина А. С. // Акушерство и гинекология. – 2006. – № 1. – С.3-8.
10. Краснопольская, непроходимости маточных труб и эффективность программы ЭКО и ПЭ/ , Калугина А. С. // Акушерство и гинекология. – 1999. – № 6. – С.31-33.
11. Краснопольская, непроходимости маточных труб и эффективность программы ЭКО и ПЭ / , //Акушерство и гинекология. – 1999. – №6. – С.31-33.
12. Краснопольская, ЭКО и ПЭ у больных с миомой матки небольших размеров / Краснопольская К. В., Сичинава Л. Г., // Акушерство и гинекология. – 2000. – № 1. – С.56-58.
13. Краснопольская, опыт использования ингибитора ароматазы анастрозола в программе ЭКО при лечении бесплодия, ассоциированного с тяжелым перитонеальным эндометриозом / Краснопольская К. В., // Проблемы репродукции. – 2001. – Т.7, № 6. – С.42-46.
14. Краснопольская, лютеинизирующего гормона в программе ЭКО с использованием антагониста гонадотропин-рилизинг-гормона у пациенток с трубно-перитонеальным бесплодием / Краснопольская К. В., //Акушерство и гинекология. – 2005. – № 6. – С.29-33.
15. Краснопольская, принципы терапии генитальных кандидозов у женщин / , , Клименко П. А. // Вестник Российской ассоциации акушеров-гинекологов. – 1998. – № 3. – С.112-115.
16. Краснопольская, «бедного» ответа на стимуляторы суперовуляции в программах ЭКО / , // Проблемы репродукции. – 2004. – № 1. – С.51-58.
17. Краснопольская, необъяснимого «бедного» ответа яичников на стимуляторы овуляции в программах ЭКО и тактика его преодоления. Тезисы XII Международной конференции Российской ассоциации репродукции человека. Вспомогательные репродуктивные технологии / , // Проблемы репродукции. – 2003. – № 5. – С.44.
18. Краснопольская, ЭКО у больных с эндометриозом: влияние на результаты лечения длительности предшествующей терапии и различных схем стимуляции овуляции / Краснопольская К. В., Калугина А. С., Мачанските О. В.// Материалы II Российского форума «Мать и дитя»: тез. докл., 18-22 сентября. – М., 2000. – С.230-231.
19. Краснопольская, ЭКО у пациенток с синдромом поликистозных яичников и яичниковой гиперандрогенией / , , //Акушерство и гинекология. – 2003. – № 2. – С.57-59.
20. Краснопольская, и терапия гиперандрогенных состояний в программах ЭКО / , // Проблемы репродукции. – 2004. – № 5. – С.25-30.
21. Криоконсервация эмбрионов: эффективность метода, поиск путей оптимизации / Коновальчикова Т. Л., , Калугина А. С., //Материалы VII Российского форума «Мать и дитя»: тез. докл. – М., 2005. – С.407-408.
22. Опыт интенсивной терапии тяжелых форм синдрома гиперстимуляции яичников / Шаталов А. Е., Лапина Е. Н., Калугина А. С., Линде В. А. // XI съезд анестезиологов и реаниматологов. – СПб., 2008.
23. Опыт интенсивной терапии тяжелых форм синдрома гиперстимуляции яичников / Шаталов А. И., Лапина Е. Н., Линде В. А., Калугина А. С. // VI Всероссийская междисциплинарная конференция «Критические состояния в акушерстве и неонатологии». – Петрозаводск, 2008.
24. Применение агонистов гонадотропин-рилизинг гормона в программе экстракорпорального оплодотворения / Краснопольская К. В., Калугина А. С., [и др.] // Акушерство и гинекология. – 2004. – № 1. – С.33-36.
25. Применение программ вспомогательных репродуктивных технологий у пациенток с эндометриозом / Калугина А. С., Каменецкий Б. А., Чежина М. В., // Ж. акуш. и жен. болезн. – 2008. – Т. LVII, вып. 1. – С.57-62.
26. Савельева, исследование клинической эффективности протоколов стимуляции суперовуляции с применением агонистов гонадотропин-рилизинг гормона / Савельева Г. М., Краснопольская К. В., // Гинекология. – 2000. – Т.2, № 5. – С.150-153.
27. Савельева, обследования и принципы терапии женщин, страдающих бесплодием. Использование методов восстановления естественной фертильности и вспомогательных репродуктивных технологий: пособие для врачей / Савельева Г. М., , – М., 2000. – 46 с.
28. Сравнение протоколов стимуляции суперовуляции рекомбинантным ФСГ с агонистами и антагонистами ГнРГ у пациенток с СПКЯ в зависимости от исходного состояния яичников / Кабанова Д. И., Калугина А. С., Краснопольская К. В., Белобородов С. М. // Проблемы репродукции. – 2004. – № 3. – С.34-41.
29. Терапия рецидивирующего герпеса у больных с бесплодием, проходящих подготовку к ЭКО / Краснопольская К. В., Калугина А. С., Клименко П. А., Сичинава Л. Г. // Вестник Российской ассоциации акушеров-гинекологов. – 1999. – № 4. – С.84-86.
30. Эффективность ЭКО после терапии наружного генитального эндометриоза / Краснопольская К. В., Калугина А. С., Мачанските О. В., Штыров С. В. // Проблемы репродукции. – 2000 . – № 1. – С.54-56.
31. Эффективность ЭКО при переносе криоконсервированных эмбрионов / Калугина А. С., Краснопольская К. В., Груненко А. П., Коновальчикова Т. Л. // Вопросы гинекологии, акушерства и перинатологии. – 2005. – Т.4, № 7.
32. Krasnopolskaya, K. V. Application of aromatase ingibitors (anastrosol) in an IVF programme for the treatment of infertility associated with severe endometriosis / Krasnopolskaya K. V., Kalugina A. S. // Hum. Reprod. – 2002. – Vol.17. – P.149.
33. Krasnopolskaya, K. V. Geno-Pevaril 150 in patients scheduled for IVF / Krasnopolskaya K. V., Kalugina A. S., Klimenko P. A. // Abstracts of 13th Congress of the European Association of Gynaecologist and Obstetricians: abstract book Jerasalem, may 10-14. – Israel, 1998. – P.84.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |




