На правах рукописи
КАЛУГИНА АЛЛА СТАНИСЛАВОВНА
ОПТИМИЗАЦИЯ КОНТРОЛИРУЕМОЙ СУПЕРОВУЛЯЦИИ
И КРИОКОНСЕРВАЦИИ В ПРОГРАММАХ
ВСПОМОГАТЕЛЬНЫХ РЕПРОДУКТИВНЫХ ТЕХНОЛОГИЙ
14.00.01 – акушерство и гинекология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора медицинских наук
Санкт-Петербург – 2009
Работа выполнена на кафедре репродуктивного здоровья женщин
Государственного образовательного учреждения дополнительного профессионального образования Санкт-Петербургской Медицинской Академии Последипломного Образования
Научный консультант:
заслуженный деятель науки РФ, доктор медицинских наук, профессор | ||
Официальные оппоненты: | ||
доктор медицинских наук, профессор | ||
доктор медицинских наук, профессор | ||
доктор медицинских наук |
Ведущая организация:
Государственное образовательное учреждение высшего профессионального образования Санкт-Петербургская Государственная Медицинская Академия им. Мечникова
Защита состоится «___» ____________2009 г. в ___ часов на заседании диссертационного совета Д 001.021.01 при Научно-исследовательском институте акушерства и гинекологии им. северо-западного округа РАМН ( Санкт-Петербург, Менделеевская линия, д. 3).
С диссертацией можно ознакомиться в библиотеке НИИ акушерства и гинекологии им. СЗО РАМН.
Автореферат разослан «___»__________2009 г.
Ученый секретарь диссертационного совета доктор медицинских наук |
|
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Неудовлетворительное состояние репродуктивного здоровья населения нашей страны, увеличение числа бесплодных браков диктуют необходимость искать новые пути для решения проблем и увеличения рождаемости. Особое значение приобретают исследования, направленные на повышение эффективности, доступности и безопасности методов вспомогательных репродуктивных технологий (ВРТ), которые предоставляют уникальную возможность реализовывать функцию деторождения практически при всех формах женского и многих мужского бесплодия (, 2005).
По показателю частоты наступления беременности в расчете на перенос эмбриона эффективность программ ВРТ составляет в среднем 35‑40% в ведущих отечественных и зарубежных клиниках (РАРЧ – 2006, ESHRE – 2004). Учитывая такой недостаточный терапевтический потенциал вспомогательных репродуктивных технологий, весьма актуальными являются исследования, направленные на совершенствование программ ВРТ ().
Очевидно, что пути повышения эффективности ВРТ заключаются в первую очередь в пересмотре подходов к протоколам контролируемой овариальной стимуляции суперовуляции у пациенток с различной эндокринной патологией, тяжелыми формами наружного генитального эндометриоза (НГЭ), т. е. теми состояниями, которые являются важнейшими причинами женского бесплодия с одной стороны и неблагоприятно влияют на исходы лечения с применением вспомогательных репродуктивных технологий – с другой.
В последнее десятилетие получили широкое распространение препараты антагонистов гонадотропин-рилизинг гормонов (ГнРГ), которые, как предполагалось, вытеснят из циклов ВРТ ранее длительно использовавшиеся агонисты ГнРГ. Но этого не случилось: в протоколах ВРТ нашлось место как антагонистам, так и агонистам ГнРГ. Вместе с тем данные относительно предпочтения одних или других препаратов спорны, им посвящена многочисленная литература, изучение которой не делает ситуацию более понятной.
Поэтому является весьма актуальной оценка потенциала действия агонистов и антагонистов ГнРГ с определением их места в протоколах контролируемой стимуляции суперовуляции в программах ВРТ, определением показаний к их назначению с учетом фоновой гинекологической патологии.
Сегодня насчитывается достаточно много публикаций, посвященных выбору наиболее оптимального протокола контролируемой стимуляции суперовуляции в программах ВРТ, который обеспечил бы адекватный фолликулогенез и получение достаточного числа зрелых ооцитов и также характеризовался бы минимальной вероятностью осложнений (, 2008; Brinsden P. R., 2005).
Приводимые в литературе данные настолько противоречивы, что требуют обязательного уточнения и систематизации. Очевидно, что проведенные в этом направлении исследования могут определить правильный выбор тех или иных схем стимуляции суперовуляции в конкретных клинических ситуациях, предопределяемых исходным гормональным фоном, состоянием яичников, включая предшествующие оперативные вмешательства и сохранившийся овариальный резерв.
Несмотря на значительные достижения в области криоконсервации, эффективность программ ВРТ при переносе криоконсервированных эмбрионов значительно ниже, чем в циклах стимуляции суперовуляции и переноса нативных эмбрионов (Royere D., 2007; Balaban B., 2008). В литературе имеются противоречивые данные о влиянии криоконсервации эмбрионов на течение беременности, родов и состояние детей в перинатальном периоде и многие вопросы, касающиеся эффективности и безопасности применения программ ВРТ с криоконсервацией эмбрионов остаются открытыми (Wennerholm U. B., 2009). Все это определяет необходимость дальнейших исследований, направленных на оптимизацию программ ВРТ при переносе размороженных эмбрионов. Остаются вопросы к применению вспомогательного лазерного хетчинга для повышения эффективности программ после переноса криоконсервированных эмбрионов.
Если данные относительно более осложненного течения беременности у пациенток после программ ВРТ в основном совпадают, то на сегодня недостаточно данных о перинатальных исходах программ ВРТ, а именно о состоянии рожденных детей после стандартных программ ЭКО, ИКСИ, а также циклов с переносом эмбрионов после криоконсервации.
Все это определяет необходимость дальнейших исследований в этих направлениях.
Цель исследования. Совершенствование программ вспомогательных репродуктивных технологий с последующей оценкой перинатальных исходов и учетом фоновой гинекологической патологии, а также сопутствующих факторов: состояние овариального резерва, предшествующие методы лечения бесплодия, криоконсервация.
Задачи исследования:
1. Исследовать эффективность разных протоколов контролируемой стимуляции суперовуляции с применением агонистов и антагонистов ГнРГ в программах ВРТ у пациенток с хронической ановуляцией вследствие эндокринной патологии и с учетом проведенного ранее лечения.
2. Исследовать эффективность разных протоколов контролируемой стимуляции суперовуляции у пациенток с трубно-перитонеальным фактором бесплодия.
3. Исследовать эффективность контролируемой стимуляции суперовуляции у пациенток с наружным генитальным эндометриозом в зависимости от степени распространения процесса.
4. Определить информативность антимюллерова гормона как критерия овариального резерва в сравнении с другими, ранее принятыми показателями.
5. Оценить эффективность предшествующих программ стимуляции суперовуляции в циклах размораживания и переноса криоконсервированных эмбрионов.
6. Изучить эффективность программ переноса криоконсервированных эмбрионов по частоте наступления беременности в зависимости от стадии развития эмбриона на момент криоконсервации.
7. Оценить эффективность и целесообразность использования лазерного хетчинга при переносе криоконсервированных эмбрионов.
8. Провести анализ перинатальных исходов в зависимости от использованных методов ЭКО, ИКСИ, а также программ переноса эмбрионов после криоконсервации.
Научная новизна и теоретическая значимость работы
Впервые разработан и обоснован индивидуальный подход к выбору протокола контролируемой стимуляции суперовуляции с использованием агонистов и антагонистов ГнРГ у пациенток с хронической ановуляцией как причиной бесплодия на фоне синдрома поликистозных яичников (СПКЯ) с учётом предшествующих методов стимуляции овуляции и оперативных вмешательств (программа ВРТ, лапароскопический дриллинг, резекция яичников и др.).
Исследованы преимущества, обоснованы показания к выбору протоколов стимуляции суперовуляции с использованием агонистов или антагонистов ГнРГ в случаях хронической ановуляции, связанной с гиперплазией коры надпочечников с поздним началом и гиперпролактинемией, а также – у пациенток с разной степенью тяжести распространения наружного генитального эндометриоза.
Установлено, что неэффективность программ ВРТ у больных эндометриозом III-IV ст. тяжести связана не только с качественными изменениями ооцитов, но и выраженным снижением параметров фолликулогенеза.
Впервые выявлено, что антимюллеровый гормон является информативным показателем функционального резерва яичников для прогноза ответа на контролируемую стимуляцию суперовуляции в протоколах ВРТ.
Показаны дополнительные преимущества метода криоконсервации жизнеспособных эмбрионов, способствующего кумулятивному повышению частоты наступления беременностей в протоколах ВРТ. Эффективность программы повышается при переносе эмбрионов после их криоконсервации на стадии бластоцисты и с использованием протоколов контролируемой стимуляции суперовуляции с агонистами ГнРГ, а также – с проведением лазерного хетчинга перед переносом бластоцист.
Проведена оценка течения беременности и перинатальных исходов с учётом фоновой гинекологической патологии, особенностей протоколов ЭКО, ИКСИ и в зависимости от переноса нативных эмбрионов или эмбрионов после криоконсервации.
Практическая значимость работы
На основании индивидуального подбора протоколов контролируемой стимуляции суперовуляции с использованием агонистов и антагонистов ГнРГ у пациенток с различной фоновой гинекологической патологией показана высокая эффективность вспомогательных репродуктивных технологий. Разработаны рекомендации разных подходов к протоколам для пациенток с синдромом поликистозных яичников в зависимости от предшествующего лечения (операции на яичниках, протоколы ВРТ в анамнезе), для пациенток с разной степенью распространения наружного генитального эндометриоза и пациенток со «слабым» ответом на стимуляцию (сниженный овариальный резерв).
Оценка антимюллерова гормона предложена в качестве одного из наиболее информативных показателей овариального резерва, и, следовательно, может быть использована для прогноза ответа на стимуляцию суперовуляции, сравнения его с другими показателями овариального резерва и ориентира для правильного выбора протокола и его стартовой дозы. Такой подход позволил снизить риск развития синдрома гиперстимуляции и получить достаточное число ооцитов, что обеспечило больше возможностей для отбора эмбрионов лучшего качества перед их переносом в матку.
Внедрение метода криоконсервации эмбрионов позволило не только повысить кумулятивную частоту наступления беременностей, но и снизить риски развития синдрома гиперстимуляции яичников.
Обоснована целесообразность выполнения криоконсервации на конечной стадии развития эмбрионов и необходимость использования лазерного хетчинга как способов, повышающих частоту наступления беременностей и, следовательно, эффективность программ ВРТ, проводимых с процедурой криоконсервации эмбрионов.
Проведенная оценка особенностей течения беременности и перинатальных исходов с выделением групп высокого риска гестационных осложнений может быть использована для отработки подходов к ведению беременности и родов у женщин после программ ВРТ и профилактики нежелательных результатов.
Основные положения, выносимые на защиту
1. Учитывая многофакторность причин бесплодия, большие различия в характере и течении фоновой гинекологической патологии, разнообразие использованных ранее методов лечения, требуется дифференцированный подход к выбору метода ВРТ, что подразумевает избирательное предпочтение агонистов (проведение «длинных» и «супердлинных» протоколов) или антагонистов ГнРГ.
2. Степень распространения НГЭ оказывает значительное влияние на эффективность программ ВРТ. При тяжёлых степенях НГЭ и сохраненном овариальном резерве следует отдавать предпочтение «длинным» и «супердлинным» протоколам с применением агонистов ГнРГ, при сниженном овариальном резерве препаратами выбора являются антагонисты ГнРГ.
3. При бесплодии, связанном с СПКЯ, выбор протокола во многом зависит от ранее проводимого лечения: у больных с оперативными вмешательствами на яичниках лучший эффект достигается при использовании агонистов ГнРГ, при интактных яичниках целесообразнее применение антагонистов ГнРГ.
4. Выбор протокола контролируемой стимуляции суперовуляции и её стартовой дозы должен основываться на правильной оценке овариального резерва. Наиболее информативным показателем овариального резерва и эффективным прогностическим критерием программ ВРТ является оценка концентрации в сыворотке крови антимюллерова гормона.
5. Метод криоконсервации эмбрионов повышает кумулятивную частоту наступления беременности в программах ВРТ. Важными условиями метода являются криоконсервация материала на стадии бластоцисты и использование метода лазерного хетчинга перед переносом размороженного эмбриона в полость матки.
6. Течение беременностей, индуцированных с помощью ВРТ, часто осложняется невынашиванием в разные сроки (самопроизвольный аборт, преждевременные роды), задержкой развития плода, гестозом. Частота указанных осложнений выше при многоплодной беременности. Преимущественным методом родоразрешения является плановая операция кесарева сечения по совокупности показаний (старший репродуктивный возраст, отягощённый акушерский анамнез, фоновая гинекологическая патология, длительное бесплодие, осложненное течение беременности).
Апробация и внедрение результатов работы в практику. Материалы диссертации доложены на конгрессах: «Новые технологии в акушерстве и гинекологии» – III Международный научный конгресс, Санкт–Петербург, 2007; VI Московская ассамблея «Здоровье столицы», Москва, 2007; Международные конференции Российской ассоциации репродукции человека «Репродуктивные технологии сегодня и завтра», 2000, 2006.
Основные положения диссертации внедрены в работу отделений ВРТ НИИАГ им. СЗО РАМН, Центр планирования семьи, г. Пушкин, «Городской Мариинской больницы» и клиники «АВА-ПЕТЕР», г. Санкт–Петербург, в учебный процесс кафедры репродуктивного здоровья женщин ГОУ ДПО СПб МАПО, в практическую работу сети Международных клиник «АВА».
По теме диссертации опубликованы 33 научные работы, в том числе 11 – в рецензируемых научных журналах и изданиях, определенных ВАК РФ.
Структура и объем диссертации. Диссертация состоит из введения, обзора литературы, трех глав по результатам собственных исследований, обсуждения полученных результатов, выводов, практических рекомендаций, списка использованной литературы, включающего 116 отечественных и 242‑зарубежных источников. Материалы диссертации изложены на 259 страницах машинописного текста, иллюстрированы 49 таблицами, 12 рисунками.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования
Для решения поставленных задач обследовано 698 пациенток репродуктивного возраста от 22 до 40 лет, из которых 48 женщин были с гиперплазией коры надпочечников с поздним началом, 81– с синдромом поликистозных яичников, 65 – с гиперпролактинемией, 84 – с трубно-перитонеальным фактором бесплодия, 73 – с НГЭ I-II степени распространения, 68 – с НГЭ III-IV степени распространения. Циклы подготовки к переносу криоконсервированных эмбрионов выполнены у 279 пациенток.
Программа исследования включала общее клиническое и гинекологическое обследование, неоднократное эхографическое исследование (ультразвуковой аппарат «Medison-8000» с использованием трансвагинального датчика частотой 7,5 Мгц). У всех пациенток согласно данным менструального цикла проведено исследование гормонов сыворотки крови: фолликулостимулирующий гормон, лютеинизирующий гормон, эстрадиол, пролактин, 17-оксипрогестерон, тиреотропный гормон, по показаниям – другие гормоны. Для оценки овариального резерва определяли антимюллеровый гормон (АМГ).
Контролируемую стимуляцию суперовуляции (КСС) проводили препаратами рекомбинантных гонадотропинов (Гонал-Ф, Пурегон). Стартовую дозу подбирали в зависимости от показателей овариального резерва.
Использовали следующие протоколы стимуляции:
– «длинный» протокол с применением ежедневных форм а-ГнРГ, введение которых начинали на 19-21 день менструального цикла и продолжали далее с последующей стимуляцией суперовуляции гонадотропинами;
– «супердлинный» протокол с предварительным введением депо-форм агонистов ГнРГ или назального спрея (Бусерелин) в течение 3-х месяцев и дальнейшем введении препаратов гонадотропинов.
– протокол с использованием антагонистов ГнРГ. Гонадотропины начинали вводить со 2-3 дня менструального цикла, при достижении лидирующим фолликулом диаметра 14 мм начинали введение антагонистов ГнРГ (оргалутран, цетротид).
Остальные этапы программы ВРТ, включавшие трансвагинальную пункцию фолликулов, оплодотворение и культивирование эмбрионов, перенос эмбрионов в полость матки, криоконсервацию оставшихся эмбрионов «хорошего» качества, ведение посттрансферного периода осуществлялись по общепринятым методикам. При переносе размороженных эмбрионов проводили лазерный хетчинг.
Статистическая обработка результатов исследования
Статистическую обработку данных проводили с помощью интегрированной системы статистического анализа. Расчет парного критерия Стъюдента и непараметрического критерия Пирсона производился для оценки достоверности различий между средними значениями количественных и абсолютными значениями качественных показателей в сравниваемых группах. Использовали стандартный пакет программ прикладного статистического анализа (Statistica for Windows v.6.0). Критический уровень достоверности нулевой статистической гипотезы (об отсутствии значимых различий или факторных влияний) принимали равным 0,05.
Результаты исследований
Трубно-перитонеальный фактор бесплодия: беременность наступила у 33 из 84 пациенток, что составило 44±5,7% в расчете на перенос эмбриона.
Показатели фолликуло-и эмбриогенеза при использовании агонистов и антагонистов ГнРГ (соответственно, 45 и 39 циклов) не имели статистически достоверной разницы, хотя отмечена тенденция к увеличению числа фолликулов, ооцитов и эмбрионов высокого качества на агонистах ГнРГ. Это увеличивало возможности выбора эмбрионов для их переноса и криоконсервации при необходимости дальнейшего использования.
Синдром гиперстимуляции яичников (СГЯ) II-III степени тяжести также чаще развивался у пациенток, находившихся на протоколе с использованием агонистов ГнРГ (соответственно 7,5±4,7% по сравнению с 5,7±3,9% у пациенток, находившихся на протоколе с антагонистами ГнРГ).
Частота наступления беременности статистически не различалась при использовании протоколов с агонистами и антагонистами ГнРГ, хотя также имелась тенденция к повышению ЧНБ при использовании агонистов ГнРГ. Частота наступления беременности на стимулированный цикл (ЧНБсц) и частота наступления беременности на перенос эмбриона (ЧНБпэ) составила соответственно 40,0±7,3% и 45,0±7,8% по сравнению с таковой у получавших антагонисты ГнРГ (соответственно, 38,4±7,7% и 42,8±8,3%). Частота родов (ЧР) также достоверно не различалась при использовании агонистов и антагонистов ГнРГ.
Оценка показателей овариального резерва проведена у 56 пациенток этой группы. Отмечена высокая корреляция АМГ с другими показателями овариального резерва, а именно с числом антральных фолликулов, с базальной концентрацией фолликулостимулирующего гормона (ФСГ). Статистически достоверная разница в концентрации базального ФСГ получена в подгруппах пациенток с АМГ<1 нг/мл и АМГ>2,5 нг/мл, она составила, соответственно, 10,4 ±0,8 и 3,8±1,2 МЕ/л (р<0,01). Концентрация базального эстрадиола в сыворотке крови имеет меньшее значение, так как не выявлено прямой корреляции между эстрадиолом и АМГ, числом антральных фолликулов и базальными концентрациями ФСГ.
Анализ концентрации АМГ показал, что у пациенток с самым низким значением АМГ 0,8±0,1 нг/мл было самое меньшее число антральных фолликулов (4,4±0,4); отмечен самый высокий уровень базального ФСГ (10,4±0,8 МЕ/л) и была использована самая большая стартовая доза ФСГ (278,4±9,0 МЕ) (Табл.1).
При средних значениях АМГ 2,3±0,2 нг/мл исследуемые показатели были благополучнее: число антральных фолликулов составило 10,3±0,3; базальная концентрация ФСГ была ниже (4,5±0,2 МЕ/л), а концентрация эстрадиола – не отличалась от таковой в других подгруппах (317,6±71,7 пмоль/л). При этом стартовая доза ФСГ оказалась меньше (215,9±4,6 МЕ). Полученные данные позволяют сделать вывод о необходимости и целесообразности подбора стартовой дозы ФСГ с учетом показателей функционального резерва яичников, и в частности, показателя АМГ, который фактически определяет ответ на стимуляцию и степень риска развития СГЯ. Правильный подбор стартовой дозы рекомбинантного ФСГ позволяет, с одной стороны, снизить риск избыточного ответа на КСС и тем самым избежать развития СГЯ, с другой стороны, предотвратить возможный «бедный» ответ на стимуляцию, что, как известно, снижает эффективность программ ВРТ.
Анализ результатов КСС и исходов ВРТ показал, что наименьшее число ооцитов (4,1±0,4) и самая низкая частота наступления беременности в расчете на перенос эмбрионов, а именно, 25,0±12,5% получены у пациенток со значениями АМГ, равными 0,8±0,1 нг/мл. У пациенток с концентрацией АМГ от 1 до 2,5 нг/мл число полученных ооцитов составило 9,2±0,5, ЧНБпэ – 37,9±9,0%. У пациенток с более высоким уровнем АМГ (>2,5 нг/мл) исследуемые показатели были самыми лучшими: число ооцитов составило 15,3±0,9, а ЧНБпэ достигла 46,6±12,8% (Табл.1).
Таким образом, у пациенток с трубно-перитонеальным фактором бесплодия эффективность ВРТ в меньшей степени зависела от использованного протокола стимуляции, а в большей степени – от исходного овариального резерва, оцениваемого по разным показателям включая определение АМГ как наиболее информативного из них.
Пациентки с СПКЯ были разделены на две подгруппы в зависимости от проводимого и не проводимого ранее оперативного вмешательства на яичниках. Основанием для такого подхода явились разноречивые данные литературы, где отмечены как преимущества использования у пациенток с СПКЯ протоколов с антагонистами ГнРГ (, 2000; , 2008; River J., 2003), так и отсутствие таких преимуществ в сравнении с агонистами ГнРГ (Grisinger G., 2003). Поэтому нашей целью явилось исследование влияния обеих вариантов протоколов (т. е. с применением агонистов и антагонистов ГнРГ) с учетом исходного состояния яичников.
Результаты КСС оказались следующими. При использовании «длинного» протокола с агонистами ГнРГ у пациенток с СПКЯ исходы КСС оказались несколько лучше в группе без предшествующих оперативных вмешательств на яичниках: меньшей оказалась потребность в рекомбинантном ФСГ (2124±95 против 2650±112 МЕ), было получено большее число аспирированных фолликулов размерами более 14 мм (15,6±1,6 против 11,5±1,5 в протоколах с антагонистами ГнРГ), большее число ооцитов (12,7±1,3 против 9,8±0,8) и большее число эмбрионов высокого качества (9,3±0,6 против 6,2±0,3 в протоколах с антагонистами ГнРГ). У пациенток с интактными яичниками в отличие от оперированных больных наилучшие результаты были получены при применении протокола с антагонистами ГнРГ в индивидуальном режиме. ЧНБсц у них составила 35±10,6%, ЧНБпэ равнялась 41,2±11,9%, ЧРсц составила 25±9,6%, ЧРпэ равнялась 29,4±11% (p>0,05).
При использовании протокола КСС с антагонистами ГнРГ, ответ у оперированных пациенток оказался хуже, чем ответ на «длинный» протокол с агонистами ГнРГ: было получено значительно меньшее количество аспирированных фолликулов размером >14 мм (8,9±1,2 против 11,5±1,5), меньшее число ооцитов (7,3±1,1 против 9,8±0,8) и меньшее число эмбрионов высокого качества (3,6±0,8 против 6,2±0,3). Значительно выше, чем в группе с агонистами ГнРГ, оказалась частота «бедного» ответа на попытку ВРТ (26,3±19,6% против 17,4±7,9%).
Сравнение дальнейших результатов двух указанных протоколов не выявило их достоверных различий так, соответственно на агонистах и антагонистах ГнРГ ЧНБсц равнялась 34,7±9,9% и 31,5±10,6%, ЧНБпэ равнялась 38,0±10,5% и 35,3±11,5%. Частота родов в расчете на перенос эмбриона (ЧРпэ) оказалась в обеих группах примерно одинаковой, т. е. 26,0±9,1% и 26,3±10,1% и 28,5±9,8% и 29,4±11%.
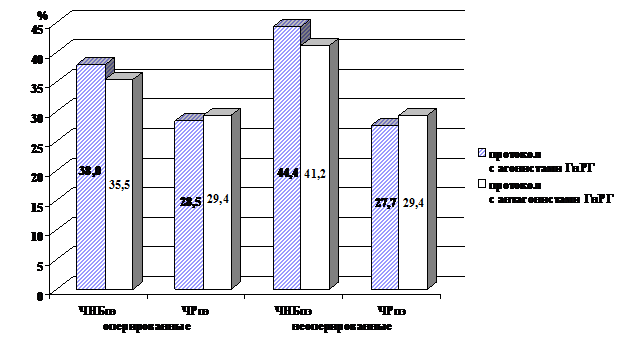
Рис. 1. Эффективность программ ВРТ у пациенток с СПКЯ
Независимо от проводимого протокола с агонистами или антагонистами ГнРГ частота синдрома гиперстимуляции яичников в 1,4‑1,9 раза была выше у пациенток с интактными яичниками при СПКЯ по сравнению с оперированными пациентками. Очевидно, что разрушение или удаление яичниковой ткани снижает овариальный резерв и ограничивает вероятность развития СГЯ.
Таким образом, представленные данные показывают, что у пациенток с СПКЯ и интактными яичниками терапевтический потенциал при ВРТ в большей степени реализуется при использовании протоколов с антагонистами ГнРГ, в отличие от больных, ранее оперированных по поводу СПКЯ, у которых более оправдано применение стандартного длинного протокола. Кроме того, у пациенток с интактными яичниками протокол с антагонистами ГнРГ также более соответствует критериям безопасности.
В целом показатели овариального резерва у пациенток с СПКЯ обеих подгрупп по сравнению с другими группами оказались самыми высокими так, концентрация АМГ составила 5,94±0,6 нг/мл у пациенток, получавших агонисты ГнРГ и 6,37±0,5 нг/мл у пациенток, которым применяли антагонисты ГнРГ. С этими данными коррелировали другие показатели овариального резерва: число антральных фолликулов равнялось 15,7±0,9 в подгруппе, проведенной с использованием агонистов ГнРГ и 16,4±0,7 у пациенток, проведенных на протоколе с антагонистами ГнРГ.
У пациенток с СПКЯ отмечен самый высокий овариальный резерв. Концентрация АМГ<1 нг/мл имелась только у 4-х из 57 пациенток с СПКЯ (7,0±3,3%). У всех отмечали в анамнезе оперативные вмешательства на яичниках.
При концентрации АМГ 1,7±0,3 нг/мл число антральных фолликулов было достаточно высоким (12,6±0,7), концентрация ФСГ на 3-5 день менструального цикла была нормальной (5,9±0,7 МЕ/л), а концентрация эстрадиола составила 573,2±137,6 пмоль/л. При этом использована достаточно низкая стартовая доза ФСГ (122,0±6,7 МЕ). В среднем было получено 11,4±0,8 ооцитов, а ЧНБпэ составила 41,6±14,2%.
При концентрации АМГ 5,4±0,2 нг/мл число антральных фолликулов было самым высоким (21,3±0,8), концентрация ФСГ на 3-5 день менструального цикла у этих пациенток была 4,6±0,2 МЕ/л, а концентрация эстрадиола – 512,5±54,3 пмоль/л. Стартовая доза рекомбинантного ФСГ была самой низкой (98,6±1,8 МЕ), а ЧНБпэ – самой высокой (43,9±7,7%).
Анализ критериев безопасности показал, что при концентрации АМГ<1 нг/мл фактически отсутствует риск развития СГЯ, при концентрации АМГ от 1 до 2,5 нг/мл этот риск достаточно низкий: нами отмечен только 1 случай развития СГЯ (8,3±7,9%). При высоких концентрациях АМГ (>2,5 нг/мл) риск развития СГЯ повышался (12,2±5,1%).
Полученные нами данные свидетельствуют о прямой корреляции концентрации АМГ с вероятностью ответа на контролируемую стимуляцию яичников, что может быть использовано как для прогноза результатов, так и для выбора оптимального протокола, подбора стартовой дозы гонадотропина и снижения риска развития СГЯ. Полагаем, что концентрацию АМГ необходимо учитывать в совокупности с другими показателями овариального резерва, в частности с базальной концентрацией ФСГ и числом антральных фолликулов. Концентрация эстрадиола имеет относительное значение: не выявлено прямой корреляции между базальной концентрацией эстрадиола и другими показателями овариального резерва у пациенток с СПКЯ.
Гиперплазия коры надпочечников с поздним началом как причина бесплодия отмечена у 48 больных. Все дополнительно получали терапию дексаметазоном (250-500 мкг в сутки) в течение 1-2х месяцев перед ВРТ.
Сравнение показателей эффективности двух протоколов контролируемой стимуляции суперовуляции с агонистами и антагонистами ГнРГ показало, что ЧНБсц и ЧНБпэ статистически не различалась, соответственно составили 39,1±10,1% и 42,8±10,8% (использование агонистов ГнРГ) и 40,0±9,7% и 43,4±10,3% (использование антагонистов ГнРГ).
Частота родов в расчете на перенос эмбриона также достоверно не различалась и составила 28,5±9,8% при назначении агонистов ГнРГ и 30,0±9,5% при использовании антагонистов ГнРГ.
В группе больных с гиперплазией коры надпочечников с поздним началом отмечен достаточно высокий овариальный резерв. Концентрация АМГ составила соответственно 2,82±0,5 нг/мл у пациенток, получивших протокол с агонистами ГнРГ и 2,91±0,4 нг/мл у пациенток, получивших протокол с антагонистами ГнРГ. Эти данные коррелировали с другими показателями овариального резерва, т. е. с числом антральных фолликулов 14,3±1,2 и 11,3±1,3, а также с базальной концентрацией ФСГ, которая составила 7,2±0,6 МЕ/л и 6,2±0,5 МЕ/л (соответственно, пациентки, находившиеся на протоколе с агонистами и антагонистами ГнРГ).
Несмотря на достаточно высокий овариальный резерв у пациенток с гиперплазией коры надпочечников, его оценка с помощью АМГ выявила зависимость, отмеченную ранее в других группах. Так, при концентрации АМГ 0,57±0,4 нг/мл число антральных фолликулов оказалось наименьшим (3,9±0,6), показатели фолликулогенеза низкими, стартовая доза самой высокой, а ЧНБпэ у этих пациенток была 20,0±17,8% (табл. 1).
Таблица 1
Зависимость стартовой дозы ФСГ от уровня АМГ и других показателей овариального резерва у пациенток с трубно-перитонеальным бесплодием, СПКЯ, ГКН с поздним началом, гиперпролактинемией
Показатель | АМГ<1 нг/мл | АМГ 1-2.нг/мл | АМГ >2 нг/мл | р | |
Трубно-перитонеальное бесплодие | n=12 | n=29 | n=15 | ||
Возраст | 36,7±3,1 | 32,4±2,8 | 31,8±2,3 | >0,05 | |
Базальная концентрация ФСГ, МЕ/л | 10,4±0,8* | 4,5±0,2 | 3,8±1,2* | >0,05 | |
Число антральных фолликулов | 4,4±0,4 | 10,3±0,3 | 16,4±0,8 | <0,01 | |
Концентрация АМГ, нг/мл | 0,8±0,1 | 2,3±0,2 | 3,8±0,7 | <0,01 | |
Стартовая доза ФСГ, МЕ | 278,4±4,5 | 215,9±3,6 | 132,1±3,8 | <0,01 | |
Число ооцитов | 4,1±0,4 | 9,2±0,5 | 15,3±0,9 | <0,05 | |
Число беременностей (ЧНБпэ) | 3 (25,0±12,5%) | 11 (37,9±9,0%) | 7 (46,6±12,85) | >0,05 | |
СГЯ II-III степени | 0 | 1 (3,4±2,3%) | 2 (13,3±8,7%) | >0,05 | |
СПКЯ | n=4 | n=12 | n=41 | ||
Возраст | 34,5±2,1 | 33,2±2,4 | 31,7±1,9 | >0,05 | |
Базальная концентрация ФСГ, МЕ/л | 11,3±0,4 | 5,9±0,7 | 4,6±0,2 | <0,05 | |
Число антральных фолликулов | 3,25±0,9 | 12,6±0,7 | 21,3±0,8 | <0,01 | |
Концентрация АМГ, нг/мл | 0,8±0,1 | 1,7±0,3 | 5,4±0,2 | <0,01 | |
Стартовая доза ФСГ, МЕ | 275,0±12,1 | 122,0±6,7 | 98,6±1,8 | <0,01 | |
Число ооцитов | 2,7±0,7 | 11,4±0,8 | 18,6±0,8 | <0,01 | |
Число берем./ЧНБпэ М±m% | 0 | 5/41,6±14,2% | 18/43,9±7,7% | >0,05 | |
СГЯ II-III степени | 0 | 1 (8,3±7,9%) | 5 (12,2±5,1%) | >0,05 | |
ГКН с поздним началом | n=5 | n=18 | n=8 | ||
Возраст | 34,4±2,3 | 35,1±2,8 | 35,6±2,0 | >0,05 | |
Базальная концентрация ФСГ, МЕ/л | 9,9±1,5* | 7,4±0,8 | 6,1±1,2* | <0,05* | |
Число антральных фолликулов | 3,9±0,6 | 15,1±0,3 | 18,4±1,8 | <0,01 | |
Концентрация АМГ, нг/мл | 0,57±0,4 | 1,92±0,8 | 3,3±0,9 | <0,01 | |
Стартовая доза ФСГ, МЕ | 264,3±9,8 | 186,7±4,9 | 118,7±9,3 | <0,01 | |
Число ооцитов | 3,4±0,4 | 12,5±0,5 | 14,2±1,8 | <0,01 | |
Число берем./ЧНБпэ М±m% | 1/20,0±17,8% | 8/44,4±11,7% | 4/50,0±17,6% | >0,05 | |
СГЯ II-III степени М±m% | 0 | 0 | 1/12,5±11,7% | >0,05 | |
Гиперпролактинемия | n=9 | n=28 | n=12 | ||
Возраст | 37,0±1,2 | 34,6±0,7 | 33,5±1,3 | >0,05 | |
Базальная концентрация ФСГ, МЕ/л | 9,2±1,2 | 5,4±0,4 | 5,1±0,8 | <0,01 | |
Число антральных фолликулов | 4,1±0,6 | 9,5±0,5 | 14,8±0,9 | <0,01 | |
Концентрация АМГ, нг/мл | 0,75±0,5* | 1,7±0,1 | 3,1±0,4* | <0,01* | |
Стартовая доза ФСГ, МЕ | 259,7±11,2 | 223,5±7,1 | 174,6±9,0 | <0,01 | |
Число ооцитов | 3,8±0,4 | 8,2±1,1 | 12,1±1,9 | <0,01 | |
Число берем./ЧНБпэ М±m% | 3/33,3±15,7% | 11/39,2±9,2% | 5/41,6±14,2% | >0,05 |
При уровне АМГ от 1 до 2,5 нг/мл число антральных фолликулов соответствовало 15,1±0,3 и стартовые дозы рекомбинантного ФСГ были средними (186,7±6,5 МЕ). Число полученных ооцитов оказалось достаточно высоким (12,5±0,5), а ЧНБпэ составила 44,4±11,7%. При концентрации АМГ>2,5 нг/мл число антральных фолликулов оказалось наиболее высоким (18,4±1,8), базальная концентрация ФСГ составила 6,1±1,2 МЕ/л. Стартовая доза рекомбинантного ФСГ оказалась меньше, чем в других подгруппах (118,7±6,3 МЕ). Число ооцитов было наибольшим (14,2±1,8), ЧНБпэ составила 50,0±17,6% (Табл. 1).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |




