На правах рукописи
ОСОБЕННОСТИ ПРОГРАММ ВСПОМОГАТЕЛЬНЫХ РЕПРОДУКТИВНЫХ ТЕХНОЛОГИЙ У ПАЦИЕНТОК С ИЗБЫТОЧНОЙ МАССОЙ ТЕЛА И ОЖИРЕНИЕМ
14.01.01 – «Акушерство и гинекология»
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
Москва – 2010
Работа выполнена в ГОУ ДПО «Российская медицинская академия последипломного образования» Росздрава
Научный руководитель:
доктор медицинских наук, профессор
Официальные оппоненты:
доктор медицинских наук, профессор
доктор медицинских наук, профессор Хашукоева Асият Зульчифовна
Ведущая организация: ГУЗ «Московский областной научно-исследовательский институт акушерства и гинекологии» Минздрава Московской области
Защита состоится «__» __________ 2010 года в ____ часов на заседании диссертационного Совета Д208.041.06 при ГОУ ВПО «Московский государственный медико-стоматологический университет» Федерального агентства по здравоохранению и социальному развитию Москва, ул. Делегатская, д.20/1.
С диссертацией можно ознакомиться в библиотеке Московского государственного медико-стоматологического университета ( Москва, ул. Вучетича, д. 10а).
Автореферат разослан «__» ___________ 2010 г.
Ученый секретарь диссертационного совета,
доктор медицинских наук, профессор
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы
Вопросы диагностики и лечения бесплодного брака относятся к числу актуальных проблем современной медицинской науки и практики. Частота бесплодного брака в России составляет 15-17%, при том, что показатель, равный 15% является критическим, и проблема бесплодия приобретает государственное значение [, 2001; Nieto A., 2006.].
Важнейшим и принципиальным этапом в лечении бесплодия стали разработка и внедрение в клиническую практику методов вспомогательных репродуктивных технологий (ВРТ).
Наряду с проблемой бесплодия в последние годы отмечается неуклонный рост ожирения. По предварительным данным, в России не менее 30% трудоспособного населения имеют избыточную массу тела и 25% - ожирение [, 2004]. Эти данные в совокупности с данными других стран позволяют говорить о существовании глобальной «эпидемии» ожирения.
Увеличение количества женщин с избыточной массой тела и ожирением приводит к тому, что всё чаще индукцию суперовуляции в рамках экстракорпорального оплодотворения (ЭКО) проводят на фоне имеющихся метаболических нарушений. В то же время ожирение само по себе очень часто приводит к нарушению менструальной и детородной функции женщины. Увеличение массы жировой ткани выше нормы на 20% и более вызывает дисфункцию гипоталамо-гипофизарно-яичниковой системы. При ожирении в 2-5 раз чаще возникают различные формы нарушений менструального цикла, такие как олигоменорея и аменорея, повышается частота маточных кровотечений и патологии эндометрия [, 2002]. Ожирение, особенно андроидного типа, является одним из главных факторов риска развития яичниковой гиперандрогении, при этом более чем у одной трети женщин может формироваться синдром поликистозных яичников (СПКЯ). Частота бесплодия у женщин с ожирением составляет 33,6% по сравнению с 18,6% женщин с нормальной массой тела [Lake J., 1997]. Также значительно снижается эффективность различных видов терапии, направленной на восстановление фертильности.
Имеющиеся в современной литературе данные о влиянии ожирения на эффективность программ ВРТ немногочисленны, но весьма актуальны [Fedorcsak P., 2004; Metwally M., 2007; Bellver J., 2009]. Перспективным является изучение гормональных и метаболических нарушений у пациенток с бесплодием и ожирением, разработка методов предварительной подготовки к ЭКО и оптимизация схем индукции суперовуляции, что позволит повысить эффективность использования ВРТ у данной категории пациенток.
Цель исследования
Повысить эффективность и безопасность программ вспомогательных репродуктивных технологий у пациенток с избыточной массой тела и ожирением путем разработки наиболее оптимального протокола индукции суперовуляции.
Задачи исследования
1. Оценить исходное состояние репродуктивной системы, гормональные и метаболические показатели у пациенток ожирением и бесплодием, нуждающимся в лечении методами вспомогательных репродуктивных технологий.
2. Изучить особенности индукции суперовуляции у пациенток с ожирением.
3. Выявить варианты ожирения, наиболее неблагоприятные для успешной реализации экстракорпорального оплодотворения.
4. Разработать наиболее эффективный и безопасный протокол индукции суперовуляции с целью оптимизации программ вспомогательных репродуктивных технологий у пациенток с избыточной массой тела и ожирением.
Научная новизна
Впервые в России выполнено исследование по оценке влияния избыточной массы тела и ожирения на программы ВРТ. В рамках диссертационной работы была изучена зависимость исходов ЭКО от степени и типа ожирения, наличия СПКЯ и метаболического синдрома (МС). Научную новизну имеют полученные данные, указывающие на отсутствие зависимости сопряженной с ожирением овуляторной дисфункции от степени выраженности ожирения. Доказана определяющая роль характера распределения жировой ткани в возникновении эндокринно-метаболических расстройств у пациенток с бесплодием и ожирением. Показано, что наличие СПКЯ и МС является определяющим фактором в генезе нарушений эндокринной функции и, как следствие, бесплодия у больных с ожирением, что в значительной степени связано с инсулинорезистентностью, гиперинсулинемией и, возможно, лептинрезистентностью. У таких пациенток индукция суперовуляции сопровождалась более высоким риском синдрома гиперстимуляции яичников (СГЯ), а эффективность программ ВРТ оказалась более низкой, чем у пациенток без эндокринных и метаболических нарушений, что позволило сформировать группы риска по неудачным исходам лечения.
Новым аспектом работы является изучение динамики гормональных и метаболических показателей в процессе индукции суперовуляции и их связь с эффективностью и безопасностью ЭКО, что позволило определить прогностические факторы риска по неудачным исходам ВРТ и СГЯ у пациенток с ожирением.
Представлен новый подход к обследованию и ведению больных с ожирением и бесплодием, нуждающихся в лечении методами ВРТ. Оценка использования рекомбинантного фолликулостимулирующего гормона (ФСГ) и ганиреликса для индукции суперовуляции у пациенток с избыточной массой тела и ожирением была проведена впервые в мире.
Практическая значимость
Полученные в работе данные о характере эндокринно-метаболических нарушений у больных с бесплодием и ожирением, а также факторах, определяющих степень их выраженности, позволили сформулировать предложения по оптимизации программ ВРТ.
На основе выявления тесной взаимосвязи ожирения с гиперандрогенией обоснована целесообразность расширения спектра гормонального обследования больных как на этапе подготовки к программе ВРТ, так и в процессе индукции суперовуляции. Полученные данные о высокой частоте метаболических расстройств у пациенток с бесплодием и ожирением, а также их связь с неразвивающейся беременностью и неудачными исходами программ ВРТ доказывают необходимость включения в комплекс обследования больных изучения секреции инсулина и диагностики нарушений углеводного и липидного обмена.
Короткий протокол с антагонистами Гн-РГ и рекомбинантным ФСГ у пациенток с избыточной массой тела и ожирением позволяет достичь таких же результатов, как и при индукции суперовуляции у пациенток с нормальной массой тела.
Основные положения, выносимые на защиту
1. С увеличением индекса массы тела потребность в гонадотропинах и продолжительность стимуляции возрастает.
2. Андроидный тип ожирения в сочетании с СПКЯ и метаболическим синдромом снижает эффективность программ ВРТ и повышает риск синдрома гиперстимуляции яичников.
3. Использование рекомбинантного ФСГ и антагонистов Гн-РГ для индукции суперовуляции у пациенток с избыточной массой тела и ожирением позволяет получить высокую частоту наступления беременности при низком риске синдрома гиперстимуляции яичников.
Личное участие автора
Автором лично была проведена индукция суперовуляции у 64 пациенток, включенных в проспективную часть исследования. Проведен анализ 58 циклов индукции суперовуляции у 51 пациентки ретроспективной части исследования. В ходе сбора материала для диссертационной работы соискателем были освоены методики индукции суперовуляции, ультразвукового мониторинга, пункции фолликулов, переноса эмбрионов.
Внедрение в практику
Результаты исследования внедрены в клиническую практику и учебный процесс на курсах повышения квалификации врачей, тематических усовершенствованиях и семинарах, проводимых сотрудниками кафедры акушерства и гинекологии ГОУ ДПО РМАПО Росздрава. Основные рекомендации используются в практической деятельности Центра репродукции и генетики «ФертиМед» г. Москвы.
Апробация работы
Основные положения диссертации были доложены на XVIII ежегодной международной конференции Российской ассоциации репродукции человека «Репродуктивные технологии сегодня и завтра» (Самара, 2008 г.), на ХIV Международном конгрессе по гинекологической эндокринологии (Флоренция, 2010 г.) и на заседании кафедры акушерства и гинекологии ГОУ ДПО РМАПО Росздрава (Москва, 09.06.2010).
Публикации
По теме диссертации опубликовано 8 работ, в том числе 3 работы в журнале, рекомендованном ВАК Минобрнауки РФ для публикации материалов диссертационных исследований.
Структура и объем диссертации
Диссертационная работа написана по традиционному плану и состоит из введения, обзора литературы, описания материалов и методов исследования, глав, отражающих результаты собственных исследований, обсуждения полученных результатов, выводов, практических рекомендаций.
Диссертация изложена на 129 страницах компьютерного текста, иллюстрирована 10 рисунками, 6 диаграммами, 14 таблицами, содержит ссылки на 22 отечественных и 165 зарубежных научных трудов.
СОДЕРЖАНИЕ РАБОТЫ
Клиническая характеристика и методы обследования больных
Были проанализированы результаты 58 циклов индукции суперовуляции у 31 пациентки с избыточной массой тела и ожирением (ср. возраст 33,3±3,9 лет, индекс массы тела (ИМТ) 30,8±3,6 кг/м2) и у 20 женщин с нормальной массой тела (ср. возраст 31,2±3,6 лет, ИМТ 20,7±1,6 кг/м2). Индукция суперовуляции у всех пациенток осуществлялась по длинному протоколу с агонистами Гн-РГ (трипторелином) и человеческими менопаузальными гонадотропинами (чМГ). При анализе результатов исследования все пациентки подразделялись на подгруппы в зависимости от степени и типа ожирения, наличия или отсутствия СПКЯ и МС.
Затем с учетом особенностей индукции суперовуляции у пациенток с избыточной массой тела и ожирением был предложен более оптимальный протокол индукции суперовуляции, эффективность и безопасность которого была исследована в проспективной части исследования, в которую вошли 32 пациентки с избыточной массой тела и ожирением (ср. возраст 30,6±4,6 лет, ИМТ 30,6±3,9 кг/м2) и 32 женщины с нормальной массой тела (ср. возраст 29,8±3,7 лет, ИМТ 20,0±1,9 кг/м2). Индукцию суперовуляции осуществляли фоллитропином-β, который пациентки вводили самостоятельно с помощью шприц-ручки, и антагонистами Гн-РГ (ганиреликсом).
Критериями включения были возраст моложе 38 лет, отсутствие вмешательств на яичниках, не более трех неудачных попыток ЭКО в анамнезе. Критериями исключения явились наличие противопоказаний к индукции суперовуляции и уровень ФСГ более 12 МЕ/л.
Ожирение и степень его выраженности диагностировались на основании величины ИМТ (ВОЗ, 1997 г.), СПКЯ − на основании критериев Роттердамской конференции (2003 г), а МС − согласно критериям Международной федерации диабета (2005 г).
У всех участников исследования проводилось комплексное обследование, которое включало следующие этапы:
- Клинико-анамнестическое исследование:
· подробное изучение соматического и гинекологического анамнеза;
· объективное исследование.
- Лабораторные исследования
· до начала стимуляции (ФСГ, ЛГ, 17-гидроксипрогестерон, дегидроэпиандростерона сульфат (ДГЭА-С), тестостерон, ПССГ, лептин, иммунореактивный инсулин (ИРИ), глюкоза, липидный спектр - холестерин, триглицериды, ЛПНП, ЛПВП);
· в конце стимуляции (тестостерон, эстрадиол, лептин, ИРИ, глюкоза).
- Ультразвуковое исследование органов малого таза до начала лечения и в процессе индукции овуляции (ультразвуковой мониторинг).
- Анкетирование (оценка безопасности и удобства шприц-ручки для введения фоллитропина-β).
- Статистические методы обработки полученных данных («Statistica-6»): были использованы критерии Вилкоксона (для связанных групп), Манна-Уитни и метод Краскела-Уоллиса (для несвязанных групп), корреляционный анализ Спирмана. Для оценки различий между качественными показателями использовали метод χ2, χ2 с поправкой Йетса при абсолютных частотах менее 10, а также односторонний критерий Фишера для небольших выборок (менее 5).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Анализ комплексного клинико-лабораторное обследования пациенток ретроспективной части исследования показал, что в 48,4% ожирение сопровождается нарушениями менструального цикла. Основными тенденциями в развитии этих нарушений стали гиперандрогения, хроническая ановуляция и формирование СПКЯ, что, в конечном счете, и привело, к бесплодию. У таких пациенток преобладал андроидный тип распределения жировой ткани (в 73,3%), а степень ожирения не оказывала влияния на частоту и выраженность нарушений ритма менструаций. Олигоменорея доминировала в подгруппах пациенток с избыточной массой тела и ожирением I степени, а при ожирении II и III степени наблюдалась даже более благоприятная ситуация, при которой часто сохранялся регулярный ритм менструаций. Это вызвало некоторое удивление, поскольку традиционно выраженность нарушений менструального цикла связывают со степенью ожирения. Хотя известны и другие факты, согласно которым женщины с ожирением часто имеют регулярный ритм менструации и сохраненную фертильность, которая не зависит от степени выраженности ожирения [Diamanti-Kandarakis E., 2001]. Низкую частоту овуляторной дисфункции у пациенток с ожирением высокой степени можно объяснить тем, что у этих пациенток преобладал феминный тип распределения жировой ткани, а у пациенток с избыточной массой тела и ожирением I степени – андроидный тип. У каждой четвертой пациентки СПКЯ сочетался с МС, что вполне закономерно. В последние годы появился целый ряд публикаций, утверждающих, что ведущим патогенетическим механизмом СПКЯ является именно инсулинорезистентность - основной маркер метаболического синдрома [, 2006]. С учетом того, что МС встречался и у женщин без СПКЯ, пациентки с метаболическими нарушениями были выделены в отдельную подгруппу. У 51,6% пациенток ожирение не сопровождалось ни СПКЯ, ни МС, менструальный цикл был регулярный и овуляторный. Эти пациентки составили подгруппу с так называемым «простым» ожирением, при этом ожирение лишь сопутствовало бесплодию.
Анализ средних значений гормональных показателей у пациенток проспективной части исследования показал, что андроидное ожирение сопровождается более высокой степенью андрогенизации. Это выражалось в тенденции к более высокому уровню ЛГ, тестостерона и ДГЭА-С, а также в снижении уровня ПССГ, что отражалось в повышении биодоступности андрогенов и достоверно более высоком индексе свободного тестостерона (ИСТ).
Инсулинорезистентность была выявлена у 46,8% пациенток основной группы. Корреляции между окружностью талии (ОТ) и ИРИ (ρ=0,284, p<0,05) и ОТ и индексом Homa (ρ =0,269, p<0,05) свидетельствуют о взаимосвязи ожирения с нарушениями углеводного обмена. У 78,1% пациенток была выявлена дислипидемия.
У 87,5% пациенток основной группы наблюдалась гиперлептинемия, при этом по сравнению с пациентками с нормальной массой тела отмечалось 4-х кратное повышение уровня лептина. Наличие положительной связи между лептином и ИМТ (ρ =0,398; p=0,024), лептином и ИРИ (ρ =0,436; p<0,012) позволяет предположить, что лептин влияет на функцию яичников через гиперинсулинемию. Для определения относительной гиперлептинемии был использован показатель лептин/ИМТ. В нашем исследовании относительная гиперлептинемия была выявлена у 100% пациенток основной группы. Имеются данные, что значение индекса лептин/ИМТ больше или равное 0,7 сопровождается ухудшением результатов программ ВРТ [Brannian J. D., 2001]. У 96,9% женщин индекс лептин/ИМТ превышал 0,7, однако корреляции с исходами лечения мы не наблюдали.
У больных с ожирением и СПКЯ гормональные и метаболические нарушения оказались более выраженные, что согласуется с результатами других исследований [, 2007]. Так, средние уровни ЛГ, тестостерона и ИСТ в этой группе оказались достоверно более высокими (9,1±1,34 ME/л; 3,1±0,2 нмоль/л; 14,3±1,42%), чем у больных с «простым» ожирением (4,6±1,6 ME/л; 1,6±0,6 нмоль/л; 2,8±0,8%). Выявленные изменения можно объяснить более высокими уровнями ИРИ (15,3±2,9 мЕД/л) у больных с СПКЯ по сравнению с «простым» ожирением (9,4±3,3мЕД/л) и его ингибирующим влиянием на секрецию ПССГ. Частота инсулинорезистентности у пациенток с ожирением и СПКЯ оказалась довольно высокой - 77,7%. Уровень лептина в этой подгруппе больных также оказался значимо выше (54,7±12,3 нг/мл), чем у женщин с «простым» ожирением (41,6±10,1 нг/мл, р<0,05). Концентрация ИРИ и лептина при МС оказалась самой высокой (17,7±2,3 мЕД/л; 65,4±23,4 нг/мл соответственно). Таким образом, СПКЯ и МС являются определяющими факторами в генезе нарушений репродуктивной системы у больных с ожирением.
Выявленные подтипы позволили рассматривать пациенток с ожирением и бесплодием как неоднородную группу больных, имеющих разную степень гормональных и метаболических нарушений, что в какой-то степени объясняет разный характер результатов исследований, связанных с ожирением и ВРТ.
При анализе суммарной дозы гонадотропинов и продолжительности индукции суперовуляции оказалось, что с увеличением ИМТ возрастает потребность в гонадотропинах и увеличивается продолжительность стимуляции, а число полученных ооцитов снижается (табл.1).
Таблица 1. Параметры индукции суперовуляции в зависимости от степени ожирения (среднее ± стандартное отклонение)
Показатель | ИМТ 25-29,9 кг/м2, n =17 | ИМТ 30-34,9 кг/м2, n=9 | ИМТ ≥ 35 кг/м2, n=5 | p |
Количество циклов | 20 | 12 | 6 | |
Суммарная доза гонадотропинов, МЕ | 2427±539 | 3070±697 | 3687±889 | 0,02 |
Продолжительность стимуляции, дни | 11,5±1,7 | 12,0±2,8 | 13,8±1,6 | 0,243 |
Количество ооцитов | 18,3±9,3** | 11,6±7,4 | 8,6±3,8** | 0,063 |
Толщина эндометрия в день переноса эмбрионов (ПЭ), мм | 11,1±2,1 | 11,2±2,3 | 12,0±2,5 | 0,958 |
Возможно, это связано с тем, что избыточная масса тела снижает чувствительность к гонадотропинам. В литературе это явление описано под названием как «гонадотропинрезистентность». Считается, что множественное развитие фолликулов возможно только тогда, когда уровень циркулирующего ФСГ превышает определенный порог. По мнению Imani и соавт. (2002), у пациенток с ожирением пороговый эффект экзогенного ФСГ снижен, что приводит к росту меньшего числа фолликулов и требует более высокой дозы ФСГ. Однако, возможно, большая доза потребность в гонадотропинах обусловлена всего лишь необходимостью поддержания определенной концентрации экзогенного ФСГ на кг массы тела. У пациенток с ожирением и СПКЯ, а также при сочетании ожирения с МС было получено большее число ооцитов, чем у пациенток с «простым» ожирением (табл.2).
Таблица 2. Параметры индукции суперовуляции в зависимости от наличия или отсутствия метаболического синдрома и СПКЯ
Показатель | «Простое» ожирение, n=15 | Ожирение и МС, n=9 | Ожирение и СПКЯ, n=15 | р |
Суммарная доза гонадотропинов, МЕ | 2977±710 | 2481±625 | 2655±889 | 0,131 |
Продолжительность стимуляции, дни | 12,2±2,3 | 11,9±2,3 | 11,8±2,0 | 0,997 |
Количество ооцитов | 10,1±6,1 | 17,5±10,9 | 18,6±9,3 | 0,006 |
Количество эмбрионов | 4,9±2,1 | 8,3±5,7 | 7,2±5,2 | 0,372 |
Толщина эндометрия в день ПЭ, мм | 11,2±2,4 | 11,8±2,5 | 11,8±2,3 | 0,904 |
Некоторые авторы связывали неблагоприятное воздействие ожирения на исходы ВРТ с влиянием на эндометрий [Wattanakumtornkul, 2003], однако мы в своей работе не наблюдали статистически значимых различий между группами по толщине эндометрия в день переноса эмбрионов (ПЭ), что согласуется с данными более поздних исследований [Seung-Yup Ku, 2006].
В литературе встречаются сведения о более трудном выполнении пункции фолликулов и у пациенток с ожирением [Tamer E., 2009]. Мы полностью солидарны с авторами данной работы, так как увеличение слоя подкожно-жировой клетчатки, а также висцерального жира, особенно у пациенток с андроидным ожирением, снижало возможность мануальной фиксации яичника через переднюю брюшную стенку во время пункции фолликулов и ухудшало качество визуализации при ультразвуковом исследовании.
Что касается клинических исходов индукции суперовуляции, то оказалось, что наиболее неблагоприятными вариантами являются андроидное ожирение, сочетание ожирения с СПКЯ и МС, где частота имплантации была самая низкая и составила 17,6%, 16,2% и 11,1% соответственно. При феминном типе распределения жировой ткани и у пациенток с «простым» ожирением частота имплантации оказалась достаточно высокой (28% и 26,0% соответственно). Самая высокая частота имплантации (30,8%) оказалась у пациенток с ожирением высокой степени (ИМТ ≥ 35 кг/м2), где преобладали феминный тип распределения жировой ткани и «простое» ожирение. Такая же ситуация наблюдалась и относительно другого основного показателя эффективности лечения - частоты наступления клинической беременности. У пациенток с андроидным ожирением, при сочетании ожирения с СПКЯ и при МС частота наступления клинической беременности также оказалась самой низкой и составила всего 17,6%, 23,5% и 18,2% соответственно. При этом у пациенток с СПКЯ и МС исходно было получено большее число ооцитов, чем у пациенток с «простым» ожирением, однако многие клетки оказались незрелыми, что привело к более низкой частоте оплодотворения у этих подгрупп пациенток. Частота родов живым плодом у пациенток с андроидным ожирением была еще ниже - 11,8% (одна беременность оказалась неразвивающейся). При феминном типе распределения жировой ткани и у пациенток с «простым» ожирением частота наступления беременности была достаточно высокой (42,9% и 40% соответственно). У пациенток с ИМТ ≥ 35 кг/м2 частота наступления беременности оказалась самой высокой (66,6%), а в подгруппе с избыточной массой тела, где преобладали пациентки с андроидным ожирением, СПКЯ и МС, составила всего 25%. Низкая частота имплантации и, как следствие, более низкая частота наступления беременности у пациенток с МС и СПКЯ, по-видимому, связаны с влиянием гиперандрогении, гиперинсулинемии и, возможно, гиперлептинемии на ранние этапы имплантации.
Помимо эффективности чрезвычайно важным аспектом лечения является его переносимость и безопасность. Одним из наиболее серьезных осложнений индукции суперовуляции является СГЯ. Анализ ретроспективной части исследования, показал, что частота СГЯ (учитывались все степени его проявления) у пациенток с избыточной массой тела и ожирением, в целом, значимо выше, чем у пациенток с нормальной массой ,7% и 12,0% соответственно). Интересно было отметить, что с увеличением ИМТ частота СГЯ снижалась. Если у пациенток с ожирением высокой (II-III) степени не наблюдалось ни одного случая СГЯ, то у пациенток с избыточной массой тела она оказалась максимальной (40%), а частота СГЯ тяжелой степени при этом составила 5%. У пациенток с феминным ожирением частота СГЯ была значимо ниже, чем у женщин с андроидным ожирением (9,5% и 35,3% соответственно). Наиболее неблагоприятными факторами риска развития СГЯ оказались сочетание ожирения с СПКЯ и МС (диаграмма 1). Именно у пациенток последней подгруппы частота СГЯ оказалась самой высокой (45,5%). У женщин с «простым» ожирением частота СГЯ оказалась наименьшей (10%).
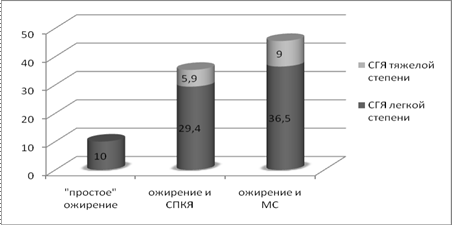
Диаграмма 1. Частота СГЯ (%) в зависимости от наличия или отсутствия СПКЯ и МС
Индукция суперовуляции ретроспективной части исследования проводилась по длинному протоколу с использованием чМГ, который содержит равное количество ФСГ и ЛГ. Препарат позволяет получить большое количество синхронно растущих ооцитов, обеспечивает хорошие показатели оплодотворения, имплантации и наступления беременности, однако сопровождается достаточно высоким риском СГЯ, особенно у пациенток с СПКЯ. Экзогенный ЛГ может дополнительно стимулировать синтез андрогенов, который и без того повышен у этой подгруппы пациенток. При инсулинорезистентности и гиперинсулинемии инсулин стимулирует собственные рецепторы и рецепторы инсулиноподобного фактора роста (ИПФР-1), увеличивает количество рецепторов к ЛГ в яичниках и оказывает ЛГ-подобное действие, что приводит к увеличению содержания андрогенов в фолликулярной жидкости и нарушает процессы фолликулогенеза. Логично предположить, что чистый ФСГ, лишенный активности ЛГ, может снизить риск СГЯ у этой группы пациенток. Именно по этой причине для индукции суперовуляции в проспективной части исследования был выбран рекомбинантный ФСГ (фоллитропин-b), а чтобы уменьшить продолжительность лечения и суммарную дозу гонадотропинов и риск СГЯ, был использован протокол с антагонистами Гн-РГ, которые в меньшей степени подавляют гипофиз, чем агонисты Гн-РГ. Антагонисты Гн-РГ также позволяют снизить риск тяжелого СГЯ.
Продолжительность стимуляции фоллитропином-β на фоне ганиреликса у пациенток основной группы оказалась выше, чем у пациенток контрольной группы (12,8±1,4 дней и 11,4±1,1 дня; p<0,05). Суммарная доза ФСГ у пациенток с избыточной массой тела и ожирением также была больше, чем у пациенток с нормальной массой ±509 МЕ и 1535±336 МЕ; p<0,05), однако в обеих группах доза потребовалось меньше гонадотропинов, чем при использовании агонистов Гн-РГ и чМГ.
Чрезвычайно важным является момент начала введения антагонистов Гн-РГ. Мы начинали вводить ганиреликс при достижении лидирующим фолликулом диаметра 14 мм, т. е. через 7,2±0,6 дней после начала стимуляции рФСГ в основной группе и через 6,3±0,7 дней – в контрольной группе. У пациенток с избыточной массой тела и ожирением латентная фаза роста фолликулов оказалась более длительной. У одной пациентки с ИМТ 35 кг/м2 произошла преждевременная овуляция, что позволяет предположить, что женщинам с ожирением высокой степени требуется более высокая доза антагонистов Гн-РГ.
Различий по толщине эндометрия в проспективной части исследования также выявлено не было. Подтверждением отсутствия негативного влияния на эндометрий является высокая частота имплантации у пациенток основной группы (26,1%), она оказалась даже выше, чем у пациенток контрольной группы, хотя различия были статистически незначимы (21,2%, р>0,05).
В проспективной части исследования количество фолликулов и аспирированных ооцитов у пациенток с ИМТ>25 кг/м2 также оказалось достоверно ниже, чем у пациенток с нормальной массой тела. Однако исходный овариальный резерв пациенток обеих групп был сопоставим, т. е. у пациенток с ожирением, несмотря на большое число антральных фолликулов, меньшее число фолликулов достигает преовуляторных размеров. Тем не менее, концентрация эстрадиола в день введения хорионического гонадотропина человека (ХГЧ) в основной группе оказалась выше, чем в контрольной группе, что, возможно, связано с его продукцией многочисленными мелкими фолликулами.
Одной из задач проспективной части исследования был анализ динамики половых гормонов и метаболических показателей в процессе индукции суперовуляции (табл.3).
Таблица 3. Динамика гормональных и метаболических показателей во время индукции суперовуляции
Показатель* | Основная группа | Контрольная группа |
Тестостерон1, нг/дл Тестостерон2, нг/дл | 1,9±0,9 4,0±0,8** | 1,4±0,6 2,3±1,3** |
Эстрадиол, пг/мл | 1505±689,7 | 1395±632,3 |
Глюкоза1, нмоль/л Глюкоза2, нмоль/л | 4,7±1,2 4,9±0,8 | 4,6±0,6 4,7±0,7 |
Инсулин1, мЕД/л Инсулин2, мЕД/л | 13,5±2,8 18,1±3,6** | 4,9±1,7 6,3±1,8 |
Лептин1, нг/мл | 48,1±6,4 68,1±8,2** | 12,3±5,2 15,6±6,4 |
*1,2 – показатели в начале и в конце стимуляции соответственно
** – различия между значениями 1 и 2 статистически значимые (p<0,05)
В нашем исследовании было выявлено закономерное увеличение уровня стероидных половых гормонов. Во время стимуляции наблюдалось статистически значимое увеличение концентрации тестостерона в обеих группах, однако в группе с избыточной массой тела это увеличение было более выраженным (в 2 раза). У 4 пациенток основной группы, у которых развился СГЯ, отмечались исходно более высокие показатели тестостерона, которые в конце стимуляции превысили базальные показатели в 2,4 раза. Таким образом, превышение уровня тестостерона более, чем в 2 раза, можно считать прогностическим фактором риска развития СГЯ.
Статистически значимых изменений концентрации глюкозы за время стимуляции выявлено не было. У пациенток с нормальной массой тела в процессе стимуляции концентрации инсулина и лептина несколько повысились (с 4,9±1,7 мЕД/л до 6,3±1,8 мЕД/л и с 12,3±5,2 н/мл до 15,6±6,4 нг/мл соответственно), однако различия оказались статистически незначимыми (p>0,05), что свидетельствует о «метаболической нейтральности» используемых для стимуляции препаратов. В отличие от контрольной группы при избыточной массе тела и ожирении отмечалось статистически значимое повышение уровня ИРИ (в 1,3 раза) и лептина (в 1,4 раза). У пациенток с СГЯ эти показатели увеличились в той же степени, таким образом, уровень ИРИ и лептина в конце стимуляции не отражает риск развития СГЯ. У пациенток с прогрессирующей, неразвивающейся беременностью и при отсутствии наступления беременности степень увеличения лептина и ИРИ оказалась одинаковой, таким образом, измерение этих показателей в конце стимуляции с практической точки зрения смысла не имеет. Однако выявление базальной инсулинорезистентности позволяет сформировать группы риска по отсутствию беременности и прекращению ее
развития (частота инсулинорезистентности у пациенток с прогрессирующей беременностью составила 14,3%, в подгруппе, где беременность не наступила – 33,3%, а при неразвивающейся беременности – 66,6%, различий по степени гиперинсулинемии выявлено не было). Что касается гиперлептинемии, то у больных с СГЯ базальный уровень лептина оказался несколько выше, чем у остальных пациенток группы, однако ввиду небольшого числа пациенток с СГЯ различия оказались незначимыми. При неразвивающейся, прогрессирующей беременности и при ее отсутствии различий по базальному уровню лептина обнаружено не было. Таким образом, не выявили связи между гиперлептинемией и исходами программ ВРТ.
В группе с нормальной массой тела ПЭ чаще осуществляли на стадии бластоцисты (53,3%), что свидетельствует о хорошем качестве эмбрионов, а в группе с избыточной массой тела – чаще на третьи сутки развития (93%), что частично обусловлено меньшим количеством полученных эмбрионов хорошего качества. Это согласуется с соответствующей частотой формирования бластоцист (49,6% при нормальной массе тела и 32,9% при избыточной массе тела и ожирении). Следует отметить, что у пациенток с «простым» ожирением, в том числе при высоком ИМТ, как правило, преобладали эмбрионы хорошего качества.
Клинические исходы лечения при использовании антагонситов Гн-РГ и фоллитропина-β представлены в таблице 4.
Таблица 4. Клинические исходы лечения
Параметр | Основная группа | Контрольная группа | р |
Число циклов с ПЭ, абс.(%) | 31 (96,9) | 30 (93,8) | 0,5 |
Частота имплантации, % | 26,1 | 21,2 | 0,32 |
Частота образования бластоцист, % | 32,9% | 49,6 % | 0,086 |
Частота наступления биохимической беременности, % | 53,1 | 53,1 | 0,8 |
Частота наступления клинической беременности, % | 53,1 | 50,0 | 1,0 |
Частота невынашивания беременности, % | 17,6 | 6,3 | 0,72 |
Частота прогрессирующей беременности, % | 43,8 | 46,9 | 1,0 |
Частота родов живым плодом, % | 43,8 | 46,9 | 1,0 |
Частота наступления биохимической беременности в расчете на пункцию оказалась достаточно высокой и составила в обеих группах по 53,1%, а частота клинической беременности равнялась 53,1% и 50,0% в основной и контрольной группах соответственно (р>0,05). Немалую роль в достижении таких высоких показателей, возможно, сыграл и тип используемого ФСГ (рекомбинантный фоллитропин-β), гарантирующий постоянство вводимой дозы, и способ введения препарата (шприц-ручка), обеспечивающий минимальную потерю препарата при введении. Высокая частота имплантации на перенесенный эмбрион в обеих группах (26,1% и 21,2%, р>0,05) свидетельствует о хорошем качестве эмбрионов. Частота прогрессирующей беременности также оказалась не ниже, чем при использовании стандартного длинного протокола, а даже выше, что возможно обусловлено уменьшением негативного влияния гиперандрогении и гиперинсулинемии на ранние этапы имплантации и эмбриогенеза при использовании рекомбинантного ФСГ.
Сложно делать какие-либо выводы относительно влияния ожирения на акушерские потери и осложнения беременности из-за относительно небольшого объема выборки. На основании анамнестических данных пациенток ретроспективной части исследования нами было выявлено, что у больных с ожирением частота неразвивающейся беременности превышает таковую у пациенток с нормальной массой тела. В проспективной части работы частота неразвивающейся беременности в основной группе оказалась выше, чем, в контрольной группе, однако различия оказались статистически незначимы. Тем не менее, следует отметить, что у двух из трех пациенток проспективной части исследования неразвивающаяся беременность возникла на фоне СПКЯ и МС. По мнению многих авторов невынашивание беременности у пациенток с ожирением после ЭКО обусловлено не ВРТ, а самим ожирением.
Несмотря на то, что у многих пациенток проспективной части исследования риск развития СГЯ изначально был достаточно высок, ни одного случая СГЯ тяжелой степени, потребовавшего лечения в условиях стационара, зарегистрировано не было, лишь в 2 случаях ПЭ был отменен из-за риска усугубления симптомов СГЯ. Это свидетельствует о безопасности протокола с антагонистами Гн-РГ и рекомбинантным ФСГ даже у пациенток с высокой фолликулярной активностью.
После окончания лечения с помощью анкетирования был проведен опрос по удобству пользования шприц-ручкой для введения ФСГ. Все пациентки отметили, что инъекции с использованием ручки-инжектора менее болезненны, чем при использовании обычного шприца. Возможно, это объясняется микроразмерами иглы и микрообъемом вводимого препарата, что значительно снижает боль в месте инъекции. Дискомфорта с психологической точки зрения от использования шприц-ручки также ни в одном из случаев выявлено не было. Для большинства пациенток очень важным оказалось самостоятельное использование ручки-инжектора без дополнительной помощи со стороны медицинского персонала. Местные реакции (кровоподтеки, покраснение, припухлость) наблюдались у 15,6% пациенток, однако они были слабо выражены и не привели к прекращению лечения.
Таким образом, влияние избыточной массы тела и ожирения на эффективность программ ВРТ неоднозначно. Контролируемая индукция суперовуляции у пациенток с высоким ИМТ, как правило, сопровождается более длительной стимуляцией, большей суммарной дозой гонадотропинов и снижением числа получаемых ооцитов. Индукция суперовуляции у пациенток с избыточной массой тела и ожирением по длинному протоколу с агонистами Гн-РГ и чМГ сопровождается повышенным риском развития СГЯ. Результаты проведенного исследования позволяют утверждать, что индукция суперовуляции с применением фоллитропина-β, вводимого с помощью шприц-ручки, на фоне антагонистов Гн-РГ позволяет достичь хороших показателей наступления беременности при невысокой дозе гонадотропинов, небольшой продолжительности стимуляции и низком риске СГЯ и является, таким образом, высокоэффективным и безопасным методом лечения пациенток с избыточной массой тела и ожирением.
ВЫВОДЫ
1. Группа пациенток с ожирением и бесплодием неоднородна. У 51,6% женщин преимущественно с феминным типом распределения жировой ткани ожирение лишь сопутствует бесплодию, а гормональные и метаболические нарушения отсутствуют. В 48,6% наблюдений инсулинорезистентность, гиперинсулинемия, гиперлептинемия и гиперандрогения приводят к формированию МС и СПКЯ, что становится причиной бесплодия.
2. Индукция суперовуляции у пациенток с ожирением сопровождается более продолжительной стимуляцией, увеличением суммарной дозы гонадотропинов и получением меньшего числа фолликулов и ооцитов по сравнению с пациентками с нормальной массой тела.
3. У пациенток с феминным типом распределения жировой ткани (54,9%) требуется большая доза гонадотропинов, чем у пациенток с андроидным типом ожирения (45,1%), у которых в свою очередь отмечается тенденция к получению большего числа ооцитов. Ожирение не влияет на толщину эндометрия в день ПЭ.
4. Наиболее неблагоприятным вариантом ожирения, негативно влияющим на исходы ЭКО, являются андроидный тип ожирения в сочетании с СПКЯ и МС, что отражается в снижении частоты имплантации, клинической и прогрессирующей беременности в 2 раза, а также в повышении риска СГЯ в 4 раза.
5. Протокол стимуляции рекомбинантным ФСГ с использованием антагонистов Гн-РГ позволяет получить хороший ответ яичников и высокую частоту наступления беременности при низком риске СГЯ.
6. Распределение пациенток в зависимости от типа и степени ожирения позволяет сформировать группы риска по СГЯ, что в свою очередь дает возможность индивидуализировать выбор протокола стимуляции в процессе лечения бесплодия с помощью ВРТ.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. У всех пациенток с ожирением и бесплодием необходимо проводить гормональное обследование и диагностику нарушений углеводного и липидного обмена ввиду высокой частоты у них СПКЯ (48,4%) и МС (29%)
2. Ожирение без метаболических и эндокринных расстройств не оказывает неблагоприятного воздействия на исходы программ ВРТ, тем не менее, учитывая высокий риск акушерских осложнений, пациенткам с ожирением высокой степени (ИМТ ≥ 40 кг/м2) необходимо снижать массу тела перед индукцией суперовуляции
3. Сочетание ожирения с СПКЯ и МС приводит к снижению частоты клинической и прогрессирующей беременности, поэтому таким пациентам при подготовке к лечению методами ВРТ требуется коррекция гормональных и метаболических нарушений
4. Всем пациенткам с ожирением необходимо выявлять базальную инсулинорезистентность, что позволит сформировать группы риска по неразвивающейся беременности и неудачному исходу программ ВРТ и определить тактику лечения, направленную на профилактику этих осложнений
5. Увеличение тестостерона в процессе индукции суперовуляции более чем в 2 раза можно считать прогностическим фактором риска развития СГЯ
6. Индукцию суперовуляции у пациенток с ожирением без метаболических и эндокринных расстройств при скудном и умеренном фолликулярном резерве лучше начинать с более высоких доз гонадотропинов (не менее 200 МЕ/сут)
7. У пациенток с андроидным ожирением, СПКЯ и МС повышен риск СГЯ, поэтому индукцию суперовуляции у этих пациенток предпочтительнее проводить по короткому протоколу с антагонистами Гн-РГ, начиная с низких доз рекомбинантного ФСГ (150 МЕ/сут), а появление первых признаков СГЯ является показанием к отмене ПЭ в цикле стимуляции и их криоконсервации с целью переноса в последующих циклах.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. , , Колода использования вспомогательных репродуктивных технологий у пациенток с ожирением (обзор литературы) // Проблемы репродукции. – 2008.– № 4.–С.44.
2. , , Абляева программ ВРТ с использованием фоллитропина-β и ганиреликса // Проблемы репродукции. – 2008.– № 5. –С.40.
3. , , Колода массы тела на эффективность программ вспомогательных репродуктивных технологий // Материалы второго международный конгресс по репродуктивной медицине «Репродуктивное здоровье и планирование семьи». – 2008.– С.366.
4. , , Смирнова стимуляции суперовуляции фоллитропином-β и ганиреликсом в программе ЭКО/ИКСИ // Сборник тезисов научно-практической конференции «Технологии XXI века в гинекологии». – 2008.– С.172.
5. Колода программ ЭКО/ИКСИ при использовании фоллитропина-β и ганиреликса у пациенток с избыточной массой тела и ожирением // Материалы IV съезда акушеров-гинекологов России. – 2008.– С.381.
6. , , Абляева индукции суперовуляции у пациенток с избыточной массой тела и ожирением // Проблемы репродукции. – 2009.– № 1.– С.65.
7. Колода факторы исходов программ ВРТ у пациенток с ожирением // Материалы конференции молодых ученых, посвященной 80-летию РМАПО– С.126.
8. Koloda Y. A., Podzolkova N. M., Anshina M. B., Shamugia N. L., Smirnova A. A., Abliaeva E. S. Effect of overweight and obesity on assisted reproductive technology outcomes (Влияние избыточной массы тела и ожирения на исходы программ вспомогательных репродуктивных технологий). Сборник тезисов 14 th World Congress of Gynecological Endocrinology (ISGE).-Florence, Italy.-4-7 March 2010



