Таким образом, было установлено, что на препаратах, приготовленных с применением 9-АМА, необходимо выбирать для исследования определенный интервал длин хромосом, который не должен превышать трёх средних размеров тех же метафазных хромосом, полученных без применения интеркалятора. В этом интервале длин можно достоверно оценивать хромосомный полиморфизм как по наличию-отсутствию С-бэндов, так и по их размерам. В указанном интервале длин на мелкохромосомных объектах можно проводить сравнительные исследования рисунков С-окраски и составлять хромосомные паспорта, аналогично тому, как это делается на крупнохромосомных объектах. Рекомендации, приведенные в этом разделе, учитывались нами при изучении полиморфизма по С-блокам разных сортов посевного льна (долгунцовые, масличные и межеумки) и в последующих исследованиях хромосом растений с использованием 9-АМА.
1.2.2.2. Сравнительное исследование рисунков OR- и С-бэндинга.
Проведенное нами исследование рисунков OR-бэндинга хромосом ромашки, гороха и цингерии позволило определить некоторые общие особенности этого типа окрашивания. Установлено, что рисунок OR-окраски выявляется на недоконденсированных прометафазных хромосомах. Рисунок OR-окрашивания воспроизводим, хромосомо - и видоспецифичен, несмотря на то, что число выявляемых на хромосомах растений OR-бэндов зависит от степени конденсации хромосом, подобно тому как это имеет место при G- или R-окрашивании хромосом животных. [
При окрашивании хромосом растений ацетоорсеином было обнаружено, что, в отличие от окрашивания по С-методу, прицентромерные гетерохроматические районы хромосом обычно окрашиваются очень слабо. Для детального сравнения двух различных методов окрашивания была проведена последовательная обработка хромосом льна крупноцветкового (Linum grandiflorum Desf.) ацетоорсеином и АТ-специфичным флуоресцентным красителем DAPI. Как известно, на хромосомах растений, в том числе у льнов, DAPI-позитивные районы обычно совпадают с С-бэндами (Рис. 5).
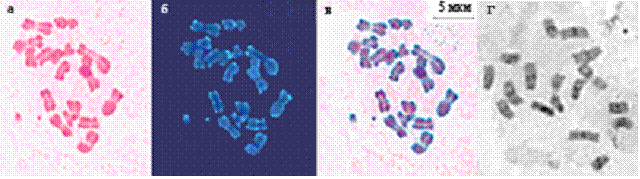
Рис. 5. Хромосомы L. grandiflorum: а – OR-бэндинг, б – последующее окрашивание DAPI, в – компьютерное совмещение DAPI- и OR-бэндинга, г –С-бэндинг.
В результате последовательного OR - и DAPI-окрашивания хромосом льна и последующего компьютерного наложения изображений выявлено, что ацетоорсеин слабо окрашивает не только околоцентромерные, но и теломерные гетерохроматические районы. Кроме того, было обнаружено, что большинство крупных блоков интеркалярного гетерохроматина также не окрашивается ацетоорсеином (Рис. 5 и см. разделы 2.3 – 2.5).
Таким образом, было установлено, что рисунок OR-бэндинга, хотя и зависит от степени компактизации хромосом, не является простым отражением рисунка дифференциальной конденсации. Вероятно, интенсивность окрашивания ацетоорсеином зависит не только от плотности упаковки отдельных районов хромосом, но и от особенностей структурной организации этих районов.
1.3. Молекулярно-цитогенетические маркеры для картирования хромосом и геномов с помощью флуоресцентной гибридизации in situ.
 В период активной интеграции молекулярной биологии и цитогенетики значительно упростилась идентификация отдельных хромосом или геномов. Стало возможным проводить молекулярное кариотипирование с помощью метода FISH, позволяющего локализовать на хромосомах молекулярные маркерные зонды – хромосомоспецифичные или геномоспецифичные последовательности ДНК, т. е. осуществлять физическое картирование хромосом. У растений в качестве маркерных зондов обычно используются различные повторяющиеся последовательности.
В период активной интеграции молекулярной биологии и цитогенетики значительно упростилась идентификация отдельных хромосом или геномов. Стало возможным проводить молекулярное кариотипирование с помощью метода FISH, позволяющего локализовать на хромосомах молекулярные маркерные зонды – хромосомоспецифичные или геномоспецифичные последовательности ДНК, т. е. осуществлять физическое картирование хромосом. У растений в качестве маркерных зондов обычно используются различные повторяющиеся последовательности.
1.3.1. Теломерные повторы.
Известно, что хромосомные слияния, имеющие место при реорганизации кариотипов растений в процессе видообразования, могут приводить к изменению числа и морфологии хромосом в родственных геномах. В некоторых случаях на месте слияния хромосом остаются теломерные повторы, обычно локализованные на концах хромосом. Наличие таких интерстициальных сайтов теломерных повторов может свидетельствовать о произошедших хромосомных перестройках и, в ряде случаев, дает возможность исследовать особенности реорганизации кариотипов в процессе видообразования. Кроме того, локализация таких дополнительных мест расположения теломерных повторов на хромосомах может служить в качестве дополнительных маркеров при распознавании трудно идентифицируемых хромосом (Рис. 6).
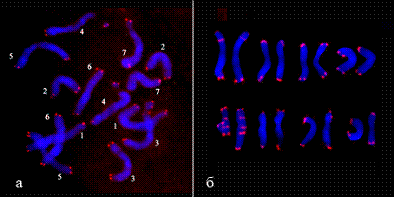 Рис. 6. FISH с зондом теломерного повтора (AAATGGG) (красный) на хромосомах: а –Pisum sativum (интерстициальные сайты гибридизации отсутствуют);
Рис. 6. FISH с зондом теломерного повтора (AAATGGG) (красный) на хромосомах: а –Pisum sativum (интерстициальные сайты гибридизации отсутствуют);
б –Linum hirsutum (в двух хромосомах выявлены интерстициальные сайты гибридизации). Хромосомы окрашены DAPI (синий).
Использование теломерного повтора в качестве дополнительного молекулярно-цитогенетического маркера достаточно перспективно для изучения мелких хромосом и уточнения точек хромосомных разрывов в генетических коллекциях растений с перестроенными кариотипами, а также при исследовании особенностей структурной организации В-хромосом (См. разделы 2.4 и 2.6).
1.3.2. Гены рибосомных РНК.
Наиболее часто в качестве эффективных хромосомных маркеров используют рисунки локализации последовательностей генов 45S и 5S рРНК. Как известно, ДНК-последовательности рибосомных генов высоко консервативны и обладают очень низкой видовой специфичностью. Это позволяет последовательности генов рибосомных РНК, выделенные из генома какого-либо одного вида, применять в качестве зондов для исследования их хромосомной локализации с помощью FISH как у близких, так и у филогенетически далеких видов. В нашей работе была продемонстрирована возможность использования последовательности 18S-28S рДНК, выделенной из генома человека (клон 22F9 из библиотеки LA-13NCO1), для гибридизации с хромосомами ячменя (Рис.7а). Также, показана возможность использования зондов 18S-26S и 5S рДНК (клоны рТа71 и рТа794 соответственно), полученных из генома мягкой пшеницы [Gerlach, Bedbrook, 1979], для гибридизации с хромосомами человека и примитивных фотосинтезирующих эукариот – красных одноклеточных водорослей (Рис. 7в и 7б).
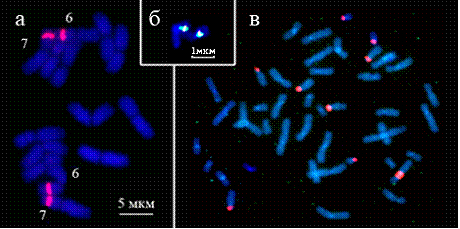
Рис. 7. FISH с зондами рибосомных генов на хромосомах:
а – H. vulgare
(22F9 - красный);
б – G. sulfuraria
(рТа71 - зеленый, рТа794-красный);
в – H. sapience (рТа71-красный).
Расположение локусов рибосомных генов на хромосомах считают синапоморфным признаком, несмотря на редкие исключения из этого правила, связанные с особенностями геномов некоторых видов. Изучение хромосомной локализации генов 45S и 5S рРНК, наряду со сравнительными исследованиями последовательностей межгенных спейсеров (ITS), успешно используется для определения филогенетических взаимосвязей родственных видов растений (См. раздел 2.5).
1.3.3. Геномная гибридизация.
Высокое содержание различных классов повторяющихся последовательностей в геномах растений привело к разработке метода геномной гибридизации in situ (GISH), который открыл тайны происхождения многих аллополиплоидных видов, в частности злаков [Paterson et al., 2000].
Метод продолжает совершенствоваться до сих пор и позволяет различать все более близкородственные геномы. Например, недавно нами был разработан высокочувствительный вариант метода GISH, позволивший нам разделить в метафазных пластинках мягкой пшеницы (Triticum aestivum L.) геномы А, В и D (Рис. 8). Кроме того, с его помощью стало возможным уточнить структуру перестроенных хромосом и определить точки разрывов на хромосомных плечах.
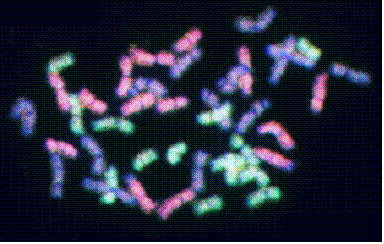
Рис. 8. A-, B-, и D- геномы гексаплоидной пшеницы, дифференцированные с помощью GISH.
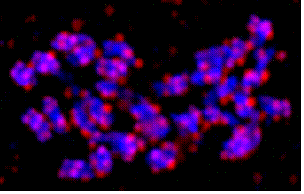 Существуют разные варианты метода GISH, использующие геномную ДНК одного или нескольких видов для выявления сайтов локализации консервативных повторяющихся последовательностей на хромосомах как родственных, так и не родственных видов растений [Belyaev, Raskina, 1998; Zoller et al., 2001]. Для хромосом льна (L. usitatissimum) нами разработан вариант метода гибридизации геномной ДНК, выделенной из того же вида. Методика заключается в совместной денатурации на препарате ДНК хромосом и зонда (геномной ДНК) в гибридизационной смеси, содержащей 50% формамида, при температуре 73ºС, и последующей ренатурации в течение 15 минут при 40ºС. В этих условиях на хромосомах льна гибридизуется часть высокоповторяющихся последовательностей ДНК, что позволяет выявлять на мелких хромосомах льна рисунок локализации зонда, напоминающий С-бэндинг (Рис. 9).
Существуют разные варианты метода GISH, использующие геномную ДНК одного или нескольких видов для выявления сайтов локализации консервативных повторяющихся последовательностей на хромосомах как родственных, так и не родственных видов растений [Belyaev, Raskina, 1998; Zoller et al., 2001]. Для хромосом льна (L. usitatissimum) нами разработан вариант метода гибридизации геномной ДНК, выделенной из того же вида. Методика заключается в совместной денатурации на препарате ДНК хромосом и зонда (геномной ДНК) в гибридизационной смеси, содержащей 50% формамида, при температуре 73ºС, и последующей ренатурации в течение 15 минут при 40ºС. В этих условиях на хромосомах льна гибридизуется часть высокоповторяющихся последовательностей ДНК, что позволяет выявлять на мелких хромосомах льна рисунок локализации зонда, напоминающий С-бэндинг (Рис. 9).
Рис. 9. GISH с собственной геномной ДНК на хромосомах L. usitatissimum.
Развитие этого подхода открывает широкие перспективы для выявления рисунков распределения высокоповторяющихся последовательностей ДНК на хромосомах небольших размеров, поскольку разрешение этого метода выше других способов дифференциальной окраски. Геномную ДНК легко выделить из любого растения, поэтому возможность ее использования при FISH-картировании в качестве зонда, позволяющего выявлять дополнительные хромосомные маркеры очень ценна, особенно для хромосом с трудновыявляемым и бедным рисунком С-бэндинга.
1.3.4. Геномные библиотеки – источник зондов для FISH.
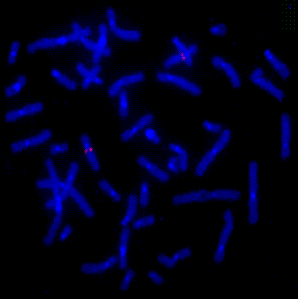 Картирование уникальных генов и различных анонимных последовательностей ДНК на хромосомах человека было начато задолго до начала тотального секвенирования его генома и во многом послужило основой для его успешного проведения. С целью исследования генома человека были разработаны различные методики получения BAC-, YAC - библиотек геномных ДНК-последовательностей, позволившие секвенировать отдельные фрагменты генома и собирать из них фрагменты генома большего размера. Был разработан метод создания NotI–библиотек, специфичных для одной хромосомы и для генома в целом. Поскольку NotI сайты ассоциированы с генами, то исследование последовательностей ДНК из этих библиотек позволило обнаружить и картировать множество генов на хромосомах человека. Можно привести пример гена Harakiri (Рис. 10), вовлеченного в процесс апоптоза клеток.
Картирование уникальных генов и различных анонимных последовательностей ДНК на хромосомах человека было начато задолго до начала тотального секвенирования его генома и во многом послужило основой для его успешного проведения. С целью исследования генома человека были разработаны различные методики получения BAC-, YAC - библиотек геномных ДНК-последовательностей, позволившие секвенировать отдельные фрагменты генома и собирать из них фрагменты генома большего размера. Был разработан метод создания NotI–библиотек, специфичных для одной хромосомы и для генома в целом. Поскольку NotI сайты ассоциированы с генами, то исследование последовательностей ДНК из этих библиотек позволило обнаружить и картировать множество генов на хромосомах человека. Можно привести пример гена Harakiri (Рис. 10), вовлеченного в процесс апоптоза клеток.
Рис. 10. Локализация на 12 хромосоме человека (12q13.1) гена Harakiri (красный). Хромосомы окрашены DAPI (синий).
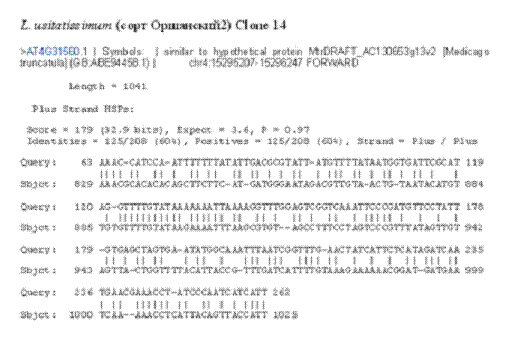
Кроме того, использование клонов ДНК из NotI–библиотек позволило уточнить последовательность расположения генов в некоторых районах хромосомы 3 человека и выявить новые предполагаемые гены-супрессоры опухолевого роста. Сконструированные на основе NotI клонов ДНК микрочипы позволили создать новую технологию сравнительного анализа геномной ДНК, выделенной из нормальных и опухолевых клеток, дающую возможность выявлять генетические и эпигенетические изменения в геномах клеток на разных стадиях канцерогенеза. Интенсивные исследования генома человека также положили начало развитию молекулярной цитогенетики растений. Методики, разработанные для изучения хромосом человека и животных, были модифицированы и широко применяются для исследования хромосомной организации геномов растений. Интенсивные исследования структуры геномов растений (в первую очередь арабидопсиса) обнаружили, что участки генов растений, также как и животных, обогащены CpG-последовательностями, содержат NotI сайты рестрикции (лат., метилирование которых и у растений является одним из способов эпигенетической регуляции [Matsuyama et al., 2003]. Нами были проведены пилотные эксперименты по получению геномных NotI библиотек из Triticum aestivum L., L. usitatissimum и L. austriacum, используя методику создания NotI – связующих библиотек человека. Из генома пшеницы (около 7 млрд. п. н.) не было получено ни одного клона. В то же время с первой попытки из геномов льнов (около 650 млн. п. н. для L. usitstissimum) получен 41 клон геномных фрагментов. В результате сравнения сиквенсов этих последовательностей с имеющимися в базах данных (NCBI Blast и Arabidopsis thaliana WU-BLAST2) для 22 ДНК клонов не было обнаружено гомологий. Среди остальных выявлены гомологии с фрагментами хлоропластных и ядерных генов, а также с ДНК-последовательностью ретротранспозонного элемента, гомология с сиквенсом которого приведена на рис. 11.
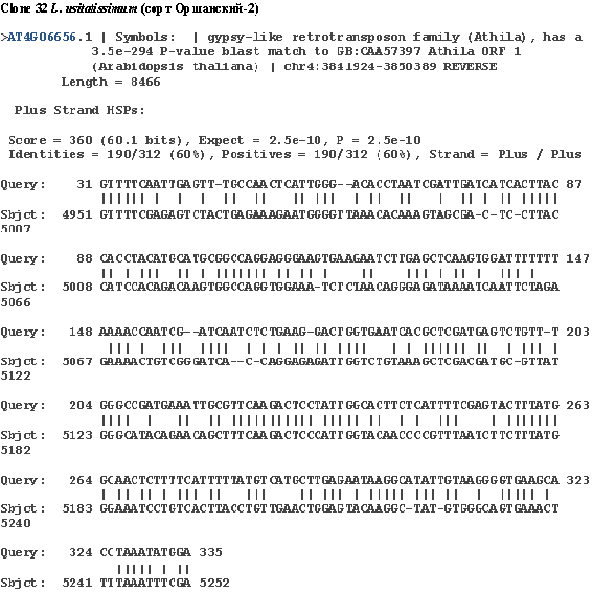 |
Рис. 11. Гомология клона 32 из генома L. usitatissimum (сорт Оршанский 2) gypsy-подобному семейству ретротранспозонов (Athila).
Таким образом, наши результаты показали перспективность использования NotI–библиотек для исследования геномов небольшого размера у растений.
1.3.4. Дифференциальное окрашивание хромосом АТ-специфичными флуоресцентными красителями.
При проведении FISH для окраски хромосом обычно используют АТ-специфичный флуоресцентный краситель DAPI, выявляющий Q-подобный рисунок окрашивания на хромосомах животных. У растений после гибридизации in situ метафазные хромосомы обычно окрашиваются DAPI монохромно. Как правило, такое окрашивание характерно для растений с крупными геномами (пшеница, ячмень). У растений с небольшими геномами на метафазных хромосомах могут выявляться рисунки DAPI-дифференциального окрашивания. Как показали наши исследования, этот бэндинг становится виден на хромосомах особенно отчетливо после предобработки 9-АМА. Такая предобработка позволила выявить рисунок DAPI-бэндинга не только у льнов (геном льна посевного около 600 млн. п.н.) и цингерии (геном около 1,5 млрд п. н.), но и у гороха (геном около 4,3 млрд п. н.) (См. разделы 2.4 – 2.6).
Рисунок DAPI-дифференциального окрашивания хромосом растений, подобен рисунку С-бэндинга (Рис. 12-I а, б). При этом, чем длиннее хромосомы, тем выше разрешение DAPI-бэндинга (Рис. 12-II, III).
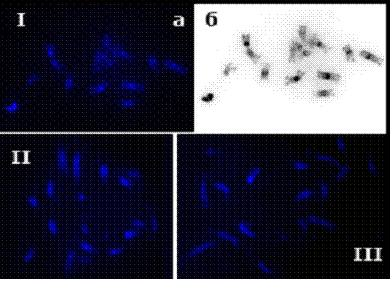
Рис. 12. Изменение рисунка DAPI-окрашивания хромосом L. grandiflorum в зависимости от степени компактизации хромосом:
I – метафаза (а – DAPI-окрашивание и
б – инвертированное изображение),
II – прометафаза,
III – поздняя профаза.
Особенно важно получение высокоразрешающих рисунков DAPI-бэндинга после FISH, поскольку это позволяет не только точно идентифицировать хромосомы, но и отдельные районы хромосом, что существенно повышает точность картирования различных зондов.
Поскольку рисунок DAPI-бэндинга на хромосомах растений не всегда бывает достаточно контрастным, с целью улучшения качества дифференциального окрашивания хромосом при FISH, была изучена возможность применения новых флуоресцентных красителей. Было протестировано 10 димерных бис-бензимидазолов (содержащих две модифицированных группы красителя Hoechst 33258), синтезированных в ИМБ РАН [Zhuze et al., 2007]. Из них были отобраны четыре соединения: DB(7), DB(8), DB(17) и DB(18), при окрашивании которыми хромосом модельного объекта – человека, выявлялся бэндинг, сходный с рисунками дифференциального окрашивания флуорохромами DAPI или Hoechst 33258. Контрастность флуорохромного бэндинга, полученного при использовании этих четырех соединений, и его устойчивость к выгоранию была несколько выше, чем в случае DAPI и Hoechst 33258 .
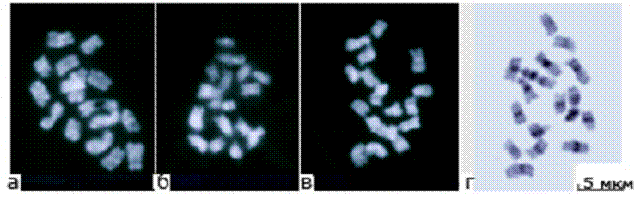
Рис. 13. Дифференциальное окрашивание хромосом L. grandiflorum флуоресцентными красителями: а – DB(8), б – DAPI, в – Hoechst 33258, г – красителем Giemsa (С-бэндинг).
При окрашивании этими флуорохромами хромосом льна (L. grandiflorum) выявляется С/DAPI-подобный рисунок дифференциального окрашивания. Бэндинг, полученный при использовании DB(8) и DB(17) имел высокую контрастность и пониженную выгораемость (Рис. 13). Таким образом, полученные результаты открывают перспективы использования новых АТ-специфичных флуорохромов в исследовании хромосом не только человека, но и растений.
1.3. Комплексный подход к анализу хромосомной организации геномов растений.
Результаты нашего исследования показали, что одновременное или последовательное использование нескольких методов выявления на хромосомах молекулярно-цитогенетических маркеров позволяет успешно идентифицировать мелкие хромосомы и более точно локализовать различные ДНК-зонды, а также получать дополнительную информацию о структурной организации митотических хромосом растений.
Наиболее информативным является сочетание различных видов дифференциального окрашивания хромосом и гибридизации in situ с одним или несколькими зондами, проводящиеся на одних и тех же хромосомных пластинках последовательно или одновременно. Такой подход не только позволяет наиболее глубоко исследовать хромосомную организацию генома изучаемого растения, но и легко решать многие конкретные задачи. В частности, именно таким образом была проведена полная идентификация трудно распознаваемых хромосом у Linum flavum L. (Рис. 14).
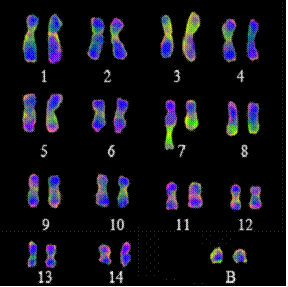
Рис. 14. Кариотип L. flafum после совмещения различных методов окрашивания хромосом: DAPI (синий) и CMA (зеленый), а также FISH с зондами теломерного повтора (AAATGGG) (красный). 1-14 – хромосомные группы, В – добавочные или В-хромосомы.
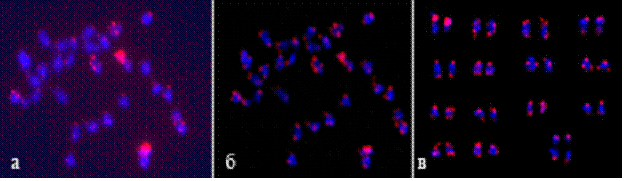
Следует отметить, что любое исследование тонкой структуры мелких митотических хромосом с помощью светооптического микроскопа практически невозможно без современных компьютерных технологий. При анализе хромосом небольших размеров и/или малоинформативным рисунком бэндинга особое значение приобретает оптимизация методов получения оцифрованных изображений хромосом и их последующей компьютерной обработки. Новые возможности по улучшению разрешения самых мелких деталей рисунка дифференциального окрашивания хромосом открывают методы деконволюции изображений. Современные методы деконволюции позволяют эффективно устранять размытие изображения (вследствие оптических аберраций и шумов регистрирующей системы) с помощью применения сложного математического аппарата для моделирования процессов формирования изображения и оценки качества восстанавливаемого изображения. В конечном итоге существенно повышается разрешающая способность оптической системы (Рис.15).
Рис.15. Локализация теломерного повтора (AAATGGG) (красный) на хромосомах льна (L.usitatissimum) методом FISH. Хромосомы окрашены DAPI (синий).
а – метафазная пластинка до деконволюции;
б – та же метафазная пластинка после деконволюции;
в – улучшение качества изображения с помощью деконволюции позволило распознать гомологи и составить кариограмму.
Анализ кариотипов мелкохромосомных растений значительно облегчают специализированные программы хромосомного анализа, работающие в интерактивном режиме. Примером такой программы, созданной фирмой ВидеоТест совместно со специалистами по хромосомному анализу, и в том числе при нашем активном участии, могут служить программы ВидеоТестКарио 1.5 и 2.0 (ВидеоТест, Санкт-Петербург).
 Разработка программы ВидеоТестКарио 1.5 была направлена на создание объективного помощника при разностороннем изучении структуры хромосом (Рис. 16). С помощью этой программы анализ изображений хромосом ведется в интерактивном режиме. Взаимодействие исследователя с различными модулями программы позволяет направленно улучшать изображения хромосом, проводить их измерения, определять центромерные индексы, а также положение и размеры бэндов, что особенно ценно при малом числе маркеров хромосом.
Разработка программы ВидеоТестКарио 1.5 была направлена на создание объективного помощника при разностороннем изучении структуры хромосом (Рис. 16). С помощью этой программы анализ изображений хромосом ведется в интерактивном режиме. Взаимодействие исследователя с различными модулями программы позволяет направленно улучшать изображения хромосом, проводить их измерения, определять центромерные индексы, а также положение и размеры бэндов, что особенно ценно при малом числе маркеров хромосом.
Рис. 16. Интерфейс программы хромосомного анализа
ВидеоТестКарио 1.5.
Идиограммы строятся в соответствии с интенсивностью окрашивания хромосомы по длине, что позволяет составлять объективные количественные идиограммы. По усредненным данным двух гомологов строится идиограмма хромосом генома изучаемого растения. Полученные результаты измерений хромосом в метафазной пластинке вносятся в таблицу, которая может быть преобразована в формат программы Microsoft Office Excel. Это позволяет накапливать результаты измерений по нужному числу хромосомных пластинок и далее использовать их для математической обработки, что очень важно при изучении полиморфизма хромосом, создании баз данных, а также при проведении сравнительных исследований. Коммерческие специализированные программы хромосомного анализа других производителей не предоставляют такой возможности, что существенно усложняет изучение хромосом разных видов растений.
Особенно эффективно сочетание комплексного подхода к изучению хромосомной организации геномов растений с различными молекулярными методами их исследования. Примерами плодотворности одновременного использования цитогенетических и молекулярных технологий (RAPD, ITS, определение количества ДНК в расчете на 1С) для изучения геномов растений могут служить сравнительные исследования различных видов красных микроводорослей, двухромосомных злаков и льнов, а также сортов и линий гороха, подробно описанные в следующей главе.
Глава 2. Хромосомная организация геномов у низших и высших видов растений с хромосомами малых размеров или неинформативным рисунком дифференциального окрашивания.
2.1. Сравнительные исследование геномов A1 G. herbaceum и (AD)2 G. barbadense.
С помощью BrdU-Hoechst-Giemsa-метода выявления рисунков ранней репликации хромосом были изучены кариотипы дикорастущей разновидности диплоидного хлопчатника (гуза) Gossypium herbaceum L. var. africanum (Watt) Mauer (2n = 26) и возделываемого аллотетраплоидного вида тонковолокнистого хлопчатника G. barbadense L. (2n = 52).

Рис. 17. Кариограмма и идиограмма BrdU-Hoechst-Giemsa - окрашенных хромосом
(a-m – обозначения хромосомных групп) хлопчатников: A1 – геном G. herbaceum; Ab и Db – субгеномы в составе генома (AD)2 G. barbadense.
На прометафазных хромосомах хлопчатников длиной 1,8-5,5 мкм число выявленных Giemsa-позитивных бэндов на хромосому варьировало от 2 до 9. Полученные рисунки ранней репликации хромосом были воспроизводимы и хромосомоспецифичны, что позволило идентифицировать все хромосомы в геноме A1 диплоида G. herbaceum и в геноме (AD)2 аллотетраплоида G. barbadense. При этом геном (AD)2 был разделен на субгеномы Ab и Db по размеру хромосом и сходству BrdU-Hoechst-Giemsa-бэндинга (Рис. 17). Сравнительное изучение рисунков BrdU-Hoechst-Giemsa-бэндинга хромосом в геномах хлопчатников выявило сходство распределения рано реплицирующихся районов по длине хромосом в A1-геноме и в Ab - и Db-субгеномах.
Проведенное исследование показало, что у растений, так же как и у животных, рисунок репликации хромосом достаточно консервативен и может применяться для решения задач цитогенетики. Однако, несмотря на хорошее разрешение этого метода для анализа мелких хромосом растений, он имеет существенные недостатки, ограничивающие его применение. Метод довольно сложен в исполнении, требует длительной предобработки прорастающих корней раствором бромдезоксиуридина в высокой концентрации. При этом высокая митотическая активность корневой меристемы сохраняется только в условиях хорошей аэрации корней. Кроме того, использованный вариант BrdU-Hoechst-Giemsa-бэндинга не совместим с другими методами дифференциального окрашивания хромосом, а также с FISH, что очень важно при исследовании хромосомной организации геномов разных растений.
2.2. Микроводоросли класса Cyanidiophyceae (Rhodophyta).
До нашего исследования митотические хромосомы в клетках автоспор одноклеточных красных водорослей с помощью микроскопического исследования обнаружить не удавалось. Использование 9-АМА позволило визуализировать митотические хромосомы одноклеточных красных водорослей Galdieria maxima, G. partita, G. sulphuraria и Cianidium caldarium в процессе формирования автоспор. Для этого была разработана методика, позволяющая одновременно обрабатывать культивируемые клетки водорослей 9-АМА и пепсином с целью размягчения белкового компонента клеточных стенок. Такой подход позволяет после фиксации клеток и окрашивания ацетоорсеином получить хорошие давленые препараты недоконденсированных митотических хромосом и провести их морфометрическое исследование.
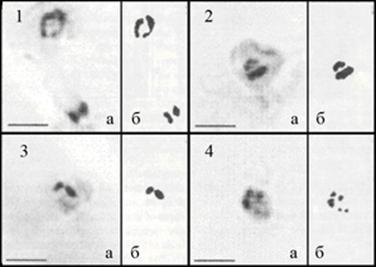 В автоспорах всех трех видов Galdieria было обнаружено по две хромосомы длиной 0,8-2,3 мкм, причем одна из хромосом была на треть больше другой (Рис. 18).
В автоспорах всех трех видов Galdieria было обнаружено по две хромосомы длиной 0,8-2,3 мкм, причем одна из хромосом была на треть больше другой (Рис. 18).
Рис. 18. Хромосомные пластинки (а) и их контрастированное изображение (б): 1 – G. maxima, 2 – G. partita, 3 – G. sulphuraria, 4 – C. caldarium.
Масштабная линейка – 3 мкм.
Статистически значимые межвидовые различия размеров хромосом G. maxima, G. partita, G. sulphuraria могут быть использованы в качестве дополнительного признака при определении видовой принадлежности этих водорослей. Больше трудностей представлял подсчет числа хромосом в геноме C. сaldarium, поскольку размеры 5 видимых хромосом были от 0,4 до 0,7 мкм (Рис. 18). Иногда с трудом различались еще 2 точечных хромосомы, размеры которых были на грани разрешающей способности светового микроскопа.
На хромосомах всех изученных видов было трудно точно определить положение центромер. Возможно, что хромосомы этих водорослей относятся к голоцентрическому типу, характерному для некоторых зеленых водорослей. Полученные результаты позволяют использовать число хромосом в качестве таксономического признака для распознавания представителей родов Cianidium и Galdieria.
Определение содержания ядерной ДНК, проведенное на профазных ядрах, окрашенных по Фельгену, показало, что представители семейства Cyanidiасеае имеют самые маленькие из известных геномов у фотосинтезирующих эукариот – 1,5-2,25х10-2 пкг ДНК в расчете на 1С (Табл.1).
Таблица 1. Средние значения суммарной длины хромосом и
количества ДНК в геномах красных микроводорослей.
Вид микроводоросли | Суммарная длина хромосом, мкм±SE | Содержание ДНК на 1C, пкг 10-2±SE |
G. maxima | 4.14±0.44 | 2.25±0.09 |
G. partita | 2.82±0.49 | 1.56±0.06 |
G. sulphuraria | 2.07±0.18 | 1.35±0.05 |
C. caldarium | 2.61±0.06 | 1.49±0.03 |
SE – стандартная ошибка среднего значения.
Это хорошо объясняет как малые размеры хромосом, обнаружить которые при микроскопическом исследовании стало возможным только после применения 9-АМА, так и отсутствие дифференциального окрашивания хромосом у исследованных видов.
Таким образом, исследование хромосомной организации геномов четырех видов микроводорослей класса Cyanidiophyceae (Rhodophyta) позволило не только установить их хромосомные числа и уточнить их систематическое положение, но и подтвердить наличие зависимости хромосомной организации генома от его размера.
2.3. Ромашка аптечная и родственные виды.
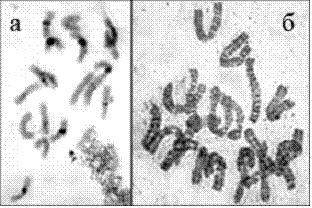
Исследование рисунков OR - и С-бэндинга хромосом (Рис. 19, 20) у двух диплоидных (Азулена и Сибирская бизаболольная) и одного автотетраплоидного (Подмосковная) сортов ромашки аптечной Matricaria chamomilla L. показало, что четкий рисунок OR-бэндинга выявляется на хромосомах ромашки размером 5,3-10,2 мкм. Это почти в 1,5 раза превышает длину хромосом, необходимую для получения С-бэндинга высокого разрешения и в 2 раза – длину метафазных хромосом, получаемых без использования 9-АМА (2,8-5,9 мкм).
 На каждой хромосоме ромашки аптечной выявляется от 12 до 22 OR-бэндов. При этом центромерные районы, а также области вторичных перетяжек не окрашиваются. Сравнительное изучение рисунков OR-окраски хромосом у разных сортов ромашки обнаружило межсортовую консервативность этого типа бэндинга.
На каждой хромосоме ромашки аптечной выявляется от 12 до 22 OR-бэндов. При этом центромерные районы, а также области вторичных перетяжек не окрашиваются. Сравнительное изучение рисунков OR-окраски хромосом у разных сортов ромашки обнаружило межсортовую консервативность этого типа бэндинга.
Рис. 19. С - (а) и OR- (б) окрашенные хромосомы M. chamomilla сорта Сибирская бизаболольная.
 При изучении рисунков С-бэндинга в кариотипах тех же трех сортов ромашки аптечной выявлено, что они отличались большей контрастностью и наличием ряда дополнительных мелких интеркалярных С-блоков по сравнению с необработанными 9‑АМА С-окрашенными хромосомами. По рисункам С-бэндинга проведена идентификация хромосом в кариотипах изученных сортов. Сорта различались в основном по размерам прицентромерных гетерохроматических районов, а также ряда небольших интеркалярных и теломерых С-бэндов на всех хромосомах, кроме 4 и 5. Хромосомы сорта Подмосковная в целом были более гетерохроматичны по сравнению с диплоидными сортами. Изучение рисунков С-бэндинга хромосом у этого сорта позволило подтвердить его автополиплоидное происхождение. Тем не менее, выявлены небольшие различия в рисунках С-окраски 2, 6 и 7 хромосом из разных субгеномов в кариотипе сорта Подмосковная. Геном ромашки аптечной был обозначен нами Mch геном.
При изучении рисунков С-бэндинга в кариотипах тех же трех сортов ромашки аптечной выявлено, что они отличались большей контрастностью и наличием ряда дополнительных мелких интеркалярных С-блоков по сравнению с необработанными 9‑АМА С-окрашенными хромосомами. По рисункам С-бэндинга проведена идентификация хромосом в кариотипах изученных сортов. Сорта различались в основном по размерам прицентромерных гетерохроматических районов, а также ряда небольших интеркалярных и теломерых С-бэндов на всех хромосомах, кроме 4 и 5. Хромосомы сорта Подмосковная в целом были более гетерохроматичны по сравнению с диплоидными сортами. Изучение рисунков С-бэндинга хромосом у этого сорта позволило подтвердить его автополиплоидное происхождение. Тем не менее, выявлены небольшие различия в рисунках С-окраски 2, 6 и 7 хромосом из разных субгеномов в кариотипе сорта Подмосковная. Геном ромашки аптечной был обозначен нами Mch геном.
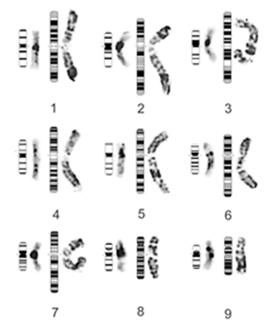
На основании оценки размеров хромосом, положения центромер и вторичных перетяжек было установлено соответствие результатов по идентификации хромосом, проведенной на основании рисунков OR - и С-окрашивания хромосом Mch генома ромашки аптечной, и построены идиограммы (Рис. 20).
Рис. 20. Идиограммы и кариограммы С - (слева) и OR- (справа) окрашенных хромосом (1-7 – обозначения гомологичных групп) Mch-генома M. chamomilla L.
Исследование хромосом двух родственных видов ромашек: диплоидной M. maritima L. (2n = 18) и тетраплоидной M. inodora L. (2n = 36), позволило идентифицировать по рисункам С-окраски и морфологическим параметрам все пары гомологов в их кариотипах. Обнаружено, что геном M. inodora по морфологии хромосом и рисункам С-бэндинга можно разделить на два практически идентичных субгенома, что указывает на автополиплоидное происхождении этого вида. Сравнение хромосом M. maritima и M. inodora выявило, что они имеют очень близкие рисунки распределения гетерохроматических сегментов и сходную морфологию. Это позволило предположить, что геном M. inodora образовался в результате удвоения генома M. maritima , который был обозначен Mm. Это подтверждается и тем, что содержание ядерной ДНК в расчете на 1С у изученных видов имеет близкие значения: у диплоидного вида – 2.75 пкг, а у тетраплоидного вида – 2,31 пкг [Garcia et al., 2005]. Сравнение хромосом Mm - и Mch-геномов выявило сходство морфологии хромосом и рисунков распределения позиций гетерохроматических районов по длине хромосом, что говорит об общности происхождения этих геномов. Однако в Mch-геноме значительно большее количество гетерохроматина содержится в прицентромерных и интеркалярных районах хромосом, тогда как в Mm-геноме более четко были выражены теломерные С-бэнды. Вероятно, дифференцировка этих геномов сопровождалась перераспределением повторяющихся последовательностей и их амплификацией в проксимальных районах хромосом Mch-генома. Это соответствует и значительно большему содержанию ядерной ДНК у ромашки аптечной – 3,87 пкг в расчете на 1С [Garcia et al., 2005].

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



