Особенностью фармакокинетики 99mTc-наноальбумина в организме крыс при разных способах введения является накопление его в паховом лимфатическом узле, превышающем в 8,5–9,7 раз (в период 5 – 60 мин) и в 58,8–135 раз (в период 3–48 ч) при подкожном введении по сравнению с внутривенной инъекцией.
Ткань щитовидной железы в течение всего периода наблюдения практически не аккумулировала активность, при исследовании 99mTc-наноальбумина после подкожного введения содержание активности в целом органе составляло на уровне тысячных или сотых долей процента. Это является показателем высокой стабильности меченого препарата in vivo, так как известно, что свободный технеций обладает тропностью к ткани щитовидной железы.
Для оценки функциональной пригодности 99mTc-наноальбумина были рассчитаны коэффициенты дифференциального уровня накопления активности в печени и лимфатическом узле по отношению к другим органам и тканям после внутривенного и подкожного введения меченого препарата (табл. 3).
Таблица 3 – Отношение удельного содержания 99mТс-наноальбумина в печени и лимфатическом узле к удельному содержанию активности в других органах и тканях крыс после внутривенного и подкожного введения препарата.
№ пп. | Наименование органа, ткани | Время после введения препарата | ||||
5 мин | 1 ч | 3 ч | 24 ч | 48 ч | ||
1 | Печень/кровь Лимфоузел/кровь | 1,74±0,58* 403,6±67,4** < 0,001 | 24,0±0,98 577,8±93,4 < 0,001 | 65,8±6,77 855,3±135,9 < 0,001 | 182,6±41,7 1008±317 < 0,02 | 55,1±13,3 233,5±42,4 < 0,002 |
2 | Печень/ЩЖ Лимфоузел/ЩЖ | 9,15±2,29 108,3±24,6 < 0,01 | 19,3±2,20 223,3±11,9 < 0,001 | 14,1±0,48 157,9±11,6 < 0,001 | 3,34±0,69 357,4±92,1 < 0,01 | 0,80±0,16 32,9±6,05 < 0,002 |
3 | Печень/легкие Лимфоузел/легкие | 5,75±1,05 1045±355 < 0,02 | 39,8±2,60 1125±342 < 0,05 | 73,6±5,59 1266±221 < 0,002 | 138,4±45,2 2029±148 < 0,001 | 54,0±6,32 1508±371 < 0,002 |
4 | Печень/почки Лимфоузел/почки | 13,4±3,24 279,2±63,8 < 0,02 | 11,9±0,41 69,2±6,56 < 0,001 | 4,74±0,37 42,8±5,95 < 0,001 | 1,97±0,43 19,8±6,13 < 0,05 | 1,00±0,05 22,1±3,85 < 0,002 |
5 | Печень/селезенка Лимфоузел/ селезенка | 2,23±0,03 348,3±81,4 < 0,02 | 2,13±0,40 198,4±62,0 < 0,05 | 1,97±0,16 71,8±13,4 < 0,002 | 2,43±0,24 177,9±28,0 < 0,001 | 2,21±0,30 144,0±32,3 < 0,01 |
* внутривенное введение **подкожное введение |
Коэффициенты дифференциального уровня накопления 99mTc-наноальбумина в печени по отношению к большинству органов и тканей постепенно увеличиваются и достигают максимального значения в период 3–24 ч после внутривенной инъекции препарата.
Сравнительные данные уровней дифференциального накопления активности в печени и лимфатическом узле по отношению к другим органам и тканям после внутривенного и подкожного введения 99mTc-наноальбумина характеризуют особенности поведения препарата в организме крыс в зависимости от способа его введения. Показано, что дифференциальный уровень накопления 99mTc-наноальбумина в лимфатическом узле в ранние сроки после инъекции препарата на 2–3 порядка выше, чем аналогичный показатель для печени. В последующие сроки эти величины повышаются в течение 24 ч по отношению к большинству органов и тканей. Эти данные свидетельствуют о том, что выведение активности из печени и лимфатического узла осуществляется существенно с меньшей скоростью, чем из других органов и тканей.
Коэффициенты дифференциального уровня характеризуют функциональную ценность РФП «99mTc-наноальбумин» для получения диагностической информации методом сцинтиграфии лимфатических узлов при подкожном введении и печени при внутривенном введении.
Особенности фармакокинетики меченых микросфер альбумина в
организме лабораторных животных в зависимости
от их физико-химических свойств
Для изучения влияния пространственного распределения радионуклида в микросферы альбумина, дисперсного состава частиц, химической природы радионуклида, денатурации белка в результате теплового воздействия или гамма-облучения, способа инъекции меченого препарата, патологического состояния легких на фармакокинетику в организме интактных животных и животных-опухоленосителей были разработаны и получены следующие препараты МСА:
· 131I-МСА диаметром 0,5–2, 0,5–5, 5–10 и 10–20 мкм, с температурой денатурации белка, равной 110, 130, 150оС и выдержкой в течение 1 ч, с поверхностным и объемным распределением радионуклида в частицах;
· 99mTc - и 111In-МСА диаметром 0,5–2 и 10–20 мкм с температурой денатурации белка, равной 150оС и выдержкой в течение 1 ч;
· 177Lu-МСА диаметром 10–20 мкм, полученные путем облучения стабильного изотопа 176Lu в составе МСА тепловыми нейтронами с потоком 2.1013 н/см2·с в течение 1 ч;
· 103Pd-МСА диаметром 5–10 и 20–40 мкм с объемным распределением радионуклида в частицах, с температурой денатурации белка, равной 136оС, 200оС и выдержкой в течение 2 и 8 ч, а также воздействием гамма-облучения в дозе 0,1 и 1,0 МГр.
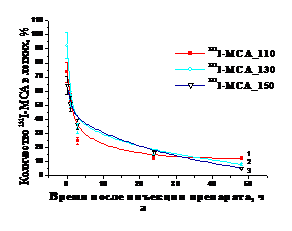
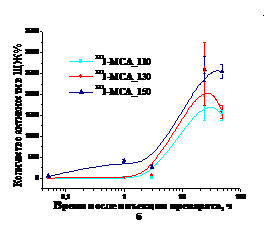
Сравнение данных биораспределений 131I-МСА, полученных при разных температурах, в организме интактных крыс после внутривенного введения показало, что не выявлено существенного влияния температуры денатурации белка в пределах 110–150оС на фармакокинетические свойства препарата (рис. 3а). Максимальный уровень накопления активности в легких меченых МСА, полученных при температуре 110, 130 и 150оС, отмечается через 5 мин после внутривенного введения и статистически достоверных различий при этом не выявлено (p > 0,1–0,25). В последующие сроки количество меченого препарата в легких снижается приблизительно с одинаковой скоростью (p > 0,05–0,1). Выведение активности из легких в течение 1–48 ч сопровождается закономерным накоплением ее в неблокированной щитовидной железе (ЩЖ). Активность ЩЖ закономерно увеличивается, что свидетельствует о постепенном гидролизе МСА и выведении свободного радиоактивного йода с поверхности частиц (рис. 3б).
|
|
Рис. 3. Динамика накопления и выведения активности из легких (а) и щитовидной железы (б) после внутривенного введения 131I-МСА, полученных при , и 150оС (3). |
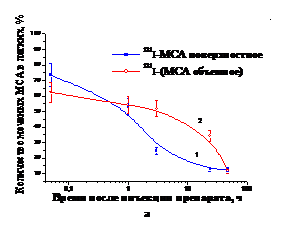
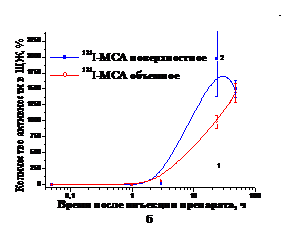
Анализ сравнительных данных распределения активности в организме крыс после внутривенного введения 131I-МСА с поверхностным и объемным распределением радионуклида в частицах показал, что в течение первого часа исследования заметных различий в уровне накопления активности в легких не выявляется (p < 0,25–0,5), тогда как содержание в легких МСА с объемным распределением радионуклида в частицах в период наблюдений 3 – 24 ч статистически достоверно выше по сравнению с поверхностным распределением активности в частицах (p < 0.02–0,001) (рис. 4а). Выведение активности из легких происходит с периодом биологического полувыведения, равным 1,6 ч, после инъекции 131I-МСА с поверхностным распределением радионуклида, и 21,1 ч – с объемным распределением радионуклида в частицах. Ускоренное выведение активности из легких, когда радионуклид распределяется на поверхности частиц, сопровождается более интенсивным накоплением активности в неблокированной щитовидной железе, по сравнению с объемным распределением радионуклида в частицах, что позволяет косвенно судить о времени внутрисосудистого рассасывания микросфер альбумина (рис. 4б).
|
|
Рис. 4. Динамика накопления и выведения активности из легких (а) и щитовидной железы (б) после внутривенного введения 131I-МСА, полученных при 110оС, с поверхностным (1) и объемным (2) распределением радионуклида в частицах. |
Детальное изучение влияния степени сшивки белковой матрицы МСА после теплового воздействия и предварительного гамма-облучения на фармакокинетические свойства после внутримышечного введения препарата мышам было проведено с помощью 103Pd-МСА диаметром 20–40 мкм с объемным распределением радионуклида в частицах.
103Pd-МСА получали методом ионной сорбции 103Pd в белковую матрицу МСА. Для инкорпорирования максимального количества 103Pd в МСА к радиоактивному палладию добавляли стабильный палладий (PdCl2). Для фиксации в пористой структуре МСА палладий восстанавливали до оксида.
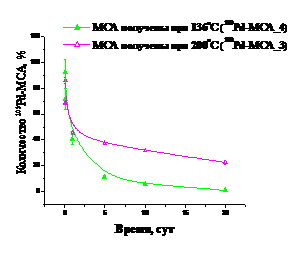
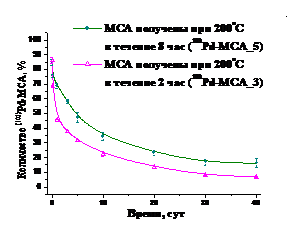
В результате исследований показано, что скорость выведения 103Pd из мышечной ткани после внутримышечной инъекции 103Pd-МСА, полученных при 136оС, выше, чем в случае 103Pd-МСА, полученных при 200оС (рис. 5). Длительность теплового воздействия на белок также оказывает влияние на скорость выведения активности из мышцы после внутримышечного введения 103Pd-МСА (рис. 6). Увеличение длительности теплового воздействия на МСА снижает интенсивность выведения активности из мышечной ткани. Это объясняется тем, что МСА, полученные при более низкой температуре и более короткого теплового воздействия, имеют пониженную степень сшивки белка, что увеличивает скорость его протеолиза и тем самым повышает скорость высвобождения 103Pd из состава микросфер.
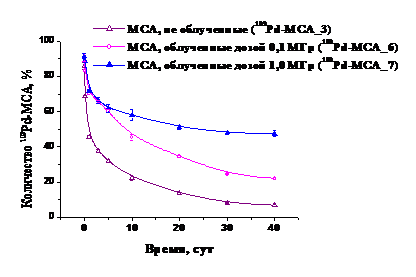
Наиболее существенное влияние на степень денатурации белка и тем самым снижение скорости выведения активности из мышцы оказывает предварительное гамма-облучение МСА (рис. 7). Из анализа параметров выведения активности из мышечной ткани после инъекции 103Pd-МСА необлученных и предварительно облученных в дозе 0,1 и 1,0 МГр следует, что периоды полувыведения различаются в значительной степени и составляют 1,02 сут, 8,57 сут и 23,6 сут, соответственно. При этом количества 103Pd-МСА в мышце в течение 40 суток снижаются в 12,6, 4,1 и 1,9 раз, соответственно, для необлученных микросфер и облученных в дозе 0,1 и 1,0 МГр.
|
|
Рис. 5. Динамика выведения активности из мышцы бедра после внутримышечного введения 103Pd-МСА, полученных при температурах 136оС и 200оС. | Рис 6. Динамика выведения активности из мышцы бедра после внутримышечного введения 103Pd-МСА, полученных при температуре 200оС в течение 2 и 8 ч. |
|
Рис. 7. Динамика выведения активности из мышцы бедра после внутримышечного
введения 103Pd-МСА, предварительно гамма-облученных в дозах 0,1 и 1,0 МГр.
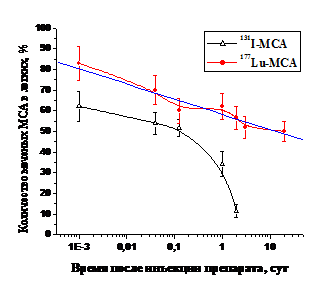
Воздействие тепловых нейтронов на степень денатурации белка оказывается еще более существенным, чем гамма-облучение. Для изучения этого феномена были разработаны и получены 177Lu-МСА путем активации стабильного 176Lu в составе МСА тепловыми нейтронами с потоком 2.1013 н/см2·с в течение 1 ч. На рис. 8 представлены кривые выведения активности из легких после внутривенной инъекции 131I-МСА, полученных тепловой сшивкой белка при 150оС и 177Lu-МСА, полученных нейтрон-активационным способом. Сравнение параметров выведения активности из легких после инъекции препаратов показало, что 177Lu-МСА выводятся значительно медленнее по сравнению с 131I-МСА: биологические периоды полувыведения – 121,5 и 0,84 сут, соответственно.
|
Рис. 8. Динамика накопления и выведения активности из легких после внутривенного
введения 131I-МСА и 177Lu-МСА с объемным распределением радионуклидов в частицах.
Дисперсный состав является важнейшей характеристикой частиц, оказывающий существенное влияние на фармакокинетические свойства меченых МСА. В связи с этим было проведено изучение фармакокинетики 131I-МСА диаметром 0,5–2, 0,5–5, 10–20 мкм и 99mTc-МСА диаметром 0,5–2 и 10–20 мкм в организме интактных крыс после внутривенного введения препаратов.
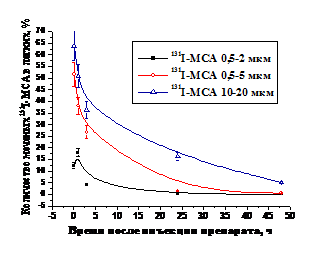
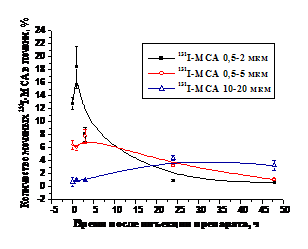
Результаты исследования показали, что через 5 мин после инъекции 131I-МСА диаметром 0,5–5 и 10–20 мкм величины накопления их в легких существенных различий не имеют и составляют, соответственно, 51,6 и 63,9% в 1 г легочной ткани (р > 0.1), тогда как у 131I-МСА диаметром 0,5–2 мкм этот показатель составляет 12,4% (p < 0,001). Это свидетельствует о том, что частицы меньше 5 мкм проходят капиллярную сеть легких. Скорость выведения активности из легких закономерно увеличивается с уменьшением размера 131I-МСА (рис. 9а). Так, например, удельная активность легких в течение 48 ч уменьшается после инъекции 131I-МСА диаметром 0,5–2 мкм в 103,3 раза, 05–5 мкм – в 95,6 раза и 10–20 – в 12,6 раз. С уменьшением размера частиц растет накопление активности в печени (рис. 9б). Аналогичные закономерности распределения активности в легких и печени наблюдаются и после внутривенного введения 99mТс-МСА диаметром 0,5–2, и 10–20 мкм
Результаты изучения фармакокинетики 131I-МСА диаметром 0,5–2 и 5–10 мкм после инъекции в бедренную артерию кроликов показали, что все частицы депонируются в мышечной ткани. Накопление 131I-МСА диаметром 0,5–2 и 5–10 мкм в мышце бедра, в пересчете на 1 г мышечной ткани, через 5 мин после
|
|
Рис. 9а. Динамика выведения активности из легких крыс после внутривенного введения 131I-МСА с разными размерами, полученных при 150оС. | Рис. 9б. Динамика выведения активности из печени крыс после внутривенного введения 131I-МСА с разными размерами, полученных при 150оС. |
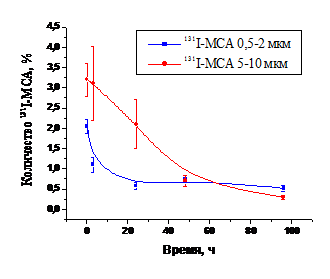
внутриартериального введения на 2–3 порядка выше, чем в большинстве других органов и тканей. В последующие сроки активность в мышце бедра быстро снижается (рис. 10). Выведение активности из мышцы бедра в течение первых
60 ч происходит более быстрыми темпами после инъекции 131I-МСА диаметром 0,5–2 мкм по сравнению 131I-МСА диаметром 5–10 мкм.
|
Рис. 10. Динамика выведения активности из мышцы бедра кроликов после
инъекции 131I-МСА диаметром 0,5–2 и 5–10 мкм в бедренную артерию.
Для оценки влияния химической природы радионуклида на динамику накопления и выведения активности из легких была изучена фармакокинетика МСА диаметром 10–20 мкм, меченных 131I, 111In и 99mTc, после внутривенного введения препаратов. Результаты исследований показали, что химическая природа радионуклида оказывает влияние на поведение меченых МСА в организме. Выведение активности из легких происходит наиболее интенсивно при инъекции 111In - и 99mТс-МСА (рис. 11). Более интенсивное выведение активности из легких после инъекции 111In - и 99mТс-МСА связано, по-видимому, с тем, что связь 111In и 99mТс с белком менее прочная, по сравнению с 131I. Подтверждением более интенсивной элиминации активности из легких 111In - и 99mТс-МСА, по сравнению 131I-МСА, является сравнительно быстрое нарастание уровня активности в печени (до 3,55% от введенного количества через 24 ч после инъекции 111In-МСА) и в почках (до 9,98% в этот же срок после инъекции 99mТс-МСА), тогда как после инъекции 131I-МСА накопление активности в печени и почках через 24 ч составляло всего 0,23% и 0,27%, соответственно.
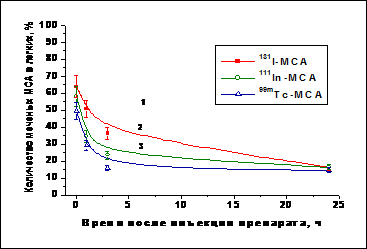
Рис. 11. Динамика выведения активности из легких интактных крыс после
внутривенного введения 131I-, 111In - и 99мТс-микросфер альбумина, полученных при 150оС.
Для изучения возможности использования меченых МСА в оценке капиллярного кровотока легких в норме и с патологией были изучены фармакокинетические свойства препарата в организме кроликов с экспериментальными моделями легочной патологии: гамма-облучение легкого, эмболия легочной артерии и рак легкого.
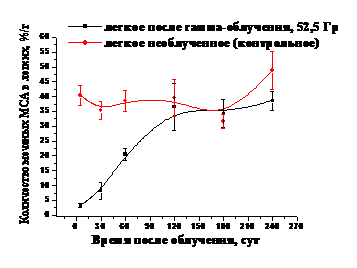
В опытах на кроликах с облученным правым легким гамма-квантами в общей дозе 52,5 Гр показано, что через 24 ч после внутривенного введения 131I-МСА диаметром 10–20 мкм минимальный уровень накопления активности в облученном легком отмечается через 5 сут после облучения и составляет 3,29% от введенного количества меченого препарата (рис. 12). Эта величина в 12,7 раз меньше по сравнению с аналогичным показателем в левом необлученном легком (p< 0,001). Через 30 и 60 сут после облучения величины накопления меченых МСА в облученном легком увеличиваются, соответственно, в 2,52 и 6,23 раз
(p < 0,02), по сравнению с 5-ю сут после облучения, однако в 4,24 (p < 0,002) и 1,88 раз (p < 0,02) ниже по сравнению с аналогичной величиной контрольного легкого. Эти данные свидетельствуют о постепенном восстановлении капиллярного кровотока в левом облученном легком в более поздние сроки после облучения. Через 120 сут и в последующие сроки вплоть до 240 сут после облучения уровень накопления активности в облученном легком изменяется незначительно, и статистически достоверные различия по сравнению с необлученным легким не выявляются (p > 0,25–0,5). Полученные результаты являются свидетельством того, что через 120 сут после облучения капиллярный кровоток в левом облученном легком практически полностью восстанавливается (рис. 12).
|
Рис. 12. Накопление 131I-МСА в легком после гамма-облучения дозой 52,5 Гр.
Изучение распределения 131I-МСА диаметром 10–20 мкм в организме кроликов с эмболией легочной артерии показало, что уровень накопления активности в непораженных участках легких через 1, 3 и 5 сут после получения модели патологического состояния изменяется незначительно и составляет 11,0–18,3% в 1 г ткани от введенного количества препарата (p > 0,05) (табл. 4). Накопление активности в пораженных участках легких регистрируется на уровне следовых количеств и не зависит от срока получения эмболии легочной артерии. Удельная активность пораженных участков легких в 524-704 раза ниже, чем непораженной ткани легкого (Р< 0,001).
Таблица 4 – Результаты распределения 131I-МСА в легких кроликов с экспериментальной эмболией легочной артерии через 3 ч после внутривенного введения препарата (в % от введенного количества на 1 г массы органов и тканей).
№ пп. | Орган, ткань | Контроль | Время после воспроизведения модели, сут. | ||
1 | 3 | 5 | |||
1 | Легкие: здоровый участок | 4,38±0,64 | 11,01±2,03 | 11,16±2,03 | 18,32±2,73 |
2 | Легкие: пораженный участок | – | 0,021±0,003 | 0,017±0,004 | 0,026±0,005 |
Результаты изучения распределения 131I-МСА диаметром 10–20 мкм в организме кроликов с экспериментальным раком показали, что удельная активность непораженных опухолевым процессом участков легочной ткани кроликов с раком легких практически не изменяется в течение 24 ч после внутривенной инъекции препарата (p > 0,1), в то время как удельная активность легких контрольных кроликов существенно снижается в течение 24 часов с 6,58 % до 1,89 % (p < 0,05) (табл. 5). Неизменный уровень активности в непораженных участках свидетельствует о нарушении протеолитической функции легких, пораженных опухолевым процессом. Напротив, в здоровых легких контрольной группы кроликов происходит активный протеолиз МСА с элиминацией активности из этого органа.
Таблица 5 – Динамика распределения активности в легких кроликов с экспериментальным раком легкого после внутривенного введении меченых МСА диаметром 10–20 мкм (в % от введенного количества на 1 г массы ткани).
№ пп. | Орган и ткань | Время после введения препарата | ||
1 ч | 3 ч | 24 ч | ||
1 | Легкие, здоровый участок | 4,02±0,71* 6,58±0,65** p > 0,05 | 5,66±1,49 4,38±0,64 p > 0,5 | 6,42±0,88 1,89±0,10 p < 0,01 |
2 | Легкое, участок с опухолью | 1,63±0,40 – | 0,92±0,18 – | 1,07±0,26 – |
* Величины удельной активности органов и тканей кроликов с раком легких. ** Величины удельной активности органов и тканей контрольных кроликов. |
При сопоставлении величин удельной активности пораженной легочной ткани было установлено, что в опухолевом очаге этот показатель через 3 ч после инъекции 131I-МСА составляет 0,92±0,18% от введенного количества, тогда как при экспериментальной эмболии легочной артерии аналогичная величина составляет 0,017±0,004%. Полученные результаты свидетельствуют о том, что

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |