нарушение капиллярного кровотока участков легких, пораженных опухолевым процессом, происходит в меньшей степени, чем при эмболии легочной артерии.
В результате экспериментальных исследований установлено, что меченые микросферы альбумина диаметром 10–20 мкм являются эффективным радиофармпрепаратом для определения с высокой точностью степени нарушения капиллярного кровотока в пораженных участках легких с различными патологическими состояниями этого органа.
Для изучения влияния патологического состояния ткани на закономерности протеолиза и снижения относительной активности в месте ее локализации были проведены сравнительные исследования фармакокинетики 103Pd-МСА диаметром 5–10 мкм и 20–40 мкм в организме интактных мышей и мышей с опухолью (карцинома Эрлиха), соответственно, при внутримышечном и внутриопухолевом введении меченых препаратов.
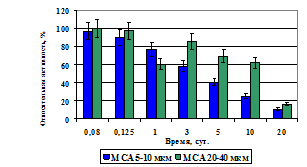
Сравнительный анализ данных активности в мышце показал, что уровни содержания 103Pd в течение первых 3 ч после внутримышечного введения 103Pd-МСА диаметром 5–10 и 20–40 мкм статистически достоверно не различаются (p > 0,25–0,05) (рис 13а). В последующие сроки наблюдений отмечается статистически достоверное снижение активности в мышце бедра, причем, наиболее заметное снижение наблюдается для 103Pd-МСА диаметром 5–10 мкм (p < 0,02).
а |
б |
Рис. 13. Сравнительные данные уровней накопления 103Pd в мышце (а) и почках (б)
после внутримышечного введения 103Pd-МСА диаметром 5–10 и 20–40 мкм.
Эта тенденция сохраняется до конца срока наблюдений. Через 10 сут содержание 103Pd в мышце составляет 24,9% при инъекции 103Pd-МСА диаметром 5–10 мкм и 61,6% при инъекции 103Pd-МСА диаметром 5–10 мкм (p < 0,001), через 20 сут – соответственно, 10,5% и 16,3% (p < 0,021). Полученные данные свидетельствуют о том, что элиминация 103Pd из МСА 5–10 мкм протекает интенсивнее, чем из МСА диаметром 20–40 мкм. Это связано, по-видимому, с наиболее высокой скоростью протеолиза денатурированного белка МСА меньших размеров за счет наибольшей удельной поверхности частиц.
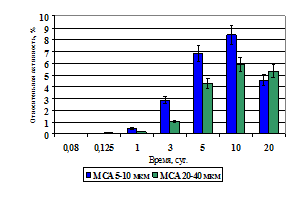
Снижение уровня 103Pd в мышце сопровождается повышенным накоплением активности в почках. В течение первых 3 часов относительное содержание активности в почках отмечается на уровне следовых количеств, так как в этот период практически весь 103Pd локализован в мышечной ткани (рис. 13а и 13б). В более поздние сроки наблюдений активность в почках постепенно увеличивается, что связано с постепенных рассасыванием МСА в мышце и выделением не связанного 103Pd. Причем, при введении 103Pd-МСА диаметром 5–10 мкм накопление активности в почках происходит более быстрыми темпами, чем при введении 103Pd-МСА диаметром 20-40 мкм.
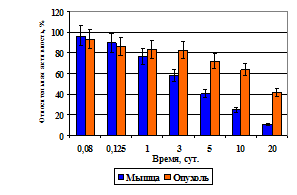
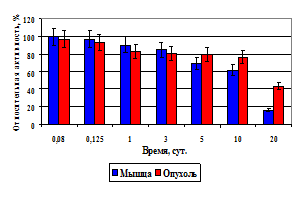
В результате исследований показано, что в течение первых 24 ч 103Pd-МСА диаметром 5–10 мкм и 20–40 мкм удерживаются в мышце и опухоли практически на одном уровне и составляют около 90% от введенного количества (p>0,25) (рис. 14а и 14б). В последующие сроки уровень активности продолжает снижаться в мышце и опухоли как в случае с 103Pd-МСА диаметром 5–10 мкм, так и 20–40 мкм, при этом наиболее заметное снижение относительной активности отмечается из мышечной ткани для микросфер меньших размеров. Выведение 103Pd-МСА из мышечной ткани происходит более быстрыми темпами, чем из опухолевой ткани. 103Pd-МСА диаметром 5–10 мкм выводятся интенсивнее из мышечной ткани, чем 103Pd-МСА диаметром 20–40 мкм. Это приводит к достоверным различиям в величинах содержания в мышце меченых МСА диаметром 5–10 мкм через 3 сут (p < 0,001), тогда как для 103Pd-МСА диаметром 20–40 мкм статистически достоверные различия в этих величинах выявляются только через 10 сут после инъекции препарата. Такая же тенденция сохраняется до 20 сут. Более интенсивная элиминация активности из мышечной ткани в случае 103Pd-МСА диаметром 5–10 мкм по сравнению с 103Pd-МСА 20–40 мкм объясняется тем, что более мелкие МСА имеют большую удельную поверхность, а значит и биодеградация их происходит интенсивнее, чем более крупных частиц. Выведение 103Pd из мышечной и опухолевой ткани находится в полном соответствии с закономерностями накопления активности в почках. Чем интенсивнее выводится 103Pd из мышцы и опухоли, тем выше накопление его в почках, что свидетельствует о наличии четкой корреляции между выведением 103Pd из мышечной и опухолевой ткани и накоплением его в почках.
а |
б |
Рис. 14. Накопление активности в опухоли после внутриопухолевого введения 103Pd-МСА
диаметром 5–10 мкм (а) и 20–40 мкм (б).
Установлено, что размер 103Pd-МСА не оказывает существенного влияния на скорость выведения активности из опухолевой ткани (рис. 15), тогда как в мышечной ткани размеры частиц влияют на этот процесс. Это явление, очевидно, объясняется более слабым кровотоком и, соответственно, низкой интенсивностью метаболических процессов в центре опухоли по сравнению с мышечной тканью.
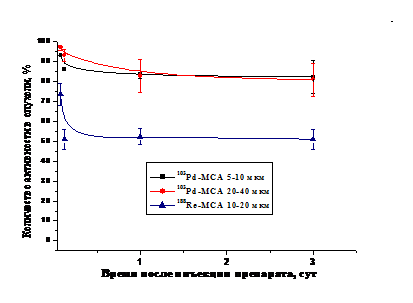
Результаты сравнительных исследований фармакокинетики в организме мышей-опухоленосителей 103Pd-МСА, с инкорпорированным радионуклидом по всему объему частиц, и 188Re-МСА с распределением радионуклида на поверхности частиц показали, что 188Re выводится из опухоли интенсивнее, по сравнению с 103Pd (рис. 16). Эти данные свидетельствуют о том, что радиоактивная
метка, связанная с поверхностью частиц, элиминируется из опухоли сравнительно быстро в результате гидролиза связи радионуклида с белком, а также в результате протеолиза поверхностного слоя МСА.
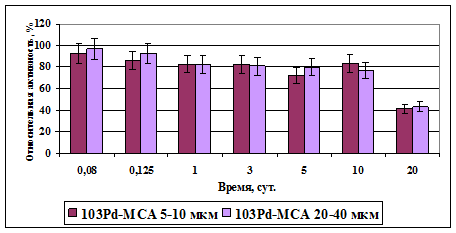
Рис. 15. Сравнительные данные уровня накопления 103Pd в опухоли после внутриопухолевого введения 103Pd-МСА диаметром 5–10 и 20–40 мкм (в % от введенного количества).
|
Рис.16. Сравнительные данные уровня накопления 103Pd-МСА и 188Re-МСА
в опухоли после внутриопухолевого введения.
Дозиметрические характеристики меченых микросфер альбумина
В процессе разработки и биологических испытаний новых диагностических и терапевтических радиофармпрепаратов в первую очередь необходимы сведения о создаваемых ими поглощенных дозах в опухоли, в органах, тканях и во всем организме. Это важно с точки зрения безопасности РФП.
Средние поглощенные дозы внутреннего облучения всего тела и некоторых органов, создаваемые препаратами, меченными диагностическими радионуклидами, такими, как 99mTc (T1/2 = 6 ч), 113mIn (T1/2 = 1,73 ч) и 123I (T1/2 = 13 ч), 131I (T1/2 = 8,04 сут), представлены в табл. 6.
Из данных таблицы видно, что поглощенные дозы во всем организме и органах, создаваемые 131I, на порядок выше по сравнению с 99mTc, 113mIn и 123I. Из перечисленных в табл. 6 органов, в легких формируется наиболее высокая поглощенная доза, в остальных органах дозы сравнительно невелики. Это связано, с тем, что в легких накапливается до 70–90% меченых МСА. Из радионуклидов 99mTc, 113mIn и 123I, наименьшая поглощенная доза в легких создается 99mTc.
Таблица 6 – Средние поглощенные дозы в организме и некоторых органов крыс после однократного внутривенного ведения меченых МСА.
№ пп. | Наименование препарата | Средние поглощенные дозы внутреннего облучения, мГр/МБк | |||||
Все тело | Легкие | Щитовидная железа | Печень | Селезенка | Тонкая кишка | ||
1 | 99mTc-МСА | 0,54 | 20,0 | 2,00 | 4,05 | 2,97 | 3,51 |
2 | 113mIn-МСА | 1,11 | 83,7 | 1,35 | 0,49 | 0,38 | 0,81 |
3 | 123I-МСА | 2,78 | 162,0 | 9,45 | 2,78 | 2,24 | 2,75 |
4 | 131I-МСА | 55,8 | 2214,0 | 220,3 | 25,4 | 22,1 | 27,0 |
Погрешность в величинах средних поглощенных доз не превышала 25% |
Патологическое состояние легких не оказывает существенного влияния на формирование поглощенной дозы внутреннего облучения. Так, например, при однократном введении 123I-МСА крысам с асептическим воспалением легких средняя поглощенная доза в этом органе составляет 2,83 мГр/МБк, против 2,78 мГр/МБк в легких здоровых животных.
Формирование поглощенной дозы в опухоли практически заканчивается через 15 – 20 суток после внутриопухолевого введения 103Pd-МСА и составляет
120 Гр/ГБк (рис. 17). В прилегающей к опухоли мышце бедра экспериментальных животных через 15 дней после введения 103Pd-МСА накопленная поглощенная доза оказалась в 15 раз меньше, чем доза облучения опухоли, а в критическом органе (почки) накопленная доза облучения в 20 раз меньше поглощенной дозы в опухоли.
При однократном введении 103Pd-МСА в центр опухоли распределения доз внутреннего облучения имеют большую степень неравномерности по объему опухоли. Для получения более равномерного распределения дозы внутри опухоли необходимо вводить препарат в несколько точек опухоли. Расчеты показали, что введение 103Pd-МСА в 10 точек создает однородное распределение поглощенной дозы по всему объему опухоли.
Таким образом, в результате выполненных исследований показано, что при разработке эффективных радиофармпрепаратов, предназначенных для радионуклидной диагностики и терапии онкологических и неонкологических заболеваний, необходимо использовать комплексный подход, включающий изучение фармакокинетических свойств и дозиметрических характеристик. Следуя этому принципу, решена проблема создания ряда эффективных радиофармпрепаратов на основе сывороточного альбумина человека.
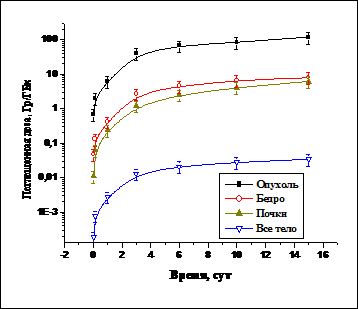
Рис. 17. Поглощенные дозы в организме мышей с карциномой Эрлиха после
внутриопухолевого введения 103Pd-МСА диаметром 20–40 мкм.
В результате экспериментальных исследований разработаны лиофилизаты с оптимальными составами для получения радиофармпрепаратов на основе генераторного радионуклида 99mTc в условиях клиники непосредственно перед инъекцией пациенту. 99mTc-альбумина прошел доклинические испытания, 99mTc-микросферы альбумина прошел доклинические и клинические испытания, и зарегистрирован в реестре лекарственных средств.
В Ы В О Д Ы
1. Разработана и оптимизирована технология получения РФП «99mTc-альбумин» и «99mTc-наноальбумин». Показано, что синтезированные РФП обладают высоким радиохимическим выходом (не менее 95%) и стабильностью in vivo, что подтверждено результатами изучения фармакокинетики РФП в организме лабораторных животных.
2. Экспериментально доказана функциональная пригодность РФП. Показано, что до 50% 99mTc-альбумина от введенного количества в течение трех часов после внутривенной инъекции циркулирует в крови, что позволяет использовать РФП для изучения гемодинамических характеристик; 99mTc-наноальбумин при подкожном введении избирательно накапливается в лимфатичеких узлах, при внутривенном введении – в печени, что позволяет использовать его для сцинтиграфии этих органов.
3. В экспериментальных исследованиях показано, что такие факторы: как дисперсный состав частиц, степень денатурации белка, пространственное распределения радионуклида в частицах, способ введения РФП, химическая природа радионуклида оказывают заметное влияние на фармакокинетику меченых МСА в организме лабораторных животных.
4. 177Lu-МСА, полученные нейтрон-активационным способом, удерживаются в легких крыс на уровне 50% от введенного количества в течение 20 суток после внутривенного введения.
5. Изучение закономерностей инкорпорирования 103Pd в белковую матрицу МСА, исследования влияния температуры денатурации белка и воздействия гамма-облучения на характер поведения 103Pd-МСА в организме лабораторных животных, явилось результатом создания оптимизированной технологии получения нового РФП «103Pd-МСА» с оптимальными характеристиками для лечения опухолей.
6. Фармакокинетика меченых МСА в организме кроликов после гамма-облучения легких, индуцированной эмболией легочной артерии и раком легких, показала функциональную пригодность препарата в оценке состояния капиллярного кровотока легких с различными патологическими состояниями.
7. После внутриопухолевого введения мышам-опухоленосителям 103Pd-МСА установлен факт длительного удержания меченого препарата опухолевой тканью.
8. В результате оценки поглощенных доз внутреннего облучения показано, что при внутриопухолевом введении нового терапевтического радиофармпрепарата 103Pd-МСА позволяет осуществлять избирательное облучение опухоли (в 15 раз больше) по сравнению с прилегающими тканями и критическими органами. После внутривенного введения диагностических РФП (113mIn-, 123I - и 99mTc-МСА) наиболее низкие поглощенные дозы внутреннего облучения легких формируются от 99mTc-МСА.
СПИСОК ОСНОВНЫХ РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. | Хачиров Дж. Г., Петриев диагностика пневмонии с помощью меченых микросфер альбумина сыворотки человеческой крови (экспериментальное исследование) // Медицинская радиология. – 1978. – Т. 23. – № 8. С. 28–34. |
2. | , , Хачиров Дж. Г. Физические и некоторые радиохимические свойства микросфер альбумина, используемых в радиоизотопной диагностике // Isotopenpraxis. – 1979. – V. 15. – No. 5. – P. 22–25. |
3. | , Хачиров Дж. Г. Диагностика экспериментального рака легких с помощью меченых микросфер альбумина // Медицинская радиология. – 1979. – Т. 24. – № 4. – С. 29–34. |
4. | , Хачиров Дж. Г., Кирьяков диагностика эмболии легочной артерии с помощью меченых микросфер альбумина в эксперименте // Медицинская радиология. – 1979. – Т. 24. – № 8. – С. 31–35. |
5. | Dz. G.Chacirov, V. M.Petriev Die vergleichende Beurteilung der markierten Humanserumalbumin-Praparate binsichtlich ihrer Dekorporirung (Experimentaluntersuchung) // Radiobiol. Radiother. – 1980. – V.21. – № 4. – C. 537–543. |
6. | , Степченков -активационный способ получения меченых микросфер альбумина // Isotopenpraxis. – 1980. – V. 16. – № 6. – P. 202–203. |
7. | , , Хачиров Дж. Г. Физико-химические свойства меченых микросфер альбумина, получаемых активацией нейтронами // Isotopenpraxis. – 1981. – V. 17. – № 8/9. – P. 315–317. |
8. | , Степаненко дозы в организме и некоторых органах животных при введении меченых микросфер альбумина // Медицинская радиология. – 1981. – Т. 26. – № 9. – С. 60–61. |
9. | , Хачиров Дж. Г., , Петриев 131I-микросфер альбумина сыворотки крови человека при их введении в лимфатические сосуды // Медицинская радиология. – 1983. – Т. 28. – № 2. – С. 18–24. |
10. | Chacirov Dz. G., Ispenkova L. I., Petriev V. M. Tierexperimentelle Radiopharmakokinetik endolymphatisch applizierter markieter Albumin-Mikrospharen zur Diagnostik regionarer Lymphknotentumoren. 3. Mitteilung // Radiology Diagnostic. – 1984. – V. 25. – No. 5. – P. 623–628. |
11. | Хачиров Дж. Г., , Петриев распределения ударного объема сердца в организме собак со спонтанным пародонтозом с помощью 125I-микросфер альбумина // Стоматология. – 1986. – Т. 65. – № 4. – С. 11–13. |
12. | , , Петриев местного капиллярного кровотока с помощью меченых микросфер альбумина при остеотомии верхней челюсти (экспериментальное исследование) // Медицинская радиология. – 1989. – Т. 34. – № 3. – С. 65–69. |
13. | , , Петриев 125I-микросфер сывороточного альбумина в организме кроликов при селективном введении препаратов в печеночную артерию // Медицинская радиология. – 1990. – Т. 35. – № 11. – С. 26–29. |
14. | , М, , Гончарова селективная терапия цитостатиками и радиофармпрепаратами при злокачественных новообразованиях (обзор) // Вопросы онкологии. – 1992. – Т. 38. – № 7 – С. 771–777. |
15. | , , Скворцов радионуклиды в экспериментальной ядерной медицине и биологических исследованиях // Ядерная энергетика. – 2000. – № 4. – С. 70–75. |
16. | , , Рыжикова микросфер альбумина, содержащих стабильный рений, для моделирования радиоактивных и нерадиоактивных аэрозолей // Ядерная энергетика. – 2000. – № 4. – С. 76–79. |
17. … | , , Скворцов фармакокинетики 99мТс-альбумина крови человека в организме лабораторных животных // Вопросы биологической, медицинской и фармацевтической химии. – 2003. – № 3. – С. 30–34. |
18. | , , Рыжикова -активационный способ получения 166Нo-микросфер альбумина – потенциального радиофармпрепарата для лечения онкологических заболеваний // Радиохимия. – 2005. – Т. 47. – № 3, – С. 274–277 |
19. | , , Шутова радионуклидных примесей в 166Нo-микросферах альбумина, получаемых активацией тепловыми нейтронами // Радиохимия. – 2005. – Т. 47, № 3. – С. 278–280 |
20. | Petriev V. M., Skvortsov V. G., Smakhtin L. A., Ryzhikova T. P. Neutron Activation Preparation of 166Ho-Albumin Microspheres as a Promising Radiopharmaceutical for Tumor Therapy // Radiochemistry. – 2005. – V. 47. – No. 3. – P. 301–304. |
21. | Petriev V. M., Skvortsov V. G., Smakhtin L. A., Shutova I. N. Monitoring of Radionuclide Impurities in 166Ho-Albumin Microspheres Prepared by Neutron Activation with Thermal Neutrons // Radiochemistry. – 2005. – V. 47. – No. 3. – P. 305–307. |
22. | , Орлов примеси в 166Но-микросферах альбумина, образующиеся при облучении тепловыми нейтронами // Ядерная энергетика. – 2006. – № 3. – C. 97–104. |
23. | , , Сморызанова способность 188-рения с микросферами альбумина крови человека // Труды регионального конкурса научных проектов в области естественных наук, КНЦ АКО, РФФИ, Калуга. – 2007. – Вып. 12. – С. 195–204. |
24. | , Закономерности образования комплексного соединения 188Re с микросферами альбумина крови человека // Радиохимия. – 2009. – Т. 51. – № 5. – С. 446–451. |
25. | Petriev V. M., Regular trends in complexation of 188Re with human blood albumin microspheres // Radiochemistry. – 2009. – V. 51. – No. 5 – P. 510–516. |
26. | , , Скворцов метода получения 103Pd-микросфер альбумина крови человека – потенциального радиофармпрепарата для лечения злокачественных опухолей. Радиохимия. – 2010. – Т. 52. – № 2. – С. 177–180. |
27. | Petriev V. M., Shiryaev V. K., Smakhtin L. A., Skvortsov V. G. Development of a Procedure for Preparing 103Pd-Microspheres of Human Blood Albumin, a Potential Radiopharmaceutical for Treatment of Malignant Tumors // Radiochemistry. – 2010. – V. 52. – No. 2. – P. 207–211. |
28. | , , Ю, , Орленко C. П., , Цыб и дозиметрические характеристики нового радиофармпрепарата 103Pd-микросферы альбумина // Радиационная биология Радиоэкология. – 2010. – Т. 50. – № 6. – С. 703–711. |
29. | , , Дозы внутреннего облучения организма в экспериментальных исследованиях нового препарата на основе 103Pd и микросфер альбумина для радионуклидной терапии // Труды регионального конкурса научных проектов в области естественных наук, КНЦ АКО, РФФИ, Калуга. – 2010. – Вып. 15. – С. 171–180. |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |