На правах рукописи
ПЕТРИЕВ
Василий Михайлович
ФАРМАКОКИНЕТИЧЕСКИЕ СВОЙСТВА И ДОЗИМЕТРИЧЕСКИЕ ХАРАКТЕРИСТИКИ РАДИОФАРМПРЕПАРАТОВ НА ОСНОВЕ
СЫВОРОТОЧНОГО АЛЬБУМИНА ЧЕЛОВЕКА
03.01.01 – Радиобиология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора биологических наук
Обнинск – 2011
Работа выполнена в Федеральном государственном бюджетном учреждении
«Медицинский радиологический научный центр»
Министерства здравоохранения и социального развития Российской Федерации
Научный консультант: доктор медицинских наук, профессор, академик РАМН ЦЫБ Анатолий Федорович
Официальные оппоненты:
доктор биологических наук, профессор УЛЬЯНЕНКО Лилия Николаевна,
доктор биологических наук, профессор ПЕТИН Владислав Георгиевич,
доктор биологических наук
КОМАРОВА Людмила Николаевна.
Ведущая организация: Учреждение Российской академии наук «Институт
мозга человека им. » РАН.
Защита состоится 25 октября 2011 года в 11.00 часов на заседании
диссертационного совета Д 208.132.01 при Федеральном государственном бюджетном учреждении «Медицинский радиологический научный центр» Министерства здравоохранения и социального развития Российской Федерации
г. Обнинск Калужской области, ул. Королева, 4.
С диссертацией можно ознакомиться в библиотеке ФГБУ «Медицинский
радиологический научный центр» Минздравсоцразвития России.
Автореферат разослан «_____»______________2011 г.
Ученый секретарь
диссертационного совета
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы.
Настоящее исследование направлено на решение актуальной радиобиологической проблемы ядерной медицины – поиску новых радиофармпрепаратов (РФП) для радионуклидной диагностики и терапии социально значимых, в том числе онкологических, заболеваний, радиобиологическому и дозиметрическому сопровождению создания новых РФП.
Актуальность проблемы обусловлена неуклонным ежегодным ростом числа онкологических заболеваний, которые продолжают оставаться в списке лидеров в структуре причин смертности населения промышленно развитых стран. Своевременная и полноценная диагностика этих заболеваний и эффективность их лечения в значительной степени обусловлены применением современных ядерно-медицинских технологий, которые, к сожалению, являются “слабым местом” отечественного здравоохранения. Решение указанных проблем во многом связано с созданием и применением в клинической практике РФП, обладающих как высокой функциональной пригодностью, так и безопасностью в широком смысле этого термина.
Как известно, разработка и создание высокоэффективных РФП носит междисциплинарный характер, но основой всего является выбор радионуклидов с оптимальными ядерно-физическими характеристиками и их носителей, среди которых важное место занимает сывороточный альбумин человека.
РФП на основе сывороточного альбумина человека характеризуются лучшей физиологичностью и технологичностью их получения, возможностью получать наночастицы и микрочастицы с заданными размерами и программируемой скоростью протеолиза их в организме, возможностью инкорпорировать практически любые радионуклиды, прочно удерживать их в составе частиц и высвобождать по мере протеолиза денатурированного белка.
В мировой литературе отсутствуют сведения о системных и комплексных сравнительных исследованиях по разработке и биологическому изучению препаратов на основе сывороточного альбумина человека, меченных радионуклидами диагностического и терапевтического назначения, имеются лишь отдельные сведения [Mayron L. G., Kaplann E., 1975; Szymendera J., et al., 1977; Hnatowich D. G., Schlegel P., 1981; O’ Donnell P. B., McGinity J. W., 1997; Wang S. J., et al., 1998; Wang Y. F. et al., 2007]. Отсутствие комплексных радиохимических, фармакокинетических и дозиметрических исследований затрудняет выбор оптимальных по составу и функциональным признакам РФП для радионуклидной диагностики и терапии онкологических и неонкологических заболеваний.
Актуальность изучения фармакокинетических свойств и дозиметрических характеристик новых РФП состоит еще и в том, что проведение этих исследований обеспечивает выбор наиболее оптимальных и безопасных препаратов, характеризующихся высокой функциональностью в радионуклидной диагностике и терапии онкологических заболеваний.
В настоящей работе изложены материалы комплексных радиохимических, фармакокинетических и дозиметрических исследований РФП на основе нативного альбумина, наноальбумина и микросфер альбумина (МСА), меченных радионуклидами 131I, 111In, 99mTc, 177Lu, 188Re, 103Pd, в зависимости от условий их получения и физико-химических характеристик.
Цель исследования.
Изучение фармакокинетических и дозиметрических характеристик РФП на основе сывороточного альбумина человека и гамма-, бета-излучающих радионуклидов в зависимости от физико-химических свойств меченых препаратов; выбор оптимальных по функциональным признакам РФП для радионуклидной диагностики и терапии онкологических заболеваний.
Задачи исследования:
1. Изучить закономерности образования комплексных соединений 99mTc с нативным альбумином и наноальбумином в зависимости от условий проведения реакции.
2. Провести сравнительные исследования фармакокинетических свойств РФП «99mTc-альбумин» и «99mTc-наноальбумин», оценить их функциональную пригодность для исследования гемодинамических характеристик и сцинтиграфии лимфатических узлов и печени.
3. Изучить особенности фармакокинетики меченых МСА в организме лабораторных животных в зависимости от химической природы радионуклида, дисперсного состава частиц, степени денатурации белка, пространственного распределения радионуклида в частицах и способа их введения в организм.
4. Изучить фармакокинетические свойства препарата «177Lu-МСА», полученного нейтрон-активационным способом.
5. Изучить закономерности инкорпорирования 103Pd в состав МСА и исследовать влияние теплового воздействия и гамма-облучения белка на показатели, характеризующие поведение препарата «103Pd-МСА» в организме лабораторных животных.
6. Изучить особенности фармакокинетики меченых МСА в организме лабораторных животных с экспериментальными моделями легочной патологии (облучение ионизирующим излучением, эмболия легочной артерии, асептическое воспаление и рак легких) после внутривенного введения препаратов.
7. Провести сравнительный анализ фармакокинетики РФП «103Pd-МСА» в организме интактных мышей и мышей-опухоленосителей после внутримышечного и внутриопухолевого введения, а также оценить уровни накопления этого препарата в опухоли и удержания его опухолевой тканью.
8. Оценить распределение поглощенных доз внутреннего облучения органов и тканей лабораторных животных разными радионуклидами, инкорпорированными в состав МСА.
Научная новизна:
В результате проведенных исследований обоснована проблема необходимости проведения комплексного исследования закономерностей инкорпорирования радионуклидов в молекулы-носители, изучения фармакокинетических свойств и дозиметрических характеристик для создания новых эффективных по функциональным признакам РФП для радионуклидной диагностики и терапии онкологических и неонкологических заболеваний.
1. Разработана технология оригинальных препаратов: 99mTc-наноальбумин, 177Lu-, 166Ho-, 103Pd-МСА.
2. Впервые показана возможность получения меченых МСА путем активации стабильных изотопов в составе белковых частиц тепловыми нейтронами. Нейтрон-активационным методом были получены и изучены физико-химические свойства МСА, меченных 152mEu, 177Lu, 186Re, 166Ho.
3. В результате исследования закономерностей введения 103Pd в белковую матрицу микросфер путем ионной сорбции впервые показана способность инкорпорировать палладий и другие ионы металлов в состав альбуминовых частиц и изучено влияние различных факторов (дисперсный состав частиц, степень денатурации белка в результате теплового воздействия и гамма-облучения МСА) на их поведение в организме лабораторных животных.
4. Впервые показано влияние предварительного гамма-облучения легких лабораторных животных на фармакокинетику меченых МСА.
5. Получены приоритетные результаты сравнительных исследований влияния степени денатурации белка, пространственного распределения метки в частицах, химической природы радионуклидов и способов введения меченых препаратов на характер поведения МСА в организме лабораторных животных.
6. В опытах на животных с индуцированными заболеваниями легких и перевивными солидными опухолями дана оценка функциональной пригодности препаратов.
7. Впервые проведена сравнительная оценка поглощенных доз внутреннего облучения органов и тканей лабораторных животных в зависимости от вида радионуклида, инкорпорированного в состав МСА.
Практическая значимость.
В ходе выполнения данного исследования созданы новые РФП, обладающие функциональной пригодностью для радионуклидной диагностики и терапии онкологических и неонкологических заболеваний. По результатам научных исследований наработаны экспериментальные и опытные образцы лиофилизатов (наборов реагентов) к генератору 99W/99mTc и на их основе РФП «99mTc-альбумин», «99mTc-наноальбумин», «99mTc-микросферы альбумина», «177Lu-микросферы альбумина» и «103Pd-микросферы альбумина».
Разработаны технологические регламенты на производство двух препаратов: «99mTc-альбумин», «99mTc-микросферы альбумина».
РФП «99mTc-альбумин» прошел доклинические испытания, РФП «99mTc-микросферы альбумина» прошел доклинические и клинические испытания, зарегистрирован в реестре лекарственных средств для медицинского применения и получено разрешение на его, промышленный выпуск (регистрационное удостоверение Минздрава России № 000/01-2001 от 01.01.2001).
Основные положения, выносимые на защиту:
1. Фармакокинетические свойства 99mTc-альбумина зависят от технологических условий его синтеза.
2. Результаты фармакокинетики 99mTc-альбумина 99mTc-наноальбумина доказали функциональную пригодность РФП для исследования гемодинамических характеристик, диагностики лимфатических узлов и печени.
3. На фармакокинетику меченых МСА оказывает влияние дисперсный состав частиц, пространственное распределения радионуклида в частицах, степень денатурации белка в результате теплового воздействия, нейтронного и гамма-облучения, химическая природа радионуклида, способ введения в организм.
4. Результаты фармакокинетики меченых МСА в организме лабораторных животных с патологическими состояниями легких: гамма-облучение легких; эмболия легочной артерии и рак легких, доказали эффективность РФП в оценке состояния капиллярного кровотока легких.
5. Поглощенные дозы внутреннего облучения органов и тканей лабораторных животных после внутривенного и внутриопухолевого введения меченых МСА определяются фармакокинетическими и ядерно-физическими характеристиками РФП.
Апробация работы.
Материалы диссертации доложены и обсуждены на 15 всероссийских и международных конференциях, симпозиумах, в том числе – на 9 конференциях в России и на 6 конференциях за рубежом:
1. Первый съезд онкологов стран СНГ (Москва,1996).
2. 2ICI Second International Conference on Isotopes (Sydney, Australia, 1997).
3. Международный конгресс «ЭНЕРГЕТИКА-3000» (Обнинск, 1998).
4. Всероссийская конференция «50 лет производства и применения изотопов в России» (Обнинск, 1998).
5. The Second Japanese-Russian Seminar on Technetium (Shizuoka, Japan, 1999).
6. International Youth Nuclear Congress 2000 (Slovakia, Bratislava, 2000).
7. Modern problems of radiobiology, radioecology and evolution, International conference dedicated to centenary of N. W.Timofeff-Ressovsky (Dubna, 2000).
8. International Conference on Current Status Medicine and Radiopharmaceuticals Congress of Russian Society of Nuclear Medicine (Obninsk, 2000).
9. Международный Конгресс «Энергетика-3000» (Обнинск, 2002).
10. Всероссийская научно-практическая конференция «Актуальные вопросы ядерной медицины». Школа «Избранные вопросы ядерной медицины» (Дубна, 2004).
11. International Symposium on Technetium (Oarai, Japan, 2005);
12. 15th Radiochemical Conference (Marianske Lazne, Czech Republic, 2006);
13. Annual Congress of the EANM (Athens, Greece, 2006);
14. Шестая Российская конференция по радиохимии «Радиохимия-2009» (Москва, 2009);
15. III Евразийский Конгресс по медицинской физике и инженерии «Медицинская физика – 2010» (Москва, 2010).
Апробация диссертации состоялась 20 апреля 2011 г. на научной конференции экспериментального радиологического сектора Федерального государственного бюджетного учреждения «Медицинский радиологический научный центр» Министерства здравоохранения и социального развития Российской Федерации, протокол
Публикации. По материалам диссертации опубликовано 29 научных статей, в том числе 18 опубликовано в отечественных научных журналах, рекомендованных ВАК МОиН РФ для докторских диссертаций, и 9 – в зарубежных журналах. Получен патент Российской Федерации на изобретение RU2359702 «Способ получения меченых радионуклидом микросфер», дата публикации 27.06.2009 г.
Реализация результатов работы. По результатам проведенных исследований подготовлены:
· лабораторные регламенты на производство двух препаратов: «Микросферы альбумина, 99mTc», «Альбумин, 99mTc»;
· опытно-промышленные регламенты на производство двух субстанций «Микросферы альбумина, 5–10 микрон» и «Микросферы альбумина, 20–40 микрон» – субстанции для получения радиофармпрепаратов «103Pd-микросферы альбумина, 5–10 микрон» и «103Pd-микросферы альбумина, 20–40 микрон»;
· стандарты предприятия для контроля качества препаратов «Микросферы альбумина (МСА), 20–40 мкм» и «Микросферы альбумина (МСА), 5–10 мкм» – субстанции для производства РФП «103Pd-МСА, 20–40 мкм» и «103Pd-МСА, 5–10 мкм»;
· проведены доклинические испытания препарата «99mTc-альбумин»;
· проведены доклинические и клинические испытания препарата «99mTc-микросферы альбумина», препарат зарегистрирован в реестре лекарственных средств, а также получено разрешение на его промышленное производство.
Объем и структура работы. Диссертация изложена на 266 страницах компьютерного текста, содержит 55 таблиц и 36 рисунков. Она состоит из введения, обзора литературы, описания материалов и методов исследований, четырех глав собственных исследований, заключения, выводов. Список цитированной литературы содержит 311 источников.
Личный вклад автора. Автору принадлежит ведущая роль в выборе направления исследования, планировании и проведении большинства экспериментов, обработке, анализе и обобщении полученных результатов. В работах, выполненных в соавторстве, вклад автора является определяющим и состоит в непосредственном участии на всех этапах исследования: от генерации идеи, формулировании задач, их экспериментально-теоретической реализации до обсуждения результатов исследований и подготовки научных публикаций и докладов.
МАТЕРИАЛЫ И МЕТОДЫ
Синтез меченых препаратов. Для синтеза препаратов использовали 10% раствор сывороточного альбумин человека для инфузий. Вспомогательные реактивы были приобретены у фирмы «Сигма-Алдрич», Москва. Радионуклиды 99mTc и 188Re получали элюированием с колонок генераторов 99Mo/99mTc и 188W/188Re производства – Физико-энергетический институт им. » (г. Обнинск). Радионуклид 103Pd приобретали у , 131I получали из » (г. Обнинск).
Синтез наноальбумина проводили путем сшивки альбумина глутаровым альдегидом с последующим фильтрованием через мембранный фильтр с размером пор 22 мкм.
Синтез МСА осуществляли эмульсионным методом [Zolle I., et al., 1970; и соавт., 1976; и соавт., 1977]. Методика была существенно модифицирована. Для этой цели был разработан специальный аппарат, в комплект которого входит блок управления температурой и скоростью вращения мешалки. Метод получения МСА основан на тепловой денатурации белка в оливковом масле. Раствор альбумина вводят по каплям в оливковое масло при постоянном перемешивании. При этом образуется эмульсия раствора альбумина в масле. Эту смесь, не прекращая перемешивания, нагревают. При этом происходит процесс тепловой денатурации альбумина с образованием твердых частиц сферической формы. Размер МСА зависит от скорости перемешивания смеси, концентрации раствора альбумина и температуры предварительного нагрева масла. Для получения МСА с заданными размерами их фракционируют с помощью ультразвуковых микросит. Разработанный метод получения МСА с помощью специального аппарата позволяет получать частицы с любыми заданными диапазонами размеров от 0,5 мкм до 850 мкм и программируемой тепловой денатурацией белка в интервале температуры от 110оС до 300оС. Кроме этого, методика позволяет получать МСА, содержащие любые металлы в виде их солей или оксидов, а также любые химические соединения, в том числе лекарственные препараты, существующие в твердом состоянии [ и соавт., 1980; и соавт., 1981; и соавт., 2000; и соавт., 2005].
Лиофилизаты (наборы реагентов) на основе альбумина, наноальбумина и микросфер альбумина к генераторному радионуклиду 99mTc получали путем лиофильной сушки раствора смеси реагентов, предварительно замороженного в жидком азоте, в сублиматоре 15-SRC-X производства фирмы “VirTis” (США) [, , и соавт., 2003]. Лиофилизаты являются субстанциями для приготовления РФП «99mTc-альбумин», «99mTc-наноальбумин» и «99mTc-микросферы альбумина». Меченые препараты готовят непосредственно перед проведением исследований, путем введения элюата 99mTc во флакон, содержащий ингредиенты, способствующие связыванию технеция с молекулой-носителем.
103Pd-микросферы альбумина получали методом ионной сорбции хлорида палладии-103 в состав белковых частиц с последующим восстановлением его до оксида палладия [ и соавт., патент RU2 2009; и соавт., 2010; Petriev V. M., et al., 2010].
177Lu - и 166Ho-микросферы альбумина получали методом активации тепловыми нейтронами стабильных изотопов 176Lu - и 165Ho в составе МСА. Облучение проводили в реакторе ВВРц в » [ и соавт., 1981; и соавт., 2005].
Методика проведения биологических исследований.
Изучение фармакокинетики меченых препаратов альбумина было проведено на 883 лабораторных животных, в том числе на 122 кроликах-самцах породы Шиншилла массой 1,5–3,0 кг, 373 белых беспородных крысах-самцах массой 130–250 г и 388 белых беспородных мышах-самцах массой 22–35 г. Экспериментальные животные содержались в условиях лабораторного вивария и получали стандартный рацион и воду без ограничений.
Фармакокинетические свойства меченых препаратов изучали в организме интактных животных и животных с разными патологическими состояниями легких кроликов: асептическим воспалением легких, эмболией легочной артерии, рак легких и после гамма-облучения легкого, а также с перевитой в мышцу бедра мышей карциномой Эрлиха. Эксперименты на животных проводили при разных способах инъекции меченых препаратов: внутривенном, внутриартериальном, внутримышечном и внутриопухолевом. Экспериментальные заболевания легких моделировали по методикам, изложенным в работах [Хачиров Дж. Г., М, 1978; и соавт., 1979].
Радиометрию образцов органов и тканей проводили по фотопику гамма-излучения соответствующего радионуклида в колодезном детекторе NZ-138, с помощью пересчетной установки NC-308 и высоковольтного блока NK-350/A производства фирмы «Гамма» (Венгрия), а также с помощью автоматического гамма-счетчика «Wizard» версии 2480 фирмы PerkinElmer/Wallac (Финляндия). По данным радиометрии рассчитывали содержание меченого препарата в 1 г массы ткани и во всем органе в процентах от введенного количества. Результаты радиометрии обрабатывали методом оценки средне-квадратичной ошибки средней величины (M ± m). Достоверность различий результатов оценивали с использованием критерия Стьюдента. Статистически значимыми признавались отличия с р < 0,05.
ОСНОВНЫЕ РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Разработка радиофармпрепаратов «99mTc-альбумин», 9mTc-наноальбумин», изучение их радиохимических и фармакокинетических свойств
Полученные результаты в ходе выполнения работы показали, что с целью создания радиофармпрепаратов на основе сывороточного альбумина человека (нативный альбумин, наноальбумин и микросферы) с оптимальными характеристиками по функциональным признакам для радионуклидной диагностики и терапии необходимо проведение комплексных исследований закономерностей связывания радионуклида с молекулой-носителем, изучение фармакокинетических свойств и дозиметрических характеристик.
Для изучения закономерностей образования комплексного соединения 99mTc с нативным альбумином в зависимости от условий проведения реакции были получены экспериментальные образцы лиофилизатов (наборы реагентов), содержащие 10 мг альбумина и разное количество двухвалентного олова (Sn2+) в пределах 15–80 мкг. Метку альбумина радионуклидом проводили путем введения элюата 99mTc, получаемого с колонки генератора 99Mo/99mTc, во флакон, содержащий ингредиенты (альбумин, Sn2+ в виде SnCl2), способствующие связыванию 99mTc с альбумином.
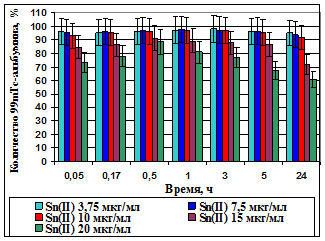
В результате исследований показано, что проведение реакции при pH среды, равной 2,5, уровень связывания 99mTc с альбумином практически не зависит от концентрации Sn2+ в реакционной смеси в пределах 3,75–10 мкг/мл (рис. 1). Причем образование комплексного соединения «99mTc-альбумин» при этих условиях происходит практически мгновенно. Радиохимический выход 99mTc-альбумина составляет около 96% через три минуты после начала проведения реакции и сохраняется на этом уровне в течение 24 ч, что свидетельствует
о высокой стабильности РФП в растворе. Увеличение концентрации Sn2+ в реакционной смеси до 15 мкг/мл снижает скорость реакции образования комплекса «99mTc-альбумин» и эффективность связывания 99mTc с альбумином.
Максимальный радиохимический выход меченого препарата составляет около 88% через 30 мин после начала проведения реакции. Дальнейшее повышение концентрации Sn2+ в реакционной смеси до 20 мкг/мл способствует еще большему снижению скорости реакции, эффективности связывания 99mTc с
альбумином и стабильности комплекса. Снижение скорости реакции и эффективности связывания 99mTc с альбумином при высоких концентрациях Sn2+ в реакционной смеси происходит за счет протекания конкурентной реакции, в
|
|
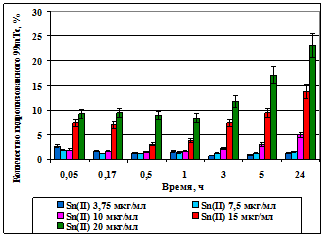
Рис. 1. Кинетика связывания 99mТс с альбумином от зависимости концентрации Sn2+ в реакционной смеси. Концентрация альбумина 2,5 мг/мл; 99mТс – 0,8мг/мл. | Рис. 2. Кинетика образования 99mТсO2 в зависимости от концентрации Sn2+ в реакционной смеси. Концентрация альбумина 2,5 мг/мл; 99mТс – 0,8мг/мл, рН 2,5. |
результате которой образуется гидролизованный технеций (99mTcO2), являющийся радиохимической примесью в препарате «99mTc-альбумин». Радиохимические примеси в препарате «99mTc-альбумин», полученном в реакции с концентрацией Sn2+ в реакционной смеси в пределах 3,75–10 мкг/мл, не превышают 4–5%, тогда как концентрация Sn2+ 15–20 мкг/мл способствует образованию 99mTcO2 на уровне 10–20% (рис. 2).
Аналогичные закономерности образования комплексных соединений 99mTc происходят с наноальбумином и микросферами альбумина.
Учитывая, что введение 99mTc в молекулу альбумина, а также воздействие Sn2+ на белок может приводить к изменению его физиологических свойств, необходимо проведение фармакокинетических исследований РФП с разными модификациями препарата в организме лабораторных животных.
Поскольку 99mТс-альбумина предназначен для радионуклидного исследования гемодинамических характеристик, поведение его в крови является важнейшей фармакокинетической характеристикой.
В экспериментах на кроликах показано, что 99mTc-альбумин, полученный из лиофилизата, содержащего 15 мкг Sn2+ (соответственно 3,75 мкг/мл в реакционной смеси), имеет наиболее оптимальные фармакокинетические свойства (табл. 1). Он циркулирует в крови в течение 3 ч на уровне около 50% от введенного количества. У 99mTc-альбумина, полученного из лиофилизатов, содержащих 30 и 40 мкг Sn2+ (соответственно 7,5 и 10 мкг/мл в реакционной смеси), накопление активности в крови также было высоким (выше 50%) через 5 мин после внутривенного введения. Однако в последующие сроки меченый препарат интенсивно выводился из кровяного русла и в течение 3 ч содержание его в крови резко снижалось (табл. 1). Получение 99mTc-альбумина из лиофилизата, содержащего 80 мкг (концентрация 20 мкг/мл в реакционной смеси) Sn2+ приводит к значительному снижению уровня накопления активности в крови во все сроки наблюдений.
Таблица 1 – Содержание 99мТс-альбумина в крови кроликов после внутривенного введения препарата (в % от введенного количества на всю массу крови).
Время после введения препарата | Концентрация Sn2+, при которой получали 99мТс-альбумина, мкг/мл | |||
3,75 | 7,5 | 10 | 20 | |
5 мин | 53,0 ± 12,6 | 62,9 ± 2,38 | 58,2 ±2,25 | 9,98 ± 1,49 |
1 ч | 45,3 ± 11,5 | 38,5 ± 3,89 | 9,92 ± 0,48 | 8,81 ± 2,43 |
3 ч | 51,1 ± 0,76 | 25,5 ± 1,23 | 4,27 ± 0,03 | 3,43 ± 0,27 |
Полученные результаты свидетельствуют о том, что повышение количества олова в составе лиофилизата с 15 до 40 мкг оказывает существенное влияние на фармакокинетические свойства РФП – ускоряет выведение его из кровяного русла. При этом радиохимические свойства 99mTc-альбумина не изменяются с повышением олова в составе лиофилизата в пределах 15–40 мкг (радиохимический выход составляет выше 95%, радиохимические примеси не превышают 5%) и стабильность препарата in vitro сохраняется на высоком уровне в течение 24 ч с момента его приготовления. Ускоренное выведение 99mTc-альбумина, полученного при повышенных концентрациях олова, объясняется изменением физиологических свойств белка.
С учетом полученных результатов комплексных радиохимических и биологических исследований, был выбран лиофилизат с оптимальным составом: флакон емкостью 10 см3 содержал лиофильно высушенную в стерильных условиях смесь альбумина – 10 мг и двухлористого олова – 0,0238 мг (Sn2+ – 15 мкг). Разработанный состав лиофилизата позволяет получать РФП «99mTc-альбумин» в течение 10 мин с радиохимическим выходом не менее 95%.
Как было показано, незначительное изменение физиологических свойств альбумина приводит к существенному изменению поведения его в организме. Это явление было подтверждено экспериментальными исследованиями на крысах при изучении фармакокинетических свойств наноальбумина, меченного 99mTc. Разработанный наноальбумин представляет собой сшитый белок со средним размером частиц 26,1 нм.
Сравнительные данные биологического распределения 99mTc-альбумина и 99mTc-наноальбумина в организме крыс после внутривенного введения характеризуются существенными различиями. Содержание активности в крови крыс через 5 мин после инъекции 99mTc-альбумина и 99mTc-наноальбумина отмечается на достаточно высоком уровне (соответственно 12,8 и 28,8% во всем объеме циркулирующей крови от введенного количества). Однако 99mTc-наноальбумин интенсивно выводится из крови и через 24 ч количество его снижается в 64 раза по сравнению с 5 минутным сроком. Напротив, содержание 99mTc-альбумина в крови существенно не изменяется в течение 6 ч (р > 0,05) и только через 24 ч этот показатель статистически достоверно снижается до 9,4% по сравнению с 6 часовым сроком (p < 0,05).
Интенсивное выведения 99mTc-наноальбумина из крови сопровождается высоким уровнем накопления его в печени (табл. 2). Динамика накопления 99mTc-наноальбумина в 1 г печени характеризуется постепенным ростом активности с 4,17 до 9,51% в течение 1 ч после внутривенной инъекции препарата и остается практически без изменения в интервале наблюдения 1 – 24 ч, а к 48 ч снижается до уровня 4,3%. Напротив, величины накопления 99mTc-альбумина в печени наблюдаются на уровне следовых количеств во все сроки проведения исследования.
Избирательное накопление 99mTc-наноальбумина в печени является результатом захвата наночастиц купферовскими клетками. Полученный результат является положительной характеристикой РФП в плане возможности использования его для получения сцинтиграфического изображения печени.
Таблица 2 – Фармакокинетика 99mТс-наноальбумина в организме крыс после внутривенного и подкожного введения препарата (в % от введенного количества на 1 г массы органов, тканей).
№ пп. | Наименование органа, ткани | Метод введения | Время после введения препарата | ||||
5 мин | 1 ч | 3 ч | 24 ч | 48 ч | |||
1 | Кровь | в/венное подкожное p | 2,94±0,67 0,015±0,003 < 0,01 | 0,40±0,03 0,021±0,004 < 0,001 | 0,13±0,02 0,046±0,006 < 0,01 | 0,046±0,004 0,065±0,005 < 0,05 | 0,087±0,014 0,17±0,02 < 0,02 |
2 | Щитовидная железа | в/венное подкожное p | 0,50±0,09 0,063±0,017 < 0,01 | 0,51±0,04 0,076±0,016 < 0,001 | 0,60±0,04 0,24±0,04 < 0,001 | 2,46±0,31 0,18±0,02 < 0,001 | 5,97±0,99 1,22±0,21 < 0,01 |
3 | Печень | в/венное подкожное p | 4,17±0,66 0,032±0,007 < 0,001 | 9,51±0,34 0,22±0,04 < 0,001 | 8,39±0,53 1,77±0,30 < 0,001 | 7,68±0,91 1,29±0,17 < 0,001 | 4,30±0,30 0,83±0,18 < 0,001 |
4 | Лимфатический узел паховый | в/венное подкожное p | 0,66±0,14 5,62±0,89 < 0,002 | 1,27±0,40 12,3±2,90 < 0,01 | 0,64±0,12 37,4±4,66 < 0,001 | 0,45±0,07 60,7±13,7 < 0,01 | 0,33±0,10 38,4±7,58 < 0,01 |
В опытах на крысах было показано, что после подкожного введения 99mTc-наноальбумина РФП имеет фармакокинетические особенности в организме, отличающиеся от таковых после внутривенного введения этого же препарата (табл. 2). Результаты биологического распределения РФП показали, что в ранние сроки после подкожного введения 99mTc-наноальбумина из всех исследуемых органов и тканей наибольшее количество активности аккумулируется в паховом лимфатическом узле. Через 5 мин после инъекции 99mTc-наноальбумина накопление активности в лимфатическом узле составляет 5,62% от введенного количества (в пересчете на 1 г массы органа), далее процент накопления активности увеличивается и достигает максимального значения (60,7%) через 24 ч, затем происходит снижение этого показателя до 38,4% через 48 ч. Такая динамика накопления активности в лимфатическом узле объясняется медленной элиминацией 99mTc-наноальбумина, депонированного под кожу после инъекции.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |