Самое высокое значение коэффициента цветности ГК древесно-травяного торфа, судя по результатам элементного анализа и оптических свойств, может быть связано, прежде всего, с максимальным содержанием кислорода и азота, наряду с низким содержанием углерода в макромолекуле этих ГК.
Полученные ИК-спектры ГК исследуемых торфов (рис. 2) имеют высокую степень подобия - основные характеристические для ГК максимумы поглощения обнаруживаются во всех образцах, это указывает на близость их химической структуры.
Максимальная интенсивность полос поглощения в спектрах ГК отмечена для: гидроксильных, карбонильных, карбоксильных групп, алифатических и ароматических фрагментов.
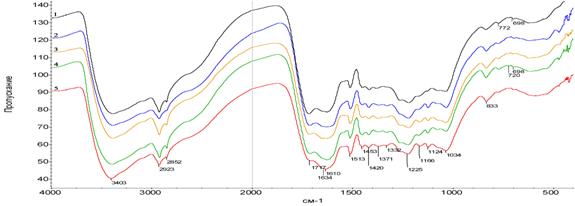
Рис. 2. ИК-спектры гуминовых кислот:1- низинного древесно-травяного; 2- низинного травяного; 3- низинного травяно-мохового; 4- переходного осокового; 5- верхового сосново-пушицевого видов торфа
Также дана количественная оценка (табл. 8) содержания функциональных групп по данным ИК-спектроскопии на основании отношений оптических плотностей полос поглощения кислородсодержащих групп к оптическим плотностям, соответствующим ароматическим полисопряженным системам и алифатическим заместителям.
Таблица 8
Соотношение оптических плотностей полос поглощения при определенных длинах волн по данным ИК-спектроскопии
Вид торфа | Низинный древесно-травяной | Низинный травяной | Низинный травяно-моховый | Переходный осоковый | Верховой сосново- пушицевый |
АО-Н 3400 /АС=С 1610 | 1,05 | 0,97 | 0,99 | 1,07 | 1,15 |
АС=О 1720 /АС=С 1610 | 1,05 | 0,97 | 0,93 | 0,91 | 0,87 |
АС-О 1225 /АС=С 1610 | 0,88 | 0,87 | 0,84 | 0,79 | 0,77 |
АC-О и С-О-С 1035 /АС=С 1610 | 0,74 | 0,74 | 0,76 | 0,64 | 0,74 |
АСалк 2920 /АС=С 1610 | 1,00 | 0,90 | 0,94 | 0,97 | 0,94 |
АО-Н 3400 /АСалк 2920 | 1,05 | 1,11 | 1,07 | 1,11 | 1,24 |
АС=О 1720 /АСалк 2920 | 1,05 | 1,11 | 0,93 | 0,93 | 0,93 |
АС-О 1225 /АСалк 2920 | 0,88 | 0,99 | 0,89 | 0,82 | 0,83 |
АC-О и С-О-С 1035 /АСалк 2920 | 0,74 | 0,84 | 0,83 | 0,66 | 0,79 |
Примечание: А – оптическая плотность.
Результаты показали, что молекулы ГК верхового и переходного торфов имеют различия в содержании карбоксильных групп, в сравнении с низинными торфами, содержащими наибольшее количество карбоксильных групп, максимальное количество которых отмечено для ГК древесно-травяного торфа. И, наоборот, в молекулах ГК верхового и переходного торфов в сравнении с ГК низинных - наблюдается большее содержание гидроксильных групп, исключение составляет один вид низинного торфа - древесно-травяной, в котором их содержание высокое, что также подтверждается данными функционального анализа (табл. 9).
В целом можно отметить, что ГК древесно-травяного торфа имеют весьма значительные отличия от других торфов и представляют собой соединения с высокой долей алифатических фрагментов и возможно меньшей степенью бензоидности, а также с высоким содержанием активных кислых групп (карбоксильных, гидроксильных).
Таблица 9
Функциональный состав гуминовых кислот исследуемых торфов
Тип, вид торфа | Активные кислые группы, мг*экв/г | ||
-СООН | -ОНфенольные | Σ | |
Низинный древесно-травяной | 2,86±0,14 | 3,22±0,19 | 6,08±0,17 |
Низинный травяной | 2,48±0,12 | 3,06±0,15 | 5,54±0,14 |
Низинный травяно-моховый | 2,38±0,14 | 3,14±0,18 | 5,52±0,16 |
Переходный осоковый | 2,29±0,11 | 3,32±0,17 | 5,61±0,17 |
Верховой сосново-пушицевый | 2,26±0,13 | 3,78±0,19 | 6,04±0,14 |
Анализ формы ЭПР спектров исследуемых ГК показал, что все они представляют собой относительно симметричную синглетную линию с фактором их спектроскопического расщепления близким к g-фактору свободного электрона, обусловленную ароматическими структурами полисопряжения. Параметры сигналов ЭПР различных ГК принципиально не отличаются между собой, что также свидетельствует о подобии строения их конденсированных ароматических ядер (табл. 10).
Таблица 10
Параметры ЭПР-спектроскопии гуминовых кислот торфов
Тип, вид торфа | Полуширина синглетной линии (∆Н, Гс) | Интенсивность сигнала Iабс, 1017 спин/грамм Концентрация ПМЦ |
Верховой сосново-пушицевый | 3,8 | 1,8 |
Переходный осоковый | 3,9 | 2,3 |
Низинный травяно-моховый | 4,5 | 1,6 |
Низинный травяной | 4,5 | 2,3 |
Низинный древесно-травяной | 4,8 | 2,6 |
По интенсивности сигнала (Iабс) можно отметить, что наибольшее содержание парамагнитных центров (ПМЦ) характерно для ГК низинных древесно-травяного и травяного, а также переходного торфов, далее по убыванию идут верховой и низинный травяно-моховый торфа. Самый высокий парамагнетизм (ПМЦ=2,6) ГК древесно-травяного торфа, вероятно, обусловлен высоким удельным содержанием карбоксильных групп и фенольных гидроксилов, принадлежащих непосредственно ароматическим кольцам. Полученные результаты хорошо согласуются с данными ИК-спектроскопии и функционального анализа.
Протонный анализ (рис. 3) показал, что спектры всех ГК выглядят одинаково сложно, сигналы протонов имеют уширенную форму, и на спектре можно выделить три основных области:
· первая область от 0.5 м. д. до 2.5 м. д. можно отнести к сигналам алифатических протонов (-СН3, - СН2-, - СН).
· вторая область от 2.5 м. д. до 4.0 м. д. можно отнести к сигналам протонов атомов углерода, связанных с гетероатомами (RО-СН2-, R2N-СН2-, где R=H, Alk, углеводы).
· третья область от 6.5 м. д. до 8.0 м. д. являются областью химических сдвигов ароматических протонов.
Интегрирование сигналов в различных областях полученного спектра позволило оценить распределение протонов по важнейшим фрагментам ГК: первая область алифатических цепей ≈ 56%, вторая область углеводов - ≈ 25% и третья область ароматических протонов ≈ 19%.
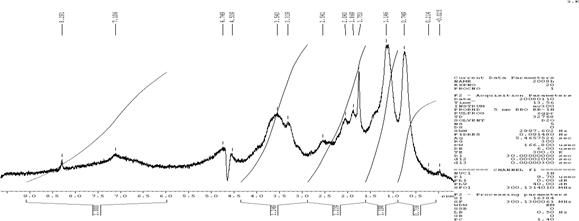
Рис. 3. ПМР – спектр гуминовых кислот низинного древесно-травяного торфа
В спектрах ЯМР 13С (рис. 4) выделены более узкие области:
· сигналы в области 10.00-43.00 м. д. соответствуют резонансным сигналам ядра 13С в Салкил.;
· сигналы в области 50.00-60.00 м. д. соответствуют резонансным сигналам ядра 13С в СН3-О-Cалкил., CH3-O-Ar, СН3-О-C=О;
· сигналы в области 62.00 – 80.00 м. д. соответствуют резонансным сигналам ядра 13С моно-, ди - и полигидроксильным (углеводным) фрагментам ГК;
· сигналы области 90.00-110.00 м. д. соответствуют резонансным сигналам ядра 13С ацетальным или кетальным углеводным фрагментам полисахаридной цепи ГК;
· сигналы в области 112.00-160.00 м. д. соответствуют резонансным сигналам ядра 13С в ароматических фрагментах ГК;
· сигналы в области 170.00-180.00 м. д. соответствуют резонансным сигналам ядра 13С в - СООН, - СOOR, - CONH2.
Как видно из спектра ЯМР13С (рис. 4) интенсивность метоксильных (-О-СН3) и метилонатных (СН3-О-С=О) групп высокое. Распределение углерода по важнейшим фрагментам ГК составляют следующие значения: алифатический С – 32,8 %; углеводный С – 21,8 %; ароматический С – 32,2 % и карбонильный С – 13,2 %.
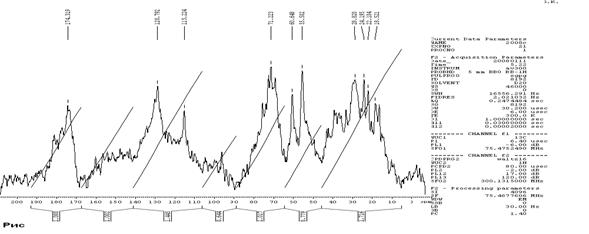
Рис. 4. ЯМР – спектр гуминовых кислот низинного древесно-травяного торфа
На основе химического исследования ГК низинного древесно-травяного вида торфа нами проведена их стандартизация, определены показатели подлинности и качества (соответствие коэффициентам экстинкции (1 см 0,001 % растворы ГК должны соответствовать: при длине волны 465 нм - 0,020±0,002, при длине волны 650 нм – 0,0041±0,0004, коэффициент цветности (465/650) должен соответствовать 4,88±0,05); совпадение спектров в УФ-, ИК-областях и молекулярно-массового распределения, а также, содержание углерода в ГК (не более 47,0 %) и азота (не менее 3,8 %); молекулярная масса должна составлять кДа). Полученные показатели внесены в проект фармакопейной статьи предприятия «Гуминовые кислоты торфа».
Таким образом, результаты исследования химической структуры ГК различных видов торфа выявили ряд индивидуальных особенностей строения их макромолекул, на основании чего был определён низинный древесно-травяном торф как наиболее перспективный источник ГК для дальнейших исследований. Высокое удельное содержание ГК в данном виде торфа, высокая концентрация парамагнитных центров, наибольшее содержание азота и кислородсодержащих функциональных групп (карбоксильных, хиноидных, фенольных гидроксилов) в структуре его ГК, а так же низкая степень бензоидности и конденсированности их макромолекулы позволяют предположить у ГК низинного древесно-травяного торфа более высокую степень тропности их молекул к биологическим структурам клеток (рецепторам, активным группам ферментов и т. д.), и, соответственно, более выраженные фармакологические эффекты. В связи с этим, исследования биологической активности проведены с данными ГК.
Исследование острой токсичности ГК. Средняя летальная доза (ЛД50) исследуемого препарата ГК при внутрижелудочном введении мышам составила 4658,40 мг/кг. При внутрижелудочном введении исследуемого препарата крысам в аналогичном диапазоне доз не наблюдали гибели животных и картины острого отравления в течение двух недель наблюдения, что возможно связано с более медленным всасыванием ГК в желудочно-кишечном тракте крыс. Таким образом, исследуемые ГК при внутрижелудочном введении мышам и крысам являются малотоксичными и относятся к III или IV классам опасности соответственно. При внутрибрюшинном введении лабораторным животным ГК проявляют более выраженные токсические свойства: ЛД50 исследуемого препарата ГК при внутрибрюшинном введении мышам составила 532,89 мг/кг, а при внутрибрюшинном ведении крысам величина ЛД50 исследованного препарата составила 480,12 мг/кг.
Патоморфологическое исследование погибших животных. Для установления причин летальности и выявления возможных органов-мишеней, поражаемых при остром токсическом воздействии, проводили патоморфологическое исследование трупов крыс, погибших при внутрибрюшинном введении заведомо летальных доз препарата ГК. Судя по результатам патологанатомического исследования гибель лабораторных животных (крыс) при введении летальных доз ГК наступала от острой сердечной недостаточности, возникающей в результате ишемической дистрофии миокарда.
Исследование кардиотоксического действия ГК. Судя по результатам патоморфологического исследования, одной из причин летальности при внутрибрюшинном введении ГК может быть их прямое кардиотоксическое действие. Мы провели регистрацию электрокардиограммы (ЭКГ) и определение порога фибрилляции желудочков (ПФЖ) у крыс-самцов после внутрибрюшинного введения ГК в заведомо летальной дозе (480,00 мг/кг).
Однократное внутрибрюшинное введение ГК вызывает значительно снижение ПФЖ (в 1,8 раза) в сравнении с интактными животными. В тоже время, наблюдалось достоверное укорочение (в 2,8 раза) комплекса QRS в сравнении с интактными животными. Судя по полученным результатам, однократная инъекция ГК в летальной дозе (480,0 мг/кг) индуцирует снижение электрической стабильности сердца, о чём наглядно говорит падение ПФЖ и снижение величины комплекса QRS. Подобное снижение электрической стабильности сердца может быть причиной внезапной сердечной смерти подопытных животных.
Исследование влияния ГК на реологические свойства крови. Другим возможным механизмом острого нарушения гемодинамики под влиянием ГК может быть их негативное влияние на реологические свойства крови. Мы исследовали влияние ГК на реологические свойства крови фотометрическим вибрационным методом. Судя по полученным результатам, ГК in vitro вызывают существенное (в 2,26 раза) в сравнении с показателями интактной пробы увеличение показателя индекса обратимой агрегации эритроцитов (ОАЭ). Это может приводить к значительному увеличению вязкости крови, усиленному тромбообразованию, нарушению кровоснабжения миокарда и обусловливать негативное кардиотропное воздействие препарата ГК в летальных дозах.
Таким образом, острое нарушение гемодинамики и последующая гибель животных могут быть обусловлены одновременно, как снижением электрической стабильности сердца, так и негативным влиянием ГК на реологические свойства крови.
Исследование динамики концентраций ГК в сыворотке крови крыс. Нами была изучена динамика концентраций ГК в сыворотке крови крыс при обоих способах введения. Для исследования суточного профиля концентраций ГК вводили крысам однократно (внутрижелудочно или внутрибрюшинно) в дозе 100 мг/кг (рис. 5).
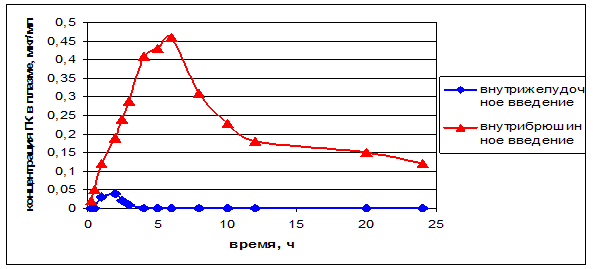
Рис. 5. Суточная динамика концентраций ГК в сыворотке крови крыс-самцов после однократного введения в дозе 100 мг/кг при внутрижелудочном и внутрибрюшинном способах введения
Из полученных результатов (рис. 5) видно, что существуют значительные различия в суточных профилях концентраций ГК сыворотке крови животных в зависимости от способа введения:
1. Наблюдается практически 10-кратное различие в максимальных уровнях концентрации Cmax ГК в сыворотке крови животных при внутрижелудочном и внутрибрюшинном введении (0,04 мкг/мл и 0,46 мкг/мл соответственно).
2. Время достижения максимальной концентрации Tmax при внутрижелудочном и внутрибрюшинном введении различается в три раза (2,0 и 6,0 часов соответственно).
3. В данных условиях эксперимента, при внутрижелудочном введении спустя 4,0 часа после введения, ГК не определяются в сыворотке крови, вследствие крайне низкой концентрации. В тоже время, при внутрибрюшинном введении ГК обнаруживаются в сыворотке крови и через 24,0 часа после последнего введения.
С полученными результатами согласуются наши экспериментальные данные о более выраженных токсических свойствах ГК и способности их к кумуляции при внутрибрюшинном введении, что на наш взгляд, может быть обусловлено значительно более длительной циркуляцией ГК в системном кровотоке по сравнению с пероральным введением. Различия в суточных профилях концентраций ГК могут указывать на весьма выраженный эффект «первичного прохождения через печень» при их пероральном введении. По-видимому, в случае внутрибрюшинного введения в брюшной полости создается «депо», из которого ГК, медленно всасываясь, попадают в системный кровоток, не подвергаясь предварительной биотрансформации в печени. Это обуславливает более длительную (более 24 часов) циркуляцию ГК в крови животных, по сравнению с внутрижелудочным введением. При этом, полученные значения Tmax, указывают на то, что ГК при внесосудистых способах введения (как при внутрижелудочном, так и при внутрибрюшинном) довольно медленно всасываются, что вероятно связанно с большими размерами их молекул. С другой стороны, медленное всасывание, существенное влияние «эффекта первичного прохождения через печень» обуславливает значительно менее длительную циркуляцию в крови и невозможность кумуляции ГК при внутрижелудочном способе введения. Вероятно, в данном случае нельзя исключать и возможность потери части невсосавшихся ГК за счет естественной перистальтики кишечника.
Исследование цитопротективных свойств ГК торфа. Анализ литературных данных показывает, что ГК, как правило, проявляют наиболее выраженную биологическую активность в условиях экспериментальных моделей связанных с повреждающим воздействием экстремальных факторов различной природы. Мы провели экспериментальную оценку цитопротективных свойств ГК в условиях острого токсического ССl4-гепатита и различных гипоксических состояний.
Оценка гепатопротективных свойств ГК. Известно, что развитие многих заболеваний обусловлено активацией свободнорадикальных процессов, приводящих к повреждению клеточных структур. Исходя из этих представлений, мы исследовали влияние ГК как потенциальных антиоксидантов на развитие острого токсического CCl4-гепатита, в патогенезе которого существенная роль принадлежит перекисному окислению липидов (ПОЛ). Исследуемые ГК обладают выраженной гепатопротекторной активностью при остром CCl4-гепатите (табл. 11).
Таблица 11
Влияние введения ГК и Карсила на биохимические показатели сыворотки крови и на содержание малонового диальдегида (МДА) в гомогенате печени крыс-самцов
при CCl4-гепатите (Χ±Δх; n=10)
Группы животных | В сыворотке крови | МДА, Мкмоль/л | |||||
ЩФ, Е/Л | γ- ГГТ Е/Л | АсАТ, Е/Л | АлАТ, Е/Л | Билирубин общий, Мкмоль/л | в сыворотке крови | в гомогенате печени | |
Интактные | 350,50 ±29,20 | 5,45 ±0,28 | 167,00 ±9,16 | 84,50 ±3,33 | 2,30 ±0,30 | 1,90 ±0,3 | 1,15 ±0,06 |
CCl4-гепатит | 447,60 ±25,00* | 8,68 ±1,53* | 416,80 ±21,50* | 148,30 ±8,16* | 12,80 ±0,72* | 3,60 ±0,28* | 11,98 ±0,66* |
ГК (25 мг/кг)+ CCl4-гепатит | 404,80 ±46,20 | 5,96 ±0,96** | 347,80 ±16,00** | 123,80 ±1,50 | 3,10 ±0,41** | 2,30 ±0,15** | 4,15 ±0,31** |
ГК (50 мг/кг)+ CCl4-гепатит | 345,60 ±18,40** | 6,02 ±0,28** | 292,30 ±33,00** | 109,50 ±8,50** | 2,30 ±0,08** | 1,80 ±0,22** | 2,62 ±0,06** |
ГК (100 мг/кг)+ CCl4-гепатит | 356,50 ±26,50** | 4,25 ±0,55** | 207,50 ±22,50** | 76,30 ±0,33** | 2,40 ±0,06** | 1,30 ±0,13** | 2,00 ±0,12** |
Карсил (100мг/кг)+ CCl4-гепатит | 395,60 ±27,00 | 6,86 ±1,74** | 356,80 ±19,80** | 119,30 ±7,19 | 9,80 ±0,86 | 2,70 ±0,19 | 7,45 ±0,43** |
Примечание: * - различия достоверны для группы CCl4-гепатит по сравнению с группой интактных животных, при р≤0,05; **для групп животных получавших ГКТ или Карсил – по сравнению с группой CCl4-гепатит, при р≤0,05; n - количество животных в группах.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |




