р=nKT
12) Скорости молекул:
Средняя квадратичная
![]()
Средняя арифметическая
![]()
Наиболее вероятная
![]()
где mi - масса одной молекулы.
Относительная скорость молекулы:
![]()
где υ - скорость данной молекулы.
13) Закон распределения молекул по скоростям (закон Максвелла) позволяет найти число молекул ![]() , относительные скорости которых лежат в интервале от и до
, относительные скорости которых лежат в интервале от и до ![]() :
:
![]()
здесь ![]() - величина интервала относительных скоростей, малая по сравнению со скоростью и.
- величина интервала относительных скоростей, малая по сравнению со скоростью и.
При решении задач на закон распределения молекул по скоростям удобно пользоваться табл. 3:
Таблица 3
№ |
| и |
| и |
|
0 | 0 | 0,9 | 0,81 | 1,8 | 0,29 |
0,1 | 0,02 | 1,0 | 0,83 | 1,9 | 0,22 |
0,2 | 0,09 | 1,1 | 0,82 | 2,0 | 0,16 |
0,3 | 0,18 | 1,2 | 0,78 | 2,1 | 0,12 |
0,4 | 0,31 | 1,3 | 0,71 | 2,2 | 0,09 |
0,5 | 0,44 | 1,4 | 0,63 | 2,3 | 0,06 |
0,6 | 0,57 | 1,5 | 0,54 | 2,4 | 0,04 |
0,7 | 0,68 | 1,6 | 0,46 | 2,5 | 0,03 |
0,8 | 0,76 | 1,7 | 0,36 |
Барометрическая формула дает закон убывания давления газа с высотой в поле силы тяжести:
![]()
где рh - давление газа на высоте h, р0 - давление на высоте h = 0; g - ускорение силы тяжести.
14) Связь между удельной с и молярной Сμ теплоемкостями:
Сμ=с
Удельная теплоемкость газа при постоянном объеме:
Удельная теплоемкость газа при постоянном давлении:
15) Внутренняя энергия газа (энергия теплового движения молекул).
16) Средняя длина свободного пробега молекул газа:
![]()
где ![]() - средняя арифметическая скорость,
- средняя арифметическая скорость, ![]() - среднее число столкновений каждой молекулы с остальными в единицу времени; σ - эффективный диаметр молекулы; п — число молекул в единице объема.
- среднее число столкновений каждой молекулы с остальными в единицу времени; σ - эффективный диаметр молекулы; п — число молекул в единице объема.
17) Масса, перенесенная за время ![]() при диффузии:
при диффузии:
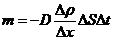
где![]() - градиент плотности в направлении, перпендикулярном к площадке
- градиент плотности в направлении, перпендикулярном к площадке ![]() , D - коэффициент диффузии:
, D - коэффициент диффузии:
![]()
![]()
где ![]() - средняя скорость; λ - средняя длина свободного пробега молекулы.
- средняя скорость; λ - средняя длина свободного пробега молекулы.
18) Количество движения, перенесенное газом за время Δt, определяет силу внутреннего трения в газе:
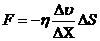
где Δυ/ΔX — градиент скорости течения газа в направлении, перпендикулярном к площади ΔS, η — коэффициент внутреннего трения (динамическая вязкость):
![]()
19) Количество тепли, переносимое за время в результате теплопроводности:
![]()
где ![]() — градиент температуры в направлении, перпендикулярном к площадке ΔS. К — коэффициент теплопроводности:
— градиент температуры в направлении, перпендикулярном к площадке ΔS. К — коэффициент теплопроводности:

![]()
20) Первое начало термодинамики:
Q=ΔU+A
где Q - теплота, сообщенная системе; ΔU - изменение внутреннем энергии системы; А — работа, совершенная системой против внешних сил.
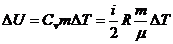
Работа расширения газа:

При изотермическом процессе:
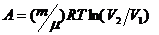
При изобарическом процессе:
A=P(V2-V1)
При адиабатическом процессе:
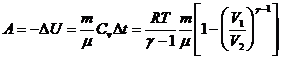
где γ=Сp/CV показатель адиабаты.
21) Уравнение Пуассона, связывающее параметры идеального газа при адиабатическом процессе:
![]() или
или ![]() Сonst
Сonst
22) Коэффициент полезного действия тепловой машины:
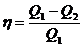
где Q1 - тепло, переданное рабочему телу; Q2 - тепло, отданное теплоприемнику.
Термический КПД цикла Карно
![]()
Где Т1 -температура теплоотдатчика; Т2 — температура теплоприемника.
23) Разность энтропии двух состояний В и А:
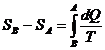
24) Коэффициент поверхностного натяжении:
α=F/l или α=ΔE/ΔS.
где F — сила поверхностного натяжения, действующая на контур l. ограничивающий поверхность жидкости; ΔE — изменение свободной энергии поверхностной пленки жидкости, связанное с изменением площади ΔS поверхности этой пленки.
25) Формула Лапласа, выражающая давление, создаваемое сферической поверхностью жидкости:
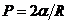
где R – радиус сферической поверхности.
26) Высота подъема жидкости в капиллярной трубке:
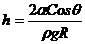
где θ-краевой угол (θ = 0 при полном смачивании стенок трубки жидкостью; θ = л при полном несмачивании) , R-радиус трубки; р — плотность жидкости; g—ускорение силы тяжести (g= 9,81 м/с2).
Высота подьема жидкости между двумя близкими и параллельными друг другу плоскостями:
![]()
где d—расстояние между плоскостями.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
Пример 1.
Определить количество вещества v и число N молекул углекислого газа массой m=200 г.
Решение.
Число N молекул, содержащихся в газе массой m, равно произведению постоянной Авогадро на количество вещества v:
N=vNa
Количество вещества v = m/μ, где μ молярная масса.
Определяем молярную массу CO2:
μ =12+16*2=44*10-3кг/моль;
![]()
N=4,5*6,02*1023=27,09 • 1023 молекул.
Пример 2.
Найти массу сернистого газа (SO2), занимающего объем 25 л при температуре 270С и давлении 101 кПа.
Решение.
Из уравнения Клапейрона — Менделеева масса газа находится:
![]()
Молярную массу сернистого газа определяем по данным таблицы Менделеева:
μ =32+16*2=64*10-3 кг/моль.
Вычисляем массу:
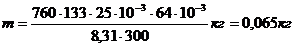
Пример 3.
В баллоне содержится m1=40 г кислорода и m2 = 240 г аргона. Давление смеси 2 МПа, температура 100 К. Определить объем баллона.
Решение.
По закону Дальтона давление газовой смеси равно сумме парциальных давлений газов, входящих и смесь.
Парциальные давления кислорода Р1, и аргона P2 находятся из уравнения Клапейрона—Менделеева:
![]() ,
, ![]()
Давление смеси газов:

Отсюда объем баллона:
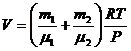
Молярные массы определяем по данным таблицы Менделеева:
μ=32*10-3кг/моль
μ=40*10-3 кг/моль
Вычислим объем:
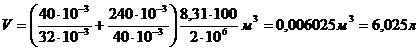
Пример 4.
В баллоне объемом4 V=10 л находится гелий под давлением P1=1 МПа и при температуре T1 = 300 К. После того, как из баллона выпущено m=10 г гелия, температура в баллоне понизилась до Т2 = 290 К. Определить давление P2 гелия, оставшегося в баллоне.
Решение.
Применим уравнение Клапейрона — Менделеева к конечному состоянию газа:
![]()
где т2 - масса гелии в баллоне в конечном состоянии; μ — молярная масса гелии; R — молярная газовая постоянная. Из этого уравнения выразим искомое давление:
![]()
Масса гелия m2 определится:
m2=m1-m,
где m1 масса гелия в начальном состоянии; m— масса гелия, взятого из баллона.
Масса гелия т1, находится из уравнения Клапейрона--Менделеева, записанного для начального состояния:
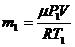
Окончательно искомое давление выразится:
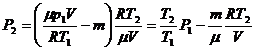
Проверим размерность искомой величины. Для этого подставим в правую часть единицы измерения величин. Первое слагаемое дает единицу давления. Для второго слагаемого:

С учетом значения μ=4*10-3 кг/моль вычислим давление P2^
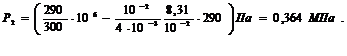
Пример 5.
Определить среднюю кинетическую энергию вращательного движения одной молекулы углекислого газа при температуре 400 К и кинетическую энергию вращательного движения всех молекул углекислого газа, находящихся в 20 г.
Решение.
На каждую степень свободы молекулы газа приходится одинаковая средняя энергия <ε> = 1/2 КТ, где К—постоянная Больцмана; Т — температура газа. Так как для трехатомной молекулы углекислого газа три степени свободы приходятся на поступательное движение и три степени свободы на вращательное движение, поэтому средняя энергия вращательного движения одной молекулы:

Кинетическая энергия вращательного движения всех молекул газа:
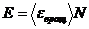
Число молекул газа n=vNa, где Nа – постоянная Авогадро; υ - количество вещества.
С учетом того, что ![]() получаем N=Na(m/μ). Полная кинетическая энергия вращения всех молекул, таки образом определяет:
получаем N=Na(m/μ). Полная кинетическая энергия вращения всех молекул, таки образом определяет:

Учитывая, что для углекислого газа μ=44*10-3кг/моль, произведем вычисления:
<εвращ>=3/2KT=3/2*1,38*10-23*400 Дж=8,28*10-21Дж
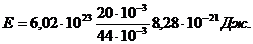
Пример 6.
Чему равны удельные теплоемкости сv и cp некоторого двухатомного газа, если плотность этого газа при нормальных условиях равна 1,43 кг/м3?
Решение.
Удельные теплоемкости выражаются
![]()
![]()
Из уравнения Клапейрона —.Менделеева выражаем μ:
PV=m/ μ RT и μ=mRT/PV=ρRT/p
так как плотность газа ρ= m/v.
Подставляя молярную массу в формулы для теплоемкости, имеем:
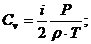
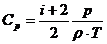
Произведем вычисления, учитывая, что для двухатомного газа число степеней слободы i = 5, а при нормальных условиях давление P= 1,01 • !05 Па и T = 273 К.
![]()
![]()
Пример 7.
В цилиндре под поршнем находится водород массой т= 0,02 кг при температуре T = 300 К. Водород сначала расширился адиабатно, увеличив объем в 5 раз, а затем изотермически сжался, уменьшив объем в 5 раз. Найти температуру в конце адиабатного расширения и работу, совершенную газом в этих процессах.
Решение.
В адиабатном процессе температура и объем газа связаны соотношением:
TVγ-1= const, то есть Т2/Т1=( V1/V2) γ-1
где γ- отношение теплоемкостей газов (γ=Cp/Cv).
Конечная температура T2,, отсюда определится:
T2=T1*( V1/V2) γ-1.
Работа при адиабатном расширении определится:
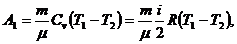
где Сv- молярная теплоемкость газа при постоянном объеме:
Работа при изотермическом процессе определится:

Проведем вычисления, учитывая, что для водорода, как двухатомного газа, i=5,
γ= 1,4, μ=2*10-3кг/моль;
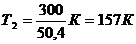
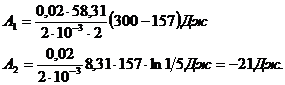
Здесь знак «минус» означает, что при сжатии работа совершается над газом внешними силами.
Пример 8.
Тепловая машина работает по обратимому циклу Карно. Температура теплоотдатчика Т1 = 600 К. Определить термический КПД цикла и температуру Т2 теплоприемника, если за счет каждого килоджоуля теплоты, получаемой от тепло-отдатчика, совершается работа А = 250 Дж.
Решение.
Термический КПД тепловой машины показывает, какая доля тепла, полученного от теплоотдатчика, затрачивается на совершение механической работы, и определяется:
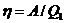
где Q1 — количество тепла, получаемое от теплоотдатчика; А — механическая работа, совершаемая рабочим телом тепловой машины.
С другой стороны, КПД цикла Карно определяется температурами теплоотдатчика и теплоприемника:
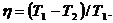
Отсюда температура теплоприемника:

Произведем вычисления:
η = 250/ 1000 = 0,25;
T2 = 600 (1—0,25)K = 450 К.
Пример 9.
Найти добавочное давление внутри мыльного пузыря диаметром d=10 см. Какую работу нужно совершить, чтобы выдуть этот пузырь?
Решение.
Пленка мыльного пузыря имеет внешнюю и внутреннюю сферические поверхности и обе оказывают давление на воздух, включенный внутри пузыря. Диаметры обеих поверхностей можно считать одинаковыми, так как толщина пленки мала. Добавочное давление поэтому определится:
P=2(2α/r),
Где α – коэффициент поверхностного натяжения; r – радиус пузыря; r=d/2.
Окончательно: P=8 α/d
Работа, затрачиваемая на увеличение поверхности пленки на величину ΔS запишется:
А= α ΔS= α(S-S0),
Где S – общая площадь двух сферических поверхностей пленки мыльного пузыря; S0 – общая площадь двух поверхностей плоской пленки, имевшейся до выдувания пузыря, которой в задаче можно пренебреч. Поэтому:
А= α S= απd2.
Произведем вычисления:

Пример 10.
Найти изменение энтропии при превращении 10 г льда при -200С в пар при 1000С.
Решение.
Изменение энтропии определяется формулой
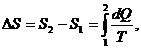
где. S1, и S2 — значения энтропии в первом и во втором состоянии соответственно.
В данном случае общее изменение энтропии складывается из изменении ее в отдельных процессах.
1) Нагревание массы т льда от температуры Т1 до температуры Т2. При этом,
dQ=mc1dT
где c1 — удельная теплоемкость льда.
Таким образом:
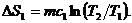
2) Плавление массы m льда при температуре Т2. Здесь
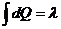 m
m
где λ — удельная теплота плавления. Определяем
ΔS=λm/T2.
3)Нагревание массы m поды от T2 до T3:
![]()
где с2 — удельная теплоемкость воды.
4)Испарение массы m поды при температуре Е3:
ΔS4=rm/T3,
Где r – удельная теплота парообразования.
Общее изменение энтропии:
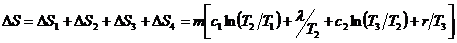
Произведем вычисления, имея в виду, что с1 = 2,1*IО3 Дж/кг. К, Т1 = 253 К. Т2= 273К, Т3 = 373 К, λ = 3,35*I05 Дж/кг, с2= 4,19*103 Дж/(кгК), r = 2,26*106 Дж/кг.
ΔS = 88 Дж/К.
Пример 11.
Найти изменение энтропии при переходе 8 г кислорода от объема в 10 л при температуре 80°С к объему в 40 л при температуре 300 °С.
Решение.
Имеем изменение энтропии
![]()
Но 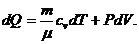
Учитывая уравнение Клапейрона — Менделеева ![]()
имеем:
![]()
или
![]()
После вычислений получаем
S2— S1=5,4 Дж/К.
КОНТРОЛЬНАЯ РАБОТА
201. Определить количество молей v и число N молекул азота массой m = 0,1 кг.
202. Определить молярную массу М и массу m одной молекулы озона O3, углекислого газа СО2 и метана СН4.
203. За время t = 10 суток из стакана полностью испарилось m= 100 г. воды. Сколько в среднем молекул вылетело с поверхности воды за 1 с?
204. Каков должен быть наименьший объем баллона, вмещающего 6,4 кг кислорода, если его стенки при температуре 20 0С выдерживают давление 15,7 МПа.
205. Идеальный газ при давлении 1,33 кПа и температуре 15°С занимает объем 2 л. Каким будет его давление, если температура газа увеличится в 2 раза, а объем уменьшится на 0,25 первоначального.
206. В дизеле в начале такта сжатия температура воздуха 400С, а давление 78,4 кПа. Во время сжатия объем уменьшается в 15 раз, а давление возрастает до 3,5 МПа. Определить температуру воздуха в конце такта сжатия.
207. Альпинист при каждом вдохе поглощает 5 г воздуха, находящегося при нормальных условиях. Найти объем воздуха который должен вдыхать альпинист в горах, где давление ниже атмосферного, а при температуре - 13 °С составляет 79,8 кПа?
208. Определить температуру газа, находящегося в закрытом сосуде, если давление газа увеличивается на 0,4% первоначального давления при нагревании газа на 1 °С.
209. Из баллона со сжатым кислородом, находящимся при постоянной температуре, израсходовано столько кислорода, что его давление упало от p1 = 9,8 МПа до р2 = 7,84 МПа. Какая часть первоначальной массы кислорода израсходована?
210. Баллон, содержащий 1 кг азота, при испытании взорвался при температуре. 350 0С. Какое количество водорода можно хранить в этом баллоне при 20°С, имея пятикратный запас прочности. Считать прочность баллона не зависящей от температуры.
211. В баллоне при 27°С и давлении 4,05 МПа находится ацетилен. Каким станет давление в баллоне после расхода половины массы газа, если температура при этом понизится до 12°С.
212. 7 г некоторого газа, заключенного в баллон при температуре 27°С, создает давление 49 кПа. В том же объеме 4 г водорода при температуре 60°С создают давление 0,435 МПа. Определить молярную массу неизвестного газа и назвать его.
213. До какой температуры при нормальном давлении нужно нагреть кислород, чтобы его плотность стала равна плотности aзотa при нормальных условиях?
214. 12 г газа занимают объем 4 л при температуре 7°С. После нагревания газа при постоянном давлении его плотность стала равной 0,6*103 кг/м3. До какой температуры нагрели газ?
215. Определить плотность смеси, состоящей из 4 г водорода и 32 г кислорода при температуре 7°С и давлении 93 кПа.
216. Сосуд емкостью 2V= 200 см3 разделен пополам полупроницаемой перегородкой. В одну половину введено т1= 2 мг водорода и т2= 4 мг гелия. Через перегородку может диффузировать только гелий. Во время процесса поддерживается постоянная температура. Т = 27°К. Какие давления р1 и р2 установятся в обеих частях сосуда?
217. Два баллона вместимостью 3 л и 7 л наполнены соответственно кислородом под давлением 200 кПа и азотом под давлением 300 кПа при одинаковой температуре. В баллонах после соединения образуется смесь газов с той же температурой. Определить давление смеси.
218. Смесь водорода и азота общей массой m = 300 г при температуре T=580°К и давлении р = 2,5 МПа занимает объем V=25 л. Определить массу m1 водорода и массу т2 азота.
219. Современная техника позволяет создать вакуум до 0,1 нПа. Сколько молекул газа остается при таком вакууме в 1 см3 при температуре 300 К?

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



