формы ГБ-115
Твердая дозированная лекарственная форма ГБ-115 – таблетки дозировкой 1 мг со средней массой 102 мг. Внешний вид – таблетки белого или почти белого цвета плоскоцилиндрической формы. Отклонения от средней массы образцов таблеток ГБ-115 не превышало установленных ГФ XI норм: ± 7,5 %. Время распадаемости не превышало 5 минут, что также соответствовало нормам, установленным ГФ XI (вып. 2. стр. 154).
Определение показателя «Посторонние примеси» в таблетках ГБ-115
Определение показателя «Посторонние примеси» в таблетках ГБ-115 проводили методом ВЭЖХ в условиях, подобранных для субстанции ГБ-115.
На хроматограммах извлечений из плацебо в указанных условиях были обнаружены пики со временами удерживания около 1,5 – 2,5 мин
Анализ модельной смеси таблеток ГБ-115 и свидетелей известных примесей показал, что в выбранных условиях хроматографирования не наблюдается разделения ТХ и пиков извлечения из плацебо (рис. 7). Однако поскольку ни в одном из образцов субстанции этой примеси обнаружено не было, мы сочли возможным ее содержание в таблетках не определять.
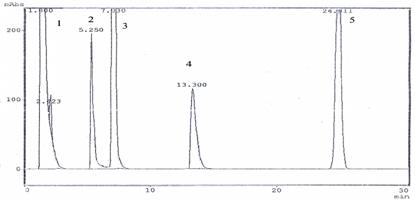
Рис. 7. Хроматограмма извлечения из таблеток ГБ-115 (концентрация 1 мг/мл) в смеси с примесями (концентрация каждого соединения 0,01 мг/мл): 1 - пики извлечения из плацебо, 2 – ФГГ, 3 - ГБ-115, 4 – ФГК, 5 - ГБ-111
В указанных условиях был проведен анализ образцов лекарственной формы ГБ-115. Содержание единичной примеси оценивали путем сравнения площадей примесей и раствора РСО ГБ-115 с концентрацией 0,01 мг/мл (1% от концентрации ГБ-115 в испытуемом растворе). В образцах таблеток ГБ-115 было обнаружено до трех примесей, в их числе примесь с относительным временем удерживания 0,8 (ФГГ). Содержание единичной примеси не превышало 0,44%, суммарное содержание примесей составляло не более 0,72%.
Проверку пригодности хроматографической системы проводили также как и при анализе субстанции.
Количественное определение ГБ-115 в таблетках
Разработку методики количественного определения ГБ-115 в таблетках с помощью УФ-СФМ проводили на модельных смесях ГБ-115 и плацебо (извлечения в спирте этиловом 95%) при аналитической длине волны 282 нм, рабочая концентрации 0,05 мг/мл.
Для проверки точности и сходимости методики готовили модельные смеси субстанции ГБ-115 и плацебо с концентрацией ГБ-115 0,05 мг/мл ± 20% (от 0,04 до 0,06 мг/мл) (табл. 7). Содержание плацебо в растворах эквивалентно содержанию в таблетке. Концентрация раствора РСО ГБ-115 – 0,05 мг/мл.
Таблица 7
Результаты количественного определения ГБ-115 в модельных смесях (УФ-спектрофотометрия)
Взято ГБ-115, г (m1) | Найдено ГБ-115, г (m2) | Абсолютная ошибка, г (d= m2–m1) | Относительная ошибка, % Х = (d´100/m1) | Найдено ГБ-115 (в % от m1) | Метрологические характеристики (P=95%, n=9) |
0,0399 | 0,0402 | 0,0003 | 0,75 | 100,75 | Хср.= 100,66% S = 0,67 Sxср=0,22
|
0,0426 | 0,0432 | 0,0006 | 1,4 | 101,41 | |
0,0452 | 0,0458 | 0,0006 | 1,3 | 101,3 | |
0.0478 | 0,0483 | 0,0005 | 1 | 101,05 | |
0,0499 | 0,0504 | 0,0005 | 1 | 101 | |
0,0523 | 0,0525 | 0,0002 | 0,38 | 100,4 | |
0,0550 | 0,0554 | 0,0004 | 0,73 | 100,7 | |
0.0574 | 0,0570 | -0,0004 | 0,7 | 99,3 | |
0,0604 | 0,0604 | 0 | 0 | 100 |
По разработанной методике были проанализированы серийные образцы таблеток. Содержание ГБ-115 в серийных образцах таблеток составляло от 0,9887 до 1,0142 мг в таблетке. Относительная ошибка не превышала 1,7%.
В качестве альтернативного метода количественного определения ГБ-115 в таблетках нами был выбран метод ВЭЖХ.
Анализ проводили в тех же условиях, что и определение посторонних примесей, за исключением аналитической длины волны, которая составила 282 нм. При этой длине волны поглощения электромагнитного излучения извлечением из плацебо практически не наблюдалось.
На модельных смесях ГБ-115 и плацебо (содержание эквивалентно содержанию в таблетке) с концентрацией ГБ-115 0,1 мг/мл ± 20% (от 0,08 до 0,12 мг/мл) было показано, что относительная ошибка единичного определения не превышает 1,6% (таблица 8).
По разработанной методике были проанализированы серийные образцы ГБ-115, содержание ГБ-115 в лекарственной форме при определении методом ВЭЖХ составляло от 0,9930 до 1,0130 мг в таблетке.
Таблица 8
Результаты количественного определения ГБ-115 в модельных смесях (ВЭЖХ)
Взято ГБ-115, г (m1) | Найдено ГБ-115, г (m2) | Абсолютная ошибка, г (d= m2–m1) | Относительная ошибка, % Х = (d´100/m1) | Найдено ГБ-115 (в % от m1) | Метрологические характеристики (P=95%, n=9) |
0,0082 | 0,00826 | +0,00006 | 0,73 | 100,73 | Хср=99,97% S=0,86 Sxср=0,29
|
0,0085 | 0,00843 | -0,00007 | 0,82 | 99,18 | |
0,0090 | 0,00899 | -0,00001 | 0,11 | 99,89 | |
0,0096 | 0,00955 | -0,00005 | 0,52 | 100,52 | |
0,0099 | 0,00994 | +0,00004 | 0,40 | 100,40 | |
0,0105 | 0,01043 | -0,00007 | 0,67 | 99,33 | |
0,0111 | 0,01093 | -0,00017 | 1,53 | 98,47 | |
0,0118 | 0,01196 | +0,00016 | 1,36 | 101,36 | |
0,0121 | 0,01208 | -0,00002 | 0,17 | 99,83 |
Определение показателя «Однородность дозирования» таблеток ГБ-115
Определение однородности дозирования таблеток ГБ-115 было проведено с помощью метода УФ-спектрофотометрии в условиях количественного определения. Отклонения в однородности дозирования ГБ-115 не превышали установленных ГФ XI норм (не более ± 15%).
Определение показателя «Растворение» таблеток ГБ-115
Субстанция ГБ-115 нерастворима в воде и 0,1М растворах хлористоводородной кислоты, в качестве среды растворения использовали 0,5% раствор натрия лаурилсульфата в воде. Анализ проводили на приборе «лопастная мешалка», при 50 оборотах в минуту, объем среды растворения – 500 мл, температура 37±0,5 °С. Количественное определение ГБ-115 проводили методом ВЭЖХ. Из-за низкой дозировки ГБ-115 чувствительность методики количественного определения при длине волны 282 нм была недостаточной, в качестве аналитической была выбрана длина волны 230 нм.
Линейная зависимость площади пика растворов ГБ-115 в 0,5% растворе натрия лаурилсульфата от концентрации наблюдалась в интервале от 0,001 до 0,05 мг/мл (коэффициент корреляции 0,9998), рабочая концентрация 0,01 мг/мл. На модельных смесях ГБ-115 и плацебо с концентрацией ГБ-115 от 0,008 до 0,012 мг/мл показано, что относительная ошибка определения не превышает 1,6%.
При определении показателя «Растворение» серийных образцов таблеток ГБ-115 в указанных условиях за 45 минут из таблеток высвобождалось более 75% ГБ-115 (рис. 8), что соответствует нормам ГФ СССР XI издания.
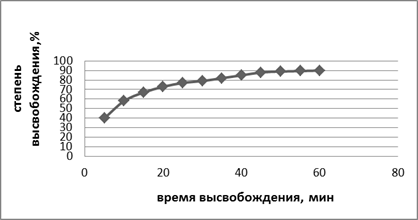
Рис. 8. Кинетика высвобождения ГБ-115 из таблеток
Установление сроков годности твердой дозированной лекарственной формы ГБ-115
Стабильность таблеток при хранении была изучена методом «ускоренного старения» при 60 ºС в течение срока, эквивалентного 2 годам хранения в естественных условиях. Качество таблеток по всем показателям по истечении срока хранения не изменилось, установлен предварительный срок годности таблеток - 2 года.
В результате проведенных исследований разработаны предварительные нормы качества таблеток ГБ-115 (табл. 9).
Таблица 9
Нормы качества таблеток ГБ-115
Показатели | Метод испытания | Нормы |
Описание | Визуально | Таблетки белого или почти белого цвета плоскоцилиндрической формы |
Подлинность | УФ-спектрофотометрия | УФ-спектр поглощения испытуемого раствора в области длин волн от 230 до 300 нм должен соответствовать УФ-спектру поглощения раствора РСО ГБ-115 |
ВЭЖХ | Время удерживания основного пика на хроматограмме испытуемого раствора должно совпадать со временем удерживания пика ГБ-115 на хроматограмме раствора РСО | |
Средняя масса | ГФ ХI, вып.2, с.154 | От 101,9 мг до 103,4 мг (102 мг ± 7,5%) |
Отклонение от средней массы | ГФ ХI, вып.2, с.154 | 18/20: ± 7,5%; 2/20: ± 15% |
Распадаемость | ГФ ХI, вып.2, с.154 | Не более 15 мин |
Однородность дозирования | УФ-спектрофотометрия | 10/10: ±15% или 28/30: ±15%, 0/30: более чем ±25% |
Посторонние примеси | ВЭЖХ | Единичной примеси: не более 0,5%; Сумма примесей: не более 1% |
Микробиологическая чистота | ГФ ХII, часть 1, с.160 | Категория 3А |
Растворение | ГФ ХI, вып.2, с.154 и ОФС ,ВЭЖХ | Не менее 75% за 45 минут |
Количественное определение | ВЭЖХ | от 0,9930 мг до 1,0130 мг (0,102±7,5%) |
Срок годности | 2 года |
ВЫВОДЫ
1. Изучены физико-химические свойства и спектральные характеристики фармакопейных образцов субстанции ГБ-115 методами ИК-, УФ - и ПМР-спектроскопии. Показана возможность использования этих методов для контроля качества субстанции ГБ-115.
2. Изучена хроматографическая подвижность ГБ-115, исходного (ФГК) и промежуточных (ТХ, ФГГ и ГБ-111) продуктов синтеза методами тонкослойной и высокоэффективной жидкостной хроматографии. Показано преимущество более селективного и чувствительного метода ВЭЖХ при определении содержания посторонних примесей в субстанции ГБ-115.
3. Проведены исследования по разработке способа количественного определения субстанции ГБ-115 с помощью химических и инструментальных методов анализа. Показана возможность применения метода определения общего азота по Къельдалю, а также методов УФ-спектрофотометрии и ВЭЖХ для количественного определения ГБ-115 в субстанции.
4. Определены основные фармакопейные показатели качества твердой дозированной лекарственной формы (таблеток) ГБ-115. Изучена хроматографическая подвижность препарата с помощью метода ВЭЖХ. Показана возможность применения метода ВЭЖХ для анализа посторонних примесей, количественного определения и определения однородности дозирования таблеток ГБ-115.
5. Разработана методика определения показателя «Растворение» таблеток ГБ-115 в среде 0,5% раствора натрия лаурилсульфата. Установлено, что за 45 минут из таблеток высвобождалось более 75% ГБ-115.
6. Изучена стабильность субстанции и таблеток ГБ-115 под действием факторов окружающей среды. Показано, что субстанция ГБ-115 не гигроскопична, относительно устойчива к окислению, но неустойчива к действию солнечного света и к щелочному гидролизу. Таблетки ГБ-115 неустойчивы к условиям повышенной влажности и действию солнечного света.
7. В результате изучения стабильности при хранении субстанции и таблеток ГБ-115 методом «ускоренного хранения» определены предварительные сроки их годности – 2 года.
8. Установлены нормы качества субстанции и твердой дозированной лекарственной формы ГБ-115. На основании проведенных исследований составлены проекты фармакопейных статей предприятия на субстанцию и твердую дозированную лекарственную форму ГБ-115.
Список работ, опубликованных по теме диссертации:
1. , , Пятин методик анализа субстанции нового анксиолитика пептидной структуры // Тезисы докладов XVII Российского Национального конгресса «Человек и лекарство» - Москва, 2010 . с. 637
2. , , Пятин хроматографического поведения препарата ГБ-115// Тез. докл.5-ой Международной конференции «Биологические основы индивидуальной чувствительности к психотропным средствам» Москва, 2010, с. 49-50
3. , , Дуденкова физико-химических свойств и разработка методик анализа субстанции нового оригинального анксиолитического средства ГБ-115// Химико-фармацевтический журнал, 2011, т. 45, № 10, стр. 53-56
4. , , , Турчинская методик анализа твердой дозированной лекарственной формы ГБ-115// Химико-фармацевтический журнал, 2011, т. 45, № 12, стр. 27-31
5. , , Иванов субстанции нового анксиолитика// Журнал Фармация, 2012, №1, с. 6-8

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



