Вместе с тем, при посеве образцов клинического материала в разработанную среду в сравнении со стандартной средой 10C наблюдали увеличение количества выделенных штаммов Ureaplasma spp. и значительное снижение роста сопутствующих микроорганизмов (табл. 2, 3).
При посеве в разработанную питательную среду всех 87 образцов клинического материала, которые были положительными в ПЦР с праймерами, специфичными для генов 16S рРНК Ureaplasma spp., наблюдался рост уреаплазм. Все выросшие культуры являлись культурами Ureaplasma spp.. Доказательством этого являлись положительный результат в ПЦР с праймерами, специфичными для генов 16S рРНК уреаплазм, и рост на агаре А7 с образованием мелких (порядка 20-60 мкм), с характерной морфологией, темно-коричневых колоний (положительный уреазный тест).
Таблица 2
Рост Ureaplasma spp. при посеве клинического материала на известной (10C) и предлагаемой среде для культивирования и выявления Ureaplasma spp.
Питательная среда | Количество произведенных посевов | Количество образцов, положительных в ПЦР | Количество выделенных культур |
10C | 197 | 87 | 76 |
предлагаемая среда | 197 | 87 | 87 |
Таблица 3
Рост сопутствующих микроорганизмов при посеве клинического материала на известной (10C) и предлагаемой среде для культивирования и выявления Ureaplasma spp.
Питательная среда | Количество произведенных посевов | Количество образцов, в которых наблюдался рост сопутствующих микроорганизмов |
10C | 197 | 42 |
предлагаемая среда | 197 | 1 |
При этом из 87 положительных в ПЦР образцов на стандартной среде 10C выделено только 76 культур уреаплазм. При посеве 42 образцов клинического материала наблюдался рост сопутствующих микроорганизмов, проявившийся в выраженном помутнении среды и образовании придонного осадка. Признаки роста сопутствующих микроорганизмов на разработанной нами среде были только при посеве только 1 образца.
Кроме того, рост Ureaplasma spp. на разработанной питательной среде наблюдался при большем разведении исследуемого материала, что свидетельствовало о более высокой ее чувствительности (табл. 4).
Таблица 4
Рост Ureaplasma spp. при посеве клинического материала в разных разведениях на известной (10C) и предлагаемой среде для культивирования и выявления Ureaplasma spp.
Разведение исследуемого материала | Количество образцов с ростом Ureaplasma spp. на среде 10C | Количество образцов с ростом Ureaplasma spp. на предлагаемой среде |
10-1 | 76 | 87 |
10-2 | 76 | 87 |
10-3 | 69 | 87 |
10-4 | 50 | 72 |
Таким образом, использование предложенной питательной и транспортной среды позволяет с высокой эффективностью выявлять бактерии рода Ureaplasma в образцах клинического материала.
Количественная оценка роста бактерий рода Ureaplasma в жидкой питательной среде
В процессе разработки питательной среды для культивирования и выявления Ureaplasma spp. мы столкнулись с необходимостью количественного учета роста уреаплазм. Одной из задач нашего исследования являлось определение концентрации бактерий в культурах Ureaplasma spp., выращенных в разработанной питательной среде. Определение количества клеток в культурах уреаплазм необходимо для оценки ростовых свойств питательной среды, а также определения чувствительности штаммов Ureaplasma spp. к антибактериальным препаратам. Кроме того, определение количества условно-патогенных бактерий рода Ureaplasma в образцах клинического материала необходимо для установления их этиологической роли в патологии человека.
Количественная оценка роста Ureaplasma spp. сопряжена с определенными трудностями, так как многие из методов определения концентрации бактериальных культур неприменимы в отношении уреаплазм.
Мы сопоставили два подхода к нахождению численности бактерий рода Ureaplasma, основанные на определении количества жизнеспособных клеток и копий генома.
Для определения количества жизнеспособных клеток уреаплазм исследуемый образец разводили в питательной среде до такой степени, чтобы при взятии пробы из образца бактерии могли как оказаться, так и не оказаться в ней (рис. 2). Значения концентрации получали путем статистического анализа экспериментальных результатов. Нами были испытаны два метода расчета численности жизнеспособных клеток Ureaplasma spp.: 1) метод определения наиболее вероятного количества (НВК) бактерий, примененный ранее для оценки количества нетребовательных к условиям культивирования микроорганизмов (Дж. Мейнелл, Э. Мейнелл, 1967); 2) метод 50% дозы цветообразующих единиц (ЦОЕ50) со статистической обработкой результатов по L. J. Reed, H. Muench (1938) и B. Behrens, C. Karber (1935).


Рис. 2. Серия последовательных 10-кратных (а) и 2-кратных (б) разведений для определения количества жизнеспособных клеток U. parvum 465.
Для различных штаммов Ureaplasma spp. в экспоненциальной фазе роста результаты, полученные методами НВК, ЦОЕ50 и ПЦР-РВ достаточно близки (табл. 5). Для уточнения того, насколько хорошо это совпадение, мы применили критерий Блэнда-Алтмана (С. Гланц, 1999). Выяснилось, что достоверностью 0,95 методы НВК и ЦОЕ50 дают те же результаты, что и ПЦР-РВ.
Таблица 5
Накопление клеток уреаплазм по данным трех методов исследования
Штамм уреаплазм | Метод | Накопление клеток на время инкубации | Количество клеточных делений за 4 часа | Время генерации, часов | |
17 часов | 21 час | ||||
2Т | ПЦР-РВ | 1,1·106 | 2,4·106 | 2,18 | 1,83 |
НВК | 1,0·106 | 2,2·106 | 2,20 | 1,82 | |
ЦОЕ50 | 1,0·106 | 2,1·106 | 2,10 | 1,90 | |
455 | ПЦР-РВ | 5,0·105 | 1,1·106 | 2,20 | 1,82 |
НВК | 4,0·105 | 9,0·105 | 2,25 | 1,78 | |
ЦОЕ50 | 4,4·105 | 8,9·105 | 2,02 | 1,98 | |
465 | ПЦР-РВ | 1,8·105 | 4,0·105 | 2,22 | 1,80 |
НВК | 1,8·105 | 3,8·105 | 2,11 | 1,90 | |
ЦОЕ50 | 2,1·105 | 4,3·105 | 2,04 | 1,96 | |
481 | ПЦР-РВ | 8·105 | 1,7·106 | 2,13 | 1,87 |
НВК | 7,8·105 | 1,7·106 | 2,19 | 1,82 | |
ЦОЕ50 | 1,0·106 | 2,1·106 | 2,10 | 1,90 |
Таким образом, примененные для Ureaplasma spp. методы НВК бактерий и ПЦР-РВ позволяли определить концентрацию уреаплазм в исследуемых образцах. Использование метода серийных разведений с соответствующей статистической обработкой дало надежный способ количественного определения бактерий рода Ureaplasma, позволяющий проводить дальнейшую идентификацию и определение чувствительности штаммов уреаплазм к антибактериальным препаратам, а также оценивать ростовые свойства разных серий разработанной нами питательной среды и отдельных ее компонентов. Определение числа жизнеспособных клеток методами НВК и ЦОЕ50 более пригодно к использованию в практических лабораториях. При этом метод ЦОЕ50 требует математических расчетов; в то время как для нахождения НВК бактерий созданы таблицы (Дж. Мейнелл, Э. Мейнелл, 1967), что позволяет оценивать концентрацию уреаплазм, не прибегая к сложным вычислениям.
Нами предложены стандартные условия культивирования. Стандартные условия обеспечиваются культивированием в 96-луночных планшетах, лунки которых имеют одинаковые размеры; в одинаковом объеме среды (в 250 мкл); под слоем минерального масла, предотвращающего улетучивание аммиака и испарение культуральной среды. Благодаря использованию стандартных условий культивирования нами были получены данные, позволяющие предположить, что изменение ОП среды в процессе роста культур Ureaplasma spp. может количественно отражать накопление клеток уреаплазм.
Изучение взаимосвязи ОП среды и количества накопленных бактериальных клеток легло в основу разработки спектрофотометрического экспресс-метода определения концентрации культур Ureaplasma spp. в процессе их роста.
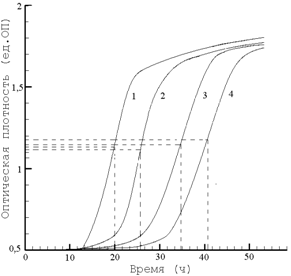 | 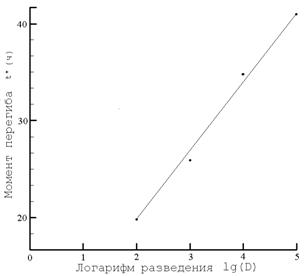 |
Показанные на рис. 3 и 5 графики изменения ОП среды в процессе роста различных штаммов Ureaplasma spp. в жидкой питательной среде, независимо от их начальной концентрации, имели типичный ступенькообразный вид и состояли из 3-х фаз: 1) длительной латентной фазы с низким постоянным значением ОП; 2) сменяющей ее короткой фазы экспоненциального роста ОП; 3) фазы замедления роста и выхода на высокий уровень ОП, далее почти не меняющийся. Кривая изменения ОП имела характерную точку – точку перегиба, до которой ОП росла с ускорением, а после нее – с замедлением, что соответствовало переходу от второй фазы к третьей. Форма кривой изменения ОП среды в процессе роста не зависела от посевной дозы, и соответственно, времени культивирования. На рис. 3 видно, что значения ОП в точках перегиба кривых, соответствующих разным разведениям, отличались незначительно, но моменты точки перегиба были существенно различны. Зависимость момента перегиба кривой изменения ОП среды от логарифма разведения культуры показана на рис. 4; эта зависимость линейная, что свидетельствовало о том, что характер роста ОП вплоть до этого момента действительно близок к экспоненциальному.
Рис. 3. Изменение оптической плотности среды в процессе роста штамма U. urealyticum 2Т в разведениях 1, 1, 1, 1Исходная концентрация уреаплазм составляла 106 клеток/мл. | Рис. 4. Зависимость момента перегиба кривой изменения оптической плотности среды в процессе роста штамма U. urealyticum 2Т от логарифма разведения культуры. |
Мы использовали два подхода для изучения накопления бактерий в процессе роста культур Ureaplasma spp., основанные на определении количества: 1) жизнеспособных клеток методами ЦОЕ50 и НВК; 2) копий генома методом ПЦР-РВ. При культивировании Ureaplasma spp. в питательной среде наблюдалась последовательная смена фаз. Графики накопления жизнеспособных клеток штаммов Ureaplasma spp. (при условии, если исходные культуры находились в экспоненциальной фазе роста) имели типичный вид и включали 3 основные фазы развития бактериальных популяций (рис. 6): 1) фазу экспоненциального роста, характеризующуюся максимальной скоростью накопления клеток и увеличением численности в геометрической прогрессии; 2) короткую стационарную фазу (всего 4 часа) – фазу максимального накопления в культуре жизнеспособных клеток (для разных штаммов Ureaplasma spp. в пределах 1,2·106-2,8·106 клеток/мл); 3) фазу отмирания с резким снижением жизнеспособности культуры (за 12 часов количество жизнеспособных клеток снижалось более, чем в 104 раз).
График накопления копий генома Ureaplasma spp. в процессе роста культуры, показанный на рис. 6, состоял из 2-х фаз: 1) фазы экспоненциального роста, практически идентичной аналогичной фазе накопления жизнеспособных клеток; 2) стационарной фазы, характеризующейся максимальным накоплением копий генома, которое соответствует максимальному накоплению жизнеспособных клеток, но без снижения в фазе отмирания культуры.
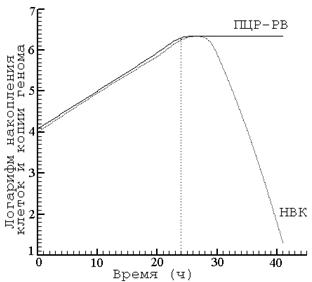 |
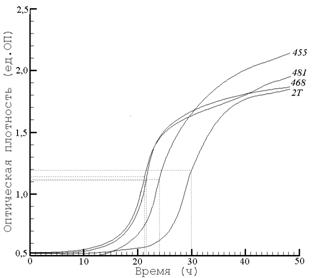
Рис. 5. Изменение оптической плотности среды в процессе роста штаммов U. parvum 455, 468, 481 и U. urealyticum 2Т. Исходная концентрация штаммов 455 – 1,2·104; 468 - 3·104; 481 - 2·104; 2Т - 4·103 клеток/мл среды. | Рис. 6. Накопление жизнеспособных клеток (НВК) и копий генома (ПЦР-РВ) штамма U. parvum 455. |
В экспоненциальной фазе роста уреаплазменных культур деление клеток происходило синхронно с репликацией ДНК, и соответственно, содержание копий генома отражало накопление жизнеспособных клеток. Полное соответствие этих двух показателей позволило сделать вывод о том, что одна ЦОЕ, выявляемая с помощью методов НВК или ЦОЕ50, соответствовала одной клетке Ureaplasma spp.. Кроме того, по-видимому, в процессе роста культур уреаплазм не происходило образования «многоядерных» клеток, содержащих несколько нуклеоидов.
Данные проведенного нами сопоставления изменения ОП среды и накопления клеток в процессе роста Ureaplasma spp. представлены в табл. 7. Латентную фазу продолжительностью 14-17 часов с низким значением ОП среды (в пределах 0,52-0,54) наблюдали от момента внесения уреаплазм в питательную среду до накопления в культуре не менее 2·105 клеток/мл. Затем происходил выраженный рост ОП: латентная фаза сменялась фазой экспоненциального роста ОП. Фаза экспоненциального роста ОП до момента максимальной скорости изменения ОП (точки перегиба) несущественно отличалась среди различных штаммов. При дальнейшем увеличении в процессе роста культуры ОП до значения в пределах 1,0-1,2, соответствующего перегибу кривой изменения ОП, скорость накопления клеток снижалась и культура вступала в стационарную фазу роста. Таким образом, экспоненциальный рост ОП среды наблюдался при накоплении в культуре достаточно большого количества клеток Ureaplasma spp., что соответствовало поздней экспоненциальной фазе роста. ОП среды и соответствующее ей накопление клеток в фазе экспоненциального роста ОП приведены в табл. 8.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



