Таблица 7
Изменение оптической плотности среды и накопление клеток в процессе роста культур Ureaplasma spp.
Фаза кривой изменения оптической плотности среды | Соответствующая фаза роста культуры |
латентная | лаг-фаза и экспоненциальная до накопления 2·105 клеток/мл |
экспоненциального роста | экспоненциальная |
точка перегиба | замедление роста и вступление в стационарную фазу |
замедления роста | стационарная и отмирания |
Таблица 8
Накопление клеток Ureaplasma spp. в экспоненциальной фазе роста оптической плотности среды
оптическая плотность среды | накопление клеток в 1 мл среды |
0,6 | 0,6·106 ± 0,2·106 |
0,7 | 0,9·106 ± 0,2·106 |
0,8 | 1,3·106 ± 0,3·106 |
0,9 | 1,6·106 ± 0,4 ·106 |
1,0 | 1,8·106 ± 0,6·106 |
1,11 | 1,9·106 ± 0,6·106 |
1,2 | 1,9·106 ± 0,6·106 |
Таким образом, измерение ОП среды в процессе роста бактерий рода Ureaplasma в разработанной питательной среде в стандартных условиях культивирования позволяет оценить накопление жизнеспособных клеток уреаплазм. Полученные нами результаты использованы для контроля качества питательной среды и стандартизации инокулята при определении чувствительности штаммов Ureaplasma spp. к антибактериальным препаратам.
Оценка ростовых свойств питательной среды для выявления Ureaplasma spp.
Оценка ростовых свойств разных серий питательной среды для выявления Ureaplasma spp., а также основных ее компонентов, является важнейшим этапом приготовления среды, необходимым для успешного обнаружения уреаплазм в образцах клинического материала.
Нами предложен оригинальный метод оценки ростовых свойств питательной среды, основанный на анализе кривых изменения ОП среды. Оценка ростовых свойств включает в себя 2 этапа: 1). Культивирование тест-штамма Ureaplasma spp. в среде сравнения и испытуемой в стандартных условиях в течение одного и того же времени при одинаковой концентрации тест-штамма в контрольных и опытных лунках. 2). Анализ кривых изменения оптической плотности среды в процессе роста тест-штамма в среде сравнения и испытуемой.
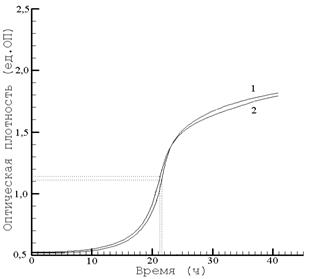
Кривые изменения ОП среды будут одинаковыми в том случае, если условия культивирования тест-штамма в контрольных и опытных лунках также одинаковы. Это возможно при соблюдении следующих условий: 1) культивировании в стандартных условиях; 2) инкубации в течение одного и того же времени; 3) одинаковой концентрации тест-штамма Ureaplasma spp. в контрольных и опытных лунках (условия 1-3 задаются при постановке методики); 4) одинаковых ростовых свойствах питательных сред (сравнения и испытуемой). На рис. 7 представлены кривые изменения ОП в процессе роста тест-штамма в средах, обладающих одинаковыми ростовыми свойствами.
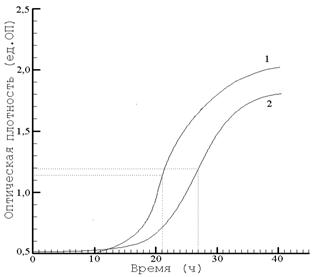
Изменение (ухудшение, обусловленное присутствием ингибиторов роста уреаплазм) ростовых свойств испытуемой среды сопровождалось изменением накопления клеток и, как следствие, изменением кривой зависимости ОП среды от времени. В процессе роста штамма U. parvum 455 в питательной среде, содержащей 250 мМ хлорида натрия (известно, что уреаплазмы высоко чувствительны к изменению осмотического давления среды), наблюдали увеличение латентной фазы, а также снижение скорости изменения ОП среды в экспоненциальной фазе (рис. 8).
Таким образом, изменение ОП среды в процессе роста культур тест-штамма в питательных средах сравнения и испытуемой, отражающее накопление жизнеспособных клеток, при соблюдении определенных условий (стандартных условий культивирования в планшетах, одинаковой концентрации клеток тест-штамма в начальный момент в контрольных и опытных лунках, одинаковом времени инкубации) позволяет сравнить ростовые свойства сред. Предложенный метод позволяет проводить сравнение сред в процессе роста культур как по интегральному показателю (площади под кривыми изменения ОП), так и по отдельным показателям (продолжительности латентной фазы, скорости изменения ОП, значения ОП в точке перегиба
 |  |
кривых).
Рис. 7. Изменение оптической плотности среды в процессе роста штамма U. parvum 468 в питательной среде сравнения (1) и испытуемой среде (2). Концентрация жизнеспособных клеток уреаплазм в начальный момент составляла 2·104 клеток/мл (1, 2). | Рис. 8. Изменение оптической плотности среды в процессе роста штамма U. parvum 455 в питательной среде сравнения (1) и испытуемой среде (2). Испытуемая среда содержала 250 мМ хлорида натрия. Концентрация жизнеспособных клеток уреаплазм в начальный момент составляла 2·104 клеток/мл (1, 2). |
Определение чувствительности штаммов Ureaplasma spp.
к антибактериальным препаратам
Бактерии рода Ureaplasma являются условно-патогенными микроорганизмами; вместе с тем при наличии клинических проявлений заболевания, при доказанной этиологической значимости уреаплазм назначают антибактериальные препараты (АБП).
Нами предложен микрометод определения чувствительности штаммов Ureaplasma spp. к АБП, являющийся модификацией метода серийных разведений в жидкой питательной среде и основанный на использовании пограничных концентраций препаратов. Пограничные концентрации АБП позволяют отнести штаммы уреаплазм к определенной группе по степени чувствительности (чувствительных, умеренно-чувствительных и устойчивых). По нашему мнению, пограничные концентрации должны отражать МИК50 и МИК90, которые являются основными показателями, характеризующими активность АБП. Минимальная пограничная концентрация, разделяющая чувствительные и умеренно-чувствительные штаммы, соответствует МИК50; максимальная, дифференцирующая умеренно-чувствительные и устойчивые штаммы - МИК90. Значения МИК, которые были определены классическим микрометодом серийных разведений АБП в жидкой питательной среде, представлены в табл. 9.
Таблица 9
Минимальные ингибирующие концентрации антибактериальных препаратов
Антибактериальный препарат | Минимальная ингибирующая концентрация, мкг/мл | |||
пределы колебаний | МИК50 | МИК90 | ||
минимальное значение | максимальное значение | |||
доксициклин | ≤ 0,125 | 16,0 | 0,25 | 2,0 |
эритромицин | 0,25 | 16,0 | 2,0 | 8,0 |
азитромицин | ≤ 0,125 | 4,0 | 0,5 | 2,0 |
кларитромицин | ≤ 0,125 | 4,0 | 2,0 | 4,0 |
мидекамицин | ≤ 0,125 | 4,0 | 2,0 | 4,0 |
джозамицин | ≤ 0,125 | 4,0 | 2,0 | 4,0 |
спирамицин | 32,0 | > 60,0 | - | - |
линкомицин | > 32,0 | - | - | - |
клиндамицин | ≥ 32,0 | - | - | - |
ципрофлоксацин | 0,5 | 8,0 | 2,0 | 4,0 |
офлоксацин | 0,5 | 4,0 | 2,0 | 4,0 |
Установленные значения МИК50 и МИК90 использовали для приготовления ряда питательных сред с АБП для оценки чувствительности клинических штаммов Ureaplasma spp. методом пограничных концентраций (рис. 9, табл. 10).

Рис. 9. Определение чувствительности одного из штаммов Ureaplasma spp. к антибактериальным препаратам методом серийных разведений с использованием пограничных концентраций. Клм5 – клиндамицин 5 мкг/мл; Лм30 – линкомицин 30 мкг/мл; Крм2, Крм4 – кларитромицин 2, 4 мкг/мл; Азм2 – азитромицин 2 мкг/мл; См50 – спирамицин 50 мкг/мл; Эм2, Эм8 – эритромицин 2, 8 мкг/мл; Мм2, Мм4 – мидекамицин 2, 4 мкг/мл; Дм2, Дм4 – джозамицин 2, 4 мкг/мл; Оф2, Оф4 – офлоксацин 2, 4 мкг/мл; Цф2, Цф4 – ципрофлоксацин 2, 4 мкг/мл; Дц2 – доксициклин 2 мкг/мл. К+ положительный контроль; К - отрицательный контроль.
Получены данные, свидетельствующие о существовании штаммов Ureaplasma spp. с различной степенью чувствительности к АБП. Большинство исследованных штаммов были высоко чувствительны к доксициклину и макролидам (за исключением эритромицина и спирамицина, обладающих меньшей активностью). Доксициклин и макролиды ингибировали рост большинства штаммов уреаплазм (от 72,8% для мидекамицина и до 100% для азитромицина) в низкой концентрации (МИК ≤ 2 мкг/мл). Однако, наряду со штаммами Ureaplasma spp., обладающими высокой чувствительностью к доксициклину и макролидам, были выявлены устойчивые штаммы. Так, 2,9% штаммов были устойчивы к доксициклину, 3,8% - к эритромицину, 0,7% - к мидекамицину, 0,2% - к джозамицину. При этом не выявлено ни одного штамма, устойчивого к азитромицину и кларитромицину. Менее эффективными in vitro в отношении Ureaplasma spp. оказались фторхинолоны. Значительное количество исследованных штаммов было устойчиво к ципрофлоксацину и офлоксацину (42,7% и 17,9%, соответственно). Высоко чувствительными к ципрофлоксацину и офлоксацину оказались только 37,2% и 44,9% штаммов, соответственно.
Таблица 10
Распределение штаммов Ureaplasma spp. (общее количество 452) по степени чувствительности к антибактериальным препаратам
Антибактериальный препарат | Абсолютное число и процент штаммов | ||
чувствительных | умеренно-чувствительных | устойчивых | |
доксициклин1 | ,1) | - | 13 (2,9) |
эритромицин | 89 (19,7) | ,5) | 17 (3,8) |
азитромицин2 | - | 0 | |
кларитромицин | 36 (8) | 0 | |
мидекамицин | ,3) | 3 (0,7) | |
джозамицин | ,7) | 59 (13,1) | 1 (0,2) |
спирамицин3 | - | ,4) | ,6) |
линкомицин | 0 | 0 | |
клиндамицин | 0 | 0 | |
ципрофлоксацин | ,2) | 91 (20,1) | ,7) |
офлоксацин | ,9) | ,2) | 81 (17,9) |
Примечание.
1, 2 Использовали одну пограничную концентрацию доксициклина и азитромицина 2 мкг/мл, дифференцирующую штаммы уреаплазм на чувствительные и устойчивые.
3 Использовали одну пограничную концентрацию спирамицина 50 мкг/мл, дифференцирующую штаммы уреаплазм на умеренно-чувствительные и устойчивые.
Как и следовало ожидать, все исследованные штаммы Ureaplasma spp. были устойчивы к линкозамидам линкомицину и клиндамицину. При этом, как отмечено ранее, все штаммы были чувствительны к макролидам азитромицину и кларитромицину. Предлагаем использовать такое различное отношение штаммов к указанным антибиотикам как дополнительный дифференциальный признак для идентификации бактерий рода Ureaplasma spp..
Таким образом, результаты проведенного исследования свидетельствовали о целесообразности определения чувствительности штаммов Ureaplasma spp. к АБП. Определение чувствительности штаммов Ureaplasma spp. к АБП in vitro может служить, во-первых, основанием для рационального выбора антибактериальной терапии, направленной на элиминацию уреаплазм из организма, и, во-вторых, дополнительным критерием идентификации штаммов уреаплазм по их чувствительности к антибиотикам группы макролидов азитромицину и кларитромицину и устойчивости к антибиотикам группы линкозамидов линкомицину и клиндамицину.
Разработка микротест-системы для выявления и идентификации Ureaplasma spp. «Уреаплазма микротест» и оценка ее диагностической эффективности в государственных испытаниях
На основе предложенных сред нами разработана микротест-система для выявления и идентификации Ureaplasma spp. «Уреаплазма Микротест». Микротест-система предназначена для культивирования штаммов Ureaplasma spp. в стандартных условиях; выявления и идентификации Ureaplasma spp. в образцах клинического материала; определения концентрации жизнеспособных клеток в культурах Ureaplasma spp. и образцах клинического материала; а также определения чувствительности штаммов Ureaplasma spp. к АБП.
В состав микротест-системы входят пять компонентов: транспортная среда, среда роста, среды с АБП, стерильное минеральное масло, стерильный 96-луночный планшет. Стандартный формат планшетов делает их пригодными для проведения как визуального, так и автоматизированного учета результатов исследования с помощью планшетных фотометров.
Основным преимуществом микротест-системы «Уреаплазма микротест» является стандартизация микробиологического метода диагностики уреаплазменной инфекции, позволяющая получить достоверные, воспроизводимые результаты. Нами это было достигнуто стандартизацией основных компонентов микротест-системы (использование стандартизованных компонентов сред, соблюдение технологии приготовления, оценка ростовых свойств питательной среды и ее отдельных компонентов) и методики проведения исследования (микротест-система содержит все необходимые для проведения исследования компоненты, методика исследования изложена в виде инструкции по применению микротест-системы).
Обусловленная широким распространением бессимптомного носительства уреаплазм и отсутствием четких клинических проявлений уреаплазменной инфекции невозможность разделения на опытную («больных») и контрольную («здоровых») группы затрудняла оценку микротест-системы «Уреаплазма микротест» в клинико-эпидемиологических испытаниях.
В связи с этим нами была разработана и использована новая методика сравнительной оценки эффективности микротест-системы, предназначенной для диагностики инфекции, вызываемой условно-патогенными бактериями рода Ureaplasma. Методика позволяет вычислять критерий диагностической эффективности U в условиях отсутствия четкого деления на опытную и контрольную группы. В такой ситуации показатель чувствительности Se нельзя найти из опытов с достаточной точностью, но показатель специфичности Sp можно определить по группе пациентов с отрицательными результатами ПЦР, т. е. с достоверным отсутствием возбудителя. Критерий диагностической эффективности: U(P) = P·Se + (1–P)·Sp характеризует точность диагностического препарата, т. е. насколько правильно микротест-система выявляет наличие или отсутствие возбудителя при распространенности заболевания P.
Нами предложено ранее не применявшееся понятие доли всех положительных результатов тестов W (отношение общего числа положительных тестов к общему числу всех тестов). Se, Sp и W связаны между собой формулой: W = P×Se + (1–P)×(1–Sp). Исходя из этого: Se = (W – (1–P)×(1–Sp)) / P и, соответственно, U (P) = W – (1–P)·(1–2Sp). На основе данных, полученных при проведении государственных испытаний и представленных в табл. 11, строили графики зависимости U от P: U = U(P).
Таблица 11
Результаты выявления Ureaplasma spp. в образцах клинического материала с использованием микротест-системы «Уреаплазма микротест» и контрольных сред (ГУ НИИЭМ им. и bioMerieux) и в ПЦР
Питательная среда | Результаты посева | Результаты ПЦР | |
положительный результат | отрицательный результат | ||
«Уреаплазма микротест» (1) | Рост Ureaplasma spp. | 141 | 2 |
Отсутствие роста Ureaplasma spp. | 2 | 60 | |
ГУ НИИЭМ (2) | Рост Ureaplasma spp. | 141 | 2 |
Отсутствие роста Ureaplasma spp. | 2 | 60 | |
bioMerieux (3) | Рост Ureaplasma spp. | 143 | 0 |
Отсутствие роста Ureaplasma spp. | 0 | 62 |
 |
Из графиков U=U(P), показанных на рис. 10, видно, что микротест-система «Уреаплазма Микротест», имеет диагностическую эффективность такую же как питательная среда ГУ НИИЭМ им. и соизмеримую с диагностической эффективностью среды bioMerieux.
Рис. 10. Диагностическая эффективность U микротест-системы «Уреаплазма микротест» (1), питательных сред для выявления Ureaplasma spp. ГУ НИИЭМ им. (2) и bioMerieux (3) в зависимости от распространенности заболевания P.
Таким образом, разработанная микротест-система для выявления и идентификации Ureaplasma spp. «Уреаплазма Микротест», обеспечивающая стандартизацию микробиологического метода диагностики уреаплазменной инфекции, обладает высокой диагностической эффективностью.
ВЫВОДЫ
1. Разработаны питательная среда для культивирования бактерий рода Ureaplasma, обладающая высокими ростовыми и селективными свойствами, и транспортная среда, обеспечивающая оптимальные условия для сохранения жизнеспособности уреаплазм. Использование сред позволяет эффективно выявлять Ureaplasma spp. в образцах клинического материала.
2. Показано, что примененные для Ureaplasma spp. методы определения наиболее вероятного количества бактерий и полимеразной цепной реакции в режиме реального времени могут быть использованы для определения концентрации уреаплазм в исследуемом материале.
3. Показано, что изменение оптической плотности среды в процессе роста бактерий рода Ureaplasma в стандартных условиях культивирования на разработанной питательной среде отражает накопление жизнеспособных клеток уреаплазм в поздней экспоненциальной фазе роста культур.
4. Разработан метод оценки ростовых свойств питательной среды для культивирования и выявления Ureaplasma spp. на основе анализа кривых изменения оптической плотности среды в процессе роста тест-штамма в стандартных условиях культивирования в средах сравнения и испытуемой. Метод позволяет дифференцировать ростовые свойства разных серий указанной среды, а также отдельных ее компонентов.
5. Предложен микрометод определения чувствительности штаммов Ureaplasma spp. к антибактериальным препаратам, являющийся модификацией метода серийных разведений в жидкой питательной среде, с использованием пограничных концентраций.
6. Разработана микротест-система для выявления и идентификации Ureaplasma urealyticum (Ureaplasma spp.) «Уреаплазма микротест», обеспечивающая стандартизацию выявления, оценки количества и определения чувствительности бактерий рода Ureaplasma к антибактериальным препаратам.
7. Разработана методика оценки качества микротест-системы «Уреаплазма микротест» в клинико-эпидемиологических испытаниях, позволяющая определить диагностическую эффективность препарата, предназначенного для выявления и идентификации условно-патогенных бактерий.
СПИСОК НАУЧНЫХ РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. , , Говорун значение определения биоваров Ureaplasma urealyticum с использованием ПЦР-диагностики. «Полимеразная цепная реакция в диагностике и контроле лечения инфекционных заболеваний» Сборник трудов под редакцией академика РАМН . Москва, 1998. С. 31-34.
2. , , «Метод оценки питательных сред для диагностики уреаплазмоза». Материалы Международной конференции «Ликвидация и элиминация инфекционных болезней – прогресс и проблемы». Санкт-Петербург, 2003, с. 50.
3. , Безруков среда для выявления Ureaplasma urealyticum и способ диагностики урогенитальных уреаплазмозов. Патент РФ 2265656 С1, 2004.
4. , Шобухова микротест-системы для выявления и идентификации Mycoplasma hominis и Ureaplasma urealyticum. Материалы Всероссийской научно-практической конференции «Медицинская микробиология - XXI век». Саратов, 2004, с. 32-33.
5. , Шобухов Ureaplasma urealyticum в жидкой питательной среде методом наиболее вероятного количества. Материалы научной конференции, посвященной 75-летию Нижегородского НИИЭМ «Новые технологии в профилактике, диагностике, эпиднадзоре и лечении инфекционных заболеваний». Нижний Новгород, 2004, с. 255-258.
6. , , Об условиях применимости метода наиболее вероятного количества для определения концентрации бактерий Ureaplasma urealyticum в жидкой питательной среде. Тезисы 1-й Всероссийской конференции по вакцинологии «Медицинские иммунобиологические препараты для профилактики, диагностики и лечения актуальных инфекций». Москва, 2004, с. 9-10.
7. , , Шобухова методов определения Ureaplasma urealyticum. Тезисы международной конференции «Развитие международного сотрудничества в области изучения инфекционных заболеваний». Новосибирск, 2004, с. 225.
8. , «Уреаплазма микротест» и «Микоплазма микротест» - новые микротест-системы для диагностики урогенитальных микоплазмозов. Сборник трудов 5-й Всероссийской научно-практической конференции «Генодиагностика инфекционных болезней» под редакцией академика РАМН , М., 2004, т.1, с. 10-12.
9. , , Парашина оценка диагностических препаратов с учетом прогностической ценности. Журнал микробиологии, эпидемиологии и иммунобиологии. 2004, № 6, с. 53-55.
10. , , Жуховицкий диагностической ценности ПЦР-тест-систем по результатам государственных испытаний. Журнал микробиологии, эпидемиологии и иммунобиологии. 2005, № 2, с. 69-73.
11. , О применении жидкой селективной питательной среды для количественного определения U. urealyticum. Клиническая лабораторная диагностика. 2005, № 9, с. 31.
12. , Безруков диагностической ценности различных сред для выделения из клинического материала U. urealyticum и M. hominis. Клиническая лабораторная диагностика. 2005, № 9, с. 32-33.
13. , , Г, , К вопросу о программе проведения государственных испытаний диагностических медицинских иммунобиологических препаратов при регистрации их в Российской Федерации. Биопрепараты. 2006, № 1 (21), с. 23-27.
14. , , Быков стандарта цветности для определения концентрации уреаплазменных культур в жидкой питательной среде. Материалы научной конференции, посвященной 85-летию со дня рождения академика РАМН «Новые технологии в профилактике, диагностике, эпиднадзоре и лечении инфекционных заболеваний». Нижний Новгород, 2006, с. 145-147.
15. , , Шобухов количественной оценки концентрации уреаплазменных культур в жидкой питательной среде. Технологии живых систем. 2006, т. 3, № 2, с. 28-37.
СПИСОК СОКРАЩЕНИЙ
АБП – антибактериальный препарат
МИБП – медицинский иммунобиологический препарат
МИК – минимальная ингибирующая концентрация
МИК50 – минимальная ингибирующая концентрация, подавляющая рост не менее 50% исследованных штаммов
МИК90 – минимальная ингибирующая концентрация, подавляющая рост не менее 90% исследованных штаммов
НВК – наиболее вероятное количество
ОП – оптическая плотность
ПЦР – полимеразная цепная реакция
ПЦР-РВ – полимеразная цепная реакция в режиме реального времени
ФСП – фармакопейная статья предприятия
ЦОЕ – цветообразующая единица

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



