б). Изобразите графически температурную зависимость мольной изобарной теплоемкости муравьиной кислоты в интервале от 0 до 90 °C, привлекая для этого [4].
2 Водно-этаноловый раствор с массовой долей этанола 0,65 содержит 25,25 моль воды. Плотность массы этанола в растворе равна 374,1 кг/м3. Найти общее число молей, массу и объем раствора, его мольную массу и удельное число молей, удельный и мольный объемы, плотности массы и общего числа молей, массы компонентов, их мольные и массовые доли, плотности чисел молей, плотности массы воды и число молей этанола.
3. Определить графически парциальный мольный объем воды и рассчитать парциальный мольный объем сульфата калия в водном растворе с мольной долей его, равной 0,0085 , по следующим данным:
![]() 0,01 0,04 0,06 0,08 0,10
0,01 0,04 0,06 0,08 0,10
![]() , кг/м3 164 1081
, кг/м3 164 1081
4. Найти изменение энтропии при смешении 750 см3 азота с 500 см3 водорода под давлением 800 мм рт ст. при температуре 273 К. Оба газа считать идеальными.
5. Вычислить состав равновесной смеси, образующейся в результате протекания в газовой фазе при 900 К и 1 атм следующей реакции 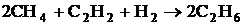 Исходные вещества взяты в стехиометрических количествах,
Исходные вещества взяты в стехиометрических количествах, ![]() = 1,398 , газы считать идеальными.
= 1,398 , газы считать идеальными.
6. Определить давление насыщенного пара четыреххлористого углерода при
60 °C, если ССl4 кипит при 75 °C и 1,013 ×10 5 Па и мольная теплота парообразования равна 30833 Дж/моль.
7.Температура кристаллизации водного раствора серной кислоты при значении ее массовой доли равной 0,091 составляет 283,7 К. Рассчитать коэффициент активности воды в этом растворе, если ее мольная теплота плавления чистой воды равна 6020 Дж/моль
Рейтинговое домашнее задание
1. В таблице приведена зависимость плотности массы r двухкомпонентного жидкого раствора вода (1 компонент) – ацетон (2 компонент) от массовой доли j 2 второго компонента ( Т= 298 К, р = 1 атм)
j 2 | 0 | 0,2 | 0,4 | 0,6 | 0,7 | 0,8 | 1,0 |
r, кг/м3 | 997,0 | 969,0 | 937,0 | 893,0 | 869,0 | 843,0 | 786,0 |
Постройте график зависимости объема раствора ![]() от числа молей
от числа молей ![]() компонента 2 при постоянной массе воды 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v 1 и v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,25; вычислите при той же N2 парциальные мольные объемы смешения Δ v 1m и Δ v 2 m
компонента 2 при постоянной массе воды 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v 1 и v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,25; вычислите при той же N2 парциальные мольные объемы смешения Δ v 1m и Δ v 2 m
2. Жидкая вода массой 0,18 кг имела в начальном состоянии ( 1 атм) при температуре 303 К мольный объем 1,807 ×10–5 м3/моль. При постоянном давлении 1 атм ее перевели в конечное состояние с температурой 363 К. Полагая, что коэффициент изобарной расширяемости ( 0,262 × 10–3) и мольная изобарная теплоемкость в данном интервале температур постоянны, вычислите мольные и полные изменения объема, энтропии и энтальпии при переходе из начального состояния в конечное.
3. При температуре 723К рассчитать значения стандартной мольной энтальпии, стандартной мольной энтропии, стандартной мольной энергии Гиббса реакции 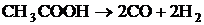 . Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
. Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
4. Найти равновесный состав системы, в которой при 600 К и давлении 1 атм протекает процесс ароматизации н-октана, согласно следующим реакциям:
1. 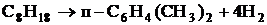
![]() = 97,2
= 97,2
2. 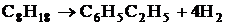
![]() = 25,3
= 25,3
Известно, что исходное вещество взято в количестве 1 моль, продуктов реакции в начальный момент времени нет.
5. Для чистого аммиака известны температурные зависимости давления насыщенного пара при равновесии
жидкость-пар | p, Па 740 Т, К 198,9 208,3 216,2 222,2 232,6 |
Кристаллы-пар | p, Па 181,3 33 Т, К 166,7 ,4 194 |
В тройной точке плотности массы чистого аммиака в кристаллическом и жидком агрегатном состоянии равны соответственно 827 и 817 кг/м3 . Определите графически координаты тройной точки и величины мольных теплот испарения и возгонки; определите мольную теплоту плавления, мольную энтропию плавления и мольную энергию Гиббса плавления; найдите температуру плавления вещества при давлении 230500 Па.
6. Гетерогенная система (жидкость-пар) содержит два компонента – этанол и воду и равновесна при 343 К и 0,65 атм. Масса воды в жидкой фазе 2,5 кг, масса воды в паровой фазе 1,61 кг. Мольная доля воды в жидкой фазе 0,612, мольная доля воды в паровой фазе 0,386. Найти массу системы.
Вариант 22
Обязательное домашнее задание
1. а) Определить энергию активации вязкого течения бромбензола.
б). Изобразите графически температурную зависимость мольной изобарной теплоемкости циклопентана в интервале от 0 до 110 °C, привлекая [4].
2 . Раствор, полученный смешением воды и уксусной кислоты, имеет массу 0,675 кг и мольный объем 2,917×10-5 м3/моль. Массовая доля кислоты в нем равна 0,65 единиц. Рассчитать общее число молей и объем раствора, его мольный и удельный объемы, мольную массу и удельное число молей, плотности массы и общего числа молей, массы и числа молей компонентов, их плотности масс и чисел молей, мольные доли и массовую долю воды.
3. Определить графически парциальный мольный объем воды и рассчитать парциальный мольный объем сульфата лития в водном растворе с мольной долей его, равной 0,0085 , по следующим данным:
![]() 0,01 0,04 0,06 0,08 0,10
0,01 0,04 0,06 0,08 0,10
v ![]() ×104, м3/кг 9,93 9,68 9,52 9,36 9,21
×104, м3/кг 9,93 9,68 9,52 9,36 9,21
4. Найти изменение энтропии при смешении 500 см3 азота с 750 см3 кислорода под давлением 800 мм рт ст. при температуре 273 К. Оба газа считать идеальными.
5. Вычислить состав равновесной смеси, образующейся в результате протекания в газовой фазе при 600 К и 1 атм следующей реакции
![]() .Исходные вещества взяты в стехиометрических количествах,
.Исходные вещества взяты в стехиометрических количествах, ![]() =1,27 , газы подчиняются законам идеальных газов.
=1,27 , газы подчиняются законам идеальных газов.
6. Давление пара этилового эфира при 20 °C равно 0,577×10 5 Па, а при 30 °C 0,846 ×10 5 Па. Определить мольную теплоту испарения эфира.
7. При 298 К давление насыщенного пара над чистой водой равно 23,76 мм рт. ст. Рассчитать (выразить в Па) давление насыщенного пара при той же температуре над раствором 13 г глюкозы в 120 г воды, считая раствор идеальным.
Рейтинговое домашнее задание
1. Для двухкомпонентного жидкого раствора вода (1компонент) - ацетон
(2 компонент) имеется в табличной форме опытная зависимость мольного объема v от мольной доли 2-го компонента N2 (Т = 298 К, р = 1 атм):
N2 | 0,00 | 0,17 | 0,27 | 0,36 | 0,46 | 0,69 | 1,00 |
v ×105, м3/моль | 1,807 | 2,654 | 3,00 | 3,44 | 4,01 | 4,77 | 7,39 |
Постройте график зависимости мольного объема смешения раствора D v m от N2 и определите для обоих компонентов парциальные мольные объемы смешения D v 1m и D v 2 m при N2 = 0,5; вычислите для тех же компонентов при той же N2 парциальные мольные объемы v 1 и v 2.
2. Жидкая вода массой 5,7 кг имела в начальном состоянии ( 1 атм) при температуре 303 К плотность массы 996 кг/ м3. При постоянном давлении 1 атм ее перевели в конечное состояние с температурой 343 К. Полагая, что коэффициент изобарной расширяемости ( 0,262 × 10–3) и мольная изобарная теплоемкость в данном интервале температур постоянны, вычислите мольные и полные изменения объема, энтропии и энтальпии при переходе из начального состояния в конечное.
3. При температуре 495 К рассчитать значения стандартной мольной энтальпии, стандартной мольной энтропии, стандартной мольной энергии Гиббса реакции 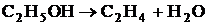 . Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
. Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
4. Найти равновесный состав системы, в которой при 600 К и давлении 1 атм протекает процесс ароматизации н-октана, согласно следующим реакциям:
1. 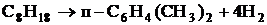
![]() = 97,2
= 97,2
2. 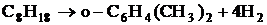
![]() = 104
= 104
Известно, что исходное вещество взято в количестве 1 моль, продуктов реакции в начальный момент времени нет.
5. На основании приведенных данных о составах жидкой и паровой фаз при различных температурах постройте диаграмму фазового состояния системы бензол ( 1 компонент) - метанол ( 2 компонент)
Т, К | 404 | 398 | 392 | 390 | 389 | 388 | 389 | 391 |
| 0 | 0,08 | 0,20 | 0,34 | 0,45 | 0,67 | 0,85 | 1 |
| 0 | 0,23 | 0,41 | 0,50 | 0,57 | 0,67 | 0,77 | 1 |
Обозначьте все поля, линии и характерные точки на этой диаграмме и укажите, сколько компонентов и фаз, находится в равновесии и чему равно число степеней свободы в каждой из указанных позиций. Ответьте, есть ли отклонения от закона Рауля и, если есть, то какие. Определите, какой компонент и в каком количестве нужно при 394 К добавить в систему (N2 = 0,2; масса системы 1 кг) , чтобы перевести ее в пар
6. Равновесная гетерогенная ( жидкость-пар) двухкомпонентная ( пиридин – метанол) система при 318 К и 0,2 атм имеет следующий состав: мольная доля метанола в жидкой фазе 0,34, мольная доля метанола в системе 0,50. Масса жидкой фазы 2,0 кг, масса паровой фазы 0,82 кг. Найти мольную долю метанола в паровой фазе.
Вариант 23
Обязательное домашнее задание
1. а) Определить энергию активации вязкого течения воды.
б). Изобразите графически температурную зависимость мольной изобарной теплоемкости пентана в интервале от 0 до 120 °C, привлекая для этого [4].
2. Водно-аммиачный раствор, где мольная доля и плотность числа молей аммиака равны соответственно 0,215 единиц и 11280 моль/м3 (298 К, 1 атм), обладает массой 0,825 кг. Определить общее число молей и объем раствора, его мольную массу и удельное число молей, мольный и удельный объемы, плотности общего числа молей и массы, числа молей и массы компонентов, их плотности масс, массовые доли, плотность числа молей и мольную долю воды.
3.Определить графически парциальный мольный объем воды и рассчитать парциальный мольный объем сульфата меди в водном растворе с мольной долей его, равной 0,0085 , по следующим данным:
![]() 0,01 0,04 0,06 0,08 0,10
0,01 0,04 0,06 0,08 0,10
![]() , кг/м3 184 1107
, кг/м3 184 1107
4. Вычислить изменение энтропии нагревания до 373 К одного моля ксенона (газ считать идеальным), занимающего при 15 оС объем 23,64 л, если конечный объем 26,51 л.
5. Вычислить состав равновесной смеси, образующейся в результате протекания в газовой фазе при 400 К и 1,0 атм следующей реакции
![]() . Исходные вещества взяты в стехиометрических количествах,
. Исходные вещества взяты в стехиометрических количествах, ![]() = - 0,578 , газы идеальны.
= - 0,578 , газы идеальны.
6. Определить нормальную температуру кипения этилового эфира, если давление его паров при 30 °C равно 0,846 ×10 5 Па, а мольная теплота испарения 28367,52 кДж/кмоль.
7. .При 298 К давление насыщенного пара над чистой водой равно 23,76 мм рт. ст. Рассчитать (выразить в Па) давление насыщенного пара при той же температуре над раствором 9 г тиомочевины в 180 г воды, считая раствор идеальным.
Рейтинговое домашнее задание
1. В таблице приведена зависимость плотности массы r двухкомпонентного жидкого раствора сероуглерод (1 компонент) – ацетон (2 компонент) от массовой доли j 2 второго компонента ( Т= 298 К, р = 1 атм)
j 2 | 0,00 | 0,13 | 0,29 | 0,35 | 0,48 | 0,60 | 0,87 | 1,0 |
r, кг/м3 | 1257 | 1153 | 1058 | 1024 | 962,1 | 914,9 | 824 | 788 |
Постройте график зависимости объема раствора ![]() от числа молей
от числа молей ![]() компонента 2 при постоянной массе сероуглерода 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v 1 и v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,6; вычислите при той же N2 парциальные мольные объемы смешения Δ v 1m и Δ v 2 m
компонента 2 при постоянной массе сероуглерода 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v 1 и v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,6; вычислите при той же N2 парциальные мольные объемы смешения Δ v 1m и Δ v 2 m
2.Жидкий бензол массой 1,2 кг имел в начальном состоянии ( 1 атм) при температуре 293 К плотность массы 879 кг/м3. При постоянном давлении 1 атм его перевели в конечное состояние с температурой 330 К. Полагая, что коэффициент изобарной расширяемости ( 1,21 × 10–3) и мольная изобарная теплоемкость в данном интервале температур постоянны, вычислите мольные и полные изменения объема, энтропии и энтальпии при переходе из начального состояния в конечное.
3. При температуре 433 К рассчитать значения стандартной мольной энтальпии, стандартной мольной энтропии, стандартной мольной энергии Гиббса реакции 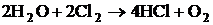 . Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
. Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
4. Рассчитать равновесный состав системы, в которой при 900 К и 1 атм протекает процесс изомеризации этилбензола по следующим реакциям:
1. 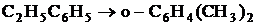
![]() =3,14
=3,14
2. 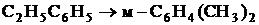
![]() = 3,65
= 3,65
Начальное количество этилбензола 1 моль, продуктов реакции в начальный момент нет.
5. Для чистого аммиака известны температурные зависимости давления насыщенного пара при равновесии
жидкость-пар | p, Па 753 Т, К 198,9 208,3 216,2 227,8 239,6 |
Кристаллы-пар | p, Па ,4 1 Т, К 164,1 172,4 181,3 192,3 194 |
В тройной точке плотности массы чистого аммиака в кристаллическом и жидком агрегатном состоянии равны соответственно 827 и 817 кг/м3 . Определите графически координаты тройной точки и величины мольных теплот испарения и возгонки; определите мольную теплоту плавления, мольную энтропию плавления и мольную энергию Гиббса плавления; найдите температуру плавления вещества при давлении 130500 Па.
6. Равновесная гетерогенная ( жидкость-пар) двухкомпонентная ( ацетон-сероуглерод) система при 322К и 1 атм имеет следующий состав: мольная доля сероуглерода в жидкой фазе 0,10, мольная доля сероуглерода в системе 0,20. Масса жидкой фазы 2,0 кг, масса паровой фазы 1,6 кг. Найти мольную долю сероуглерода в паровой фазе.
Вариант 24
Обязательное домашнее задание
1. а) Определить энергию активации вязкого течения октана.
б). Изобразите графически температурную зависимость мольной изобарной теплоемкости перекиси водорода в интервале от 0 до 210 °C, привлекая [4].
2. Массовая доля и плотность числа молей глицерина в водноглицериновом растворе с общим числом молей 45,680 равны соответственно 0,110 единиц и
7520 моль/м3. Рассчитать массу и объем раствора, его мольный и удельный объемы, мольную массу и удельное число молей, плотности массы и общего числа молей, массы и числа молей компонентов, их плотности масс, мольные доли, плотности числа молей и массовую долю воды.
3. Определить графически парциальный мольный объем воды и рассчитать парциальный мольный объем хлорида натрия в водном растворе с мольной долей его, равной 0,0085 , по следующим данным:
![]() 0,01 0,04 0,06 0,08 0,10
0,01 0,04 0,06 0,08 0,10
![]() , кг/м3 156 1071
, кг/м3 156 1071
4. Вычислить изменение энтропии нагревания до 423 К одного моля неона (газ считать идеальным), занимающего при 15 оС объем 23,64 л, если конечный объем 26,51 л.
5. Вычислить состав равновесной смеси, образующейся в результате протекания в газовой фазе при 400 К и 1атм следующей реакции ![]() . Исходные вещества взяты в стехиометрических количествах,
. Исходные вещества взяты в стехиометрических количествах, ![]() = 2,617 , газы подчиняются законам идеальных газов.
= 2,617 , газы подчиняются законам идеальных газов.
6. Давление пара хлороформа при 20 °C равно 0,215 ×10 5 Па, а при 30 °C равно 0,331 ×10 5 Па. Определить мольную теплоту испарения хлороформа.
7. При давлении 1,013 × 10 5 Па определить температуру кипения раствора нелетучего вещества с мольной долей N2 = 0,01 в ацетоне.
Рейтинговое домашнее задание
1. В таблице приведена зависимость плотности массы r двухкомпонентного жидкого раствора вода H2O (1 компонент) – этанол С2Н6О (2 компонент) от массовой доли j 2 второго компонента ( Т= 298 К, р = 1 атм)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



