Федеральное агентство по образованию
ГОУ ВПО «Уральский государственный технический университет -УПИ»
ФИЗИЧЕСКАЯ ХИМИЯ
Сборник задач домашних заданий по 1 части курса
для направления 240400 – Технология органических веществ и топлив
специальностей: 240401 – химическая технология органических веществ
и для направления 240900 – Биотехнология
специальности 240901– биотехнология
Екатеринбург 2007
УДК 544(076)С79
Составитель:
Научный редактор доц., к. х.н.
Физическая химия. Сборник задач домашних заданий по 1 части курса / - Екатеринбург: ГОУ ВПО УГТУ-УПИ, 20с
В данном пособии приведено 30 вариантов домашних заданий для студентов химико-технологического факультета и факультета строительного материаловедения по курсу: «Физическая химия» (1 часть). В каждом варианте имеется 13 задач, которые составляют 4 домашних задания по физической химии: (№ 1 – первый и второй законы термодинамики; № 2 – свойства растворов; № 3 – химическое равновесие; № 4 – гетерогенное равновесие). Точное указание, к какому именно домашнему заданию относится каждая задача приведено в начале сборника. Кроме того, все задачи разделены по уровню сложности на два больших класса: первый – обязательный для решения, второй – желательный, содержащий более сложные задачи. Соответственно этому делению полное домашнее задание разделено на ОДЗ (обязательное домашнее задание) и РДЗ (рейтинговое домашнее задание). Указаны требования к оформлению домашнего задания, ссылки на использованную литературу.
Библиогр.: 9 назв.
Подготовлено кафедрой «Физическая и коллоидная химия»
© Уральский государственный
технический университет –УПИ, 2007
Пояснения к домашним заданиям
Соответствие задач типу домашнего задания приведено ниже.
ДЗ № 1 | ДЗ № 2 | ДЗ № 3 | ДЗ № 4 | |||||
ОДЗ | РДЗ | ОДЗ | РДЗ | ОДЗ | ОДЗ | |||
Номера задач | 1; 4 | 2; 3 | 2; 3 | 1 | 5 | 4 | 6; 7 | 5; 6 |
Сборник задач предназначен для самостоятельной работы студентов по усвоению материала курса физической химии. Начинать работу нужно с решения задач обязательного домашнего задания (ОДЗ). Решение обязательного домашнего задания вместе с отчетами по прохождению лабораторных работ является допуском до экзамена по физической химии. При оформлении решений задач ОДЗ учтите, что задачи можно сдавать по мере решения каждой задачи, а не все задачи единовременно, поэтому оформлять их лучше на отдельных листах из тетради, а не в целой тетради. Вместо условия задач можно приложить ксерокопию варианта домашнего задания. Краткое условие задачи обязательно. Расчет производится в СИ.
Для углубленного изучения курса нужно решить рейтинговое домашнее задание (РДЗ). В этом виде домашнего задания сгруппированы более сложные задачи, требующие пояснений при решении, графических отображений зависимостей, анализа полученных результатов.
Требования к оформлению этого вида задания (РДЗ).
1. Рейтинговое домашнее задание сдается на проверку целиком.
2. Запись решения задач осуществляется на листах бумаги формата А4, с одной стороны листа. Листы не сшиваются, и без всяких скрепок сдаются преподавателю на проверку в файл-папке.
3. Титульного листа не делается, однако на каждом листе сверху (2 см) проводится горизонтальная черта, над которой указывается необходимая информация: Например, гр. Х-359, РДЗ - 4, задача 3, лист 2.
(РДЗ-4 – означает 4 вариант рейтингового домашнего задания, лист 2 - обозначает номер листа, соответствующего решению 3 задачи, а не общее количество листов).
4. Допускается полное условие задачи приводить в виде ксерокопии домашнего задания Вашего варианта. Краткое условие задачи обязательно.
5. В начале решения нужно привести необходимые уравнения и формулы с пояснениями обозначений величин и смысла формул. Уравнения нужно пронумеровать. Уместны словесные связки между формулами, чтобы была понятна логика решения задачи. Искомые величины нужно найти в общем виде в буквенных обозначениях. При подстановке данных обязательно получение необходимых размерностей. Во все расчетные формулы должны входить только те величины, которые заданы в условии.
6. Рисунки выполняются с использованием чертежных принадлежностей на миллиметровой бумаге. На плоскости рисунка допускается лишь цифровое или буквенное обозначение линий (если их больше одной) и необходимые для решения задачи графические построения. Названия рисунков и расшифровка обозначений приводятся внизу. Нумерация уравнений, таблиц и рисунков относится непосредственно к решаемой задаче.
Решение рейтингового домашнего задания является необходимым условием получения студентом экзаменационной оценки досрочно, до сессии.
Вариант 1
Обязательное домашнее задание.
1. а) Определить энергию активации вязкого течения бензола.
б). Изобразите графически температурную зависимость мольной изобарной теплоемкости ацетона в интервале от 0 до 120 °C, привлекая для этого [4].
2. Раствор, полученный смешением аммиака с водой, имеет массу 1,258 кг. Его мольный объем и плотность числа молей аммиака в нем равны соответственно 1,983×10-5 м3/моль и 16100 моль/м3 . Определить общее число молей и объем раствора, его мольную массу и удельное число молей, плотности массы и плотность общего числа молей, удельный объем, числа молей и массы компонентов, их мольные и массовые доли, плотности масс, а также плотность числа молей воды в растворе.
3. Определить графически парциальный мольный объем воды и рассчитать
парциальный мольный объем сульфата меди в водном растворе с мольной долей его, равной 0,0085 , по следующим данным:
![]() 0,01 0,04 0,06 0,08 0,10
0,01 0,04 0,06 0,08 0,10
vуд×104, м3/кг 9,91 9,62 9,42 9,23 9,03
4. Рассчитать мольную энтропию оксида углерода при 473 К и 50 атм. Необходимые для расчета данные взять из справочника [4].
5. Вычислить состав равновесной смеси, образующейся в результате протекания в газовой фазе при 600 К и 1 атм следующей реакции ![]() . Исходные вещества взяты в стехиометрических количествах,
. Исходные вещества взяты в стехиометрических количествах, ![]() =1,27 , газы близки к идеальным.
=1,27 , газы близки к идеальным.
6. Удельная теплота испарения амилового спирта С5Н11ОН при температуре кипения 138 °C и давлении 1,013 ×10 5 Па равна 592 кДж/кг. Определить давление при 140 °C.
7. При 298 К давление насыщенного пара над чистой водой равно 23,76 мм рт. ст. Рассчитать ( выразить в Па) давление насыщенного пара при той же температуре над раствором 6 г мочевины в 180 г воды, считая раствор идеальным.
Рейтинговое домашнее задание.
1. В таблице приведена зависимость плотности массы r двухкомпонентного жидкого раствора вода H2O (1 компонент) – этанол С2Н6О (2 компонент) от массовой доли j 2 второго компонента ( Т= 298 К, р = 1 атм)
j 2 | 0,00 | 0,20 | 0,40 | 0,60 | 0,80 | 1,00 |
r, кг/м3 | 997,1 | 966,4 | 931,5 | 887,0 | 839,1 | 785,1 |
Постройте график зависимости объема раствора ![]() от числа молей
от числа молей ![]() компонента 2 при постоянной массе воды 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v1 и v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,280; вычислите для тех же компонентов 1 и 2 при той же N2 парциальные мольные объемы смешения Δ v 1m и Δ v 2 m.
компонента 2 при постоянной массе воды 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v1 и v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,280; вычислите для тех же компонентов 1 и 2 при той же N2 парциальные мольные объемы смешения Δ v 1m и Δ v 2 m.
2. Жидкая вода массой 0,18 кг имела ( 1 атм) при температуре 303 К мольный объем 1,807 ×10–5 м3/моль. При постоянном давлении 1 атм ее перевели в конечное состояние с температурой 363 К. Полагая, что коэффициент изобарной расширяемости ( 0,262 × 10–3) и мольная изобарная теплоемкость в данном интервале температур постоянны, вычислите мольные и полные изменения объема, энтропии и энтальпии при переходе в конечное состояние.
3. При температуре 687 К рассчитать значения стандартной мольной энтальпии, стандартной мольной энтропии, стандартной мольной энергии Гиббса реакции 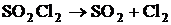 . Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
. Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
4. При 600 К и давлении 1 атм возможно одновременное протекание следующих реакций:
1. ![]()
![]() = 0,00154
= 0,00154
2. ![]()
![]() = 10,6
= 10,6
Найти состав равновесной смеси, если начальные количества исходных веществ равны стехиометрическим, а продуктов реакции вначале нет.
5. Для чистой воды известны температурные зависимости давления насыщенного пара при равновесии
жидкость-пар
| p, Па 871,2 1704,1 3166,3 5621,7 8955 Т, К 278,2 288,2 298,2 308,2 317,5 |
Кристаллы-пар | p, Па 40,5 73,7 ,9 Т, К 273,2 |
В тройной точке плотности массы чистой воды в кристаллическом и жидком агрегатном состоянии равны соответственно 918 и 1000 кг/ м3. Определите графически координаты тройной точки и величины мольных теплот испарения и возгонки; определите мольную теплоту плавления, мольную энтропию плавления и мольную энергию Гиббса плавления; найдите температуру плавления вещества при давлении 88100 Па.
6. При 318 К парожидкостное равновесие в двухкомпонентной системе : вода-перекись водорода, где паровая фаза близка к идеальному газовому раствору, характеризуются следующими данными:
р, Па | 9384 | 3066 | 1040 |
массовая доля перекиси водорода в паровой фазе | 0 | 0,28 | 1,0 |
массовая доля перекиси водорода в жидкой фазе | 0 | 0,74 | 1,0 |
Найти коэффициент активности перекиси водорода для жидкой фазы с массовой долей перекиси водорода в ней 0,74.
Вариант 2
Обязательное домашнее задание
1. а) Определить энергию активации вязкого течения ацетона.
б) изобразите графически температурную зависимость мольной изобар-
ной теплоемкости этанола в интервале от 0 до 120 °C, привлекая для этого [4].
2. Общее число молей в растворе, состоящем из воды и серной кислоты, равно 28,32 моль. Плотность массы раствора и плотность массы серной кислоты в нем составляют соответственно 1730 кг/ м3 и 1389 кг/ м3 . Вычислить массу и объем раствора, его мольную массу и удельное число молей, плотность общего числа молей, мольный и удельный объемы, массы и числа молей того и другого компонентов, их массовые и мольные доли, плотности чисел молей и плотности массы воды в растворе.
3. а). Плотность массы раствора вода-метанол при 293 К и 105 Па составляет
989,6 кг/м3 при массовой доле метанола 0,6. Парциальный мольный объем спирта в растворе равен 3,937 ×10-5 м3 /моль. Рассчитать парциальный мольный объем воды.
б) Плотность массы раствора вода-этанол (с массовой долей этанола 0,4), плотности масс воды и этанола в чистом виде равны соответственно: 935,5; 997,1; 785,1 (кг/ м3). Рассчитать мольное изменение объема при смешении.
4. Рассчитать мольное изменение энтропии бензола при его нагреве от 298 до 373К. Необходимые для расчета данные взять из справочника [4].
5. Вычислить состав равновесной смеси, образующейся в результате протекания в газовой фазе при 799 К и 10 атм следующей реакции ![]() . Исходные вещества взяты в стехиометрических количествах,
. Исходные вещества взяты в стехиометрических количествах, ![]() = - 4,613, газы близки к идеальным.
= - 4,613, газы близки к идеальным.
6. Под каким давлением будет кипеть диэтиламин при 20 °C, если нормальная температура кипения его 58 °C, а теплота парообразования 27,844 кДж/моль?
7. При давлении 1,013 × 10 5 Па определить температуру кипения раствора нелетучего вещества с мольной долей N2 = 0,01 в бензоле
Рейтинговое домашнее задание.
1. В таблице приведена зависимость изобарной теплоемкости двухкомпонентного жидкого раствора вода (1 компонент) - ацетон (2 компонент) от массы кислоты m2 при постоянной массе воды m1=0,5 кг
m2, кг | 0,000 | 0,125 | 0,333 | 0,750 | 2,00 |
Сp, Дж/К | 2090 | 2551 | 3227 | 4394 | 7430 |
(Т = 298 К, р = 1 атм):
Постройте график зависимости изобарной теплоемкости смешения раствора DС рm от числа молей ацетона n2 , имея в виду, что удельные изобарные теплоемкости чистых компонентов 1 и 2 равны 4180 и 2153 Дж/К×кг; Определите для обоих компонентов их парциальные мольные изобарные теплоемкости смешения D ![]() m и D
m и D![]() m при мольной доле 2-го компонента N2 = 0,3; вычислите для тех же компонентов при той же N2 парциальные мольные изобарные теплоемкости
m при мольной доле 2-го компонента N2 = 0,3; вычислите для тех же компонентов при той же N2 парциальные мольные изобарные теплоемкости ![]() и
и ![]() .
.
2.Жидкий бензол массой 1,17 кг имел в начальном состоянии ( 1 атм) при температуре 283 К мольный объем 8,76 ×10-5 м3/моль. При постоянном давлении 1 атм его перевели в конечное состояние с температурой 335 К. Полагая, что коэффициент изобарной расширяемости ( 1,19 × 10-3) и мольная изобарная теплоемкость в данном интервале температур постоянны, вычислите мольные и полные изменения объема, энтропии и энтальпии при переходе из начального состояния в конечное.
3. При температуре 744 К рассчитать значения стандартной мольной энтальпии, стандартной мольной энтропии, стандартной мольной энергии Гиббса реакции 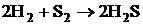 . Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
. Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
4. Определить равновесный состав системы, в которой при температуре 700 К, давлении 5 атм, при стехиометрическом начальном составе и отсутствии продуктов в исходной смеси протекают следующие реакции
1. ![]()
![]() = 0,685
= 0,685
2. ![]()
![]() = 0,239.
= 0,239.
5. Для чистой воды известны температурные зависимости давления насыщенного пара при равновесии
жидкость-пар | p, Па 871,2 3166,3 4 Т, К 278,2 298,2 ,5 323,2 |
Кристаллы-пар | p, Па 22,2 73,7 ,9 Т, К ,7 266,7 273,2 |
В тройной точке плотности массы чистой воды в кристаллическом и жидком агрегатном состоянии равны соответственно 918 и 1000 кг/ м3. Определите графически координаты тройной точки и величины мольных теплот испарения и возгонки; определите мольную теплоту плавления, мольную энтропию плавления и мольную энергию Гиббса плавления; найдите температуру плавления вещества при давлении 90100 Па.
6. Равновесная гетерогенная ( жидкость-пар) двухкомпонентная ( ацетон-сероуглерод) система при 316 К и 1 атм имеет следующий состав: мольная доля сероуглерода в жидкой фазе 0,26, мольная доля сероуглерода в системе 0,40. Масса жидкой фазы 1,0 кг, масса паровой фазы 1,4 кг. Найти мольную долю ацетона в паровой фазе.
Вариант 3
Обязательное домашнее задание
1. а) Определить энергию активации вязкого течения бромбензола.
б). Изобразите графически температурную зависимость мольной изобарной теплоемкости метанола в интервале от 0 до 120 °C, привлекая для этого [4].
2. В растворе вода-хлороводород с общим числом молей 38,45 моль и плотностью массы 1100 кг/ м3 массовая доля хлороводорода составляет 0,210. Найти массу и объем раствора, его мольную массу и удельное число молей, мольный и удельный объемы, плотность общего числа молей, массы и числа молей компонентов, их мольные доли, плотности масс и чисел молей, а также массовую долю воды.
3. Определить графически парциальный мольный объем воды и рассчитать парциальный мольный объем хлорида калия в водном растворе с мольной долей его, равной 0,0085 , по следующим данным:
![]() 0,01 0,04 0,06 0,08 0,1
0,01 0,04 0,06 0,08 0,1
v уд ·104, м3/кг 9,95 9,77 9,64 9,52 9,40
4. Найти изменение энтропии при нагревании 1 моль ацетона от 298 до 373 К. Необходимые для расчета данные взять из справочника [4].
5. Вычислить состав равновесной смеси, образующейся в результате протекания в газовой фазе при 600 К и 2 атм следующей реакции
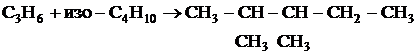
Исходные вещества взяты в стехиометрических количествах, ![]() = 0,014, газы идеальны.
= 0,014, газы идеальны.
6. Температура кипения жидкого метанола при 0,267 ×10 5 Па равна 34,7°C, а при давлении 0,533 ×10 5 Па равна 49,9 °C. Вычислить температуру кипения при нормальном давлении.
7. Температура кристаллизации водного раствора серной кислоты при значении ее массовой доли равной 0,129 составляет 271 К. Рассчитать коэффициент активности воды в этом растворе, если мольная теплота плавления чистой воды равна 6020 Дж/моль.
Рейтинговое домашнее задание.
1. Для двухкомпонентного жидкого раствора ацетон С3Н6О (1компонент) - трихлорметан СНCl3 (2 компонент) имеется в табличной форме опытная зависимость мольного объема v от мольной доли 2-го компонента N2
(Т = 298 К, р = 1 атм):
N2 | 0,000 | 0,255 | 0,424 | 0,617 | 0,870 | 1,000 |
v ×105, м3/моль | 7,400 | 7,982 | 8,359 | 8,790 | 9,379 | 9,690 |
Постройте график зависимости мольного объема смешения раствора D v m от N2 и определите для обоих компонентов парциальные мольные объемы смешения D v 1m и D v 2 m при N2 = 0,500; вычислите для тех же компонентов при той же N2 парциальные мольные объемы v 1 и v 2.
2. Кристаллическая соль KNO3 массой 0,101 кг имела в начальном состоянии ( 1 атм) при температуре 273 К мольный объем 4,78 ×10–5 м3/моль и мольную изобарную теплоемкость 96,29 Дж/(К моль). При постоянном давлении 1 атм ее перевели в конечное состояние с температурой 333 К. Полагая, что коэффициент изобарной расширяемости ( 0,181 × 10–3) и мольная изобарная теплоемкость в данном интервале температур постоянны, вычислите мольные и полные изменения объема, энтропии и энтальпии при переходе из начального состояния в конечное.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



