j 2 | 0,00 | 0,20 | 0,40 | 0,60 | 0,80 | 1,00 |
r, кг/м3 | 997,1 | 966,4 | 931,5 | 887,0 | 839,1 | 785,1 |
Постройте график зависимости объема раствора ![]() от числа молей
от числа молей ![]() компонента 2 при постоянной массе воды 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v 1 и
компонента 2 при постоянной массе воды 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v 1 и
v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,32; вычислите для тех же компонентов 1 и 2 при той же N2 парциальные мольные объемы смешения Δ v 1m и Δ v 2 m.
2.Жидкий бензол массой 1,2 кг имел в начальном состоянии ( 1 атм) при температуре 293 К плотность массы 879 кг/м3. При постоянном давлении 1 атм его перевели в конечное состояние с температурой 330 К. Полагая, что коэффициент изобарной расширяемости ( 1,21 × 10–3) и мольная изобарная теплоемкость в данном интервале температур постоянны, вычислите мольные и полные изменения объема, энтропии и энтальпии при переходе из начального состояния в конечное.
3. При температуре 588 К рассчитать значения стандартной мольной энтальпии, стандартной мольной энтропии, стандартной мольной энергии Гиббса реакции 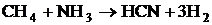 . Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
. Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
4. Рассчитать равновесный состав системы, где при 500 К и 1 атм осуществляется процесс изомеризации 1-бутена по следующим реакциям:
1. 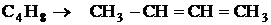 (цис)
(цис) ![]() = 2,05
= 2,05
2. 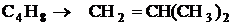
![]() =10,3
=10,3
Известно, что начальное количество бутена равно стехиометрическому, продуктов реакции в начальный момент нет.
5. На основании приведенных данных о составах жидкой и паровой фаз при различных температурах постройте диаграмму фазового состояния системы пропанон ( 1 компонент) -трихлорметан( 2 компонент)
Т, К | 329 | 330 | 333 | 335 | 336 | 337 | 337,6 | 337 | 336 | 334 |
| 0 | 0,1 | 0,20 | 0,35 | 0,43 | 0,53 | 0,67 | 0,73 | 0,85 | 1 |
| 0 | 0,05 | 0,11 | 0,22 | 0,32 | 0,47 | 0,67 | 0,8 | 0,91 | 1 |
Обозначьте все поля, линии и характерные точки на этой диаграмме и укажите, сколько компонентов и фаз, находится в равновесии и чему равно число степеней свободы в каждой из указанных позиций. Ответьте, есть ли отклонения от закона Рауля и, если есть, то какие. Определите, какой компонент и в каком количестве нужно при 334 К добавить в систему (N2 = 0,25; масса системы 5 кг) , чтобы перевести ее в пар.
6. Равновесная гетерогенная ( жидкость-пар) двухкомпонентная ( ацетон-сероуглерод) система при 322К и 1 атм имеет следующий состав: мольная доля сероуглерода в жидкой фазе 0,10, мольная доля сероуглерода в системе 0,20. Масса жидкой фазы 2,0 кг, масса паровой фазы 1,6 кг. Найти массу ацетона в системе.
Вариант 25
Обязательное домашнее задание
1. а) Определить энергию активации вязкого течения толуола.
б). Изобразите графически температурную зависимость мольной изобарной теплоемкости циклогексана в интервале от 0 до 110 °C, привлекая [4].
2. Концентрация метанола в водно-метаноловом растворе составляет 21172 моль/м3. Раствор содержит 13,333 моль воды и имеет массу 1,15 кг. Определить общее число молей и объем раствора, его мольную массу и удельное число молей, мольный и удельный объем, плотности общего числа молей и массы, плотности масс компонентов, их массы, мольные и массовые доли, число молей метанола и плотность числа молей воды.
3. а) Мольный объем раствора вода-пропанол при 293 К и 105 Па составляет 3,503 ×10–5 м3 /моль при массовой доле пропанола 0,6. Парциальный мольный объем спирта в растворе равен 7,501 ×10–5 м3 /моль. Рассчитать парциальный мольный объем воды.
б). Плотность массы раствора вода– метиловый спирт (с массовой долей метанола 0,4), плотности масс воды и метанола в чистом виде равны соответственно: 934,5; 998,2 и 791,7 ( кг/ м3). Рассчитать мольное изменение объема при смешении.
4. Как изменится энтропия при нагревании 1 моль хлорида натрия от 298 до
1194 К. Мольная изобарная теплоемкость жидкого хлорида натрия равна 66,53 Дж/(моль К). Необходимые для расчета данные взять из справочника.
5. Вычислить состав равновесной смеси, образующейся в результате протекания в газовой фазе при 900 К и 0,4 атм следующей реакции 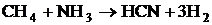 . Исходные вещества взяты в стехиометрических количествах,
. Исходные вещества взяты в стехиометрических количествах, ![]() = -2,361, газы считать идеальными.
= -2,361, газы считать идеальными.
6. Давление пара хлороформа при 40 °C равно 0,492 ×10 5 Па, а при 50 °C
0,713 ×10 5 Па. Вычислить мольную теплоту испарения хлороформа.
7. При давлении 1,013 × 10 5 Па определить температуру кипения раствора нелетучего вещества с мольной долей N2 = 0,01 в хлороформе.
Рейтинговое домашнее задание
1. В таблице приведена зависимость плотности массы r двухкомпонентного жидкого раствора метанол (1 компонент) – ацетон (2 компонент) от массовой доли j 2 второго компонента ( Т= 298 К, р = 1 атм)
j 2 | 0,00 | 0,08 | 0,32 | 0,50 | 0,76 | 0,88 | 1,00 |
r, кг/м3 | 796 | 797,6 | 800,5 | 801,5 | 800,7 | 799,2 | 790,0 |
Постройте график зависимости объема раствора ![]() от числа молей
от числа молей ![]() компонента 2 при постоянной массе метанола 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v 1 и v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,4;
компонента 2 при постоянной массе метанола 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v 1 и v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,4;
вычислите при той же N2 парциальные мольные объемы смешения
Δ v 1m и Δ v 2 m
2. Жидкая вода массой 5,7 кг имела в начальном состоянии ( 1 атм) при температуре 303 К плотность массы 996 кг/ м3. При постоянном давлении 1 атм ее перевели в конечное состояние с температурой 343 К. Полагая, что коэффициент изобарной расширяемости ( 0,262 × 10–3) и мольная изобарная теплоемкость в данном интервале температур постоянны, вычислите мольные и полные изменения объема, энтропии и энтальпии при переходе из начального состояния в конечное.
3. При температуре 773 К рассчитать значения стандартной мольной энтальпии, стандартной мольной энтропии, стандартной мольной энергии Гиббса реакции 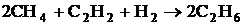 . Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
. Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
4. Рассчитать равновесный состав системы, в которой при 700 К и 1 атм протекает процесс изомеризации этилбензола по следующим реакциям:
1. 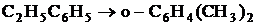
![]() =3,36
=3,36
2. 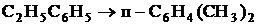
![]() = 2,70
= 2,70
Начальное количество этилбензола 1 моль, продуктов реакции в начальный момент нет.
5 Для чистого аммиака известны температурные зависимости давления насыщенного пара при равновесии
жидкость-пар | p, Па 729 Т, К 198,9 204,8 212,8 217,4 227,8 |
Кристаллы-пар | p, Па ,4 897,8 1 Т, К ,4 178,6 |
В тройной точке плотности массы чистого аммиака в кристаллическом и жидком агрегатном состоянии равны соответственно 827 и 817 кг/м3 . Определите графически координаты тройной точки и величины мольных теплот испарения и возгонки; определите мольную теплоту плавления, мольную энтропию плавления и мольную энергию Гиббса плавления; найдите температуру плавления вещества при давлении 160500 Па.
6. Гетерогенная система (жидкость-пар) содержит два компонента – ацетон и сероуглерод и равновесна при 322 К и 1 атм. Масса сероуглерода в жидкой фазе 1,5 кг, масса сероуглерода в паровой фазе 1,3 кг. Мольная доля сероуглерода в жидкой фазе 0,10, мольная доля сероуглерода в паровой фазе 0,28. Найти массу системы.
Вариант 26
Обязательное домашнее задание
1. а) Определить энергию активации вязкого течения гексана.
б). Изобразите графически температурную зависимость мольной изобарной теплоемкости гексана в интервале от 0 до 130 °C, привлекая для этого [4].
2. Концентрация метанола в водно-метаноловом растворе составляет
21172 моль/м3. Раствор содержит 13,333 моль воды и имеет массу 1,15 кг. Определить общее число молей и объем раствора, его мольную массу и удельное число молей, мольный и удельный объем, плотности общего числа молей и массы, плотности масс компонентов, их массы, мольные и массовые доли, число молей метанола и плотность числа молей воды.
3. а). Плотность массы раствора вода-этанол при 293 К и 105 Па составляет 909,9 кг/ м3 при массовой доле этанола 0,5. Парциальный мольный объем спирта в растворе равен 5,687 ×10–5 м3 /моль. Рассчитать парциальный мольный объем воды.
б). Плотность массы раствора вода– метиловый спирт (с массовой долей метанола 0,6), плотности масс воды и метанола в чистом виде равны соответственно: 894,6; 998,2 и 791,7 ( кг/ м3). Рассчитать мольное изменение объема при смешении.
4. Рассчитать мольное изменение энтропии бензола при его нагреве от 298 до 500 К. Необходимые для расчета данные взять из справочника.
5. Вычислить состав равновесной смеси, образующейся в результате протекания в газовой фазе при 600 К и 1 атм следующей реакции
![]() .Исходные вещества взяты в стехиометрических количествах,
.Исходные вещества взяты в стехиометрических количествах, ![]() =1,27 , газы подчиняются законам идеальных газов.
=1,27 , газы подчиняются законам идеальных газов.
6. Давление пара этиламина при 5,8 °C равно 0,642 ×10 5 Па, а при 16,2 °C равно 1,000 ×10 5 Па. Рассчитать мольную теплоту испарения этиламина
7. При 298 К давление насыщенного пара над чистой водой равно 23,76 мм рт. ст. Рассчитать (выразить в Па) давление насыщенного пара при той же температуре над раствором 11 г глюкозы в 120 г воды, считая раствор идеальным.
Рейтинговое домашнее задание
1. В таблице приведена зависимость плотности массы r двухкомпонентного жидкого раствора метанол (1 компонент) – ацетон (2 компонент) от массовой доли j 2 второго компонента ( Т= 298 К, р = 1 атм)
j 2 | 0,00 | 0,08 | 0,32 | 0,50 | 0,76 | 0,88 | 1,00 |
r, кг/м3 | 796 | 797,6 | 800,5 | 801,5 | 800,7 | 799,2 | 790,0 |
Постройте график зависимости объема раствора ![]() от числа молей
от числа молей ![]() компонента 2 при постоянной массе сероуглерода 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v 1 и v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,4; вычислите для компонентов 1 и 2 при той же N2 парциальные мольные объемы смешения Δ v 1m и Δ v 2 m
компонента 2 при постоянной массе сероуглерода 0,20 кг и найдите с помощью полученного графика парциальные мольные объемы v 1 и v 2 обоих компонентов 1 и 2 в растворе, где мольная доля второго компонента N2 = 0,4; вычислите для компонентов 1 и 2 при той же N2 парциальные мольные объемы смешения Δ v 1m и Δ v 2 m
2.Жидкий бензол массой 1,2 кг имел в начальном состоянии ( 1 атм) при температуре 293 К плотность массы 879 кг/м3. При постоянном давлении 1 атм его перевели в конечное состояние с температурой 330 К. Полагая, что коэффициент изобарной расширяемости ( 1,21 × 10–3) и мольная изобарная теплоемкость в данном интервале температур постоянны, вычислите мольные и полные изменения объема, энтропии и энтальпии при переходе из начального состояния в конечное.
3. При температуре 773 К рассчитать значения стандартной мольной энтальпии, стандартной мольной энтропии, стандартной мольной энергии Гиббса реакции 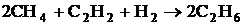 . Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
. Определить, возможно ли самопроизвольное протекание газовой реакции слева направо при этой температуре. В какую сторону будет смещаться равновесие данной реакции при изобарическом повышении температуры? Исходная смесь соответствует стехиометрическому составу, газы близки по свойствам к идеальным.
4. Рассчитать равновесный состав системы, в которой при 700 К и 1 атм протекает процесс изомеризации этилбензола по следующим реакциям:
1. 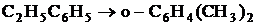
![]() =3,36
=3,36
2. 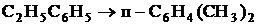
![]() = 2,70
= 2,70
Начальное количество этилбензола 1 моль, продуктов реакции в начальный момент нет.
5. На основании приведенных данных о составах жидкой и паровой фаз при различных температурах постройте диаграмму фазового состояния системы пропанон ( 1 компонент) - трихлорметан( 2 компонент)
Т, К | 329 | 330 | 333 | 335 | 336 | 337 | 337,6 | 337 | 336 | 334 |
| 0 | 0,1 | 0,20 | 0,35 | 0,43 | 0,53 | 0,67 | 0,73 | 0,85 | 1 |
| 0 | 0,05 | 0,11 | 0,22 | 0,32 | 0,47 | 0,67 | 0,8 | 0,91 | 1 |
Обозначьте все поля, линии и характерные точки на этой диаграмме и укажите, сколько компонентов и фаз, находится в равновесии и чему равно число степеней свободы в каждой из указанных позиций. Ответьте, есть ли отклонения от закона Рауля и, если есть, то какие. Определите, какой компонент и в каком количестве нужно при 334 К добавить в систему (N2 = 0,25; масса системы 5 кг) , чтобы перевести ее в пар

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |



