1.7.1 Тематика и планы практических занятий.
Практическое занятие № 1 (2 ч.)
ТЕМА: Водород. Кислород. Галогены.
План:
1.Водород в природе. Получение водорода – лабораторные и промышленные методы.
2. Физические и химические свойства водорода. Применение водорода.
2. Пероксид водорода. Физические и химические свойства. Применение.
3.Кислород в природе. Характеристика состава воздуха.
4. Получение, физические и химические свойства кислорода. Озон.
5. Галогены, их соединения, состав, свойства.
6. Кислородсодержащие соединения галогенов. Физические и химические свойства.
Вопросы для коллективного обсуждения:
1. Охарактеризуйте способы получения водорода в лаборатории и промышленности.
2. Охарактеризуйте химические свойства водорода.
3. В чем выражается участие кислорода в окислительно-восстановительных реакциях?
4. Почему наблюдается резкое различие в свойствах воды и пероксида водорода?
5. Объясните, в каких случаях пероксид водорода может проявлять окислительные и в каких восстановительные свойства. Напишите уравнения реакций.
6. Какие вещества называют аллотропными видоизменениями, какие аллотропные видоизменения кислорода вам известны? Можно ли считать химической реакцией превращение одного аллотропного видоизменения в другое?
7. В чем выражается участие кислорода в окислительно-восстановительных реакциях?
8. Охарактеризуйте химические свойства водорода.
9. Перечислите способы получения (лабораторные и промышленные методы) кислорода.
10. Перечислите лабораторные способы получения галогенов, галогеноводородов.
Можно ли хлороводород назвать кислотой? Почему?
11. Составьте уравнения реакций, с помощью которых можно осуществить следующие превращения:
![]() NH3
NH3
![]() KOH → H2 → KH → H2 → HCl → H2
KOH → H2 → KH → H2 → HCl → H2
CH3OH.
12. Закончите уравнения реакций:
F2 + KCl = Cl2 + KI =
F2 + NaBr = Br2 + KI =
Напишите уравнения реакций в молекулярной и ионной формах.
Расчетные задачи:
13. Смесь азота и кислорода имеет относительную плотность по водороду 15,5. Вычислите молярную долю кислорода в смеси.
Задания для самостоятельной работы:
1. Даны вещества H2, O2, Zn, HCl, CuO. Составьте уравнения пяти реакций возможного
взаимодействия этих веществ друг с другом.
2. Какую роль – окислителя или восстановителя – играет H2O2 в следующих реакциях:
KMnO4 + H2O2 + H2SO4 → MnSO4 + O2 + K2SO4 + H2O
H2O2 + KJ +H2SO4 = K2SO4 + J2 + 2H2O
Составьте уравнения методом электронного баланса.
3. Составьте уравнения реакций, с помощью которых можно осуществить следующие превращения:
H2O→NaH→ HCl → H2O → СаH2
4. К оксиду серы (IV), массой 3,2 г, добавили кислород, массой 2,4 г. Вычислите
объемную долю оксида серы в полученной газовой смеси.
5. В соляной кислоте растворили магний, массой 6 г, и цинк, массой 6,5 г. Определите
объем водорода, измеренный при н. у., который выделится при этом.
6.При действии избытка воды на сплав натрия и калия массой 0,85 г выделилось 336 мл (н. у.) газа. Сколько атомов натрия приходится в этом сплаве на один атом калия?
7. В твердом остатке, полученном после частичного термического разложения перманганата калия, на два атома марганца приходится семь атомов кислорода. Вычислите массовую долю перманганата калия в этом остатке.
8. Какой минимальный объем водорода нужен для полного восстановления оксида меди (II), полученного при термолизе 37,5 г нитрата меди(II)?
9. Исходя из теплот реакций окисления As2O3 кислородом и озоном:
As2O3 + O2 = As2O5, ΔH° = -271кДж,
3As2O3 + 2О3 = 3As2O5, ΔH° = -1096кДж,
вычислите теплоту образования озона из молекулярного кислорода.
10. Плотность галогеноводорода по воздуху равна 4,41. Определите плотность этого газа
по водороду и назовите его.
Литература
С, и др. Лабораторные и семинарские занятия по общей и неорганической химии.- М.: Академия,1999.-360с. Ахметов и неорганическая химия.- 4-е изд., - М.: Высшая школа, 2001.-743с. Глинка и упражнения по общей химии.- Ленинград: Химия, 1988. Глинка химия.- Л.: Химия, 1973. Мень к контрольным и лабораторным работам по общей и неорганической химии.- М.: МГПУ, 2004.Практическое занятие №2(2 ч.)
ТЕМА: Сера и ее соединения.
1. Сера в природе. Получение серы.
2. Физические и химические свойства серы.
3. Сероводород, получение, физические и химические свойства, применение. Сульфиды. 4. Диоксид серы. Сернистая кислота.
5. Триоксид серы. Серная кислота, получение, свойства, применение.
Вопросы для коллективного обсуждения:
1. Какие аллотропные видоизменения серы вам известны? Охарактеризуйте их строение и свойства.
2. Какие соединения серы могут вести себя в химических реакциях как восстановители? Напишите уравнения реакций.
3. Какие соединения серы могут вести себя в реакциях как окислители? Напишите уравнения реакций.
4. Можно ли сероводородную воду назвать сероводородной кислотой? Почему?
5. Почему оксид серы (IV) и сернистая кислота могут проявлять как окислительные, так и восстановительные свойства?
6. Охарактеризуйте химические свойства сернистой кислоты, напишите уравнения соответствующих химических реакций.
7. Охарактеризуйте химические свойства разбавленной и концентрированной серной кислоты, напишите уравнения соответствующих химических реакций.
8. Какое вещество образуется в результате реакции:
Са + H2SO4 (конц.) →
9. Осуществить превращения:
S → SO2 → H2SO3 → Na2SO3 → SO2 → S
Напишите все уравнения реакций в ионной и молекулярной формах, для окислительно-восстановительных реакций составьте ионно-электронный баланс.
Расчетные задачи:
10. Газовая смесь состоит из кислорода (2,24 л) и оксида серы (IV) (3,36 л). Объемы
газов приведены к н. у. Рассчитайте массу смеси.
Задания для самостоятельной работы:
1.Составить структурные (графические) формулы следующих соединений: Na2S2O3, H2S2O7, (NH4)2S2O8, Na2SO5.
2.Напишите уравнения окислительно-восстановительных реакций, протекающих в растворах, и подобрать необходимые коэффициенты методами электронного и электронно-ионного баланса.
Аg + H2SO4, конц. →
Аg + H2SO4, разб. →
Mg + H2SO4, конц. →
Mg + H2SO4, разб. →
4. Осуществить превращения:
H2SO4 → SO2 → SO3 → H2SO4 → Na2SO4 → NaCl
Напишите все уравнения реакций в ионной и молекулярной формах, для окислительно-восстановительных реакций составьте ионно-электронный баланс.
5. Напишите уравнения окислительно-восстановительных реакций, расставьте коэффициенты методами электронного и электронно-ионного баланса.
а) KMnO4 + H2S + H2SO4 = S +…..+ H2O
б) H2S + H2SO3 = S +….
в) J2 + H2SO3 + H2O = H2SO4 +HJ
6. Какое вещество образуется при растворении углерода в концентрированной азотной кислоте? Напишите уравнение окислительно-восстановительной реакции.
7. Вычислите нормальность 61,4 %-го раствора MgSO4 · 7 Н2О (ρ = 1,31 г/мл).
8. Вычислите молярную концентрацию 98%-го раствора серной кислоты (ρ = 1,84 г/мл)
Литература
С, и др. Лабораторные и семинарские занятия по общей и неорганической химии.- М.: Академия,1999.-360с. Ахметов и неорганическая химия.- 4-е изд., - М.: Высшая школа, 2001.-743с. Глинка и упражнения по общей химии.- Ленинград: Химия, 1988. Глинка химия.- Л.: Химия, 1973. Мень к контрольным и лабораторным работам по общей и неорганической химии.- М.: МГПУ, 2004.Практическое занятие №3 (2 ч.)
ТЕМА: Азот и его соединения.
План:
1. Получение и свойства азота.
2. Аммиак. Соли аммония.
3. Оксиды азота.
4. Азотистая кислота, химические свойства, получение применение. Нитриты.
5. Азотная кислота, химические свойства, получение применение. Нитраты.
Вопросы для коллективного обсуждения:
1. Охарактеризуйте химические свойства азота.
2. Охарактеризуйте способы получения азота в лаборатории и промышленности.
3. Перечислите способы получения аммиака и солей аммония, напишите соответствующих уравнения химических реакций.
4. Охарактеризуйте химические свойства азотистой кислоты, напишите уравнения соответствующих химических реакций.
5. Охарактеризуйте химические свойства разбавленной и концентрированной азотной кислоты, напишите уравнения соответствующих химических реакций.
6. Напишите уравнения реакций, с помощью которых можно осуществить следующие
превращения:
NH3 → NO2 → NO→ NaNO3→ HNO3→ O2
7. Напишите схему окислительно-восстановительной реакции получения оксида азота (IV). Составьте электронный баланс и расставьте коэффициенты.
8. Допишите схемы реакций и составьте уравнения по методу электронного баланса
а) С + HNO3 (конц.) → CO2 + …
б) Ag + HNO3 (разб.) →…
в) Fe + HNO3 (разб.) →…
Расчетные задачи:
9. Какой объем аммиака может быть получен при взаимодействии с натронной известью 20 г хлорида аммония, содержащего 10% примесей?
10. Сколько хлорида аммония и гидроксида кальция (в г) потребуется для получения 8 л аммиака, если выход последнего равен 80% от теоретического?
Задания для самостоятельной работы:
1. Напишите уравнения окислительно-восстановительных реакций, расставьте коэффициенты методами электронного и электронно-ионного баланса.
а) KJ + NaNO2 + H2SO4 = J2 + ….+ N2 +….
б) KMnO4+NaNO2+H2SO4 = NaNO3 +…..
2.Какое вещество образуется при растворении углерода в концентрированной азотной кислоте? Напишите уравнение окислительно-восстановительной реакции.
3. Какое соединение фосфора образуется в реакции его с азотной кислотой? Напишите уравнение окислительно-восстановительной реакции.
4. Какова процентная концентрация раствора аммиака, если в 106 г воды растворено 44,8 л аммиака?
5. Аммиак, полученный при взаимодействии 10,7 г хлорида аммония и 15 г гашеной извести, растворили в 56,6 г воды. Какова процентная концентрация полученного раствора?
6. Какой объем оксида азота (II) может быть получен из 50,4 г азотной кислоты?
7. Вычислите объем азота (н. у.), который может прореагировать с магнием, массой 3 г.
8. Рассчитайте массу аммиака, который потребуется для получения азотной кислоты,
массой 3,15 т. Производственные потери веществ составляют 15%.
9. Какой объем аммиака может быть получен при взаимодействии с натронной известью 20 г хлорида аммония, содержащего 10% примесей?
10. Сколько хлорида аммония и гидроксида кальция (в г) потребуется для получения 8 л аммиака, если выход последнего равен 80% от теоретического?
Литература
С, и др. Лабораторные и семинарские занятия по общей и неорганической химии.- М.: Академия,1999.-360с. Ахметов и неорганическая химия.- 4-е изд., - М.: Высшая школа, 2001.-743с. Глинка и упражнения по общей химии.- Ленинград: Химия, 1988. Глинка химия.- Л.: Химия, 1973. Мень к контрольным и лабораторным работам по общей и неорганической химии.- М.: МГПУ, 2004.Практическое занятие №4 (2 ч.)
ТЕМА: Элементы главной подгруппы IV группы.
План:
1. Углерод в природе. Аллотропные модификации углерода.
2. Химические свойства углерода. Карбиды.
3. Диоксид углерода, угольная кислота, их получение и химические свойства.
4. Оксид углерода (II).
5. Соединения углерода с серой и азотом. Биогеохимический круговорот углекислого газа.
6. Кремний в природе. Получение и свойства кремния.
7. Диоксид кремния, его химические свойства. Кремниевые кислоты и их соли.
Вопросы для коллективного обсуждения:
1. Охарактеризуйте аллотропные модификации углерода, их строение и физико-химические свойства.
2. Охарактеризуйте химические свойства углерода, напишите уравнения соответствующих химических реакций.
3. Перечислите способы получения оксидов углерода, напишите соответствующих уравнения химических реакций.
4. Сравните химические свойства оксида углерода (II) и оксида углерода (IV), напишите уравнения соответствующих химических реакций.
5. Сравните химические свойства угольной и кремниевой кислот, напишите уравнения соответствующих химических реакций.
6. Напишите уравнения реакций, с помощью которых можно осуществить следующие
превращения:
CaCO3 → CO2 → CO → NaHCO3 → Na2CO3→ NaHCO3→ CO2
7. Объясните сущность гидролиза силиката натрия.
8. Сравните гидролиз силикатов с гидролизом карбонатов, если обнаружится сходство, объяснить его. Составьте уравнения гидролиза в молекулярной и ионных формах.
Расчетные задачи:
9. Вычислите массовую долю углерода в карбонате натрия и гидрокарбонате натрия.
10. В суперфосфате массовая доля оксида фосфора (V) составляет 25%. Рассчитайте
массовую долю Ca(H2PO4)2 в этом удобрении.
Задания для самостоятельной работы:
1. Напишите уравнения реакций, с помощью которых можно осуществить следующие
превращения:
а) Si → SiO2 → Na2SiO3 → H2SiO3.
б) NH4HCO3 → CO2→ CO→ Cu→ CuCl2
2. Определите массовую долю оксида фосфора (V) в преципитате CaHPO4·2H2O.
3. Смесь кремния и угля массой 5 г обработали концентрированным раствором щелочи при нагревании (щелочь в избытке). В результате реакции выделился водород объемом 2,8 л (н. у.). Вычислите массовую долю углерода в этой смеси.
4. Какой объем оксида углерода (IV) израсходуется на реакцию с 20 мл 10% раствора едкого натра при условии образования кислой соли.
5. Какая соль и в каком количестве образуется при пропускании 5,6 л СО2 через 200 г 5% раствора едкого натра?
6. В раствор гидроксида калия (масса растворенного KOH равна 14 г пропустили оксид углерода (IV), объемом 2,8 л (н. у.). Какая соль образуется при этом? Определить массу соли в полученном растворе.
7. Смешано 17 г аммиака, 500 мл воды и 22,4 л (н. у.) углекислого газа. Рассчитайте массовую долю вещества в полученном растворе.
8. Константа равновесия реакции CO(г) + Cl2(г) = COCl2(г) при некоторой температуре равна 9. найти равновесные концентрации всех веществ, если их исходные концентрации равны C(CO) –2 моль/л, C(Cl2) –0,25 моль/л, C(COCl2) –3моль/л.
Литература
С, и др. Лабораторные и семинарские занятия по общей и неорганической химии.- М.: Академия,1999.-360с. Ахметов и неорганическая химия.- 4-е изд., - М.: Высшая школа, 2001.-743с. Глинка и упражнения по общей химии.- Ленинград: Химия, 1988. Глинка химия.- Л.: Химия, 1973. Мень к контрольным и лабораторным работам по общей и неорганической химии.- М.: МГПУ, 2004.Практическое занятие №5(2 ч.)
ТЕМА: Свойства металлов.
План:
1. Электронное строение металлов. Кристаллическое строение металлов.
2. Физические и химические свойства металлов.
3.Получение металлов. Сплавы.
4.Щелочные металлы.
5.Магний, нахождение в природе, получение, физические и химические свойства, применение.
6. Кальций, нахождение в природе, получение, физические и химические свойства, применение.
7. Алюминий и хром, нахождение в природе, получение, физические и химические свойства, применение.
8. Железо, нахождение в природе, получение, физические и химические свойства, применение.
Вопросы для коллективного обсуждения:
1. Охарактеризуйте электронное строение металлов.
2. Напишите электронную формулу натрия, кальция, алюминия, меди, железа.
3. Охарактеризуйте типичные химические свойства металлов.
4. Сделайте вывод об отношении меди к концентрированным и разбавленным кислотам в связи с ее положением в электрохимическом ряду напряжений.
5. Можно ли гидроксокарбонат меди (II) перевести снова в сульфат меди (II), напишите уравнение этой реакции.
6. Напишите уравнения реакции, характеризующих химические свойства щелочных металлов.
7.Сравните строение и химическую активность магния, кальция, алюминия.
8.Охарактеризуйте химические свойства магния.
9.Охарактеризуйте химические свойства кальция.
10.Какие соединения называются амфотерными? Как доказать их амфотерность?
11. Напишите уравнения реакций, с помощью которых можно осуществить следующие
превращения:
Na → NaOH → NaCl → NaOH → Na.
12. Почему для получения карбоната цинка реакцией обмена используют не карбонат натрия, а гидрокарбонат?
Расчетные задачи:
13. Серебро, массой 5,4 г, растворили в концентрированной азотной кислоте. К
полученному раствору прилили избыток раствора бромида натрия. Рассчитайте
массу образовавшегося осадка.
14. Вычислите объем соляной кислоты (массовая доля HCl 20%, плотность 1,1 г/мл),
которая потребуется для растворения смеси цинка и никеля, массой 9,8 г (массовая
доля никеля в смеси 60,2%).
Задания для самостоятельной работы:
1. Напишите уравнения реакций, протекающих при электролизе водного раствора и расплава бромида калия. Какие вещества можно получить при этом?
2. Допишите схемы тех реакций, которые протекают практически до конца:
а) Li + H2O →
б) NaOH (изб.) + H3PO4 →
в) Na2O + SO2 →
г) NaOH + BaCl2 →
д) LiOH + CuSO4 →
3. С помощью каких реакций можно осуществить следующие превращения:
KCl → KOH → KHS → K2S → KNO3.
Напишите уравнения реакций в молекулярной и ионной формах.
4. Натрий получают электролизом расплава хлорида натрия, а для получения чистого
железа используют электролиз водного раствора сульфата железа (II). Напишите
уравнения реакций, протекающих при этих процессах.
5. При взаимодействии щелочного металла, массой 4,6 г, с йодом образуется иодид,
массой 30 г. Какой щелочной металл был взят для реакции?
6. Сколько технического цинка, содержащего 4% примесей, и сколько 30% соляной кислоты потребуется для приготовления 50 кг 45% раствора хлорида цинка?
7. Сколько цинка и серной кислоты можно получить из 1 т цинковой обманки, содержащей 85% сульфида цинка?
8. Какой должна быть реакция среды в растворе нитрата меди (II)?
9. Как осуществить следующие превращения, напишите уравнения реакций:
А)
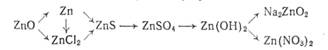
В)

10. Осуществите превращения:
![]()
![]()
Литература
С, и др. Лабораторные и семинарские занятия по общей и неорганической химии.- М.: Академия,1999.-360с. Ахметов и неорганическая химия: учебник для химико-технол. Спец. Вузов.- 4-е изд., - М.: Высшая школа, 2001.-743с. Глинка и упражнения по общей химии.- Ленинград: Химия, 1988. Глинка химия.- Л.: Химия, 1973. Мень к контрольным и лабораторным работам по общей и неорганической химии.- М.: МГПУ, 2004.1.7.2 Тематика и планы практических занятий.
ЛАБОРАТОРНАЯ РАБОТА № 1(2 ч.)
Тема: Водород, кислород и их соединения.
1. Получение водорода.
 В сухую пробирку помещают кусочек алюминиевой фольги или гранулу цинка. Добавляют
В сухую пробирку помещают кусочек алюминиевой фольги или гранулу цинка. Добавляют
2 мл 20 %-го раствора серной кислоты. Пробирку закрывают пробкой с отводной трубкой (рис. 1), слегка подогревают до начала реакции, затем нагревание прекращают. Водород
собирают в перевернутую пробирку и периодически проверяют водород на чистоту, поднося пробирку к пламени спиртовки. Звучный хлопок свидетельствует о недостаточной чистоте водорода, и наполнение пробирки повторяют. Если водород в пробирке воспламеняется без «выстрела», то значит газ чистый, и его можно поджечь на конце трубки.
 2. Получение кислорода и изучение его свойств.
2. Получение кислорода и изучение его свойств.
 а) Около 1 г перманганата калия помещают в сухую пробирку, закрепленную в штативе, и закрывают ее пробкой
а) Около 1 г перманганата калия помещают в сухую пробирку, закрепленную в штативе, и закрывают ее пробкой
с г-образной трубкой (рис.2). Вместо указанной трубки
можно воспользоваться прямым газоотводом со шлангом. Наполненный водой цилиндр опускают в кристаллизатор с водой и под цилиндр вводят газоотводную трубку. Содержимое пробирки осторожно подогревают, собирая кислород в цилиндр над водой. По окончании реакции, не вынимая из воды цилиндр, закрывают его пробкой, а затем извлекают из воды. В полученном кислороде сжигают вещества, указанные преподавателем (серу, уголь, фосфор, железо).*
 б) Перед сжиганием S и Р в цилиндры добавляют по 5 мл 0,1 н раствора NаОН и 1 каплю фенолфталеина. По окончании сжигания цилиндр закрывают пробкой и встряхивают. Следят за изменением окраски индикатора.
б) Перед сжиганием S и Р в цилиндры добавляют по 5 мл 0,1 н раствора NаОН и 1 каплю фенолфталеина. По окончании сжигания цилиндр закрывают пробкой и встряхивают. Следят за изменением окраски индикатора.
в) Перед сжиганием угля в цилиндр добавляют 10 мл 5 %-го раствора хлорида кальция.
г) Перед сжиганием железа в цилиндр вносят 5 мл 10 %-ой соляной кислоты. После растворения окалины раствор
сливают в пробирку и добавляют 1 к. раствора роданиза аммония (или калия).
*---
Для сжигания веществ их помещают в металлическую ложечку для сжигания, заполняя ее примерно на 1/3 объема. Вещество либо поджигают от спиртовки, либо накаляют. Затем быстро вносят в цилиндр с кислородом.
3. Восстановительные свойства водорода.
В пробирку наливают 1 мл 0,1 н перманганата калия, добавляют 1 мл 50 %-го раствора серной кислоты, а затем вносят гранулу цинка. Наблюдают за ослаблением окраски раствора.
4. Образование аквакомплексов.
а) в сухую пробирку вносят на кончике шпателя безводный сульфат меди и добавляют 1 каплю воды.
б) на листе бумаги напишите формулу сульфата кобальта его разбавленным раствором. Когда надпись подсохнет, осторожно погрейте лист над спиртовкой. Объясните наблюдаемое явление.
5. Окислительно-восстановительные свойства пероксида водорода.
а) К 1 мл раствора иодида калия добавляют 1 мл 20 %-го раствора серной кислоты и 1 мл 5 %-го пероксида водорода.
б) К подкисленному раствору перманганата калия добавляют равный объем 5 %-го пероксида водорода. Какова роль Н2О2 в реакциях а и б?
в) К щелочному раствору хлорида хрома добавляют равный объем концентрированного раствора пероксида водорода, затем смесь осторожно подогревают, следя за изменением окраски. По окончании реакции пробирку охлаждают и добавляют две капли раствора хлорида бария.
ЗАДАНИЯ
Написать все уравнения реакций в ионной и молекулярной формах, а окислительно-восстановительные реакции - по методу ионно-электронного баланса. Сделать выводы и объяснить наблюдаемые явления для каждого опыта. Привести все способы получения кислорода и водорода в лаборатории. Как изменяются свойства бинарных соединений водорода и кислорода в периоде (на примере III периода), и как эту закономерность можно объяснить? На основании опытов 2 (а - в) определить составы растворов после окончания всех реакций, считая, что весь полученный кислород полностью прореагировал, а плотности растворов равны 1 г/моль. Объясните, почему лед легче воды? Вычислите значение ΔG˚298 реакций разложения (см. табл.1):2 КСlO3 → 2 КСl + 3 О2 (ΔН = 2 ΔН˚KCl - 2 ΔН˚KClO3)
2 Na2SO4 → 2 Na2SO3 + O2 (ΔН = 2 ΔН˚Na2SO3 - 2 ΔН˚Na2SO4)
8. Какое из указанных веществ предпочтительнее использовать для получения кислорода? Термодинамические параметры для веществ задания 7.
Таблица 1.
ВЕЩЕСТВО | ΔН˚f | S˚298 |
KClO3 | - 391.20 | 142.97 |
KCl | - 435.85 | 82.68 |
Na2SO4 | - 1384.00 | 149.40 |
Na2SO3 | - 1090.00 | 146.00 |
O2 | --- | 205.03 |
8. Написать уравнение по схеме: NaNО2 + Н2О2 + Н+ → NОзˉ + ...
ЛАБОРАТОРНАЯ РАБОТА № 2 (2 ч.)
Тема: Галогены и их соединения.
1. Получение галогенов.
а) В пробирку помещают около 1 г МnО2 и столько же кристаллического хлорида натрия, затем добавляют 1 мл концентрированной серной кислоты. Пробирку быстро закрывают
 пробкой с газоотводной трубкой и слегка подогревают. Хлор собирают в сухой цилиндр, при этом газоотводная трубка должна быть опущена да дна сосуда (рис. З). Сосуд с хлором плотно закрывают и оставляют для следующих опытов.
пробкой с газоотводной трубкой и слегка подогревают. Хлор собирают в сухой цилиндр, при этом газоотводная трубка должна быть опущена да дна сосуда (рис. З). Сосуд с хлором плотно закрывают и оставляют для следующих опытов.
б) в сухой стакан на 50 мл помещают 3-4 кристаллика КI и столько же МnО2, добавляют 5-6 капель концентрированной серной кислоты и слегка подогревают стаканчик, поместив его на асбестовую сетку (рис. 4) и накрыв часовым стеклом или чашкой Петри с холодной водой.
в) Предметное стекло покрывают слоем парафина. На парафине делают надпись (рисунок) острым предметом. Ватой удаляют избыток парафина. В пробирку помещают кристаллический KF (или NH4F) и добавляют несколько капель концентрированной H2SO4. Сразу же накрывают пробирку подготовленным выше предметным стеклом. Пробирку слегка подогревают. Наблюдается надпись на стекле после удаления парафина в горячей воде. Опыт проводится под тягой.
2. Растворимость йода.
а) 2 кристаллика иода поместить в пробирку и добавить 1 мл
четыреххлористого углерода или хлороформа. Затем наблюдают за изменением окраски после добавления бензола, этилового эфира. Объясните различие в окраске растворов.
б) к кристаллику иода добавляют 1 мл воды, а затем 1 кристаллик КI. Сравнить растворимость иода в отсутствие и в присутствии КI.
3. Окислительная активность кислородных соединений галогенов.
а) в сосуд с хлором (опыт 1а) приливают 10 мл 0,1м раствора NаОН, закрывают и растворяют газ, встряхивая сосуд. В полученный раствор добавляют 2 капли раствора КI и 1 каплю крахмала.
б) в две пробирки наливают по 1 мл раствора хлораста калия и равные объемы раствора КI. Затем в одну из пробирок добавляют разбавленную серную кислоту. Сравнить наблюдаемые результаты.
в) смесь белильной извести («хлорки») с оксидом меди (II) осторожно нагреть в пробирке. Зажженной лучинкой доказать выделение кислорода.
4. Получение хлороводорода.
В пробирку с газоотводной трубкой помещают около 0,5 г NаСl, добавляют 1 мл концентрированной серной кислоты и слегка подогревают. К отверстию трубки подносят палочку, смоченную раствором аммиака. После этого трубку отводят в стакан с водой, не погружая трубку в воду. Полученный раствор в стакане проверяют лакмусом. Можно ли таким образом получить НI и НВr?
5. Осаждение галогенов.
а) К 1 мл раствора NaCl добавить 3-4 капли нитрата свинца. Полученную смесь подогреть,
а затем охладить в проточной воде, наблюдая за изменением растворимости хлорида
свинца.
б) К 1 мл раствора нитрата свинца добавить 5 капель раствора КI, смесь, нагреть до растворения осадка, а затем охладить в проточной воде. К полученному осадку добавить еще 0,5
мл раствора КI до растворения осадка.
в) К солям Ca2+ и Mg2+ добавить по 2-3 капли раствора KF. Проверить растворимость полученных осадков в HCl и H2SO4.
6. Гидролиз хлоридов.
Исследуйте характер среды в растворах NaCl, ZnCl2, АlClз с помощью лакмуса.
7. Иодометрия.
К 1 мл хлорной воды добавляют 2 мл раствора КI и 2 капли крахмала. Затем из пипетки по каплям добавляют 0,1 н раствор тиосульфат натрия до исчезновения синего окрашивания. Принимая, что 1 капля тиосульфата составляет 0,1 мл, рассчитывают количество активного хлора в воде по формуле: g =· N · Э Cl2 · 0,1 · n, г
Э - эквивалентная масса хлора, г/моль;
N - нормальность раствора Na2S2Оз, моль/л;
n - число капель тиосульфата, пошедшего на обесцвечивание иода;
0,1 - объем 1 капли тиосульфата, мл.
Для нашего случая: g Cl2= 35,5 ·· n, г
ЗАДАНИЯ
1.Привести способы получения в лаборатории иодо - и бромоводородной кислот.
2.В какой последовательности будут выпадать из раствора бромид-, иодид - и хлорид-ионы
при добавлении по каплям нитрата серебра к их смеси?
3.Как изменяется восстановительная активность в ряду НF - НСl - НВr - НI и чем это
объясняется?
4.Как изменяется окислительная активность в ряду СlOˉ - С1О2ˉ - С1О3ˉ - С1О4ˉ ?
 |
ЛАБОРАТОРНАЯ РАБОТА № 3 (2 ч.)
Тема: Сера и ее соединения.
1. Диспропорционирование серы.
В пробирку наливают I мл концентрированной щелочи и добавляют на кончике шпателя элементарной серы. Смесь нагревают в течение пяти минут. С помощью свинцовой бумажки обнаруживают образующийся сероводород.
2. Окислительные свойства серы.
В фарфоровой ступке тщательно растирают и перемешивают цинковую (или алюминиевую) пыль с порошком серы. Затем к смеси добавляют 2 капли воды. По запаху определяют выделение сероводорода.
3. Растворимость сульфидов.
На стеклянную пластинку помещают по капле растворов, содержащих катионы К+, Cd 2+, Pb2+, Cu2+, Mn2+, Zn2+. К каждой капле добавляют по 1 капле сероводородной воды. Отметить образование сульфидов и их цвет. К тем катионам, которые не дали осадка добавляют по 1 капле сульфида аммония.
4. Гидролиз сульфидов.
а) исследуйте характер среды в растворе Na2S;
б) к 0,5 мл соли алюминия добавляют 2 капли раствора (NH4)2S. Добавлением нескольких капель щелочи к образовавшемуся осадку докажите природу осадка.
5.Восстановительные свойства сульфидов.
К 0,5 мл раствора нитрата свинца добавляют 2 капли сероводородной воды, а затем 1 мл щелочного раствора пероксида водорода. Следят за изменением окраски осадка от черной до белой.
6.Получение диоксида серы и его восстановительные свойства.
а) в пробирку с отводной трубкой вносят 0,5 г сульфита натрия и добавляют 1 мл 40 %-го раствора серной кислоты. Пробирку закрывают, а трубку опускают в подкисленный раствор перманганата калия. Пробирку с сульфитом периодически подогревают и следят за изменением окраски перманганата.
б) диоксид серы, пропускают через разбавленный раствор иода в воде, содержащей 2 капли крахмала, до обесцвечивания раствора. После этого определяют образование SO42- - иона добавлением 1 капли раствора хлорида бария.
вкристаллика Na2SO3 помещают в сухую пробирку и осторожно нагревают в течение 3-5 минут. После охлаждения содержимое пробирки растворяют в воде. В растворе обнаруживают сульфид - и сульфат - ионы, добавлением соответственно в одну пробирку 2 капли раствора нитрата свинца, а в другую - хлорида бария.
1.Водоотнимающие свойства серной кислоты.
На листке бумаги пишут 20 %-ным раствором серной кислоты ее формулу, лист подсушивают на воздухе, а затем осторожно подогревают над спиртовкой. Надпись проявляется
ЗАДАНИЯ.
3.Сделать выводы и объяснить наблюдаемые явления в каждом опыте.
4.Написать все уравнения реакций в ионной и молекулярной формах, а окислительно-
восстановительные реакции - по методу ионно-электронного баланса.
5.Составить структурные (графические) формулы следующих соединений: Na2S2O3, H2S2O7, (NH4)2S2O8, Na2SO5.
6.Составить уравнение реакции по схеме: Sb2S3 + HNO3 → SbO43-+ SO42-+NO+…
ЛАБОРАТОРНАЯ РАБОТА № 4-5 (4 ч.)
Тема: Азот и фосфор.
1. Получение азота.В отдельных пробирках нагревают по 1 мл насыщенных растворов хлорида аммония и нитрата натрия (калия). Нагретые растворы сливают, а выделяющийся азот определяют зажженной лучиной.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



