2. Получение аммиака.Смешивают в чашке равные объемы хлорида аммония и гидроксида кальция. Смесь помещают в сухую пробирку с газоотводной трубкой, на которую надевают перевернутую вверх дном пробирку для сбора аммиака. . Пробирку со смесью подогревают. После сбора аммиака пробирку с ним, не переворачивая, закрывают пробкой с короткой трубкой с оттянутым концом и погружают в стакан с водой, содержащей фенолфталеин. Наблюдают окраску раствора в пробирке.
3. Образование солей аммония.
а) смачивают дно и стенки стакана на 200 мл концентрированной соляной кислотой. Этим стаканом накрывают мерный стакан (50 мл), в котором находится раствор аммиака в воде. Следят за появлением «дыма» .
б) измеряют электропроводность раствора аммиака. Затем к раствору добавляют 2-3 капли серной кислоты. Наблюдают за изменением электропроводности.
в) в сухую пробирку помещают смесь гидроксида кальция и хлорида аммония и закрывают пробкой с газоотводной трубкой, которую погружают в 1 %-ый раствор соляной кислоты с 1 каплей метилового красного. Пробирку со смесью осторожно нагревают, следя за изменением окраски индикатора.
Восстановительные свойства аммония.
1) Несколько мл 25%-го аммиака помещают в плоскодонную колбу и подогревают на водяной бане. А колбу всыпают немного оксида хрома Cr2O3. Наблюдают горение.
2) К 0,1 н раствору перманганата добавляют несколько капель 25%-го аммиака и подогревают. Наблюдают изменение окраски раствора.
3) К бромной воде добавляют несколько капель 25%-го аммиака и подогревают. Следят за изменением окраски.
Написать все уравнения реакций, имея в виду, что аммиак окисляется до элементарного азота.
4. Гидролиз солей аммония.В 1 мл воды помещают кусочек магния (порошок). Затем добавляют на кончике шпателя кристаллический хлорид аммония, и пробирку слегка подогревают. Определяют характер среды в растворе с помощью лакмуса.
5. Отношение солей аммония к нагреванию.
а) исследуют отношение к нагреванию твердых солей: NН4С1, (NН4)Н2РО4 и (NН4)2СОз,
нагревая их в сухих пробирках и контролируя выделяющиеся газы смоченной водой лакмусовой бумажкой.
б) в тигель помещают 1 г дихромата аммония и поджигают до начала реакции. Наблюдают
вулканообразный ход реакции.
6. Получение оксида азота (II).В пробирку 1 (рис.2) помещают медные стружки и добавляют до покрытия меди разбавленную азотную кислоту, нагревают до начала реакции. Оксид азота собирают методом вытеснения воды. По окончании реакции цилиндр под водой закрывают стеклом (или пробкой), извлекают из воды. Раскаленный уголек в ложечке для сжигания вносят в цилиндр с оксидом азота, наблюдая горение угля.
7. Свойства нитритов.а) к раствору нитрита натрия добавляют 2 капли серной кислоты. 1 каплю крахмала и 2 капли раствора КI;
б) к раствору нитрита натрия добавляют 2 капли подкисленного перманганата калия. Следят
за изменением окраски.
8. Определение нитрат - ионов. К алюминиевым стружкам добавляют 1 мл нитрата натрия и 1 мл концентрированной щелочи. Пробирку закрывают пробкой с газоотводной трубкой, которую опускают в воду, содержащую 2 капли фенолфталеина.
9. Разложение нитратов.
а) в сухую пробирку, укрепленную вертикально над чашкой с песком, помещают немного
натриевой селитры и нагревают. В расплав бросают кусочек раскаленного угля.
б) в тугоплавкую пробирку помещают немного нитрата свинца и прогревают. В пробирку
вносят зажженную лучинку.
в) в тугоплавкую пробирку помещают кристаллический нитрат натрия на кончике шпателя и нагревают до расплавления соли. В расплав бросают кусочек угля и серы. Наблюдают горение. Опыт проводят под тягой.
10. Гидролиз фосфатов. Исследуют характер среды в растворах фосфата, гидрофосфата и дигидрофосфата натрия. Объясните различие в значениях рН указанных солей.
1. Растворимость фосфатов.
а) сравнить растворимость в воде и в кислоте фосфата, гидрофосфата и дигидрофосфата
кальция.
б) к суспензии фосфата кальция добавляют по каплям фосфорную кислоту. Наблюдают рас
творение осадка.
ЗАДАНИЯ
Объяснить все наблюдаемые явления. Написать все уравнения в ионной и в молекулярной форме, а окислительно-восстановительные реакции - по методу ионно-электронного баланса. Объясните высокую полярность молекулы аммиака и его склонность к донорно-акцепторному взаимодействию. Как влияет температура и давление на процесс синтеза аммиака из азотоводородной смеси? Из нитратов каких металлов можно получить NO2? Составить уравнение реакции по схеме: РН3 + КМnО4 + ОН ˉ → МnО2 + РО3 3- + ...
ЛАБОРАТОРНАЯ РАБОТА № 6 (2 ч.)
Тема: Углерод и его соединения.
1. а) Свойства активированного угля.
1) В пробирке нагревают Pb(NO3)2. При появлении бурого газа в пробирку вносят активированный уголь и наблюдают за изменением окраски газа.
2) В пробирку со светло-розовым раствором фуксина вносят на кончике шпателя активированный уголь. Наблюдают за изменением окраски.
3) К 10 каплям 0,01 н раствора Pb(NO3)2 добавляют 1 каплю 0,1 н KI.
В другой пробирке к 10 каплям 0,01 н раствора нитрата свинца добавляют несколько кусочков активированного угля, перемешивают стеклянной палочкой и оставляют на 2-3 минуты. Жидкую фазу отбирают пипеткой, переносят в другую пробирку и добавляют 1 каплю 0,1 н раствора KI. Сравнивают количество осадка в первой и во второй пробирках. Почему во второй пробирке осадка меньше?
4) В пробирку помещают немного оксида свинца (II), вносят несколько кусочков угля и подогревают на спиртовке. Выделяется свободный свинец.
1. б) Свойства диоксида углерода.
Наполняют три цилиндра диоксидом углерода, проверяя полноту заполнения горящей лучиной.
1) Поджигают ленту магния и быстро вносят в один из цилиндров.
2) Во второй цилиндр вносят горящий фосфор в ложечке для сжигания.
3) В фарфоровой чашке поджигают горючую жидкость (спирт, ацетон, бензин) и на пламя
«выливают» диоксид углерода из третьего цилиндра.
4) В пробирку с газоотводной трубкой вносят 3 мл муравьиной кислоты и добавляют 1 мл концентрированной серной кислоты под тягой), закрывают пробкой и пропускают выделяющийся оксид углерода через подогретую на спиртовке трубку с помещенным внутри оксидом меди (II). Наблюдают за покраснением черного порошка оксида меди.
5) Оксид углерода, полученный в п.4, пропускают через 0,1 н раствор KMnO4 в кислой среде. Наблюдают за изменением окраски раствора.
2. Растворимость карбонатов.В пробирке с газоотводной трубкой получают СО2, действуя на кусочек мрамора соляной кислотой. Трубку помещают в стаканчик с известковой водой и пропускают СО2 до тех пор, пока выпавший вначале осадок не растворится.
3. Гидролиз карбонатов.Исследуют характер среды в 5 %-ых растворах Na2CO3, NaНСО3 и (NН4)2СОз.
4. Термическая устойчивость карбонатов.В двух пробирках с газоотводными трубками нагревают СаСО3 и Nа2СОз. Наблюдают за появлением ионов СОз 2- в известковой воде, в которую погружают газоотводную трубку.
5. Растворимость карбонатов. К 5 пробиркам, содержащим соли А1 3+, Са 2+, Ва 2+, Рb 2+, Zn 2+ добавляют по 1 мл 10 %-го раствора карбоната аммония. Проверяют отношение выпавших осадков к разбавленной соляной кислоте.
6. Гидролиз силикатов.
а) проверяют на лакмус раствор силиката натрия.
б) к силикату натрия добавляют равный объем раствора хлорида аммония. Какие вещества
образуются?
в) в пробирку помещают немного SiO2 и порошок Mg. Нагревают на спиртовке. После охлаждения добавляют несколько капель концентрированной соляной кислоты. Наблюдают за горением. На дне собрался кремний.
г) к кремниюдобавляют 30%-ую щелочь. Проверяют выделение водорода.
д) в трёх пробирках к раствору NaSiO3 добавляют по 2 капли растворов солей Co2+, Ni2+, и Cu2+. Наблюдают образование нитей силикатов.
Сравнение силы угольной и кремниевой кислот. Через раствор силиката натрия пропускают углекислый газ. Наблюдают за помутнением раствора.Вопросы и задания:
1. Объясните сущность гидролиза силиката натрия. Составьте уравнение реакции в молекулярной и ионных формах.
2. Сравнить гидролиз силикатов с гидролизом карбонатов, если обнаружится сходство, объяснить его.
3. Почему карбонаты и силикаты легко гидролизуются?
4. Какой объем оксида углерода (IV) израсходуется на реакцию с 20 мл 10% раствора едкого натра при условии образования кислой соли.
5. Какая соль и в каком количестве образуется при пропускании 5,6 л СО2 через 200 г 5% раствора едкого натра?
ЛАБОРАТОРНАЯ РАБОТА № 7-8 (4 ч.)
Тема: МЕТАЛЛЫ
Цель работы - изучить химические свойства металлов и их соединений.
Опыт 1. Амфотерные свойства алюминия.
Налейте в первую пробирку разбавленную серную кислоту, во вторую — соляную, в третью — азотную. Опустите в каждую пробирку по грануле алюминия.
Вопросы и задания:
1. Есть ли разница в протекании реакции в этих трех пробирках? В чем она заключается?
2. Чем объясняется такая разница в ходе реакции?
3. Можно ли сказать на основании этого опыта, что алюминий обладает металлическими свойствами и более активен, чем водород?
4. Напишите уравнение протекающих реакций.
Налейте в пробирку концентрированный (30%) раствор едкого натра и опустите туда алюминиевую гранулу.
Вопросы и задания:
5. Что вы можете сказать о выделяющемся газе?
6. Какими свойствами алюминия можно объяснить вытеснение им водорода из кислоты и из щелочи?
7. Напишите уравнение протекающей реакции.
Опыт 2. Амфотерные свойства гидроксида алюминия.
Налейте в пробирку 10 капель какой-нибудь растворимой соли алюминия и добавьте 1—2 капли разбавленной щелочи до образования легкого студенистого осадка гидроксида алюминия. Разделите содержимое пробирки с осадком пополам и добавьте к одной половине избыток соляной кислоты, а к другой — избыток едкого натра.
Вопросы и задания:
1. Напишите уравнение реакции получения гидроксида алюминия.
2. Что происходит с осадком в обеих пробирках при добавлении щелочи и кислоты?
3. Почему осадок растворяется в щелочи? Напишите уравнение реакции.
4. Почему осадок растворяется в кислоте? Напишите уравнение реакции.
5. Сделайте вывод о характере свойств гидроксида алюминия, исходя из проделанного опыта?
Опыт 3. Отношение меди к кислотам.
Цель опыта — проанализировать и сравнить поведение металлической меди в разных кислотах и объяснить причины различия. Прежде чем выполнять опыт, вспомните, какое положение занимает медь в ряду напряжений. Может ли она вытеснять водород из кислот?
Возьмите кусочек медной стружки, слегка нагрейте ее и нанесите на нее в трех разных местах по капле разбавленной серной, разбавленной соляной и разбавленной азотной кислоты. Внимательно наблюдайте некоторое время за поведением капель.
Проделайте тот же опыт, но вместо разбавленных кислот возьмите концентрированные. Сравните полученные результаты с предыдущим вариантом опыта.
Вопросы и задания:
1. В каком случае наблюдаются изменения? Почему?
2. Отмечается ли выделение газов? Если да, то где оно наиболее интенсивное?
3. Составьте уравнение протекающих реакций и объясните, являются ли они окислительно-восстановительными?
4. Сделайте вывод об отношении меди к концентрированным и разбавленным кислотам в связи с ее положением в электрохимическом ряду напряжений.
5. 40,625 г смеси опилок меди и цинка обработали соляной кислотой, в результате чего выделилось 5,6 л водорода. Каков процентный состав смеси?
6. Сколько 5 н. азотной кислоты израсходуется на реакцию с 16 г меди, если в процессе реакции выделяется оксид азота(II).
Опыт 4. Восстановление оксида меди (II) углем.
Поместите в пробирку 1 микрошпатель порошка оксида меди (II) и 1 микрошпатель мелко растертого древесного угля, хорошо перемешайте. Обратите внимание на цвет смеси. Сильно нагрейте в пробирке приготовленную смесь.
Вопросы и задания:
1. Меняется ли окраска? Объясните причину.
2. Составьте химическое уравнение.
3. Как экспериментально доказать, что оксид меди (II) —основной оксид.
3. Предложите способ получения из оксида меди (II) гидроксида меди (II).
Опыт 5. Гидролиз солей меди.
Цель опыта — изучить тип гидролиза растворимых солей меди и его особенности.
На синюю лакмусовую бумажку нанесите каплю сильно разбавленного раствора хлорида меди (II).
Вопросы и задания:
1. Изменяется ли окраска лакмуса? Почему?
2. Составьте уравнение реакции, объясняющее это явление.
В пробирку поместите 3—4 капли раствора сульфата меди (II) и добавьте 2—3 капли раствора карбоната натрия. Выпавший зеленый осадок представляет собой гидроксокарбонат меди (СuОН)2СО3.
Вопросы и задания:
3. Почему в результате реакции образуется именно эта соль, а не СuСОз?
4. Сделайте вывод о подверженности солей меди гидролизу.
5. Можно ли полученный гидроксокарбонат меди (II) перевести снова в сульфат меди (II), напишите уравнение этой реакции.
6. Осуществить следующие превращения:
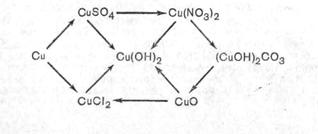
7. Какой должна быть реакция среды в растворе нитрата меди (II)?
8. Какой объем 0,5 н. серной кислоты израсходуется на реакцию с 20 г оксида меди (II)?
Опыт 6. Отношение цинка к кислотам и щелочам.
Цель опыта— изучить поведение цинка в кислотах и щелочах и сравнить его с алюминием.
Поместите в две пробирки по микрошпателю цинковой пыли и прилейте в одну 10 капель соляной кислоты, а в другую — столько же раствора щелочи. Пробирку со щелочью слегка нагрейте.
Вопросы и задания:
1. В какой пробирке энергичнее выделяется водород?
2. О каком свойстве цинка это говорит? Составьте уравнения соответствующих реакций.
3. Укажите еще один изученный вами элемент с аналогичными свойствами.
4. Сделайте заключение о поведении цинка в кислотах и щелочах.
Опыт 7. Получение гидроксида цинка и изучение его свойств.
В предыдущем опыте вы убедились в амфотерных свойствах цинка.
Можно ли предположить эти свойства у его гидроксида? Как это проверить?
Сначала получите гидроксид цинка. Поместите в пробирку 10 капель раствора любой соли цинка и добавьте 2—3 капли (не больше!) разбавленного раствора щелочи.
Вопросы и задания: какие изменения наблюдаются; составьте уравнение реакции.
Перенесите пипеткой половину раствора с осадком в другую пробирку и добавьте 5—10 капель щелочи. Хорошо размешайте.
Вопросы и задания: что происходит с осадком; составьте уравнение реакции образования цинката.
В пробирку с оставшимся гидроксидом цинка добавьте 5—10 капель кислоты.
Вопросы и задания: какие происходят изменения; составьте уравнение реакции и назовите образовавшееся соединение цинка. Сделайте вывод о свойствах гидроксида цинка, его отношении к кислотам и щелочам.
В пробирку с цинкатом натрия добавляйте по каплям разбавленный раствор соляной кислоты. После появления помутнения добавление прекратите.
Вопросы и задания: какое вещество вызвало это помутнение; обоснуйте свой ответ уравнением реакции.
Задание: получите известным вам способом цинкат калия, а затем выделите из него гидроксид цинка.
Опыт 8. Гидролиз солей цинка.
Цель опыта — наблюдать гидролиз солей цинка, определить, по какому типу он протекает, и сравнить его с гидролизом солей меди, алюминия, натрия.
Нанесите каплю разбавленного раствора сульфата цинка на синюю лакмусовую бумажку.
Вопросы и задания: объясните изменение окраски лакмуса, обосновав ответ уравнением реакции гидролиза.
Поместите в пробирку 5—6 капель раствора соли цинка и добавьте 1—2 капли раствора карбоната натрия. Выделяется ли при этом газ? Обратите внимание на цвет выпавшего осадка гидроксокарбоната цинка.
Вопросы и задания: составьте уравнение реакции и объясните, почему вместо карбоната цинка образуется гидроксокарбонат. Какой газ при этом выделился?
Вопросы и задания:
3.Почему для получения карбоната цинка реакцией обмена используют не карбонат натрия, а гидрокарбонат?
4. Как осуществить следующие превращения:
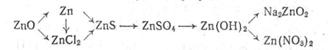
5. Сколько технического цинка, содержащего 4% примесей, и сколько 30% соляной кислоты потребуется для приготовления 50 кг 45% раствора хлорида цинка?
6. Сколько цинка и серной кислоты можно получить из 1 т цинковой обманки, содержащей 85% сульфида цинка?
ЛАБОРАТОРНАЯ РАБОТА № 9 (2 ч.)
Тема: Железо.
1. Отношение железа к кислотам и щелочам:
а) В три пробирки помещают железную стружку. В каждую добавляют по 2 мл 2н НСl, Н2SО4, НNО3. После окончания реакций в каждую пробирку вводят по 2 капли 0,01н КSСN. Наблюдать появление окраски.
б) к сульфату железа (II) добавляют по 1 мл 2н NaОН. Наблюдают за изменением окраски осадка.
в) в пробирку помещают З мл соли Fе(III), добавляют 2 мл 2н NaОН. Выпавший осадок делят на три части.
К первой порции добавляют 1 мл 2н НСl,
ко второй - 2 мл 2н NaОН.
Третью пробу помещают в тигель, добавляют на кончике шпателя кристаллический Nа2СО3 и нагревают на спиртовке до упаривания воды. Остаток охлаждают. Добавляют несколько капель воды, всё переносят в пробирку и наблюдают за гидролизом феррита.
2. Гидролиз солей железа:
а) 2-3 кристаллика FеSО4 помещают на предметное стекло и добавляют 2-3 капли воды. После растворения проверяют рН раствора индикаторной бумажкой.
б) в 2 пробирки помещают раствор FеCl3. В первой проверяют рН раствора, а вторую нагревают на водяной бане в течение 5 мин. Проверяют рН. Изменился ли рН во второй пробирке?
3. Отношение железа к сульфид-иону:
а) в 2 пробирки помещают по несколько кристалликов FеSО4 и добавляют по 2 капли воды. В первую пробирку вносят несколько капель сероводородной воды, в другую – (NH4)2S. Наблюдают за выпадением осадка. Проверить растворимость FеS в НСl и Н2SО4.
б) в 2 пробирки вносят по 3 капли раствора FеС13. Проделывают те же операции, что и в опыте а). Наблюдают за цветом осадка.
4. Качественные реакции на катионы железа.
а) К соли Fе2+ добавляют 2 капли красной кровяной соли К3 [Fе(СN)6]. Оставить.
б) К соли Fе²+ добавляют 2 капли жёлтой кровяной соли К4 [Fе(СN)6]. Оставить.
в) К соли Fе3+ добавляют 2 капли 0,01 н раствора КSСN.
Во всех случаях наблюдают за цветом осадка.
г) В 2 пробирки помещают по 3 кристаллика FеSО4. В первую добавляют 1-2 капли воды и 1 мл 0,01 н КSСN. Во вторую - 1 каплю концентрированной НNО3 и 2 капли 0,01 н КSСN. Наблюдают за окраской раствора в обоих случаях.
д) В 2 пробирки помещают 2-3 кристаллика FеSО4. В первую вносят1-2 капли воды, во вторую - 1-2 капли Н2SО4. Затем в обе пробирки прибавляют 2 капли Н2О2 (3%-ой) и по 2 капли КSСN. Наблюдать за окраской растворов. Проделать то же в щелочном растворе.
5. Комплексные соединения железа.
а) К соли железа (III) добавить 2 капли 0,01 н роданида калия (или аммония). Разделить на две порции. К первой добавляют Н3 РО4, ко второй - фторид калия или аммония. Следить за изменением окраски.
К оставленным в опытах а) и б) добавить 2 н щелочь. Выпадают ли осадки?
3. Окислительно-восстановительные свойства солей железа.
а) Fе2++ Вr-вода → Fе3+ (доказать)
б) Fе3++ Nа2SО3 → Fе2+ (доказать)
в) В пробирку вносят кристаллик КОН, добавляют раствор FеСl3, пропускают хлор (хлорную воду). Наблюдают окраску раствора.
Разделяют на три порции.
В первую пробирку вносят хлорид бария,
во вторую - серную кислоту,
в третью - сульфид аммония.
Наблюдают за изменениями в растворах.
Во всех опытах составить уравнения реакций и дать объяснения происходящим процессам.
ЛАБОРАТОРНАЯ РАБОТА № 10(4 ч.)
Тема: Цинк, кадмий, ртуть.
1. Отношение к кислотам и щелочам.
а) В четыре пробирки помещают по грануле цинка. В первую пробирку добавляют 3 мл 2н Н2SO4, во вторую - 3 мл 2н НСl, в третью - 3 мл 0,5н НNО3, в четвёртую - 2мл концентрированной азотной кислоты. В первой и второй пробирках проверяют выделение водорода, в третьей - лакмусовой бумажкой определяют выделение аммиака, в четвертой наблюдают выделение бурого газа NО2.
То же проделать с металлическим кадмием.
б) К Zn-порошку добавить 2 мл 2н NаОН. Подогреть на спиртовке. Наблюдать горение водорода.
Проверить растворимость Cd в щелочи при нагревании.
в) Проверить растворимость Zn в концентрированном (25%) растворе аммиака.
2.Взаимодействие с кислородом и серой.
а) В ложечку для сжигания помещают немного Zn-пыли, подогревают на спиртовке до появления свечения и быстро переносят в цилиндр с кислородом. Наблюдают горение цинка.
б) В ступке растирают цинковую пыль с несколькими кристалликами серы. Затем к смеси подносят зажжённую лучинку. Наблюдают вспышку. Затем добавляют 3 капли воды и по свинцовой бумажке определяют выделение сероводорода.
3. Активность цинка.
На две гранулы цинка помещают по капле растворов CdSO4, CuSO4 и НgSO4. Наблюдают изменение окраски цинковой гранулы.
4. Амфотерность.
а) К 2 мл раствора сульфата цинка по каплям добавляют 1 мл 2н щелочи. Наблюдают выпадение осадка. Делят осадок на две части. К одной части добавляют избыток щёлочи, ко второй - 1 мл 2н соляной кислоты. Наблюдают за растворением осадка.
То же проделывают с раствором CdSO4.
б) К осадку Cd(OH)2 добавляют твёрдую щёлочь и нагревают на спиртовке. Что происходит?
4.Отношение гидроксндов к аммиаку.
а) Получить гидроксиды Zn и Cd по п. а). К осадкам добавить по 5 капель 25%-го аммиака. Что наблюдается?
б) К обоим осадкам добавить по 3 капли насыщенного раствора NH4Cl.
5. Отношение оксида цинка к нагреванию.
В пробирку на кончике шпателя вносят оксид цинка и нагревают на спиртовке. Наблюдают за изменением окраски при нагревании и последующем охлаждении пробирки.
6. Свойства сульфидов.
Получить сульфиды Cd ²+, Zn²+ и Hg²+, добавив к соответствующим сульфатам на на предметном стекле по 1 капле раствора Nа2S. Наблюдать цвета сульфидов. Проверить растворимость сульфидов в НСl и в НNО3.
7. Гидролиз.
Универсальной индикаторной бумажкой проверить среду в растворах сульфатов цинка, кадмия и ртути (II). Составить уравнения гидролиза.
8. Свойства карбонатов цинка и кадмия.
К растворам сульфатов Zn и Сd добавляют на кончике шпателя карбонат натрия и нагревают на спиртовке в течение 5 минут. Затем содержимое переносят в тигли и прокаливают досуха на плитке. Наблюдают за изменением окраски.
9.Окислительно-восстановительные свойства солей ртути (I) и ртути (II).
а) К сульфату ртути (II) добавляют кристаллический SnС12 и нагревают на водяной бане. Наблюдают за появлением белого осадка.
б) Медную пластинку (или монетку) обрабатывают азотной кислотой до появления бурого газа. Кислоту смывают водой и протирают ватой. На обработанное место помещают 1 каплю раствора соли ртути. Наблюдают за выделением металлической ртути.
в) Соль одновалентной ртути обрабатывают 2 мл концентрированной азотной кислоты при нагревании в течение 5 минут. К раствору добавляют 1 каплю раствора NаС1. Что наблюдается?
г) К раствору соли Hg²+ добавляют 3 капли раствора КI. К полученному осадку добавляют кристаллический КI до растворения осадка. Раствор делят на две части.
К первой части добавляют несколько капель раствора Nа2S, а ко второй - раствор нитрата серебра. Наблюдают за изменениями в пробирках. Дать объяснения происходящему. Составить все уравнения реакций. Что можно сказать об устойчивости ртутного комплекса
[HgI4]²- ?
1.8 Учебно-методическое обеспечение дисциплины.
1.8.1 Рекомендуемая литература
ОСНОВНАЯ ЛИТЕРАТУРА
1. С, и др. Лабораторные и семинарские занятия по общей и неорганической химии.- М.: Академия,1999.-360с.
2. Ахметов и неорганическая химия: учебник для химико-технол. Спец. Вузов.- 4-е изд., - М.: Высшая школа, 2001.-743с.
3. Глинка химия.- Л.: Химия, 1973.
4. Мень к контрольным и лабораторным работам по общей и неорганической химии.- М.: МГПУ, 2004.
5. , , Неорганическая химия.- Ленинград: Химия, 1981.
6. Курс неорганической химии. - М.: Мир,1972.
ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА
1. Глинка и упражнения по общей химии.- Ленинград: Химия, 1988.
2. Гольбрайх задач и упражнений по химии.- М.: Высшая школа, 1984.
3. , Дракин вещества.- М.: Высшая школа, 1976.
4. Уилкинсон Дж. Основы неорганической химии.- М.: Мир, 1979.-677с.
5. Николаев химия.- М.: Просвещение, 1970.
6. , Цветков химия.- Высшая школа, 1994.-542с.
7. Химия: Справочник / Под ред. , .- М.: Химия, 1989.-647с.
1.9 Материально-техническое обеспечение дисциплины
1.9.1. Перечень используемых технических средств
Лабораторная посуда: пробирки, мерные цилиндры, колбы конические, круглодонные, химические стаканы, воронки.
Лабораторное оборудование: спиртовки, лабораторные штативы, штативы для пробирок, планшетки для капельных реакций, подносы, зажимы-пробиркодержатели, шпатели - ложечки, подставки для реактивов, приборы для получения газов, прибор для измерения скорости химических реакций.
Наборы химических реактивов (неорганическая химия): металлы и неметаллы, кислоты, основания, хлориды, сульфаты, карбонаты, нитраты, фосфаты, кислые соли, индикаторы.
1.9.2. Перечень используемых пособий.
«Основные понятия химии» (комплект фолий с сопроводительным текстом)/Под ред , . М.: Росучприбор.
Периодическая система химических элементов .
Ряд активности металлов.
Таблица «Растворимость солей, кислот и оснований в воде»
Таблица «Плотность растворов щелочей и кислот»
Таблица «Относительная электроотрицательность атомов элементов»
Плакаты.
Видеофильмы.
1.10 Примерные зачетные тестовые задания.
Вариант 1.
1. Определить нормальность раствора, содержащего 15 г Са(НСО3)г в 100 мл.
2. Сколько атомов содержится в 16 г кислорода?
3. В лаборатории имеется гидрид кальция, оксид меди (П), 98-% серная кислота и вода. Сколько граммов каждого вещества надо взять для получения 2.24 л сернистого газа (н. у.)?
4. При обработке 11,14 г хлоридов калия и цинка серной кислотой и выпаривании досуха образовалось 13,14 г остатка. Определить состав исходной и образовавшейся смеси.
5. Zn + NaNO2 + NaOH -----> Na2 [Zn(OH)4] +NH3 + ...
Вариант 2.
1. Для нейтрализации 200 мл 0,5 M раствора азотной кислоты израсходовали 6,26 г смеси карбонатов калия и натрия. Определить состав смеси солей.
2. Анализ газа показал, что соединение содержит 5,9 % водорода и серу. Литр этого газа весит 1,52 г (н. у.). Определить, какой это газ.
3. Сколько молекул содержится в 7 г аммиака?
4. Чему равен эквивалент КМnО4 при переходе его в Мn+2?
КМnО4 + SO2 + Н2О → MnO2 + SO4 2+ + ...
Вариант 3.
1. Какой объем SO2 выделится при сжигании серы в 5 л кислорода при выходе 80%?
2. При разложении 80 г одноосновной кислоты, образованной пятивалентным элементом, получился 71 г ангидрида этой кислоты. Каким элементом образована кислота?
3. При растворении в растворе щелочи 2 г сплава алюминия с цинком выделилось 1.904 л водорода (н. у.). Определить состав сплава.
4. При окислении 12 г металла получено 16.8 г продукта реакции. Какой металл был окислен и какой объём кислорода (н. у.) при этом израсходовали?
5. Fe2++ К2Сг2О7 + Н+ → Fe3++ Сг3++....
Вариант 4.
1. При разложении 8.06 г смеси бертолетовой соли и перманганата калия выделилось 1.568 л кислорода (н. у.). Определить состав исходной смеси.
2. Чему равна молярность 10%-й серной кислоты (ρ =1.11 г/мл)?
3. Определить массовую долю бромида калия, если из 200 г раствора выделилось 8 г брома. Какой объем хлора при Р=101.3 кПа и температуре 27°С при этом израсходовали?
4. Через озонатор пропущено 15 л кислорода, 10% которого перешло в озон. Какой объём занимает озонированный кислород?
5. СrС13 + Н2О2 + NaOH → СrO4 2- + ...
Вариант 5.
1. Определить концентрацию в растворе иодида калия, если известно, что при обработке 100 г этого раствора дихроматом калия в кислой среде выделилось 76.2 г иода.
2. При обработке соляной кислотой 9.92 смеси карбидов кальция и алюминия образовалось 4.48 л смеси метана и ацетилена (н. у.). Определить состав смеси карбидов.
3. Сколько моль азотной кислоты можно получить при окислении 5 л аммиака (Н. У.)?
4. Сколько г серы прореагирует с газом, выделившимся при взаимодействии 6.5 г цинка с избытком разбавленной серной кислоты, если используется только 80% газа?
5. PbS + Н2О2 → PbSO4 + ....
Вариант 6.
1. К раствору, содержащему 5.48 г сульфата и силиката натрия, прибавили избыток хлорида бария, в результате чего образовалось 9.12 г смеси силиката и сульфата бария. Определить состав исходной и образовавшейся смеси.
2. Сколько молей кислорода нужно для сжигания 16 кг серы?
3. При растворении в воде 1.6 г металла выделилось 0.896 л водорода (н. у.). Что это за металл?
4. Определить плотность газовой смеси по гелию, содержащей 20? Моноксида углерода, 20% азота и 60% водорода.
5. FeS2 + О2 →
Вариант 7.
1. Определить объемы кислорода и воздуха, необходимые для сжигания 30 л пропан-бутановой смеси, содержащей 60% пропана и 40% бутана.
2. В 500 мл воды растворили 23 г металлического натрия. Рассчитать молярность полученного раствора.
3. Чему равна нормальность 4М Н3РО4 в реакции нейтрализации.
4. Вычислить, сколько граммов хлорида натрия и 70%-ой серной кислоты прореагировали без нагревания, если объём выделившегося газа составил 4.48 л (н. у.).
5. Н2О2 + KJ →
Вариант 8.
В лаборатории имеются хлорид калия, перманганат калия, гидроксид калия, 98%-ная серная кислота и вода. Как можно, используя эти реактивы, получить жавелевую воду? При термическом разложении 25 г карбоната кальция образовалось 17.3 г твердого остатка. Определить степень разложения карбоната. Сколько атомов содержится в 4 л азота (н. у.)? Чему равна нормальность 2 М раствора серной кислоты в реакции образования гидросульфата калия? NaBr + NaBrO3 + H2SO4 → Br2 + ....Вариант 9.
В лаборатории имеются ВаО2, бертолетова соль и перманганат калия. Какое из них при термическом разложении в пересчете на одну и ту же массу даст наибольшее количество кислорода? При нагревании 6.06 г нитрата калия образовалось 5.34 г твердого остатка. Определить степень разложения нитрата калия. Смесь Mg и его оксида массой 5.1 г обработали соляной кислотой. При этом выделилось 3.74 л водорода (н. у.). Определить процентный состав смеси. Чему равна нормальность 10%-го раствора сульфата алюминия (ρ = 1.12 г/л)? НСlO + НС1 →Вариант 10.
Вариант 11.
1. В лаборатории имеется гидрид кальция, оксид меди (II), 98%-ная серная кислота и вода. Сколько граммов каждого вещества надо взять для получения 2.24 л сернистого газа (н. у.)?
2. Определить нормальность раствора, содержащего 15 г Са(НСО3)2 в 100 мл.
3. При обработке 11,14 г хлоридов калия и цинка серной кислотой и выпаривании досуха образовалось 13.14 г остатка. Определить состав исходной и образовавшейся смеси.
4. Zn + NaNO2 + NaOH → Na2 [Zn(OH)4] +NH3 + ...
5. Сколько атомов содержится в 16 г кислорода?
Вариант 12.
1. Для нейтрализации 200 мл 0.5 М раствора азотной кислоты израсходовали 6.26 г карбонатов калия и натрия. Определить состав смеси солей.
2. Сколько молекул содержится в 7 г аммиака?
3. Анализ газа показал, что соединение содержит 5.9% водорода и серу. Литр этого газа весит 1.52 г (н. у.) Определить, какой это газ.
4. KMnO4+ SO2 + Н2О → MnO2 + SO42- + ....
5. Чему равен эквивалент КМnО4 при переходе его в Мn+2?
Вариант 13.
1. При растворении в растворе щелочи 2 г сплава алюминия с цинком выделилось 1.904 л водорода (н. у.). Определить состав сплава.
2. При разложении 80 г одноосновной кислоты, образованной пятивалентным элементом, получился 71 г ангидрида этой кислоты. Каким элементом образована кислота?
3. Fe 2+ + К2Сr2О7 + Н+ → Fe 3+ + Cr 3+ +...
4. Какой объем SO2 выделится при сжигании серы в 5 л кислорода при выходе 80%?
5. При окислении 12 г металла получено 16.8 г продукта реакции. Какой металл был окислен и какой объём кислорода (н. у.) при этом израсходовали?
Вариант 14.
1. Определить массовую долю бромида калия, если из 200 г раствора выделилось 8 г брома. Какой объем хлора при Р-101.3 кПа и температуре 27°С при этом израсходовали?
2. Чему равна молярность 10%-ой серной кислоты (ρ = 1.11 г/мл)?
3. При разложении 8.06 г смеси бертолетовой соли и перманганата калия выделилось 1.568 л кислорода (н. у.). Определить состав исходной смеси.
4. СrС13 + Н2О2 + NaOH → СrO4 2- + ...
5. Через озонатор пропущено 15 л кислорода, 10% которого перешло в озон. Какой объём занимает озонированный кислород?
Вариант 15.
1. Сколько моль азотной кислоты можно получить при окислении 5 л аммиака (н. у.)?
2. Сколько г серы прореагирует с газом, выделившимся при взаимодействии 6.5 г цинка с избытком разбавленной серной кислоты, если используется только 80% газа?
3. Определить концентрацию в растворе иодида калия, если известно, что при обработке 100 г этого раствора дихроматом калия в кислой среде выделилось 76.2 г иода.
4. PbS + Н2О2 → PbSO4 + ...
5. При обработке соляной кислотой 9.92 смеси карбидов кальция и алюминия образовалось 4.48 л смеси метана и ацетилена (н. у.). Определить состав смеси карбидов.
Вариант 16.
1. При растворении в воде 1.6 г металла выделилось 0.896 л водорода (н. у.). Что это за металл?
2. Определить плотность газовой смеси по гелию, содержащей 20% моноксида углерода, 20% азота и 60% водорода.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



