3. К раствору, содержащему 5.48 г сульфата и силиката натрия, прибавили избыток хлорида бария, в результате чего образовалось 9.12 г смеси силиката и сульфата бария. Определить состав исходной и образовавшейся смеси.
4. FeS2 + О2 →
5. Сколько молей кислорода нужно для сжигания 16 кг серы?
Вариант 17.
1. Определить объемы кислорода и воздуха, необходимые для сжигания 30 л пропан-бутановой смеси, содержащей 60% пропана и 40% бутана.
2. Вычислить, сколько граммов хлорида натрия и 70%-ой серной кислоты прореагировали без нагревания, если объём выделившегося газа составил 5.26 л (н. у.).
3. Н2О2 + KJ →
4. В 500 мл воды растворили 23 г металлического натрия. Рассчитать молярность полученного раствора.
5. Чему равна нормальность 4М Н3РО4 в реакции нейтрализации.
Вариант 18.
1. NaBr + NaBrO3 + H2SO4 → Вr2 + ....
2. В лаборатории имеются хлорид калия, перманганат калия, гидроксид калия, 98%-ая серная кислота и вода. Как можно, используя эти реактивы, получить жавелевую воду?
3. Чему равна нормальность 2 М раствора серной кислоты в реакции образования гидросульфата калия?
4. Сколько атомов содержится в 4 л азота (н. у.)?
5. При термическом разложении 25 г карбоната кальция образовалось 17.3 г твердого остатка. Определить степень разложения карбоната.
Вариант 19.
1. Чему равна нормальность 10%-го раствора сульфата алюминия (ρ = 1.12 г/л)?
2. Смесь Mg и его оксида массой 5.1 г обработали соляной кислотой. При этом выделилось 3.74 л водорода (н. у.). Определить процентный состав смеси.
3. В лаборатории имеются ВаО2, бертолетова соль и перманганат калия. Какое из них при термическом разложении в пересчете на одну и ту же массу даст наибольшее количество кислорода?
4. При нагревании 6.06 г нитрата калия образовалось 5.34 г твердого остатка. Определить степень разложения нитрата калия.
5. НСlO + НС1 →
Вариант 20.
1. При взрыве смеси, полученной из одного объема неизвестного газа и двух объемов кислорода, образуется два объема СО2 и один объем азота. Найти молекулярную формулу газа.
2. Сколько потребуется сульфида железа (П) и 7.3% - ой соляной кислоты (считая 50%-ый избыток), чтобы при пропускании газа, образующегося при их взаимодействии, через раствор нитрата свинца выпало 2.39 г осадка?
3. Масса 3.28 л смеси моноксида углерода и метана при 27°С и 3.75 атм. равна 10.4 г. Определить количество воздуха, необходимое для сжигания данной смеси.
4. Чему равен эквивалент BiOH(NO3)2?
5. Zn + HNO3 (разб.) → NH3 + ....
Вариант 21.
1. Определить нормальность раствора, содержащего 15 г Са(НСО3)2 в 100 мл.
2. Сколько атомов содержится в 16 г кислорода?
3. В лаборатории имеется гидрид кальция, оксид меди (П), 98%-ая серная кислота и вода. Сколько граммов каждого вещества надо взять для получения 2.24 л сернистого газа (н. у.)?
4. При обработке 11,14 г хлоридов калия и цинка серной кислотой и выпаривании досуха образовалось 13.14 г остатка. Определить состав исходной и образовавшейся смеси.
5. Zn + NaNO2 + NaOH → Na2 [Za(OH)4] +NH3 + ...
Вариант 22.
1. Для нейтрализации 200 мл 0.5 M раствора азотной кислоты израсходовали 6.26 г смеси карбонатов калия и натрия. Определить состав смеси солей.
2. Анализ газа показал, что соединение содержит 5.9% водорода и серу. Литр этого газа весит 1.52 г (н. у.) Определить, какой это газ.
3. Сколько молекул содержится в 7 г аммиака?
4. Чему равен эквивалент КМnO4 при переходе его в Мn+2?
5. KMnO4 + SO2 + Н2О → MnO2 + SO4 2-....
Вариант 23.
1. Какой объем SO2 выделится при сжигании серы в 5 л кислорода при выходе 80%?
2. При разложении 80 г одноосновной кислоты, образованной пятивалентным элементом, получился 71 г ангидрида этой кислоты. Каким элементом образована кислота?
3. При растворении в растворе щелочи 2 г сплава алюминия с цинком выделилось 1.904 л водорода (н. у.). Определить состав сплава.
4. При окислении 12 г металла получено 16.8 г продукта реакции. Какой металл был окислен и какой объём кислорода (н. у.) при этом израсходовали?
5. Fe2+ + К2Сr2О7 + Н+ → Fe3+ + Сr3+ +....
Вариант 24.
1. При разложении 8.06 г смеси бертолетовой соли и перманганата калия выделилось 1.568 л кислорода (н. у.). Определить состав исходной смеси.
2. Чему равна молярность 10%-ой серной кислоты (ρ =1.11 г/мл)?
3. Определить массовую долю бромида калия, если из 200 г раствора выделилось 8 г брома. Какой объем хлора при Р=101.3 кПа и температуре 27°С при этом израсходовали?
4. Через озонатор пропущено 15 л кислорода, 10% которого перешло в озон. Какой объём занимает озонированный кислород?
5. СrС13 + Н2О2 + NaOH → СrО42- + ...
Вариант 25.
1. Определить концентрацию в растворе иодида калия, если известно, что при обработке 100 г этого раствора дихроматом калия в кислой среде выделилось 76.2 г иода.
2. При обработке соляной кислотой 9.92 смеси карбидов кальция и алюминия образовалось 4.48 л смеси метана и ацетилена (н. у.). Определить состав смеси карбидов.
3. Сколько моль азотной кислоты можно получить при окислении 5 л аммиака (н. у.)?
4. Сколько г серы прореагирует с газом, выделившимся при взаимодействии 6.5 г цинка с избытком разбавленной серной кислоты, если используется только 80% газа?
5. PbS + Н2О2 → PbSO4 + ....
Вариант 26.
1. К раствору, содержащему 5.48 г сульфата и силиката натрия, прибавили избыток хлорида бария, в результате чего образовалось 9.12 г смеси силиката и сульфата бария. Определить состав исходной и образовавшейся смеси.
2. Сколько молей кислорода нужно для сжигания 16 кг серы?
3. При растворении в воде 1.6 г металла выделилось 0.896 л водорода (н. у.). Что это за металл?
4. Определить плотность газовой смеси по гелию, содержащей 20% моноксида углерода, 20% азота и 60% водорода.
5. FeS2 + О2 →
Вариант 27.
1. Определить объемы кислорода и воздуха, необходимые для сжигания 30 л пропан-бутановой смеси, содержащей 60% пропана и 40% бутана.
2. В 500 мл воды растворили 23 г металлического натрия. Рассчитать молярность полученного раствора.
3. Чему равна нормальность 4М Н3РО4 в реакции нейтрализации.
4. Вычислить, сколько граммов хлорида натрия и 70%-ой серной кислоты прореагировали без нагревания, если объём выделившегося газа составил 4.26л (н. у.).
5. Н2О2 + KJ →
Вариант 28.
1. В лаборатории имеются хлорид калия, перманганат калия, гидроксид калия, 98%-ая серная кислота и вода. Как можно, используя эти реактивы, получить жавелевую воду?
2. При термическом разложении 25 г карбоната кальция образовалось 17.3 г твердого остатка. Определить степень разложения карбоната.
3. Сколько атомов содержится в 4 л азота (н. у.)?
4. Чему равна нормальность 2 М раствора серной кислоты в реакции образования гидросульфата калия?
5. NaBr + NaBrO3 + H2SO4 → Вr2 + ....
1.11 Примерный перечень вопросов к экзамену.
Водород в природе. Получение водорода. Свойства и применение водорода. Перекись водорода. Получение, свойства, применение. Кремний в природе. Получение и свойства кремния. Соединения кремния с водородом и галогенами. Диоксид кремния. Получение, применение, свойства. Стекло. Кремниевые кислоты и их соли. Кислород в природе. Воздух. Получение и свойства кислорода. Озон. Получение, свойства. Сера в природе. Получение серы. Свойства и применение серы. Сероводород. Получение и свойства. Диоксид серы. Сернистая кислота. Получение и свойства. Оксид серы (VI). Серная кислота. Получение и свойства. Селен. Теллур. Получение, свойства. Галогены в природе. Физические свойства. Химические свойства галогенов. Получение и применение галогенов. Соединения галогенов с водородом. Кислородсодержащие соединения галогенов. Углерод в природе. Аллотропия углерода. Химические свойства углерода. Диоксид углерода. Угольная кислота. Угарный газ. Соединения углерода с серой и азотом. Азот. Получение и свойства. Аммиак. Соли аммония. Фиксация атмосферного азота. Оксиды азота. Азотная кислота. Круговорот азота в природе. Фосфор. Получение и свойства. Фосфор в природе. Оксиды и кислоты фосфора. Минеральные удобрения. Физические и химические свойства металлов. Кристаллическое строение металлов. Сплавы. Коррозия металлов. Щелочные металлы. Получение и свойства. Комплексные соединения. Алюминий. Получение и свойства. Хром. Получение и свойства. Марганец. Получение и свойства. Железо в природе. Физические свойства железа. Сплавы железа. Химические свойства железа. Соединения железа. Общая характеристика платиновых металлов.1.11 Примерный перечень заданий экзамену.
1. При термическом разложении 25 г карбоната кальция образовалось 17.3 г твердого остатка. Определить степень разложения карбоната.
2. При обработке 11.14 г хлоридов калия и цинка серной кислотой и выпаривании досуха образовалось 13.14 г остатка. Определить состав.
3. Для нейтрализации 200 мл 0,5 М раствора азотной кислоты израсходовали 6.26 г смеси карбонатов калия и натрия. Определить состав смеси солей.
4. При растворении в растворе щелочи 2 г сплава алюминия с цинком выделилось 1.904 л водорода (н. у.). Определить состав сплава.
5. Определить массовую долю бромида калия, если из 200 г раствора выделилось 8 г брома. Какой объем хлора при Р=101.3 кПа и температуре 27°С при этом израсходовали?
6. Определить концентрацию в растворе иодида калия, если известно, что при обработке 100 г этого раствора дихроматом калия в кислой среде выделилось 76.2 г иода.
7. К раствору, содержащему 5.48 г сульфата и силиката натрия, прибавили избыток хлорида бария, в результате чего образовалось 9.12 г смеси силиката и сульфата бария. Определить состав исходной и образовавшейся смеси.
8. В 500 мл воды растворили 23 г металлического натрия. Рассчитать молярность полученного раствора.
9. В лаборатории имеются хлорид калия, перманганат калия, гидроксид калия, 98%-ая серная кислота и вода. Как можно, используя эти реактивы, получить жавелевую воду?
10. При нагревании 6.06 г нитрата калия образовалось 5.34 г твердого остатка. Определить степень разложения нитрата калия.
11. Mассa 3.28 л смеси моноксида углерода и метана при 27°С и 3.75 атм. равна 10.4 г. Определить количество воздуха, необходимое для сжигания данной смеси.
12. В лаборатории имеется гидрид кальция, оксид меди (П), 98%-ая серная кислота и вода. Сколько граммов каждого вещества надо взять для получения 2.24 л сернистого газа (н. у.)?
13. При разложении 80 г одноосновной кислоты, образованной пятивалентным элементом, получился 71 г ангидрида этой кислоты. Каким элементом образована кислота?
14. При разложении 8.06 г смеси бертолетовой соли и перманганата калия выделилось 1.568 л кислорода (н. у.). Определить состав исходной смеси.
15. Сколько г серы прореагирует с газом, выделившимся при взаимодействии 6.5 г цинка с избытком разбавленной серной кислоты, если используется только 80% газа?
16. Сколько потребуется сульфида железа (II) и 7.3%-ой соляной кислоты (считая 50%-ый избыток), чтобы при пропускании газа, образующегося при их взаимодействии, через раствор нитрата свинца выпало 2.39 г осадка?
17. При взрыве смеси, полученной из одного объема неизвестного газа и двух объемов кислорода, образуется два объема СО2 и один объем азота. Найти молекулярную формулу газа.
18. При обработке соляной кислотой 9.92 смеси карбидов кальция и алюминия образовалось 4.48 л смеси метана и ацетилена (н. у.). Определить состав смеси карбидов.
19. Анализ газа показал, что соединение содержит 5.9% водорода и серу. Литр этого газа весит 1.52 г (н. у.) Определить, какой это газ.
20. Сколько моль азотной кислоты можно получить при окислении 5 л аммиака (н. у.)?
21. Определить нормальность раствора, содержащего 15 г Са(НСО3)2 в 100 мл воды.
1.12 Комплект экзаменационных билетов
(утвержден на заседании кафедры 08.12.08, протокол )
Экзаменационный билет № 1 Вопрос 1. Водород в природе. Получение водорода. Свойства и применение водорода. Вопрос 2. Сколько грамм серы прореагирует с газом, выделившимся при взаимодействии 6,5 г цинка с избытком разбавленной серной кислоты, если используется только 80% газа? |
Экзаменационный билет № 2 Вопрос 1. Перекись водорода. Получение, свойства, применение. Перекись водорода как восстановитель. Вопрос 2. В соляной кислоте растворили магний, массой 6 г, и цинк, массой 6,5 г. Определите объем водорода, измеренный при н. у., который выделится при этом. |
Экзаменационный билет № 3 Вопрос 1. Кислород в природе. Воздух. Получение и свойства кислорода. Озон. Вопрос 2. Рассчитайте массу азота, который потребуется для получения аммиака, массой 3,15 г. Производственные потери веществ составляют 15%. |
Экзаменационный билет № 4 Вопрос 1. Сера в природе. Получение серы. Свойства и применение серы. Вопрос 2. Серебро, массой 5,4 г, растворили в концентрированной азотной кислоте. К полученному раствору прилили избыток раствора бромида натрия. Рассчитайте массу образовавшегося осадка. |
Экзаменационный билет № 5 Вопрос 1. Сероводород. Получение и свойства. Вопрос 2. Вычислите массу технического алюминия (массовая доля алюминия 98,4%), который потребуется для алюмотермического получения ванадия, массой 45,9 кг, из оксида ванадия (V). |
Экзаменационный билет № 6 Вопрос 1. Диоксид серы. Сернистая кислота. Получение и свойства. Вопрос 2. Объясните, почему раствор хлорида алюминия имеет кислую реакцию. Ответ подтвердите уравнениями реакций гидролиза (по всем ступеням). |
Экзаменационный билет № 7 Вопрос 1. Оксид серы (VI). Серная кислота. Получение и свойства. Вопрос 2. При растворении в растворе щелочи 2 г сплава алюминия с цинком выделилось 1,904 л водорода (н. у.). Определить состав сплава. |
Экзаменационный билет № 8 Вопрос 1. Галогены в природе. Физические свойства. Химические свойства галогенов. Получение и применение галогенов. Вопрос 2. Чугун содержит углерод в виде карбида (Fe3C). Массовая доля углерода в чугуне равна 3,6%. Вычислите массовую долю карбида в чугуне. |
Экзаменационный билет № 9 Вопрос 1. Соединения галогенов с водородом. Получение, применение, свойства. Вопрос 2. В 500 мл воды растворили 23 г металлического натрия. Рассчитать молярность полученного раствора. |
Экзаменационный билет № 10 Вопрос 1. Углерод в природе. Аллотропия углерода. Химические свойства углерода. Вопрос 2. При нагревании 6.06 г нитрата калия образовалось 5.34 г твердого остатка. Определить степень разложения нитрата калия. |
Экзаменационный билет № 11 Вопрос 1. Диоксид углерода. Угольная кислота. Угарный газ. Соединения углерода с серой и азотом. Вопрос 2. Железо, массой 7 г, прореагировало с хлором (в избытке). Полученный хлорид растворили в воде, массой 200 г. Вычислите массовую долю соли в полученном растворе. |
Экзаменационный билет № 12 Вопрос 1. Азот. Получение и свойства. Вопрос 2. Оксид хрома (VI), массой 2 г, растворили в воде, массой 500 г. Рассчитайте массовую долю хромовой кислоты H2CrO4 в полученном растворе. |
Экзаменационный билет № 13 Вопрос 1. Аммиак. Соли аммония. Получение, применение, свойства. Вопрос 2. Смесь Mg и его оксида массой 5,1 г обработали соляной кислотой. При этом выделилось 3,74 л водорода. Определить процентный состав смеси. |
Экзаменационный билет № 14 Вопрос 1. Оксиды азота. Азотная кислота. Получение, применение, свойства. Вопрос 2. К оксиду серы (IV), массой 3,2 г, добавили кислород, массой 2,4 г. Вычислите объемную долю оксида серы в полученной газовой смеси. |
Экзаменационный билет № 15 Вопрос 1. Фосфор. Получение, применение, свойства. Вопрос 2. Натрий получают электролизом расплава хлорида натрия. Напишите уравнения реакций, протекающих при этих процессах. |
Экзаменационный билет № 16 Вопрос 1. Оксиды и кислоты фосфора. Получение, применение, свойства. Вопрос 2. Вычислите массовую долю углерода в карбонате натрия и гидрокарбонате натрия. |
Экзаменационный билет № 17 Вопрос 1. Кристаллическое строение металлов. Физические и химические свойства металлов. Вопрос 2. В раствор гидроксида калия (масса растворенного KOH равна 14 г) пропустили оксид углерода (IV), объемом 2,8 л (н. у.). Какая соль образуется при этом? Определить массу соли в полученном растворе. |
Экзаменационный билет № 18 Вопрос 1. Щелочные металлы. Получение, применение, свойства. Вопрос 2. Вычислить, сколько граммов хлорида натрия и 70%-ой серной кислоты прореагировали без нагревания, если объём выделившегося газа составил 4.48 л (н. у.). |
Экзаменационный билет № 19 Вопрос 1. Алюминий. Получение, применение, свойства. Вопрос 2. В серной кислоте растворили магний, массой 6 г, и медь, массой 6,5 г. Определите объем водорода, измеренный при н. у., который выделится при этом. |
Экзаменационный билет № 20 Вопрос 1. Хром. Получение, применение, свойства. Вопрос 2. При термическом разложении 25 г карбоната кальция образовалось 17,3 г твердого остатка. Определить степень разложения карбоната. |
Экзаменационный билет № 21 Вопрос 1. Железо. Физические и химические свойства железа. Сплавы железа. Вопрос 2. Какой объем SO2 выделится при сжигании серы в 5 л кислорода при выходе 80%? |
Экзаменационный билет № 22 Вопрос 1. Общая характеристика благородных газов. Гелий, нахождение в природе, получение, применение, физические и химические свойства. Вопрос 2. При взаимодействии железа, массой 28 г, с хлором образовалась смесь хлоридов железа (II) и (III), массой 77,7 г. Рассчитайте массу хлорида железа (III) в полученной смеси. |
Экзаменационный билет № 23 Вопрос 1. Диоксид кремния. Получение, применение, свойства. Кремниевые кислоты и их соли. Вопрос 2. Вычислите массу технического алюминия (массовая доля алюминия 80,5%), который потребуется для алюмотермического получения магния, массой 50 кг, из оксида магния. |
Экзаменационный билет № 24 Вопрос 1. Кремний в природе. Получение и свойства кремния. Соединения кремния с водородом и галогенами. Вопрос 2. Рассчитайте объем SO2, который потребуется для получения серной кислоты, массой 15 кг. Производственные потери веществ составляют 15%. |
Экзаменационный билет № 25 Вопрос 1. Магний. Нахождение в природе, получение, физические и химические свойства, применение. Вопрос 2. Сколько г серы прореагирует с газом, выделившимся при взаимодействии 6,0 г магния с избытком разбавленной серной кислоты, если используется 90% газа? |
Экзаменационный билет № 26 Вопрос 1. Кальций. Нахождение в природе, получение, физические и химические свойства, применение. Вопрос 2. Для получения чистого железа используют электролиз водного раствора сульфата железа (II). Напишите уравнения реакций, протекающих при этих процессах. |
Экзаменационный билет № 27 Вопрос 1. Химические свойства концентрированных неорганических кислот (в т. ч. серной и азотной). Вопрос 2. Смесь кальция и его оксида массой 5.1 г обработали соляной кислотой. При этом выделилось 3.74 л водорода (н. у.). Определить процентный состав смеси. |
1.14 Примерная тематика курсовых работ.
1.15 Примерная тематика квалификационных (дипломных) работ.
1.16 Методика исследования.
По учебному плану выполнение не предусмотрено.
1.17 Балльно-рейтинговая система, используемая преподавателем для оценивания знаний студентов по данной дисциплине.
Посещение лекций – 120 баллов (по 4 балла за каждую)
Работа на практических занятиях (семинарах) – до 10 баллов (итого 50 баллов)
Самостоятельная работа студента:
ПЗ №1 – до10 баллов.
ПЗ №2 – до 10 баллов.
ПЗ №3 – до 10 баллов.
ПЗ №4 – до 10 баллов.
ПЗ №5 – до 10 баллов.
Работа на лабораторном занятии – до 5 баллов (итого 50 баллов)
Самостоятельная работа студента, в том числе защита лабораторной работы, выполнение заданий, ответы на контрольные вопросы):
ЛБ №1 – до10 баллов.
ЛБ №2 – до 10 баллов.
ЛБ №3 – до 10 баллов.
ЛБ №4 – до 10 баллов.
ЛБ №5 – до 10 баллов.
ЛБ №6 – до 10 баллов.
ЛБ №6 – до 10 баллов.
ЛБ №7 – до 10 баллов.
ЛБ №9 – до 10 баллов.
ЛБ №9 – до 10 баллов.
ЛБ №10 – до 10 баллов.
Зачетное тестирование – 20 баллов.
Итого: 390 баллов.
Примеры рейтинговых заданий представлены в разделе «Примерные зачетные тестовые задания »
Задания для самостоятельной работы выполняется студентом с использованием лекций и учебных пособий и оформляется в письменном виде. Задание должно быть сдано студентом в строго определенные сроки в соответствии с учебным календарным планом. Целью самостоятельной работы студента является подготовка тестированию по соответствующим темам и экзамену.
Для оценки 5 сумма баллов за все модули должна быть не менее 340, для оценки 4 – не менее 280 баллов и для оценки 3 – не менее 210 баллов. Если оценка студента не устраивает или он набрал менее 210 баллов, студент сдает экзамен по дисциплине.
Выполнение практической части обязательно.
РАЗДЕЛ 2. Методические указания по изучению дисциплины
Мень к контрольным и лабораторным работам по общей и неорганической химии.- Мурманск: МГПУ, 200с.
РАЗДЕЛ 3. Содержательный компонент теоретического материала.
Лекция 1. Водород и кислород.
1.1 Водород в природе.
1.2 Получение водорода – лабораторные и промышленные методы.
1.3 Физические и химические свойства водорода. Применение водорода.
1.4 Пероксид водорода. Физические и химические свойства. Применение.
1.5 Кислород в природе. Характеристика состава воздуха.
1.6 Получение, физические и химические свойства кислорода. Биогеохимический круговорот кислорода.
1.7 Озон. Превращения озона в кислород и взаимодействия оксида азота (II) с озоном.
Лекция 2. Галогены и их соединения.
2.1 Общая характеристика галогенов. Галогены в природе.
2.2 Физические свойства галогенов.
2.3 Химические свойства галогенов.
2.4 Получение (лабораторные и промышленные методы) и применение галогенов.
2.5 Соединения галогенов с водородом, их физические и химические свойства.
2.6 Соединения галогенов кислородом, их физические и химические свойства.
Лекция 3-4. Сера и ее соединения.
1. Сера в природе. Получение серы.
2. Физические и химические свойства серы. Применение серы.
3. Сероводород, получение, физические и химические свойства, применение.
4. Сульфиды, получение, физические и химические свойства, применение.
5. Диоксид серы, получение, физические и химические свойства, применение.
6 .Сернистая кислота, получение, физические и химические свойства, применение.
7. Триоксид серы, получение, физические и химические свойства, применение.
8. Серная кислота, получение, физические и химические свойства, применение.
9. Круговорот серы и факторы, влияющие на него.
Лекция 5-6. Азот в природе и промышленности.
1. Азот в природе. Получение и свойства азота.
2. Аммиак. Соли аммония. Свойства, получение, применение аммиака.
3. Оксиды азота. Свойства, получение, применение.
4. Азотистая кислота, химические свойства, получение применение. Нитриты.
5. Азотная кислота. Химические свойства разбавленной и концентрированной азотной кислоты. ОВР.
6. Получение, применение.
7. Нитраты.
Лекция 7. Фосфор и его соединения.
7.1 Фосфор в природе.
7.2 Получение и свойства фосфора.
7.3 Соединения фосфора с водородом и галогенами.
7.4 Оксиды и кислоты фосфора.
7.5 Круговороты азота и фосфора и факторы, влияющие на них. Реакций связывания 7.6фосфора в природе.
7.7 Фосфорные удобрения.
Лекция 8. IV группа элементов.
8.1 Углерод в природе. Аллотропные модификации углерода.
8.2 Химические свойства углерода. Карбиды.
8.3 Диоксид углерода, угольная кислота, их получение и химические свойства.
8.4 Оксид углерода (II).
8.5 Соединения углерода с серой и азотом.
8.6 Биогеохимический круговорот углекислого газа.
8.7 Кремний в природе. Получение и свойства кремния.
8.8 Соединения кремния с водородом и галогенами.
8.9 Диоксид кремния, его химические свойства.
8.10 Кремниевые кислоты и их соли.
Лекция 9. Общие свойства металлов.
9.1 Электронное строение металлов.
9.2 Кристаллическое строение металлов.
9.3 Физические свойства металлов.
9.4 Общие химические свойства металлов.
9.5 Получение металлов. Сплавы.
9.6 Проблемы загрязнения природных объектов тяжелыми металлами.
7.8 Коррозия металлов.
Лекция 10. Щелочные и щелочно-земельные металлы.
10.1 Щелочные металлы в природе.
10.2 Получение и свойства щелочных металлов.
10.3 Натрий, физические и химические свойства, получение, применение.
10.4 Калий, физические и химические свойства, получение, применение.
Лекция 11. Щелочно-земельные металлы.
11.1 Магний, нахождение в природе, получение, физические и химические свойства, применение.
11.2 Кальций, нахождение в природе, получение, физические и химические свойства, применение.
11.3 Жесткость воды и методы ее устранения.
Лекция 12. АЛЮМИНИЙ.
12.1 Алюминий, нахождение в природе.
12.2 Получение алюминия (лабораторные и промышленные методы).
12.3 Физические и химические свойства алюминия, применение.
12.4 Оксиды алюминия, нахождение в природе, получение (лабораторные и промышленные методы), физические и химические свойства, применение.
Лекция 13. ХРОМ.
13. 1Хром, нахождение в природе.
13.2 Получение хрома (лабораторные и промышленные методы).
13.3 Физические и химические свойства хрома, применение.
13.4 Оксиды хрома, нахождение в природе, получение (лабораторные и промышленные методы), физические и химические свойства, применение.
Лекция 14. СЕМЕЙСТВО ЖЕЛЕЗА.
14.1 Железо. Нахождение в природе. Физические свойства железа.
14.2 Диаграмма состояния железо-углерод.
14.3 Производство чугуна и стали. Сплавы железа.
14.4 Химические свойства железа. Соединения железа и их свойства.
Лекция 15. БЛАГОРОДНЫЕ ГАЗЫ. ПЛАТИНОВЫЕ МЕТАЛЛЫ.
15.1 Общая характеристика благородных газов.
15.2 Гелий, нахождение в природе, получение, применение, физические и химические свойства.
15.3 Общая характеристика платиновых металлов.
15.4 Платина, палладий, иридий, нахождение в природе, получение, применение, физические и химические свойства.
РАЗДЕЛ 4. Словарь терминов (Глоссарий).
Оксиды — соединения двух элементов, один из которых кио лород в степени окисления -2 (СаО, СО2, Р2О5 ).
Пероксиды — соединения водорода и некоторых металлов с кислородом в степени окисления -1 (Н2О2, Na2O2, CaO2 и др.).
Гидроксиды (гидраты оксидов) — продукты прямого или косвенного соединения оксидов с водой. Делятся на три типа: основания, кислоты и амфотерные гидроксиды.
Основания (основные гидроксиды) — электролиты, которые при диссоциации образуют катионы металлов и только один вид анионов — гидроксид-ионы ОН - (NaOH, Ca(OH)2, Bi(OH)3 и др.).
Основные оксиды — оксиды, гидраты которых являются основаниями (Na2O, CaO, Bi2O3 и др.).
Кислоты — электролиты, которые при диссоциации образуют только катионы водорода Н+ и анионы кислотных остатков (H2SO4, HNO3, HC1O4 и др.).
Кислотные оксиды — оксиды, гидраты которых являются кислотами (кислотными гидроксидами) (SO3, NOO5, С12О7 и др.).
Амфотерные гидроксиды — электролиты, способные диссоциировать как по типу оснований, так и по типу кислот (Zn(OH)2, А1(ОН)3 и др.).
Амфотерные оксиды — оксиды, гидраты которых являются амфотерными гидроксидами (ZnO, A12O3 и др.).
Солеобразующие оксиды — общее название основных, кислотных и амфотерных оксидов, которые образуют соли при взаимодействии с кислотами или с основаниями.
Несолеобразующие (безразличные, индифферентные) оксиды — оксиды, которые не образуют ни гидратов, ни солей (N2O, NO, CO, SiO).
Кислотность основания — число гидроксидных групп в молекуле (формульной единице) основания.
Щелочи — растворимые в воде основания. Наиболее известными щелочами являются гидроксиды щелочных и щелочноземельных металлов (NaOH, Ca(OH)2 и др.).
Основность кислоты — число атомов водорода в молекуле кислоты, которые могут отщепляться в виде ионов Н+.
Кислородсодержащие кислоты — гидраты кислотных оксидов (H2SO4, HNO3, H3PO4 и др.).
Бескислородные кислоты — водные растворы газообразных нодородных соединений некоторых неметаллов (НС1, HBr, H2S и
др.).
Реакция нейтрализации — взаимодействие между кислотой и основанием, в результате которого образуются соль и вода (например: НС1 + NaOH=NaCl + Н2О). Реакции нейтрализации относятся к типу реакций обмена.
Реакции обмена — реакции, в ходе которых исходные сложные вещества обмениваются своими составными частями и образуют новые сложные вещества; происходят без изменения степеней окисления элементов.
Нормальные (средние) соли — продукты полного замещения атомом водорода в молекулах кислот атомами металла или продукты полного замещения гидроксидных групп в молекулах оснований кислотными остатками (NaCl, FeBr3, A12(SO4)3 и др.).
Кислые соли — продукты неполного замещения атомов водорода в молекулах многоосновных кислот атомами металла (NaHCO3, CaHPO4, Са(Н2РО4)2 и др.).
Основные соли — продукты неполного замещения гидроксидных групп в молекулах многокислотных оснований кислотными остатками (CuOHCl, A1(OH)2NO3 и др.).
Смешанные соли — соли, состоящие из катионов одного металла и анионов двух различных кислотных остатков (PbFCl, Са(С1О)С1 и др.).
Двойные соли — соли, состоящие из катионов двух различных металлов (аммония) и анионов одной кислоты (KA1(SO4)2, NH4Fe(SO4)2 и др.).
Комплексные соли — соли, состоящие из катионов металла и комплексных анионов (K4[Fe(CN)6] , Na2[PtCl6] и др.) или из комплексных катионов и анионов кислотных остатков.
Неметалличность элемента — способность его атомов присоединять электроны.
Электроотрицательность элемента — количественный критерий металличности и неметалличности, характеризующий способность атома данного элемента притягивать к себе электроны, участвующие в образовании химической связи с другим атомом.
Степень окисления элемента — это реальный (в случае ионных соединений) или условный (в случае ковалентных соединений) заряд атома данного элемента в данном соединении.
Гидратация в растворах — взаимодействие частиц растворяемого вещества с молекулами воды, не связанное с разрушением этих молекул.
Гидратированные ионы — ионы, связанные с молекулами воды.
Электролитическая диссоциация (ионизация) — процесс распада ионных соединений или соединений с ковалентной полярной связью на ионы; происходит в водных растворах и в расплавах.
Электролиты — вещества, которые в водных растворах и в расплавах диссоциируют на ионы.
Степень электролитической диссоциации — отношение числа молекул, распавшихся на ионы, к общему числу растворенных молекул.
Сильные электролиты — вещества, которые в водных растворах полностью распадаются на ионы (степень диссоциации равна 1).
Слабые электролиты — вещества, которые в водных растворах лишь частично распадаются на ионы (степень диссоциации меньше 1).
Аллотропия — явление образования нескольких простых веществ атомами одного и того же химического элемента.
РАЗДЕЛ 5. Практикум по решению задач (практических ситуаций) по темам лекций.
Задачи решают в единой системе измерения.

Пример 1. При н. у. в воде массой 100 г растворяется хлороводород объемом 50,5 л. При температуре 50 °С и нормальном давлении коэффициент растворимости хлороводорода равен 59,6 г. Насыщенный при температуре 0 °С раствор HCl массой 40 г нагрели до температуры 50 °С. Определите массу полученного раствора.
а) п. 1. Дано:
V(HCl) = 50,5 л (н. у.),
Kраств(HCl) = 59,6 г (50 °С, 1 атм),
m(насыщ. р-ра) = 40 г (0 °С). Найти: m(р-ра HCl) – ?
б) п. 2.
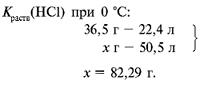
в) п. 3.
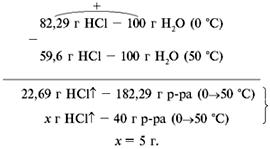
5 г HCl улетучится при нагревании. Ответ. m(полученного р-ра HCl) = 40 – 5 = 35 г.
Пример 2. В воде массой 100 г растворяется при температуре 30 °С бромид аммония массой 81,8 г. При охлаждении насыщенного при температуре 30 °С раствора NH4Br массой 300 г до температуры 0 °С выпадает в осадок соль массой 36,8 г. Определите, какая масса бромида аммония может быть растворена в воде массой 100 г при t = 0 °С.
а) п. 1. Дано:
Kраств = 81,8 г (30 °С),
m(насыщ. р-ра) = 300 г (30 °С),
m(осадка) = 36,8 г (0 °С). Найти: K'раств(0 °С) – ?
б) п. 2.

Ответ. K'раств(0 °С) = 59,5 г.
РАЗДЕЛ 6. Изменения в рабочей программе, которые произошли после
утверждения программы.
Характер изменений в программе | Номер и дата протокола заседания кафедры, на котором было принято данное решение | Подпись заведующего кафедрой, утверждающего внесенное изменение | Подпись декана факультета (проректора по учебной работе), утверждающего данное изменение |
РАЗДЕЛ 7. Учебные занятия по дисциплине ведут:
Ф. И.О., ученое звание и степень преподавателя | Учебный год | Факультет | Специальность |
|
Ст. преподаватель | 2005/2006 | Естественно-географический | 032400- Биология-География |
|
Ст. преподаватель | 2006/2007 | Естественно-географический | 050102- Биология |
|
Ст. преподаватель | 2007/2008 | Естественно-географический | 032400- Биология-География |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



