Так как вычисленное значение коэффициента Фишера для всех исследуемых биологических объектов меньше табличного (tтабл.=10,97), можно сделать вывод о том, что разработанные методики количественного определения пароксетина с помощью методов ВЭЖХ и ГХ не отличаются по своей воспризводимости.
3 Схема химико-токсикологического исследования пароксетина в биологических объектах
3.1 Апробация разработанных методик на лабораторных животных
Разработанные методики обнаружения и количественного определения пароксетина были апробированы на лабораторных животных (крысах). Экспериментальные исследования выполнялись в соответствии с правилами европейской конвенции по защите позвоночных животных, используемых в эксперименте для научных целей. Исследования проводили на белых крысах в возрасте 2,0–2,5 месяца массой 180-300 г.
Группе крыс (по 6 на каждую концентрацию) вводились перорально токсические дозы пароксетина (850, 1000, 1200 мг) с водной нагрузкой в пересчете на массу животных (соответственно 14,3; 16,9; 20,2 мг). Параллельно проводился контрольный опыт. Через 5,2 часа (время максимальной концентрации в плазме) биологические объекты исследовали.
Идентификацию пароксетина осуществляли с помощью предварительного и подтверждающего исследований (п. 2-3).
Количественное содержание пароксетина в извлечениях из биологических объектов (кровь, моча, печень, почки) лабораторных животных определяли методами ВЭЖХ и ГХ (п.
Полученные результаты представлены в таблице 6.
Таблица 6 – Результаты количественного определения пароксетина в крови, моче, печени, почках лабораторных крыс методами ВЭЖХ и ГХ
Объект | Введено (перорально) субстанции пароксетина крысе (мг) | |||
14,3 | 16,9 | 20,2 | ||
Метод ВЭЖХ | кровь |
Δ |
Δ |
Δ |
моча |
Δ |
Δ |
Δ | |
печень |
Δ |
Δ |
Δ | |
почки |
Δ |
Δ |
Δ | |
Метод ГХ | кровь |
Δ |
Δ |
Δ |
моча |
Δ |
Δ |
Δ | |
печень |
Δ |
Δ |
Δ | |
почки |
Δ |
Δ |
Δ |
Исходя из данных таблицы 6, относительная погрешность определения не превышает 12,07%.
Разработанные методики позволяют достоверно обнаружить и количественно определить пароксетин в извлечениях из биологических объектов (кровь, моча, печень, почки) лабораторных животных (крыс).
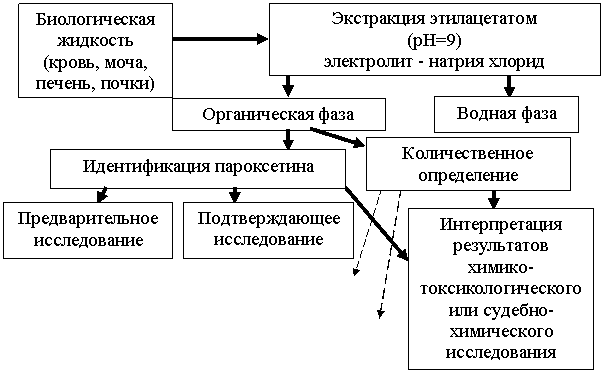
3.2 Схема химико-токсикологического исследования пароксетина в биологических объектах (кровь, моча, печень, почки)
Результаты проведенных исследований были использованы для разработки схемы химико-токсикологического анализа пароксетина в биологических жидкостях (кровь, моча) и во внутренних органах трупа (печень, почки).
Метод ГХ Хромогенные и микрокристаллоскопические реакции (анализ мочи или вещественных доказательств) Заключение Метод ВЭЖХ Метод ГХ/МС Метод ТСХ |
Рисунок 1 – Схема химико-токсикологического исследования пароксетина в извлечениях из мочи
Заключение о присутствии пароксетина в исследуемых биологических объектах дают при положительном результате предварительного исследования методом ТСХ и подтверждающего исследования методами ГХ/МС и ВЭЖХ.
Таким образом, химико-токсикологический анализ биологических жидкостей (крови, мочи) и внутренних органов трупа (печени, почек) позволяет достоверно диагностировать факт отравления пароксетином.
Выводы
1. Изучена зависимость степени экстракции пароксетина из водных растворов от природы органического растворителя, значения рН среды, присутствия электролита. Выбраны оптимальные условия изолирования пароксетина: экстрагент – этилацетат, значение рН среды – 9, электролит– 5% раствор натрия хлорида. Выход в найденных условиях составляет около 96%.
2. Разработаны методики изолирования пароксетина из мочи, крови, печени и почек. Выход изучаемого лекарственного вещества составил в среднем 86%, 79%, 72% и 71% соответственно.
3. Разработаны методики идентификации пароксетина в извлечениях из биологических объектов (кровь, моча, печень, почки) с помощью предварительного исследования (методом ТСХ) и подтверждающего исследования химическими (хромогенными и микрокристаллоскопическими реакциями) и физико-химическими методами (ГХ/МС, ВЭЖХ).
4. Найдены оптимальные системы для хроматографирования пароксетина методом ТСХ: бензол – диоксан – аммиака раствор 25% (60:35:5); диоксан – бутанол - 25% раствор аммиака (25:20:5); этанол-25% раствор аммиака (100:1,5). Значение Rf (n=6) пароксетина соответственно равно: 1) 0,50±0,01; 2) 0,49±0,01; 3) 0,36±0,02. Детекцию зон адсорбции предложено проводить путем просмотра хроматографических пластин в УФ свете при длине волны 254 нм и с последующей обработкой хроматограммы реактивом Драгендорфа.
5. Показана возможность использования хромогенных и микрокристаллоскопических реакций для идентификации пароксетина при анализе как биологической жидкости (мочи) при остром отравлении пароксетином, так и вещественных доказательств (лекарственного препарата). Предел обнаружения пароксетина с помощью хромогенных реакций составляет от 0,6 до 1,2 мкг в пробе, микрокристаллоскопических реакций от 0,5 до 0,8 мкг в пробе.
6. Разработана методика идентификации пароксетина методом хромато – масс – спектрометрии. Методика отличается высокой чувствительностью (3,34 мкг/мл), специфичностью и прецизионностью.
7. Разработаны методики количественного определения пароксетина в извлечениях из биологических объектов (кровь, моча, печень, почки) методами ВЭЖХ и ГХ. Валидационная оценка методики по параметрам: прецизионность, предел количественного определения подтвердила пригодность её использования.
8. Вычисленное значение коэффициента Фишера меньше табличного (tтабл=10,97) для всех исследуемых биологических объектов, поэтому сделан вывод о том, что разработанные методики количественного определения пароксетина с помощью методов ВЭЖХ и ГХ не отличаются по своей прецизионности.
9. Предложена схема химико-токсикологического анализа биологических жидкостей (кровь, моча) и внутренних органов (печень, почки) при отравлении пароксетином.
10. Разработанные методики апробированы на биологических объектах (кровь, моча, печень, почки) лабораторных животных (крыс) при введении токсических доз препарата, тем самым было показано определение пароксетина при отравлениях.
Список работ, опубликованных по теме диссертации:
1. Аполлонская, -токсикологический анализ пароксетина в крови методом высокоэффективной жидкостной хроматографии/ // Токсикологический вестник.-2010.-№3.-С.44-46.
2. Аполлонская, Я. Е. Поиск оптимальных условий экстракции пароксетина из водных растворов///Разработка, исследование и маркетинг новой фармацевтической продукции: сб. науч. тр. - Пятигорск, 2009.– Вып.64.- С. 319-320
3. Аполлонская, пригодности ВЭЖХ методики для идентификации и количественного определения пароксетина/ // О проблемных вопросах организации производства судебно-медицинских экспертиз: материалы. всерос. науч.-практ. конфноября 2009г.– М.: РИО ФГУ «РЦСМЭ Росздрава»,2009.-С.362-365.
4. Аполлонская, пароксетина с помощью химических реакций/ // Актуальные вопросы судебно - химических, химико - токсикологических исследований и фармацевтического анализа: материалы Рос. науч.- практ. конф. с междунар. участием 28 сентября - 3 октября 2009г. – Пермь, 2009. –С.121-123.
5. Аполлонская, и количественное определение пароксетина в моче методом высокоэффективной жидкостной хроматографии/ //Разработка, исследование и маркетинг новой фармацевтической продукции: сб. науч. тр.-Пятигорск, 2010.–Вып.65.-С.368-370.
6. Аполлонская, хромато-масс-спектрометрии для идентификации пароксетина в биологических объектах / // Вестник Пермской государственной фармацевтической академии№ 7. – С. 258-259.
7. Аполлонская, и количественное определение пароксетина в извлечениях из печени крыс/ // Разработка, исследование и маркетинг новой фармацевтической продукции: сб. науч. тр.- Пятигорск, 2011.-Вып.66.- С. 345-347
АПОЛЛОНСКАЯ ЯНА ЕВГЕНЬЕВНА
ХИМИКО-ТОКСИКОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ ПАРОКСЕТИНА
14.02.04. – фармацевтическая химия, фармакогнозия
АВТОРЕФЕРАТ
ДИССЕРТАЦИИ НА СОИСКАНИЕ УЧЕНОЙ СТЕПЕНИ
КАНДИДАТА ФАРМАЦЕВТИЧЕСКИХ НАУК
Подписано к печати 26.04.2012г. формат бумаги 60х84-1/16
Бумага книжно-журнальная. Печать ротапринтная. Усл. печ. л. 0,8. Тираж 100 экз. Заказ №_____
Государственное бюджетное образовательное учреждение
высшего профессионального образования
«Пятигорская государственная фармацевтическая академия»
Министерства здравоохранения и социального развития Российской Федерации
( г. Пятигорск, пр. Калинина, 11)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |