Химический состав поверхности. Кислотно-основные свойства
Химический состав.
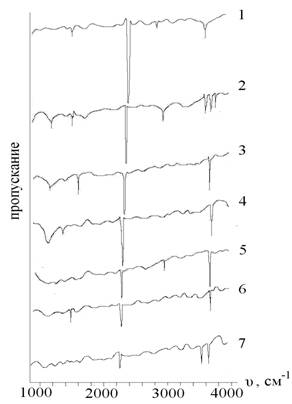
Рис. 1. ИК–спектры пропускания компонентов системы, хранившихся на воздухе: 1 – CdS,
2 – (CdS)0,9(ZnTe)0,1, 3 – (CdS)0,75(ZnTe)0,25, 4 – (CdS)0,5(ZnTe)0,5, 5 – (CdS)0,25(ZnTe)0,75, 6 – (CdS)0,1(ZnTe)0,9, 7 – ZnTe
ИК–спектроскопические ис-следования показали, что химический состав исход-ной поверхности компонен-тов системы CdS–ZnTe в целом не отличается от химического состава других алмазоподобных полупро-водников: представлен преимущественно адсор-бированными молекулами воды (3520 – 3690 см–1), группами ОН– (3750 см–1, 3400 – 3500 см–1,), угле-водородными и углекис-лородными соединениями (2220–2400 см–1) и продук-тами окисления поверх-ностных атомов.
Методами определения рН–изоэлектрического состояния, кондуктометрического титрования, механохимии была проведена оценка кислотно-основных характеристик поверхности компонентов системы
CdS–ZnTe (табл. 2).
Таблица 2
Кислотно-основные характеристики поверхности компонентов системы CdS–ZnTe
Состав | 0 | 10 | 25 | 50 | 75 | 90 | 100 |
рНизо | 6,64 | 6,7 | 6,8 | 6,82 | 6,79 | 6,76 | 6,32 |
рНизо в аммиаке | 7,42 | 7,74 | 7,65 | 7,31 | 7,34 | 7,38 | 7,21 |
ΔрНизо | 0,78 | 1,04 | 0,85 | 0,49 | 0,55 | 0,62 | 0,89 |
с·10–4, г–экв/г | 0,58 | 0,84 | 0,93 | 1,32 | 1,48 | 1,68 | 1,85 |
Водородный показатель рН–изоэлектрического состояния (рНизо). Найденные показатели рН–изоэлектрического состояния для всех образцов, длительное время хранившихся на воздухе, меньше 7, что указывает на превалирование на поверхности кислотных центов. Ответственными за данные активные центры, как и на других алмазоподобных полупроводниках [6], являются преимущественно координационно-ненасыщенные атомы (центры Льюиса), адсорбированные молекулы воды и группы ОН (центры Бренстеда), присутствие которых установлено методом ИК–спектроскопии МНПВО. Обнаруженное нелинейное, но плавное изменение рНизо с составом является дополнительным свидетельством образования в системе CdS–ZnTe твердых растворов замещения.
Кондуктометрическое неводное титрование. Дифференциальные кривые кондуктометрического неводного титрования свидетельствуют о присутствие на поверхности всех образцов различных по силе кислотных центров, подтверждая взаимную связь с данными по определению рНизо, за которые ответственны координационно-ненасыщенные атомы (центры Льюиса), адсорбированные молекулы воды и группы ОН- (центры Бренстеда), их наличие на поверхности подтверждают ИК–спектры. Зависимость общей концентрации кислотных центров (рассчитанной по первому, второму и третьему пикам) от состава системы CdS−ZnTe демонстрирует плавное нарастание этой величины с увеличением содержания CdS, на котором наблюдается наибольшая концентрация кислотных центров (с = 1,85 · 10–4, г–экв/г).
Механохимические исследования. Результаты механохимических исследований приведены в виде зависимостей рН–среды от времени диспергирования в воде компонентов системы. Процесс диспергирования сопровождается подщелачиванием среды. На свежеобразованной поверхности присутствуют адсорбированные молекулы H2O и группы OH– с разной подвижностью ионов H+[7].
Оптические свойства
В ИК–спектрах с уменьшением мольной доли CdS наблюдается смещение полос пропускания молекулярно-адсорбированного CO2 в области 2220 – 2400 см-1 и уменьшение их интенсивности. При расположении ИК–спектров образцов в ряд CdS → (CdS)х(ZnTe)1– х → ZnTe прослеживается закономерность: с изменением состава наблюдается смещение пиков, отвечающих колебаниям молекулярно-адсорбированного СO2, а также изменение их интенсивности. Данный факт является дополнительным подтверждением образования твердых растворов в данной системе.
По данным УФ–спектров получена зависимость ширины запрещенной зоны системы CdS–ZnTe от состава. Она нелинейна и имеет минимум при содержании CdS 50 мол. %. Рассчитанная ширина запрещенной зоны бинарных компонентов практически совпадает с литературными данными. Для сульфида кадмия она равна 2,44 эВ (2,53 эВ – табличное значение), а для теллурида цинка – 2,24 (2,23 – табличное значение).
По результатам КР–спектроскопических исследований найдены значения частоты максимальной люминесценции для бинарных соединений и твердых растворов представлены. В КР–спектрах твердых растворов в стоксовской области присутствуют узкие пики, соответствующие частотам ωLO и ωTO колебаний кристаллической решетки исходных бинарных соединений с частотами ωLO = 305 см-1 и ωTO = 234 и 243 см-1 для CdS и
ωLO = 206 см-1 и ωTO = 177 см-1 для ZnTe. Это позволяет идентифицировать исходные вещества и согласуется с данными рентгеноструктурного анализа (рис. 2, 3).
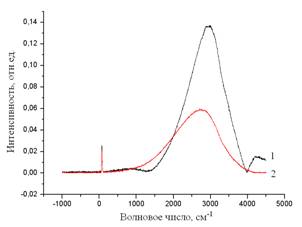
Рис. 2. Спектры комбинационного рассеяния твердых растворов
системы CdS−ZnTe:
1 – (CdS)0,9(ZnTe)0,1; 2 – CdS
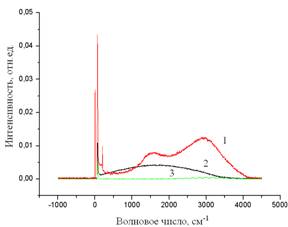
Рис. 3. Спектры комбинационного рассеяния бинарных соединений и твердых растворов системы CdS−ZnTe:
1 – (CdS)0,75(ZnTe)0,25; 2 – (CdS)0,1(ZnTe)0,9; 3 – ZnTe
Каталитические свойства
Результаты прямых каталитических исследований приведены в табл. 3.
Таблица 3
Зависимость степени восстановления NO2 при различных температурах от состава системы CdS–ZnTe
Температура, К | ZnTe | (CdS)0,1(ZnTe) 0,9 | (CdS)0,25(ZnTe) 0,75 | (CdS)0,5(ZnTe) 0,5 |
Степень восстановления NO2, % | ||||
303 | 45,3 | 65,2 | 32,7 | 29,8 |
323 | 40,7 | 57,4 | 24,4 | 24,7 |
353 | 43,9 | 60,3 | 19,2 | 15,4 |
383 | 35,1 | 45,8 | 10,5 | 10,1 |
423 | 44,8 | 62,9 | 23,9 | 7,6 |
Как показали каталитические исследования, реакция восстановления оксида азота (IV) аммиаком наиболее интенсивно протекает уже при комнатной температуре на твердом растворе (CdS)0,1(ZnTe) 0,9.
Фотокаталитические свойства компонентов системы CdS–ZnTe
Фотокаталитическую реакцию часто рассматривают как окислительно-восстановительную [8]. При межзонном фотовозбуждении при всем многообразии процессов захвата, рекомбинации и транспорта носителей в твердом теле достаточно быстро устанавливаются стационарные концентрации электронов и дырок на поверхности. Фотогенерированные носители на поверхности выступают в роли восстановителей и окислителей.
Реакция разложения воды для гетерогенных систем катализатор–раствор представляется как
2Н2О – 4 е → О2 + 4 Н+ (а)
2Н2О + 2 е → Н2 + 2 ОН– (б)
Н+ + еs → Н· (Н· + ·Н → Н2)
ОН– + hs → ОН· (ОН· + ·ОН → О2 + Н2)
или
2Н2О + К → Н2 + О2 + Н2 + К
из 2 Н+ из 2 ОН–
Очевидна также аналогия между гетерогенными фотокаталитическими и электрохимическими реакциями. Так, реакция (а) представляет собой аналог анодного, а (б) – катодного процессов, в котором энергия света, расходуемая на перенос электрона из валентной зоны в зону проводимости полупроводника, эквивалентна энергии источника, расходуемой на поддержание тока в цепи и химической реакции.
По данным УФ–спектроскопии установлено, что края полос отражения для исследованных полупроводников лежат почти во всем диапазоне спектра, т. е. компоненты системы CdS–ZnTe могут проявлять фотокаталитическую активность при длине волны от 364 до 670 нм (табл. 4).
Таблица 4
Оптимальная длина волны для преодоления энергетического барьера в
полупроводниках системы (CdS)x−(ZnTe)1–x
Состав | l, нм |
CdS | l ≤ 509 |
(CdS)0,9(ZnTe)0,1 | l ≤ 575 |
(CdS)0,75(ZnTe)0,25 | l ≤ 466 |
(CdS)0,5(ZnTe)0,5 | l ≤ 763 |
(CdS)0,25(ZnTe)0,75 | l ≤ 615 |
(CdS)0,1(ZnTe)0,9 | l ≤ 555 |
ZnTe | l ≤ 554 |
Из полученных данных зависимостей изменения концентрации ионов водорода в водных суспензиях полупроводников системы
CdS–ZnTe при облучении длинами волн видимой части спектра
(λ = 364–670 нм) видно: происходит выделение водорода, что подтверждено потенциометрически (рН изменяется от ~12,90 до ~9,25) и хроматографически. Наибольший скачок разницы водородного показателя наблюдается не только в течение первого часа облучения, но и при последующей выдержки суспензии в свете облучения.
Изменение концентрации ионов водорода в процессе облучения водной суспензии наиболее интенсивно протекает при λ = 364нм (табл. 5).
Таблица 5
Изменение концентрации ионов водорода в процессе облучения водной суспензии (CdS)х(ZnTe)1-х при разных длинах волн в течение 5 часов
[Н+] ∙ 103, нмоль/л Образец | λ = 364нм | λ = 490нм | λ = 540нм | λ = 590нм | λ = 670нм |
CdS | 456,2 | 9,42 | – | – | – |
(CdS)0,9(ZnTe)0,1 | 119,52 | 12,09 | 4,11 | – | – |
(CdS)0,75(ZnTe)0,25 | 20,09 | – | – | – | – |
(CdS)0,5(ZnTe)0,5 | 5,12 | 3,15 | 1,28 | 1,01 | 0,96 |
(CdS)0,25(ZnTe)0,75 | 3,75 | 2,36 | 1,74 | 0,55 | – |
(CdS)0,1(ZnTe)0,9 | 1,45 | 0,9 | 0,39 | – | – |
ZnTe | 1,05 | 0,96 | 0,54 | – | – |
По интенсивности выделения ионов водорода в процессе облучения водной суспензии системы CdS–ZnTe можно говорить о следующих зависимостях:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |


