λ = 364 нм –
CdS>(CdS)0,9(ZnTe)0,1>(CdS)0,75(ZnTe)0,25>(CdS)0,5(ZnTe)0,5>(CdS)0,25(ZnTe)0,7>
(CdS)0,1(ZnTe)0,9> ZnTe
457,09 > 120,23 > 21,38 > 5,13 > 3,77 > 1,54 > 1,09
λ = 490 нм –
(CdS)0,9(ZnTe)0,1>CdS>(CdS)0,5(ZnTe)0,5>(CdS)0,25(ZnTe)0,7>
(CdS)0,1(ZnTe)0,9> ZnTe
12,59 > 9,55 > 3,25 > 2,38 > 0,97 > 1,02
λ = 540 нм –
(CdS)0,9(ZnTe)0,1>(CdS)0,5(ZnTe)0,5>(CdS)0,25(ZnTe)0,7>(CdS)0,1(ZnTe)0,9> ZnTe
4,47 > 1,33 > 1,84 > 0,41 > 0,59
λ = 590 нм –
(CdS)0,5(ZnTe)0,5>(CdS)0,25(ZnTe)0,7
1,03 > 0,64
Как показали исследования, теллурид цинка, а также твердые растворы содержащие 50, 75 и 90 об. % ZnTe, значительной фотокаталитической активностью в реакции разложения воды не обладают. Возможно, это связано с влиянием свойств легирующей примеси – ZnTe.
При облучении полупроводников системы CdS–ZnTe при разных длинах волн наибольшая концентрация ионов водорода в водной суспензии при λ = 364нм отмечалась для CdS ([Н+] ∙ 103 = 457,09 нмоль/л) и для (CdS)0,9(ZnTe)0,1 ([Н+] ∙ 103 = 120,23 нмоль/л), об этом свидетельствуют результаты хроматографического анализа (табл. 6).
Таблица 6
Результаты хроматографического анализа (λ = 364нм)
Концентрации, % Образец | Х кислорода | Хводорода |
CdS | 19,42 | 80,58 |
(CdS)0,9(ZnTe)0,1 | 27,75 | 72,25 |
Мы предлагаем по впервые разработанной методике создание модельной установки (рис. 4) по получению водорода из воды. Началом для работы стало участие в конкурсе молодежных инноваций «У. М.Н. И.К» в 2009 году.
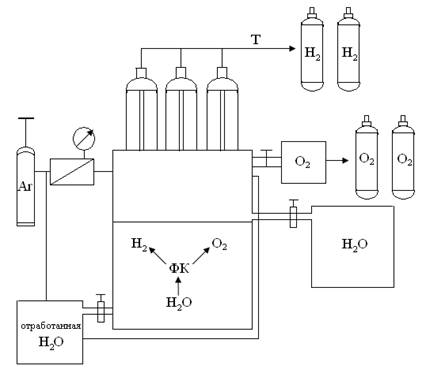
Рис. 4. Принципиальная схема получения водорода из воды с использованием в качестве фотокатализатора исследуемые бинарные соединения и твердые растворы системы CdS–ZnTe
Основные закономерности изменения изученных поверхностных свойств в зависимости от состава
Исследования, проведенные в настоящей работе, позволили сопоставить свойства бинарных компонентов и твердых растворов на их основе, выделить общность и различия в их поведении и провести системный анализ данных, полученных на каждом этапе исследования.

Так, при идентификации полученных твердых растворов, наблюдается закономерное изменение параметров решетки (а и с), межплоскостного расстояния (dhkl) и рентгеновской плотности (ρ) от состава твердых растворов (CdS)х(ZnTe)1–x (табл. 1):
– параметр решетки а для CdS и твердых растворов содержащих 10, 25 и 50 мол. % ZnTe, имеющих структуру вюрцита, увеличивается с ростом мольной доли ZnTe, а параметр решетки с уменьшается. Параметр решетки а для ZnTe и твердых растворов содержащих 10 и 25 мол. % CdS, имеющих структуру сфалерита, уменьшается с ростом мольной доли ZnTe;
– значения межплоскостных расстояний для полупроводников системы CdS–ZnTe типа вюрцит уменьшается с ростом мольной доли ZnTe в растворе (индексы (110) и (220)), а для полупроводников системы типа сфалерит для одних значений кристаллографических индексов плоскостей (111) уменьшается с ростом мольной доли ZnTe в растворе, а для других значений (222) растет;
– рентгеновская плотность для полупроводников системы CdS–ZnTe плавно увеличивается с ростом мольной доли ZnTe в растворе.
Исходная поверхность полупроводников системы CdS–ZnTe обладает преимущественно кислыми свойствами (рис. 5). Значения рН–изоэлектрического состояния исследуемых образцов, экспонированных на воздухе, увеличиваются с ростом мол.% ZnTe. Обратная зависимость состояния поверхности полупроводниковой системы CdS−ZnTe прослеживается также после хранения в атмосфере аммиака. С ростом мольной доли CdS в системе CdS–ZnTe возрастает общая концентрация кислотных центров (с·10–4, г–экв/г).
После экспонирования в атмосфере NH3 исчезают льюисовские и частично бренстедовские кислотные центры. Соответственно значения рНизо смещаются в щелочную область. При этом максимальное изменение
рНизо (ΔрНизо= рНизоNH3 – рНизовозд) под действием NH3 проявилось для твердого раствора (CdS)0,1(ZnTe)0,9, следовательно, максимальная чувствительность к NH3.
Таким образом, кислотно-основные характеристики рационально использовать для прогнозирования адсорбционной чувствительности, вместо проведения прямых измерений адсорбции, что значительно сокращает время и трудоемкость проведения эксперимента.
Сочетание минимальной концентрации кислотных центров и максимального значения рНизо в аммиаке для твердого раствора (CdS)0,1(ZnTe)0,9 соответствует максимальной каталитической активности данного образца. Каталитическая активность оценивалась по степени восстановления NO2 и составляла 65,2 % уже при комнатной температуре.
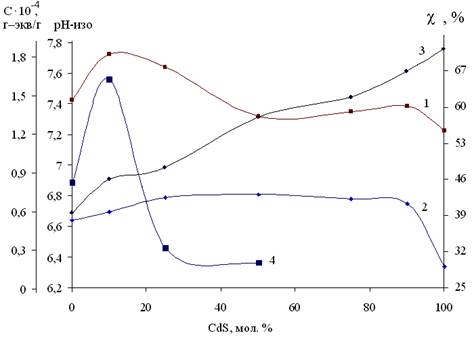
Рис. 5. Диаграммы зависимостей показателей кислотности поверхности:
рНизо при экспонировании в атмосфере аммиака (1), рНизо при хранении на воздухе (2),
концентрация кислотных центров, С×10–4, г–экв/г (3) и
каталитической активности c NO2, % при 303 К (4)
Обращает на себя внимание аналогия в закономерностях протекания фотокаталитических реакций (рис. 6).
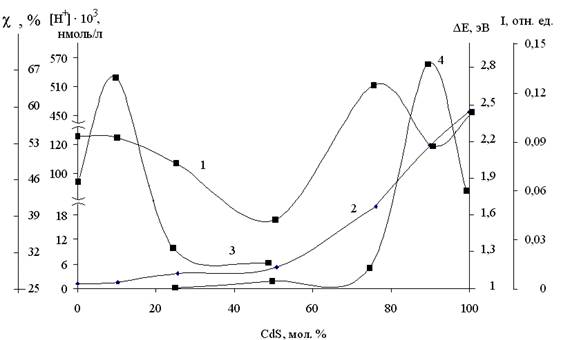
Рис. 6. Диаграммы зависимостей показателей оптических, каталитических и
фотокаталитических свойств поверхности:
значение ширины запрещенной зоны ΔЕ, эВ (1), выделения ионов водорода из водной суспензии от состава системы CdS–ZnTe при λ=364нм, [H+] · 103 нмоль/л (2), каталитическая активность c NO2, % при 303 К (3 ),
максимум интенсивности излучения по КР–спектрам I, отн. ед (4)
Так при увеличении мольной доли сульфида кадмия в полупроводниковой системе CdS–ZnTe наблюдается увеличение выделения ионов водорода с максимальной концентрацией при использовании в качестве фотокатализатора CdS и (CdS)0,9(ZnTe)0,1. При проведении темнового катализа – реакции селективного восстановления оксида азота (IV) аммиаком указанные катализаторы каталитической активности не проявляют.
Каталитическая активность полупроводниковой системы CdS–ZnTe уменьшается с увеличением мол. доли CdS в твердом растворе, при этом наблюдается обратная зависимость – рост интенсивности излучения, с максимумом для твердого раствора (CdS)0,9(ZnTe)0,1, который проявляет заметную фотоактивность.
Основные закономерности процессов, протекающих на поверхности полупроводниковой системы CdS–ZnTe, заключены в природе активных центров (рис. 7).
Разница электроотрицательности в атомах полупроводниковых соединений напрямую связана с долей ионной связи и определяет координационно ненасыщенные атомы.
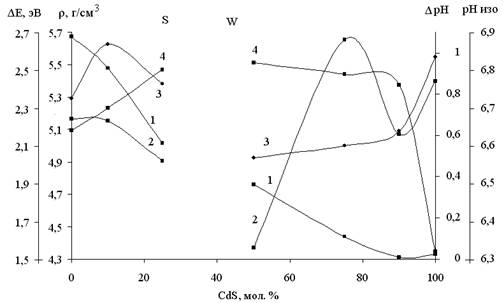
Рис. 7. Диаграммы зависимостей показателей объемных и поверхностных свойств сфалерита и вюрцита: значение рентгеновской плотности r, г/см3 (1),
значение ширины запрещенной зоны ΔЕ, эВ (2), изменение рНизо (3), рНизо (4)
Плавный характер кривых зависимостей говорит о связи между представленными свойствами (рентгеновская плотность, ширина запрещенной зоны, значение рН изоэлектрического состояния), в основе чего лежит изменение доли ионной связи и изменение силы и природы кислотных центров, их активность.
Твердые растворы в зависимости от состава (сфалерит или вюрцит) проявляют различные свойства (табл. 7).
Таблица 7
Объемные и поверхностные свойства полупроводниковой системы CdS–ZnTe
Состав | Структура | Δ ОЭО | ρ, г/см3 | Δ Е, эВ | рН | Δ рН | c, % | [Н+] ∙ 103, нмоль/л |
CdS | Вюрцит | 0,89 | 4,3307 | 2,44 | 6,32 | 0,89 | 456,2 | |
(CdS)0,9(ZnTe)0,1 | – | 4,3099 | 2,16 | 6,76 | 0,62 | 119,52 | ||
(CdS)0,75(ZnTe)0,25 | – | 4,4438 | 2,66 | 6,79 | 0,55 | 20,04 | ||
(CdS)0,5(ZnTe)0,5 | – | 4,7696 | 1,56 | 6,82 | 0,49 | 5,12 | ||
(CdS)0,25(ZnTe)0,75 | Сфалерит | – | 5,0167 | 2,02 | 6,8 | 0,85 | 45,3 | |
(CdS)0,1(ZnTe)0,9 | – | 5,4780 | 2,23 | 6,7 | 1,04 | 65,2 | ||
ZnTe | 0,45 | 5,6742 | 2,24 | 6,64 | 0,78 | 32,7 |
В закономерностях между объемными (плотность и ширина запрещенной зоны) и поверхностными (рН изоэлектрического состояния, Δ рН, каталитическими и фотокаталитическими) свойствами, во взаимосвязи между ними лежит следующая причина:
– по мере нарастания доли ионной связи и увеличения прочности отмечается уменьшение рентгеновской плотности (усредненное значение поглощения материалом излучения) и увеличение значения ширины запрещенной зоны (как для вюрцита, так и для сфалерита);
– вся закономерность отмечается в каталитической активности (рН, рНNH3, Δ рН, c). В роли центров каталитических реакций выступают координационно-ненасыщенные атомы А (Сd, Zn);
– при исследовании фотокаталитических свойств прослеживается та же закономерность. Свет (hυ) падает на атомы, происходит его поглощение координационно-ненасыщенными атомами, при этом облегчается прохождение электронами в полупроводнике ширины запрещенной зоны.
Выводы
1. Синтезированы по разработанной методике и аттестованы на основе рентгенографических и оптических исследований твердые растворы системы CdS–ZnTe. Формирование твердых растворов происходит уже на стадии механохимической активации. Их структура (сфалерит или вюрцит) зависит от состава.
2. Выполнены ИК–, УФ–, КР–спектроскопические исследования компонентов системы CdS–ZnTe:
– по результатам ИК–спектроскопических исследований химический состав исходной поверхности бинарных компонентов и твердых растворов системы CdS – ZnTe, как и на других алмазоподобных полупроводниках, представлен преимущественно адсорбированными молекулами воды, группами ОН–, углеродными соединениями и продуктами окисления поверхностных атомов;
– рассчитанным по УФ–спектрам значения ширины запрещенной зоны компонентов системы CdS–ZnTe изменяются в интервале (1,52 – 2,66);
– по КР–спектрам найдены значения частоты наибольшей люминесценции (νm) и максимума интенсивности излучения (I) кристаллической решетки компонентов системы CdS–ZnTe. Они составляют 2991 см–1 и 0,1373 отн. ед. соответственно.
3. Методами измерения рН–изоэлектрического состояния, механохимического диспергирования, кондуктометрического титрования изучены кислотно-основные свойства поверхности компонентов системы CdS–ZnTe. Определены природа, сила и концентрация кислотно-основных центров:
– исходная поверхность всех компонентов имеет слабокислый характер (рНизо изменяется в пределе 6,32 – 6,82);
– ответственными за кислотность поверхности выступают преимущественно центры Льюиса (координационно–ненасыщенные атомы), что подтверждают ИК–спектры и поведение поверхности при экспонировании в атмосфере NH3;
– с увеличением в системе CdS–ZnTe мольной доли ZnTe растет рНизо и уменьшается общая концентрация кислотных центров.
– общая концентрация кислотных центров (с·10–4, г–экв/г) при изменении состава системы CdS–ZnTe возрастает с ростом мольной доли сульфида кадмия.
4. На основе исследований каталитических свойств компонентов системы CdS–ZnTe по отношению к реакции селективного восстановления оксида азота (IV) аммиаком установлены:
– степень восстановления NO2 уменьшается с увеличением в системе мольной доли CdS;
– реакция на всех компонентах заметно протекает уже при комнатной температуре;
– максимальная степень превращения NO2 приходится на твердый раствор состава (CdS)0,1(ZnTe)0,9;
5. Проведенные исследования фотокаталитической активности компонентов системы CdS–ZnTe в реакции разложения воды показали:
– концентрация ионов водорода в процессе облучения их водных суспензий зависит от длины волны облучающего света, которая непосредственно связана со значением ширины запрещенной зоны;
– на основе значений ширины запрещенной зоны найдены оптимальные длины волн;
– в частности, наибольшая концентрация ионов водорода в водных суспензиях CdS и твердого раствора (CdS)0,9(ZnTe)0,1 отмечается при λ = 364нм.
6. Найдены закономерности в изменении объемных (ρ, ΔЕ) и поверхностных (рНизо, ΔрНизо, каталитических и фотокаталитических) свойств. В зависимости от внешних условий и состава системы CdS–ZnTe построены диаграммы состояния «свойство – состав», установлена взаимосвязь между ними. Разработаны рекомендации практического применения результатов исследования:
– твердый раствор состава (CdS)0,1(ZnTe)0,9 предложен в качестве материала модельного катализатора реакции восстановления NO2;
– твердый раствор состава (CdS)0,9(ZnTe)0,1 – в качестве фотокатализатора реакции разложении воды для получения водорода – экологически чистого, нетрадиционного источника топлива;
– создана принципиальная схема установки для получения водорода.
Подана заявка на изобретение.
Список цитируемой литературы
1. Кировская, свойства алмазоподобных полупровод-ников. Твердые растворы / . – Томск: Изд-во Томск. ун-та, 1984. – 133 с.
2. Кировская, растворы бинарных и многокомпонентных полупроводниковых систем: монография / . – Омск: Изд-во ОмГТУ, 2010. – 400 с.
3. Кировская, . Полупроводниковые катализаторы: Монография. / . – Омск: Изд-во ОмГТУ, 2004. – 272 с.
4. Замараев, К. И., Пармон, преобразование солнечной энергии: гетерогенные, гомогенные и молекулярно-организованные системы: Сб. науч. тр. / , – Новосибирск: Наука. Сиб. Отд-ние, 1991. – 358с.
5. Гуревич, Ю. Я., Плесков, полупроводников / , . – М.: Наука, 1983. – 342с
6. Кировская, состояние поверхности компонентов системы ZnSe – CdSe / , . // ЖФХ. – 2001. – Т. 75. – № 10. – с. 1837 – 1842.
7. Кировская, исследований физико-химических свойств поверхности алмазоподобных полупроводников и основные направления практических разработок. / // Омский научный вестник. – 2001. – Вып. 14. – с. 66 – 68.
8. Саката, Т., Каваи, Т. Фотосинтез и фотокатализ на полупроводниковых порошках / Т. Саката, Т. Каваи // Энергетические ресурсы сквозь призму фотохимии и катализа. – М.: Мир, 1986. – С. 361 – 388
Основные результаты диссертации опубликованы в работах:
1. Кировская, чувствительности поверхности полупроводников – первичных преобразователей сенсоров-датчиков по кислотно-основным свойствам / , , // Современные наукоемкие технологии, VIII научная межд. конф., 22–29 февраля 2008г., Хургада (Египет), №12. – С. 82-85.
2. Кировская, способ оценки чувствительности поверхности полупроводников – первичных преобразователей сенсоров-датчиков / , , // Материалы VIII научной конференции «Аналитика Сибири и Дальнего Востока».– Томск, 2008. – С 131.
3. Кировская, фотокатализ – наиболее эффективный и экологически чистый способ прямого использования солнечной энергии для получения водорода как нетрадиционного горючего / , , // Материалы Всероссийской научно–технической конференции «Россия Молодая: передовые технологии – в промышленность».– Омск, 2008. Кн.2. – С. 218-222.
4. Кировская, способ оценки чувствительности первичных преобразователей сенсоров-датчиков / , , // Материалы Всероссийской научно–технической конференции «Россия Молодая: передовые технологии – в промышленность».– Омск, 2008. Кн.2. – С. 228-234.
5. Кировская, эффективный и экологически чистый способ прямого использования солнечной энергии для получения нетрадиционного горючего / , , //Материалы II–ой Всероссийской научно–технической конференции «Россия Молодая: передовые технологии – в промышленность».– Омск, 2009. Кн.2. – С. 161-165.
6. Кировская, и фотокаталитические свойства компонентов системы InP-CdS, ZnTe–CdS / , , // ЖФХ. – 2011. –Т. 85. –№ 4. –С. 633-636.
7. Кировская, фотокаталитические свойства компонентов системы CdS–ZnTe / , , // Материалы VII–ой Международной научно–технической конференции «Динамика систем механизмов и машин».– Омск, 2009.– Кн. 3. – С. 179-183.
8. Кировская, и фотокатализ полупроводниковых систем InP–CdS, ZnTe–CdS / , , // Материалы региональной научно-методической конференции «Омское время – взгляд в будущее». – Омск, 2010.– Кн. 2. – С. 46-52.
9. Кировская, фотокаталитические свойства полупроводников системы ZnTe-CdS / , , // Материалы II Региональной молодежной науч.-техн. конф. Омский регион – месторождение возможностей. – Омск, 2011. – С. 227-229.
10. Кировская, полупроводниковые материалы и фотокатализаторы для получения нетрадиционного горючего / , , и др. // Омский научный вестник – Омск, 2012. №1 (107) – С. 35-39.
11. Кировская, по созданной технологии и физико-химические исследования новых адсорбентов / , , // Омский научный вестник – Омск, 2012. №2 (110) – С. 61-64.
12. I. A. Kirovskaya, O. T. Timoshenko, and E. O. Karpova. The Catalytic and Photocatalytic Properties of InP–CdS and ZnTe–CdS System Components // J. Phys. Chem., –2011. –Vol. 85. –Nо 4. –РР. 557-560.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |


