ОКСИД ФОСФОРА (+5), Р2О5 ( Р4Ою). Белый гигроскопичный порошок, получают его при горении фосфора в избытке воздуха или кислорода. Он очень энергично взаимодействует с водой, а так же отнимает воду от других соединений, его используют как осушитель газов и жидкостей:
Р205 + ЗН20 = 2НРОз, метафосфорная кислота,
Р205 + ЗН20 = 2Н3Р04, ортофосфорная кислота, избыток
Оксиды фосфора намного прочнее аналогичных соединений азота, что можно объяснить ослаблением неметаллических свойств у фосфора. ОРТОФОСФОРНАЯ КИСЛОТА, Н3Р04. В чистом виде кристаллическое вещество с температурой плавления, равной +42° С. С водой кислота смешивается в любых соотношениях. В отличии от азотной кислоты не является окислителем и не разлагается при нагревании, что объясняется наибольшей устойчивостью степени окисления (+5) из всех возможных у фосфора. Кислота имеет большое практическое значение, т. к. ее соли - фосфаты - используют в качестве удобрений. В промышленности ортофосфорную кислоту получают двумя способами: экстракционным и термическим. По первому способу измельченный фосфат кальция обрабатывают серной кислотой:
Са3(Р04)2 + 3H2S04 = 2Н3Р04 + 3CaS04| .
Сульфат кальция выпадает в виде осадка, а кислота остается в растворе. Вместе с кислотой в раствор переходят многие примеси - сульфаты железа, алюминия и др. Такая кислота идет на производство удобрений. По второму способу сначала получают фосфор восстановлением природного фосфата в электропечи, затем он окисляется до оксида фосфора (+5), который взаимодействует с водой. Получается чистая кислота с концентрацией до 80%.
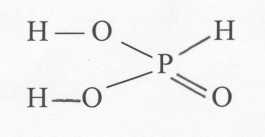
СОЛИ ОРТОФОСФОРНОЙ КИСЛОТЫ. В молекуле ортофосфорной кислоты все атомы водорода соединены с атомами кислорода:
Н-0\
Н-О-Р = О Н-О/
В водном растворе кислота подвергается ступенчатой диссоциации. Будучи трехосновной, она образует соли - фосфаты - трех видов:
1) фосфаты - замещены все атомы водорода в фосфорной кислоте, например: К3Р04 - фосфат калия, (NH4)3 Р04 - аммония;
2) гидрофосфаты - замещены два атома водорода кислоты, например: К2НР04 - гидрофосфат калия, (NH4)2HP04 - гидрофосфат аммония;
3) дигидрофосфаты - замещен один атом водорода кислоты, например: КН2Р04 - дигидрофосфат калия, NH4H2P04 - дигидрофосфат аммония.
Все фосфаты щелочных металлов и аммония растворимы в воде.
Из кальциевых солей фосфорной кислоты растворяется в воде лишь дигидрофосфат кальция Са(Н2Р04)2. Гидрофосфат кальция СаНР04 и фосфат кальция Са3(Р04)2 растворимы в органических кислотах (органические кислоты содержатся в подзолистых и торфяных почвах) [9].
1.4 Фосфор в почве. Значение для развития растений.
Общее количество фосфора на нашей планете примерно 1019 тонн, из них Ю15 тонн сосредоточено в земной коре, которая в среднем содержит 0,08-0,12 весовых процентов фосфора; атомы фосфора составляют 0,04-0,07% от общего числа атомов земной коры (Соколов, 1960г). Благодаря высокой реак-ционой способности фосфор в свободном состоянии в природе не встречается. В почвах он всегда содержится в пятивалентном виде, т. е. соответствует оксиду фосфора(+5), который с водой и другими элементами образует обширную группу кислородсодержащих соединений-фосфорных кислот и фосфатов. В зависимости от числа молекул воды, замещённых водородов, а так же количества тетраэдров Р04 " и способов их соединения между собой фосфаты образуют химические соединения, различные по растворимости в воде, содержанию фосфора, физическим, химическим и другим свойствам. Почти все соединения почвенных фосфатов (минеральных и органических форм) являются ортофосфатами (мономерами и полимерами). Последние время фосфаты вносятся в почву в виде удобрений, а так же в составе дизенфицирующих веществ. Валовый фосфор почвы состоит из органических и минеральных соединений. Соотношение между фракциями органических и минеральных форм фосфора, их качественный и количественный состав в различных типах почв различен. Определение запаса фосфора и отдельных фракций имеет теоретическое и практическое значение.
Содержание фосфора в тканях растений 230-3 50мг на 100 г сухого вещества. Определение степени обеспеченности растений питательными веществами может быть визуальным и химическим. Нарушение нормального питания растений и обмена веществ в них вызывает не только недостаток, но и избыток отдельных элементов.
НЕДОСТАТОК ФОСФОРА. Общим признаком фосфорного голодания служит тёмно-зелёная с голубоватым оттенком, фиолетовая или пурпуровая окраска листьев, по краям нижних листьев появляются пятна бурого цвета [8]. Резко уменьшается образование и развитие репродуктивных органов, цветки мелкие, опадающие, соцветия плохо озернённые. У картофеля, в частности, ухудшается качество клубней, в мякоти образуются бурые пятна, которые при варке затвердевают. У всех видов капусты вдоль жилок снизу старых листьев пурпуровая окраска, рост задержан. У томатов при дифиците фосфора сначала краснеют снизу старые листья, а позже-всё растение. Плоды поздно развиваются, мелкие. У бобовых недостаток фосфора вызывает задержку роста (растения-карлики), покраснение стеблей, цветение и плодоношение задержаны [8]. Чтобы полнее выявить условия питания растений и более эффективно применять удобрения, очень важно располагать данными диагностики в отдельные фазы развития растений и результатами анализа почвы.
1.5 Фосфор в организме человека и животных: значение, поступление.
Фосфор - один из важнейших биогенных элементов, необходимый для жизнедеятельности всех организмов. Присутствует в живых клетках в виде орто - и пирофосфорных кислот и их производных. Благодаря особенностям химического строения, атом фосфора способен к образованию богатых энергией связей. В процессе биологической эволюции именно фосфорные соединения стали основными, универсальными хранителями генетической информации и переносчиками энергии во всех живых системах. Другая важная роль соединений фосфора в организме заключается в том, что ферментативное присоединение фосфорильного остатка к различным органическим соединениям служит как бы « пропуском « для участия в обмене веществ, и, наоборот, отщепление фосфорильного остатка исключает эти соединения из активного обмена. Главную роль в превращениях соединений фосфора в организме человека и животных играет печень. Обмен фосфорных соединений регулируется гормонами и витамином Д. Содержание фосфора в тканях морских животных мг на 100 г сухого вещества, у наземных , у бактерий - около 3000, в организме человека особенно много фосфора в костной ткани (более 500), в тканях мозга (около 4000) и в мышцах (1Суточная потребность человека в фосфоре 1-2 грамма (у детей она выше, чем у взрослых). Баланс фосфора в организме зависит от общего состояния обмена веществ. Нарушение фосфорного обмена приводит к глубоким биохимическим изменениям, в первую очередь в энергетическом обмене. При недостатке фосфора в организме животных и человека развиваются остеопороз и другие заболевания костей.
Животные обычно получают достаточное количество фосфора с пищей, растениями фосфор извлекается в виде растворимых фосфатов.
Важная роль фосфора в регуляции обменных процессов обуславливает высокую чувствительность многих ферментативных систем живых клеток к действию фосфорорганических соединений. Это обстоятельство используется в медицине при разработке лечебных препаратов [5].
2. Практическая часть
2.1 Краткие теоретические сведения оптических методов анализа
Любое вещество поглощает и отражает электромагнитное излучение. Вещества, поглощающие излучение с длиной волны от 400 до 760 ммк (видимый свет), окрашены. Наряду с поглощением и отражением видимого света для анализа часто используют поглощение излучения в ультрафиолетовом ( 200-400 ммк ) и инфракрасном ( 0,мк) участках спектра. Характер и величина поглощения и отражения света зависят от природы вещества и его концентрации в растворе. Это и используют для качественного и количественного анализа оптическими методами, в частности методами светопоглоще-ния.
• Если пропустить через слой вещества (раствора) пучок света с интенсивностью 10, то после прохождения интенсивность уменьшается до It. Отношение It/Io = T (1) характеризует пропускание (поглощение) света. Величина
Т может изменяться от 0 до 1. Её выражают в процентах. Если Т отнесена к слою в 1 см толщиной, то она называется коэффициентом пропускания. Обычно используют отрицательный логарифм Т: - lgT = D (2) или D = lg I0 / It, D называют оптической плоскостью. Она может быть любой от 0 до бесконечности, но современные приборы позволяют определять D не более 2.
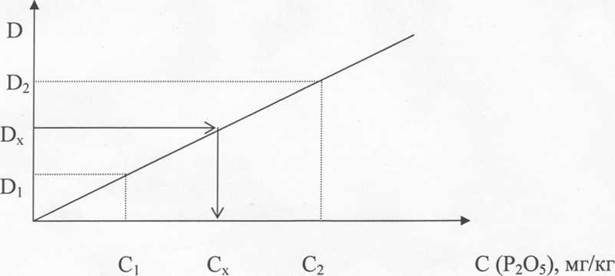
• В соответствии с основным законом калориметрии - законом Бугера --Ламберта - Бера между поглощением излучения раствором и концентрации в нём поглощающего вещества (С) существует зависимость: It = 1о *Ю'Е 1 с (3), где С - концентрация вещества, поглощающего свет, г моль / л; 1 - толщина слоя раствора, поглощающего свет, см; в - молярный коэффициент поглощения, он зависит от природы вещества, поглощающего свет, от выбранной длины волны и от температуры. Используя уравнение 1: Т = 10 "81 с (4). Используя уравнение 2: D = sic, откуда видно, что D прямопропорционально концентрации вещества в растворе, и график зависимости D от С будет выражаться прямой линией, идущей из начала координат [1].
Фотоколориметрия Интенсивность прошедшего через раствор света меняется не только от концентрации и высоты слоя раствора, но и от изменения интенсивности входящего светового потока. При фотоколориметрических определениях об интенсивности прошедшего через раствор света можно судить по силе фототока.
Определения проводят в фотоколориметрах (ФЭКах). Наиболее распространены ФЭКи « двуплечие » - с 2 фотоэлементами, каждый из которых снабжен диафрагмой. И оба фотоэлемента включены в общую схему так, чтобы даваемые ими фототоки имели противоположные направления. При одинаковой освещенности обоих фотоэлементов (одинаковая окраска стандартного и испытуемого растворов) токи от них в цепи гальванометра взаимо компенсированы и стрелка гальванометра стоит на «О». Разница в интенсивности окраски вызовет изменение фототока, которое можно будет заметить по отклонению стрелки гальванометра.
В лабораторных условиях применяют ФЭК-56, ФЭК-56М и др. Источником света в приборе служит лампа накаливания и ртутнокварцевая лампа сверхвысокого давления. С этими лампами возможна работа в диапазоне длин волн от 315 до 630 ммк. Световой поток от источника света через светофильтр попадает на призму, делящую пучок на правый и левый. Источник света помещен так (в фокусе линз), что световые пучки, отражаясь от зеркала, выходят параллельными. Далее световые потоки проходят через кюветы и попадают на линзы. В фокусе линз помещены матовые стекла, за которыми расположены фотоэлементы. В правый поток могут последовательно включаться кюветы с раствором и растворителем. Раздвижная диафрагма при вращении связанного с ней барабана меняет свою площадь, поэтому меняет интенсивность светового потока, падающего на правый фотоэлемент. Диафрагма, расположенная в левом пучке, ослабляет интенсивность светового потока, который падает на левый фотоэлемент. Левый пучок является компенсационным, правый - измерительным. На задней стенке корпуса помещен осветитель, позволяющий регулировать положение ламп вращением нескольких винтов [4].
2.2 Колориметрический метод определения подвижного фосфора в почве и удобрениях по Кирсанову
РЕАКТИВЫ: 1. раствор 0,2 молярной соляной кислоты;
2. раствор 0,1 молярной соляной кислоты;
3. молибденовые реактивы А и Б;
4. оловянная палочка или хлорид олова (+2) с концентрацией
2,5%;
5. образцовые растворы фосфатов.
ПРИГОТОВЛЕНИЕ РАСТВОРА МОЛИБДАТА АММОНИЯ (РЕАКТИВ А)
На аналитических весах отвешивают 50 г молибдата аммония и помещают в стакан, приливают 200-300 мл дистиллированной воды и нагревают до 50-60 градусов Цельсия. После растворения пореносят в мерную колбу на 500 мл, охлаждают, доводят объём дистиллированной водой до метки. К 100 мл приготовленного раствора приливают 200 мл соляной кислоты (плотность раствора = 1,18- 1,19 г/мл) и 100 мл диет. воды. Реактив бесцветный или имеет жёлтый оттенок. Его можно хранить долгое время в склянке из коричневого стекла с притертой пробкой. Из реактива А готовят реактив Б. Берут один объём реактива А, к нему добавляют четыре объёма диет. воды. Реактив должен быть бесцветным и его хранят в склянке из коричневого стекла. ИЗГОТОВЛЕНИЕ ОЛОВЯННОЙ ПАЛОЧКИ. Палочку размером 3-4 мм готовят из химически чистого олова. Его расплавляют в фарфоровой чашке, т. к. олово легко окисляется при повышенной температуре, необходимо избегать перегрева. Для этого следует нагревать чашку на электроплитке или на горелке с асбестовой сеткой, положенной на чашку. Расплавленное олово при помощи водоструйного насоса втягивают в тонкостенную трубочку с внутренним диаметром 3-4 мм, предварительно нагретую. Когда трубка с оловом остынет, её разбирают. Т. о. получают хорошую оловянную палочку (без пустот и раковин на поверхности).
ПРИГОТОВЛЕНИЕ РАСТВОРА ХЛОРИДА ОЛОВА (+2). 2,5 г олова при температуре растворяют на водяной бане в 100 мл с массовой долей НС1 10%
(раствор готовят в день проведения анализа). Для устранения мути, обусловленной присутствием в реактиве некоторого количества хлорида олова (+4), к горячему раствору добавляют несколько крупинок металлического олова, наструганного напильником.
ПРИГОТОВЛЕНИЕ ОБРАЗЦОВЫХ РАСТВОРОВ ФОСФАТОВ. На
аналитических весах отвешивают 0,2424 г химически чистого Са(Н2Р04)2, навеску растворяют в 0,2 М растворе соляной кислоты и этой же кислотой раствор доводят до 1л ( Са(Н2Р04)2 может быть заменен КН2Р04 - тогда
0,1917г вещества растворяют в 0,2 М растворе соляной кислоты ). Из этого основного раствора (100 мг Р205 в 1л) готовят рабочий раствор фосфата. В мерные колбы по 100 мл, пронумерованные от 1 до 12, наливают пипеткой 2,5; 5,0; 7,5; 10,0; 12,5; 15,0; 17,5; 20,0; 25,0; 25; 30,0; 40,0; 50,0 мл основного раствора фосфата. Колбы доливают 0,2 М раствором соляной кислоты до 100 мл, закрывают пробками и хорошо перемешивают. Полученными растворами пользуются для приготовления шкалы образцов в пробирках, с которыми сравнивают исследуемые растворы.
ПРИГОТОВЛЕНИЕ ШКАЛЫ СТАНДАРТНЫХ РАСТВОРОВ. Отобрать 12 одинаковых пробирок. Разместить их в штативе и пронумеровать. В каждую пробирку пипеткой перенести по 5 мл соответствующего образцового раствора стандартной шкалы из мерных колб ёмкостью 100 мл и прилить по 5 мл реактива Б. При наличии одной пипетки, её нужно постоянно ополаскивать диет, водой или начинать отбор проб с образцовых растворов, имеющих наименьшую концентрацию и постоянно переходить к растворам с большей концентрацией. Растворы в пробирках перемешивать оловянной палочкой пока не появится устойчивая окраска (20-30 сек). Можно воспользоваться 0,2% раствором хлорида олова (+2), прибавляя его по 0,5 мл Растворы колориметрировали на ФЭКе (длина волны = 670 нм, кювета 5,075) Результаты измерений приведены в таблице 3.
№ п/п | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
Устанд. р-ра, мл | 2,5 | 5,0 | 7,5 | 10,0 | 12,5 | 15,0 | 17,5 | 20,0 | 25,0 | 30,0 | 40,0 | 50,0 |
Р2О5 в мг в 100мл | 0,25 | 0,5 | 0, 75 | 1,0 | 1,25 | 1,50 | 1,75 | 2,0 | 2,5 | 3,0 | 4,0 | 5,0 |
Р205 в ст. р-ре на 100г | 1,25 | 2,5 | 3, 75 | 5,0 | 6,25 | 7,5 | 8,75 | 10,0 | 12,5 | 15,0 | 20,0 | 25,0 |
Р2О5, мг/кг | 12,5 | 25 | 37, 5 | 50,0 | 62,5 | 75 | 87,5 | 100 | 125 | 150 | 200 | 250 |
D станд р-ра | 0,01 | 0, 05 | 0, 15 | 0,20 | 0,25 | 0,33 | 0,37 | 0,41 | 0,55 | 0,75 | 0,89 | 1,12 |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



