Для определения условий эффективного извлечения ионов меди и других компонентов из сточных вод путем их осаждения был проведен термодинамический анализ химических процессов взаимодействия ионов меди с другими компонентами жидкой фазы сточных и оборотных вод. Расчеты, представленные в виде уравнений реакций межфазных переходов, термодинамических характеристик этих реакций (ΔG0 и lgK), а также соответствующих им соотношений между концентрациями ионно-молекулярных компонентов реакций и термодинамически стабильных соединений в координатах Lg[Cu2+] – pH, Lg[HnCO3m-] – pH, представляют собой физико-химическую модель, позволяющую оценить равновесные концентрации компонентов в стоках [6].
Таблица 2
Результаты анализа состава жидкой фазы различных участков хвостохранилища.
Параметры | Зона освет- ленной воды | Зона свежих песков | Зона окислен- ных песков | Зона фильтрации |
[o2], мг/л | 5,0-6,3 | 4,6-5,6 | 0,4-5,1 | 0,4-0,8 |
[НСo3-], мг/л | 45-83 | 23-54 | 34-113 | 13-65 |
рН | 8,0-8,6 | 9,8 – 10,3 | 7,6-8,5 | 5,4 – 6,9 |
[Сu2+], мг/л | менее 0,1 | менее 0,1 | 0,1-1,5 | 3,5-6,0 |
[Fe3+], мг/л | менее 0,1 | менее 0,1 | менее 0,1 | 0,15-3,6 |
[SO42-], мг/л |
При моделировании учитывались фактически имеющиеся концентрации ионно-молекулярных компонентов в стоках и требования технологического процесса, в котором предполагается использование очищенных вод.
Построенная и представленная на рис. 2 диаграмма рассчитана для следующих граничных условий: [HnCO3m-] = [H2C03 + HCO3- + CO32-] = 10-4 моль/л, [HOl +Ol-] = 10-5 моль/л, что соответствует вышеперечисленным условиям и требованиям.
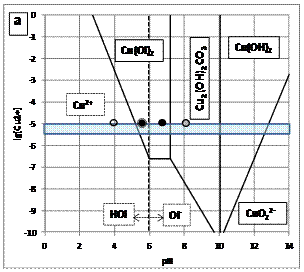
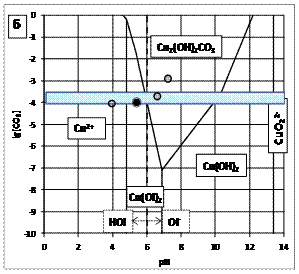
Рис. 2. Диаграммы термодинамической стабильности соединений меди в сточных водах в присутствии жирных кислот и растворенных форм угольной кислоты с результатами спектральной проверки состава образующихся соединений: ![]() – олеиновая кислота;
– олеиновая кислота; ![]() - олеат меди и олеиновая кислота;
- олеат меди и олеиновая кислота; ![]() - олеат меди;
- олеат меди; ![]() - гидроксидокарбонат меди;
- гидроксидокарбонат меди; - технологически допустимые концентрации ионов меди и угольной кислоты
- технологически допустимые концентрации ионов меди и угольной кислоты
На диаграммах приведены результаты проверки состава осадков, образующихся при подщелачивании и карбонатизации исследуемых оборотных вод, проведенной с использованием метода инфракрасной спектроскопии получаемых осадков и тонкодисперсных образований, устойчиво сохраняющихся в жидкой фазе пульпы.
Анализ результатов расчетов и проверки состава осадков показывает, что при наличии в стоках ионов и соединений олеиновой кислоты суммарной концентрацией более чем 10-6 моль/л (0,3 мг/л) происходит их взаимодействие с ионами меди, сопровождающееся образованием нормального олеата меди. Реакция протекает в слабокислой и нейтральной средах. При снижении концентрации ионов меди и олеиновой кислоты образования олеата меди не происходит. При увеличении рН до слабощелочной олеат меди переходит в гидроксокарбонат меди.
Равновесие олеата меди и гидроксокарбоната меди в стоках иллюстрируется диаграммой на рис.3б, при построении которой в качестве исходных условий были выбраны: равновесная концентрация ионов меди 10-4 моль/л (6 мг/л), концентрация олеат-ионов – 10-6 моль/л (0,3 мг/л). Такие концентрации отражают состав сточных вод при исходном смешивании фильтратов хвостохранилища и очищенных хозбытовых стоков.
Анализ диаграммы показывает, что при одновременном воздействии ионов и соединений олеиновой кислоты и карбонат-ионов различной концентрации форма осаждения меди меняется. При малых концентрациях карбонат-ионов происходит преимущественное образование олеата меди. Реакция устойчиво протекает в слабокислой и нейтральной средах.
При повышении щелочности среды олеат меди переходит в гидроксид меди, а при одновременном повышении концентрации карбонатов – в гидроксокарбонат меди. Смещение рН в кислую область является также нежелательным процессом, поскольку приводит к растворению олеата меди с переходом в раствор катионов меди и молекул олеиновой кислоты, отрицательно влияющим на показатели флотационного обогащения.
Использование результатов моделирования, представленных в виде диаграмм в координатах lg[Cu2+] – pH и lg[НnCО3m-] – pH (рис. 3), показывает, что условием поддержания концентраций ионов меди в фильтратах на технологически приемлемом уровне (10-5 моль/л или 0,6 мг/л) является поддержание рН фильтрата в интервале от 5,6 до 7,3. Эти же условия обеспечивают поддержание концентраций ионов меди на экологически безопасном уровне.
Разработанная физико-химическая модель может быть использована для выбора условий наиболее полного осаждения олеат-ионов. Анализ диаграмм на рис.3 показывает, что областью приоритетного образования олеата меди является граница перехода меди из ионной формы в форму гидроксокарбоната, описываемого реакцией
2Cu2++НCO3- + 2H2О = Cu2(OH)2CO3 + 3H+ (pH > 6,
Следовательно, соотношение между ионно-молекулярными компонентами при этом переходе выражаются уравнением
2lg [Cu2+] +lg [НCO3- ] + 3pH = - lgK1 (2)
Преобразовав уравнение 2 и, подставив в него требуемую концентрацию ионов меди (0,6 мг/л или 10-5 моль/л) и среднюю концентрацию бикарбонат ионов для рассматриваемых условий, можно рассчитать необходимое значение рН среды:
рН = lgK1/3 - 2lg [Cu2+]/3 - lg[НCO3-]/3 = 6,
Поддержание расчетного значения рН фильтрата является необходимым условием для наиболее полного осаждения олеат-ионов в олеат меди при любой их концентрации.
Однако, при высокой исходной концентрации ионов меди, существенно превышающей мольную концентрацию олеат-ионов, полное связывание последних не будет условием полного связывания самих ионов меди в нерастворимые соединения. В таких условиях целесообразно вести процесс осаждения в условиях одновременного протекания реакции 1 и реакции
Cu2++2Ol - = Cu(Ol)2 , (4)
описываемых суммарным уравнением
2Cu(Ol)2+НCO3- + 2H2О = Cu2(OH)2CO3 +4Ol - + 3H+ (5)
и соответствующим соотношением между концентрациями ионов:
lg[НCO3- ] - 4lg[Ol-] + 3pH = - lgK5 (6)
Преобразовав уравнение 6 и подставив в него требуемую концентрацию олеат-ионов (0,1 мг/л или 3*10-6 моль/л) и среднюю концентрацию бикарбонат ионов для рассматриваемых условий, можно рассчитать необходимое значение рН среды:
pH = - lgK5/3 + lg[НCO3- ]/3 + 4lg[Ol-]/3 = 7,24 (7)
Таким образом, проведенный термодинамический анализ позволил разработать физико-химическую модель, описывающую протекание химических процессов в сточных водах и позволяющую определять оптимальные условия проведения процессов кондиционирования сточных вод, в частности рН среды.
Для проверки результатов расчетов была использована лабораторная установка, моделирующая процессы взаимодействия компонентов жидкой и твердой фаз в сточных водах. Установка обеспечивала поддержание заданной температуры и необходимого режима контакта растворов с углекислотой воздуха. Состав жидкой фазы подбирался в соответствии со значениями параметров, характерными для промышленных стоков ГОКа. Продолжительность осаждения изменялась в интервале от 10 до 240 мин.
В исходный раствор, который содержал заданное количество растворимой соли меди, добавляли заданное количество раствора гидроокиси натрия, необходимое для создания определенной щелочности. При необходимости поддерживался контакт раствора с воздухом для обеспечения равновесных концентраций растворенной углекислоты и бикарбонатных ионов - до 43,3 мг/л.
Полученные зависимости осаждения соединений меди от щелочности (кислотности) раствора при продолжительности взаимодействия 240 мин (рис. 3), демонстрируют, что оборотные воды характеризуются переменными значениями ионно-молекулярного состава, обусловленными протекающими процессами образования нерастворимых соединений.
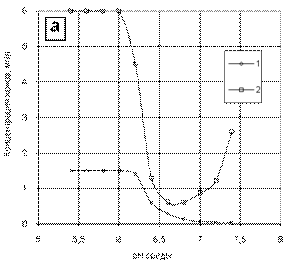
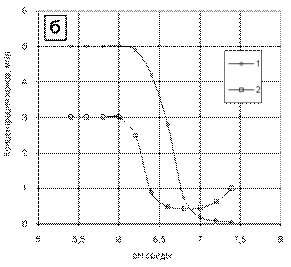
Рис. 3. Зависимости изменения концентраций ионов меди (1) и олеиновой кислоты (2) при варьировании рН сточных вод с преобладанием жирных кислот (а) и ионов меди (б)
Анализ данных зависимостей показывает, что с повышением рН концентрация ионов меди закономерно снижается, в то время как зависимость концентрации олеат-ионов от рН носит более сложный характер и имеет минимум в области рН от 6,5 до 6,8, что соответствует результатам термодинамического моделирования.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



