Выявленные с помощью множественного критерия Дункана различия средних величин фактора С показали, что наилучшие результаты по насыпной массе обеспечивают наполнители, имеющие наибольший размер частиц. В результате комплексного анализа установлено рациональность использование в прописи порошка микрокристаллической целлюлозы, имеющей перед лактозой биологические, технологические и экономические преимущества.
Ранжирование фактора В позволило определить, что оптимальное количество аэросила находится в интервале 0,5 % до 2,5 %, что позволяет использовать аэросил в составе порошка в минимальном количестве (0,5 %). На прирост влагопоглощения, факторы, используемые в данном эксперименте, влияния не оказывают.
Обобщение полученных результатов позволило выявить основные технологические параметры порошкообразных смесей, позволяющие получать качественные дозированные порошки на основе бифидобактерий: наполнитель с наибольшим размером частиц независимо от его химической природы, соотношение наполнителя – лиофилизированную биомассы бифидобактерий 2:1, а также содержание антифрикционного вещества (аэросила) не более 1 %. В процессе получения порошков отмечено, что стадия измельчения и смешивания порошков достаточно трудоемкая, на что надо обратить внимание в процессе перехода к промышленным сериям получения порошка
Определенные нами составы и технология дозированных порошков на основе бифидобактерий признаны рациональными и использованы нами при разработке лабораторного регламента «Бифидобактерин, порошок».
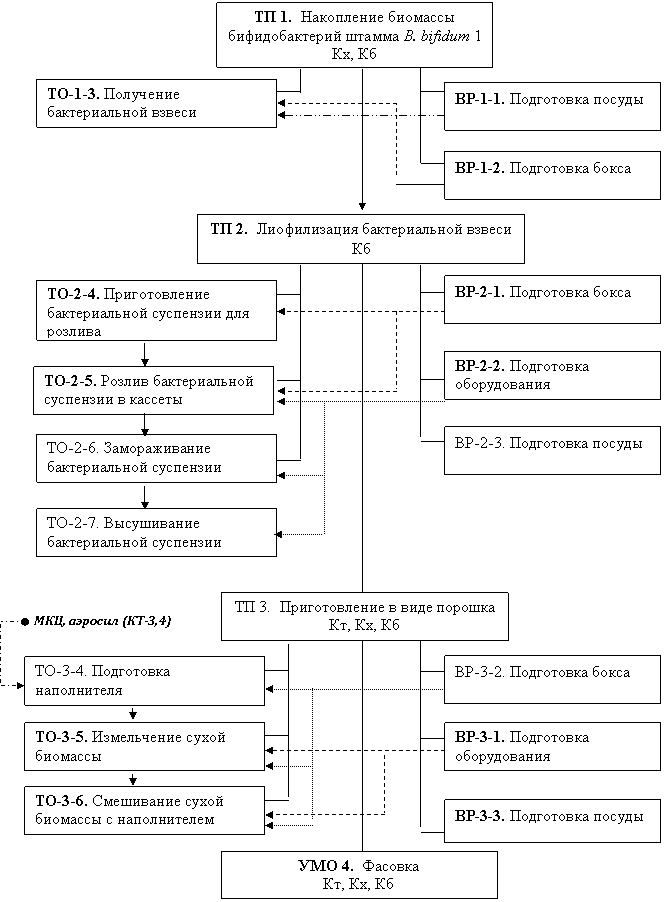
Разработанная технологическая схема получения дозированных порошков бифидобактерий, представленная на рис.5.
Производство дозированных порошков с лиофилизатами бифидобактерий включает несколько этапов:
1 этап: получение нативной микробной взвеси (ТП 1);
2 этап: лиофильная сушка (ТП 2);
3 этап: получение порошка (ТП 3);
4 этап: фасовка и упаковка порошка (УМО 4).
Перечень контрольных точек технологического процесса производства представлен в табл. 7.
Анализ качества лекарственной формы в виде дозированного порошка в пакетах было установлено, что во всех сериях порошок имел беловато-серый цвет со специфическим запахом и вкусом. При определении подлинности бактериоскопическим методом в мазках, окрашенных по Граму, обнаруживались грамположительные полиморфные палочки с бифуркациями, располагающиеся в виде скоплений или отдельных клеток.
При определении растворимости содержание пакетов растворялось в течение 5 минут с образованием гомогенной массы беловато-серого цвета.
Отклонение от средней массы при взвешивании содержимого пакетов находилось в пределах ±5 %. Показатель потери массы при высушивании не превышал 5 % от всех исследуемых образцов. Значения рН порошков определялись потенциометрически и находились в пределах 5,7-6,7.
Все серии препарата были безвредны для белых мышей при пероральном введении 0,5 мл взвеси препарата, полученной при разведении раствором натрия хлорида 0,9 % из расчета 0,5 мл на 1 дозу.
 |
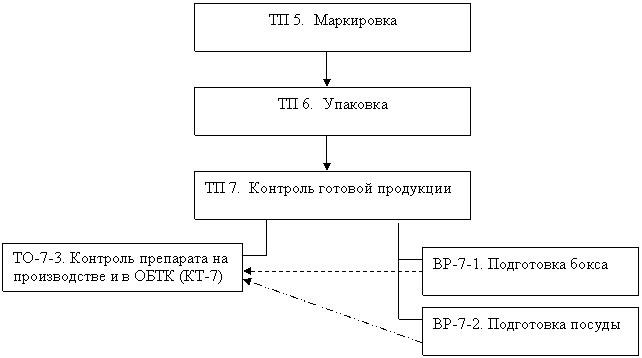 |
Рис. 5. Технологическая схема получения дозированных порошков
с бифидобактериями
Таблица 7
Перечень контрольных точек технологического процесса производства
КТ | Наименование этапа | Контролируемый показатель |
КТ-1 | ТП-1Накопление биомассы бифидобактерий штамма B. bifidum 1 | Контроль бактериальной взвеси: - рН=5,5-6,5; - активность кислотообразования не ниже 900Т; - содержание живых бифидобактерий в 1 мл не менее 1×108; - не должна содержать посторонней микрофлоры |
КТ-2 | ТП-2. Лиофилизация бактериальной культуры | Контроль сухой биомассы: - рН=5,5-6,5; - активность кислотообразования не ниже 90 0Т; - содержание живых бифидобактерий в 0,3 г не менее 1×108; - не должна содержать посторонней микрофлоры |
КТ-3 | ТП-3. Приготовление порошка | Испытания микрокристаллической целлюлозы |
КТ-4 | ТП-4. Приготовление порошка | Испытания аэросила по показателям безопасности ГОСТ |
КТ-5 | ТП-5. Приготовление порошка | Контроль порошка в производственном подразделении: -рН=5,0-6,5; -активность кислотообразования не ниже 900Т; -содержание живых бифидобактерий не менее |
КТ-6 | УМО-4. Фасовка | Средняя масса порошка 0,90+0,045 г |
КТ-7 | Контроль готовой продукции | Контроль препарата в ОБТК: - органолептические свойства; - подлинность; - рН=5,0-6,5; - потеря в массе при высушивании не более 5,0 %; - средняя масса порошка 0,90+0,045 г; - активность кислотообразования не ниже 90 0Т; - содержание живых бифидобактерий не менее - микробиологическая чистота |
Контролируемые серии характеризовались отсутствием посторонних микроорганизмов и грибов. При определении количества живых микробных клеток в 1 дозе препарата содержание жизнеспособных бифидобактерий не менее 108 КОЕ. Показатель активности кислотообразования во всех испытуемых образцах не менее 90 ºТ.
Полученный и проконтролированный препарат «Бифидобактерии порошок» в количестве 5 серий заложен на хранение в сухое, защищенное от света место при температуре от 2 до 10 ºС.
Порошки всех серий через 1 год 3 месяца не изменили своих свойств и соответствовали, предъявляемым требованиям по всем показателям: внешнему виду, подлинности, растворимости, средней массе, показателю рН, потери в массе при высушивании, безвредности, отсутствию посторонних микроорганизмов и грибов, специфической активности. Полученные материалы позволили установить срок хранения для данной лекарственной формы – 1 год.
Получение и исследование биологических и технологических свойств синбиотических препаратов бифидобактерий с лактулозой
(глава 5).
В 5 главе описаны экспериментальные исследования, связанные с созданием комбинированного препарата на основе бифидобактерий с лактулозой в виде дозированного порошка. При этом проведена оценка биологического и технологического влияния лактулозы на бифидобактерии, обоснована методика количественного определения этого пребиотика в экспериментальных образцах, а также установлен оптимальный способ введения лактулозы в состав комплексного препарата.
В ходе создания комбинированного препарата на основе бифидобактерий в виде дозированного порошка, с учетом предполагаемой сферы применения препарата, представляло научный интерес оценить биологическое и технологическое влияние лактулозы на качество порошков с бифидобактериями.
Экспериментально в условиях «in vitro» показано, что традиционные культуральные микробиологические способы не позволяют выявить бактериотропные свойства лактулозы. Анализируя возможные методические подходы к оценке биологической активности пребиотика нами апробирован новый методический подход к оценке эффективности пребиотических препаратов с помощью экспресс - теста ингибирования биолюминесценции индикаторного штамма (, 2003). В качестве критерия эффективности использовали показатель индекса анагонистической активности пребиотика, определяемый методом ингибирования биолюминесценции тест-штамма Escherichia coli lum + C-50 при кратковременной совместной экспозиции с образцом лактулозы.
При анализе полученных данных установлена существенная зависимость биолюминесценции Escherichia coli lum + C-50 от концентрации лактулозы в изучаемых пробах. При этом достаточно высокий уровень на протяжении всего периода экспозиции (до ИАА = 60) обеспечивал наиболее разбавленный раствор лактулозы (0,3 % раствор лактулозы) (рис.6).
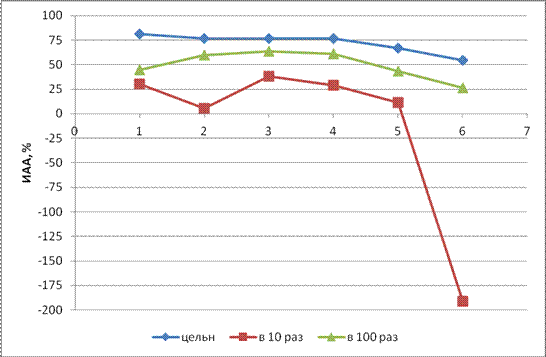
Рис. 6. Уровень стимуляции (гашения) свечения Escherichia coli lum+ С-50
растворами лактулозы
Полученные результаты хорошо согласуются с литературными данными по исследованию влияния лактулозы на бифидобактерии в кисломолочных напитках и учитывались нами при разработке состава комплексного препарата на основе бифидобактерий, содержащего лактулозу.
При исследовании технологических свойств порошков лактулозы установлено, что, хотя она обладает очень хорошей насыпной плотностью (714,29±0,02) кг/м³ и отличной сыпучестью (12,70±3,94)г/с, лактулоза относится в категории гигроскопичных веществ с высокой скоростью прироста влагосодержания. Учитывая гигроскопичные свойства порошка лактулозы, в последующих экспериментах ее вводили в виде раствора в состав защитной среды на этапе получения биомассы. Комплексным анализом технологических свойств установлено, что биомасса V, в состав которой был введен раствор лактулозы, характеризуется увеличением показателей насыпной плотности и сыпучести, а также уменьшением прироста влагопоглощения по сравнению с другими биомассами. Это говорит о перспективности использования данной биомассы в дозированных порошках.
Все композиции порошков показали удовлетворительную сыпучесть, и высокие показатели насыпной плотности. Наименьший прирост влагопоглощения показала серия 21, содержащая в своем составе биомассу I (1:2), лактозу и 1% аэросил, 45% МКЦ и 10% лактулозу.
Таблица 8
Составы порошков бифидобактерий с лактулозой
Компоненты | Составы | ||||||
15 | 16 | 18 | 19 | 20 | 21 | ||
Биомасса I | 1:1,5 | + | + | + | |||
1:2 | + | + | + | ||||
Лактоза | + | + | |||||
Аэросил | 1% | + | + | + | |||
2% | + | + | |||||
МКЦ | 45% | + | + | ||||
90% | + | + | + | + | |||
Лактулоза 10% | + | + | + | + | + | + |
Таким образом, введение лактулозы в состав защитной среды позволяет получить качественные порошки, имеющие удовлетворительные технологические свойства. На основании полученных результатов внесены изменения в технологическую схему получения дозированных порошков бифидобактерий с лактулозой на стадии получения защитной среды и внесения вспомогательных веществ.
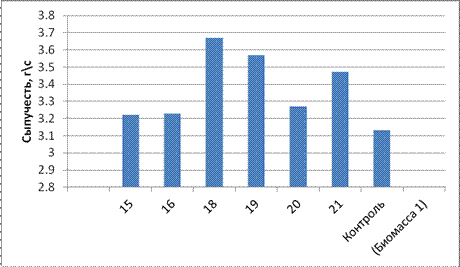
рис.7. Сыпучесть порошков с лактулозой
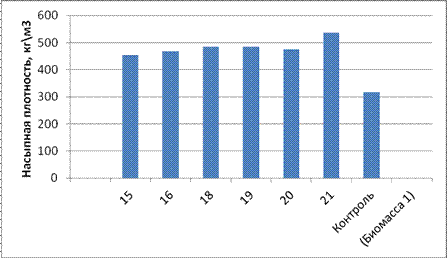
Рис.8. Насыпная плотность порошков с лактулозой

Рис. 9. Хроматограмма доз порошка с лактулозой
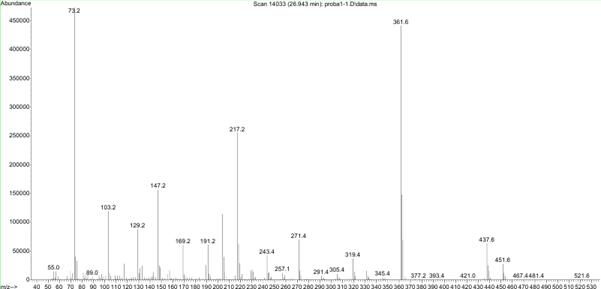
Рис. 10. Масс-спектр силированной лактулозы
По предложенной технологии наработано и простандартизировано 5 серий комплексного препарата бифидобактерий с лактулозой. В количестве 5 серий синбиотик заложен на хранение в сухое, защищенное от света место при температуре от 2 до 10 ºС. Кроме показателей стандартизации дозированных порошков с бифидобактериями по методике газохромато-масс-спектрометрии (рис.9 и 10) установлено, что содержание лактулозы в одной дозе составляет 70±0,07 мг. При хранении в течение 1 года 3 месяцев порошки всех серий не изменили своих свойств и соответствовали, предъявляемым требованиям по всем показателям: внешнему виду, подлинности, растворимости, средней массе, показателю рН, потери в массе при высушивании, безвредности, отсутствию посторонних микроорганизмов и грибов, специфической активности и содержанию лактулозы. Полученные материалы позволили установить срок хранения для данной лекарственной формы – 1 год.
ВЫВОДЫ
1. Обоснован методологический подход к созданию структуры дозированных порошков с лиофилизатами бифидобактерий пригодных для промышленного производства, включающий выбор фракционного состава используемого наполнителя, а также оптимального соотношения биомассы и вспомогательных веществ.
2. С использованием математических методов планирования установлены рациональные параметры технологического процесса получения дозированных порошков на основе бифидобактерий
3. В результате проведенного комплекса технологических и биологических исследований определены оптимальные составы дозированных порошков синбиотиков бифидобактерий с микрокристаллической целлюлозой и лактулозой.
4. Показана целесообразность применения методики газохромато-масс-спектрометрии с использованием О-триметилсилиловых производных для определения лактулозы в составе дозированных порошков синбиотиков на основе бифидобактерий. Оптимальное содержание лактулозы в порошке составило 70±0,7 мг.
5. Разработаны показатели стандартизации дозированных порошков синбиотиков на основе бифидобактерий и исследована стабильность экспериментальных образцов лекарственных форм.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Григорян, Л. Г., Москотина, состава наполнителя для дозированных порошков на основе бифидобактерий/ , // Вестник Пермской государственной фармацевтической академии, 2009 – № 5.- С.218-220.
2. Молохова, Е. И., Григорян, исследования по разработке дозированных порошков бифидобактерина с лактулозой // Разработка, исследование и маркетинг новой фармацевтической продукции Сборник научных трудов. – Пятигорск, 2009.- вып.64.- С. 190-192.
3. Молохова, Е. И., Биофармацевтическая оценка лекарственных форм препаратов-пробиотиков / , , / сборник материалов XVII Российского национального конгресса «Человек и лекарство», 2010.- С.683.
4. Молохова, Е. И., Выбор марки лактозы для дозированных порошков с бифидобактериями / , // Сборник трудов III Всероссийской конференции «Биотехнология и биомедицинская инженерия». - Курск, 2010.- С.124-126.
5. Молохова, Е. И., Влияние технологических параметров вспомогательных веществ на качество порошков с бифидобактериями / , // Вестник РУДН 2010.-Медицина. – Москва, 2010.- С. .357-360 (статья ВАК).
6. Молохова, Е. И., Вспомогательные вещества, перспективные для создания лекарственных – форм пробиотиков/ , , // тезисы Всероссийской научно-практической конференции «Вакцинология 2010. Совершенствование иммунобиологических средств профилактики, диагностики и лечения инфекционных болезней»- М.,2010, С.85.
7. Зерда Тешфа, Использование микрокристаллической целлюлозы в составе дозированных порошков с бифидобактериями / Зерда Тешфа, // Вестник Пермской государственной фармацевтической академии. – Пермь, 2010. - № 6. – С. 248-250.
8. Григорян, Л. Г., О возможности использования лактулозы в качестве компонента дозированных порошков с бифидобактериями / , // Разработка, исследование и маркетинг новой фармацевтической продукции Сборник научных трудов. – Пятигорск, 2011.- вып.66.- С. 249-251.
9. Молохова, Е. И., Экспериментальное обоснование состава твердых дозированных лекарственных форм с бифидобактериями / , , // Сибирский медицинский журнал. – Томск, 2011. – Т.26, вып. 2. – С. 85-88 (статья ВАК).
(Россия)
Разработка технологии и стандартизация дозированныхпорошков симбиотиков на основе бифидобактерий
Изучены технологические характеристики лиофилизированных биомасс бифидобактерий с модифицированными защитными средами и различных марок лактозы и микрокристаллической целлюлозы, рекомендуемых для промышленного производства дозированных порошков. Комплексным анализом технологических свойств показано, что лиофилизат, в состав которой был введен раствор лактулозы, характеризуется увеличением показателей насыпной плотности и сыпучести, а также уменьшением прироста влагопоглощения по сравнению с другими биомассами. Это говорит о перспективности использования данной биомассы в дозированных порошках.
Установлены технологические факторы, влияющие на процесс получения дозированных порошков с бифидобактериями: фракционный состав наполнителей, количество антифрикционного вещества, режимы перемешивания. Разработана технология дозированных порошков на основе бифидобактерий с использованием дисперсионного метода анализа латинского квадрата. Обоснован состав дозированных порошков с бифидобактериями: сухая биомасса бифидобактерий – 0,300 г, микрокристаллическая целлюлоза МКЦ МС 500 (Vivapur 14) – 0,595 г, аэросил – 0,005 г
Проведена оценка биологического и технологического влияния лактулозы на бифидобактерии, разработана методика количественного определения газохромато-масс-спектрометрии этого пребиотика в экспериментальных образцах, а также подобран состав симбиотика, содержащего бифидобактерии и лактулозу.
Technological characteristics of freeze-dried biomass of bifidobacteria with modified protective environments as well as different grades of lactose and microcrystalline cellulose, which are recommended for the industrial production of powders, were studied. It was found that lyophilizate with lactulose solution is characterized by increased parameter of bulk density, flow properties and reduced water absorption rate compared to other biomass. Application of this biomass was found to be perspective for powder production.
Technological factors such as the size distribution of fillers, the amount of anti-friction material, mixing regimes were studied and found to be important for the production of powders with bifidobacteria. Technology of powders with bifidobacteria was developed. The composition of powders with bifidobacteria was proved (dry biomass of bifidobacteria - 0,300 g, microcrystalline cellulose MCC MS 500 (Vivapur 14) – 0,595 g, аerosil - 0,005 g).
Evaluation of biological and technological influence of lactulose on bifidobacteria was carried out. GC-MS method for quantitative determination of this prebiotic was position of symbiotic with bifidobacteria and lactulose was determined.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



