Министерство образования Российской Федерации
Алтайский государственный технический университет
Бийский технологический институт
ёв,
МАТЕРИАЛОВЕДЕНИЕ И ТЕХНОЛОГИЯ КОНСТРУКЦИОННЫХ МАТЕРИАЛОВ
Курс лекций
Барнаул 2001
УДК 621.385
, Обложкина и технология конструкционных материалов: Курс лекций.
Алт. гос. техн. ун-т, БТИ. - Бийск.
Изд-во Алт. гос. техн. ун-та, 2001. - 224 с.
В курсе лекций, читаемых авторами в БТИ АлтГТУ, рассмотрены основы физических явлений, происходящих в диэлектрических, проводниковых, полупроводниковых и магнитных материалах, проведена классификация материалов по их электротехническим, физико-химическим и механическим свойствам и областям применения. Рассматриваются технологии производства конструкционных материалов и изготовления из них различных изделий.
Курс лекций предназначен для подготовки специалистов по направлению 653700 «Приборостроение» и специальности 190900 «Информационно-измерительная техника и технологии».
Лекции 1-12 разработаны , лекции 13-15 -
Рассмотрен и одобрен на
заседании кафедры
методов и средств измерений
и автоматизации.
Протокол №17 от 01.01.2001 г.
Рецензент: к. т.н., зав. каф. МРСиИ
ISBN 5-9257-0015-5
ã , , 2001
ã БТИ АлтГТУ, 2001
Лекция 1
ОБЩИЕ СВЕДЕНИЯ О СТРОЕНИИ ВЕЩЕСТВА
1.1 Виды связи
Основными элементарными частицами, из которых строятся все известные нам вещества, являются протоны, нейтроны и электроны.
Из протонов и нейтронов состоят атомные ядра, электроны заполняют оболочки атома, компенсируя положительный заряд ядра. Строение ядер атомов, периодичность заполнения оболочек электронами можно находить с помощью таблицы .
Газы, жидкие и твердые тела могут состоять из атомов, молекул или ионов. Размеры атомов - порядка ангстрема, размеры положительных ионов, получившихся из атомов, лишившихся части электронов, меньше, чем размеры атомов, а размеры отрицательных ионов, присоединивших дополнительные электроны, больше, чем размеры соответствующих атомов. Ионами могут быть и группы атомов, потерявших или присоединивших электроны.
Молекулы газов содержат различное число атомов. Так, например, гелий, аргон, неон - одноатомные газы, водород, азот, кислород, окись углерода состоят из двухатомных молекул, углекислый газ, водяной пар - из трехатомных. Молекула аммиака построена из четырех атомов, а метана - из пяти. В зависимости от строения внешних электронных оболочек атомов могут образовываться различные виды связи.
Ковалентной называется связь атомов друг с другом, достигаемая за счет электронов, которые становятся общими, как это схематически показано для двухатомной молекулы на рисунке 1.1. Ковалентная связь наблюдается в молекулах, образованных металлоидными атомами, например, в молекуле хлора и др.
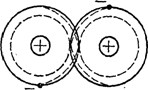
Рисунок 1.1 - Двухатомная молекула с ковалентной связью
Молекулы, в которых центры положительных и отрицательных зарядов совпадают, являются нейтральными.
Если же в отдельных молекулах центры противоположных по знаку зарядов не совпадают и находятся на некотором расстоянии друг от друга, то такие молекулы называются полярными или дипольными.
Полярная молекула характеризуется величиной дипольного момента, который определяется произведением заряда и расстояния между центрами положительного и отрицательного зарядов.
Ковалентная связь может быть как в молекулах (в трех агрегатных состояниях вещества), так и между атомами, образующими решетку кристалла. Примерами таких кристаллов служат алмаз, кремний, германий. Ковалентной связью могут удерживаться не только одинаковые атомы, но и различные.
Второй вид связи - ионная связь - определяется силами притяжения между положительными и отрицательными ионами. Твердые тела ионной структуры характеризуются повышенной механической прочностью и относительно высокой температурой плавления. Типичными примерами ионных кристаллов являются галоидные соли щелочных металлов.
На рисунке 1.2 показаны структуры хлористого натрия и хлористого цезия - плотная упаковка ионов первого вещества и неплотная - второго.
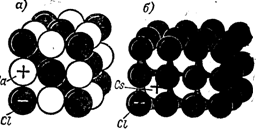
Рисунок 1.2 - Структурная плотная упаковка ионов
хлористого натрия (а), структура и неплотная упаковка
ионов хлористого цезия (б)
Третьим видом связи является металлическая связь. Она также приводит к образованию твердых кристаллических тел. Металлы можно рассматривать как системы, построенные из расположенных в узлах решетки положительно заряженных атомных остовов, находящихся в среде свободных электронов. Притяжение между положительными атомными остовами и электронами является причиной монолитности металла. Наличие свободных электронов приводит к высокой электропроводности и теплопроводности металла, а также является причиной блеска металлов. Ковкость металла объясняется перемещением и скольжением отдельных слоев атомных остовов.
Четвертым видом связи является молекулярная связь (связь Ван-дер-Ваальса). Такая связь существует у ряда веществ между молекулами с ковалентными внутримолекулярными связями. Межмолекулярное притяжение в этом случае обусловливается согласованным движением валентных электронов в соседних молекулах (рисунок 1.3). В любой момент времени электроны максимально удалены друг от друга и максимально приближены к положительным зарядам. При этом силы притяжения валентных электронов положительно заряженными остовами соседних молекул оказываются сильнее сил взаимного отталкивания электронов внешних орбит. Связь Ван-дер-Ваальса наблюдается между молекулами некоторых веществ, например парафина, имеющих низкую температуру плавления, свидетельствующую о непрочности их кристаллической молекулярной решетки.
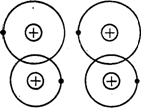
Рисунок 1.3 - Схематическое изображение двух взаимодействующих молекул (связь Ван-дер-Ваальса)
1.2 Строение и дефекты твердых тел
Русский ученый почти на 40 лет раньше, чем были найдены методы рентгеноструктурного анализа, рассчитал возможные расположения частиц в кристаллических решетках различных веществ.
Геометрическая классификация кристаллов недостаточна для распознавания структур, кажущихся тождественными. Они могут обнаруживать различие по двойному лучепреломлению, по пьезо - и пироэлектрическим свойствам, образованию адсорбционных центров, работе выхода электронов и т. п. Это обусловлено различными видами симметрии, насчитывающих 32 класса и объединяющих 230 возможных пространственных групп.
Причина образования каким-либо элементом или соединением данной пространственной решетки в основном зависит от размеров атома и электронной конфигурации его внешних оболочек.
Нарушение правильности строения кристаллов и возможность изменения этих нарушений надо считать таким же неотъемлемым свойством реальных кристаллов, как и правильность их построения из атомов.
Представлению о порядке в мире атомов отвечает кристаллическая решетка со строго периодичным электростатическим полем. Известно, что наиболее высоким порядком как ближнего (в пределах элементарной ячейки), так и дальнего (на больших расстояниях) расположения частиц отличаются химические соединения, когда они находятся в твердом (кристаллическом) состоянии. В случае твердых растворов кристаллических веществ, а также при стеклообразном состоянии можно говорить лишь о той или иной степени ближнего и дальнего порядка расположения частиц (рисунок 1.4). Упорядоченное и неупорядоченное состояние можно наблюдать и в случае высокомолекулярных - полимерных материалов.
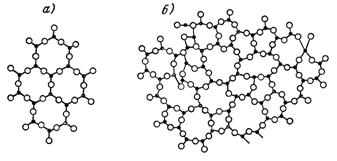
Рисунок 1.4 - Схематическое двумерное изображение строения:
а - решетки кристалла, б - стекла
Практически полное отсутствие порядка в расположении частиц должно быть у аморфных тел.
В электротехнике находят широкое применение материалы с упорядоченным и неупорядоченным строением, и трудно отдать предпочтение тем или иным в отношении практической значимости.
Дефекты строения вещества, от которых зависят особые физические свойства материалов, используются для получения в технике изготовления самых различных материалов и приборов. Сюда относится, в частности, люминесцентная техника, применяющая кристаллы фосфора для осветительных целей, оптических преобразователей, светящихся красок и т. д.
К дефектам кристаллического твердого тела относятся любые нарушения периодичности электростатического поля кристаллической решетки: нарушение стехиометрического состава, наличие посторонних примесей, механически напряженные участки структуры, дополнительные кристаллографические плоскости (дислокации, трещины, поры) и т. д.
По своей природе перечисленные дефекты могут быть или тепловыми или «биографическими». Последние связаны с технологическим процессом получения данного материала.
1.3 Классификация веществ по электрическим свойствам
Все вещества в зависимости от их электрических свойств относят к диэлектрикам, проводникам или полупроводникам. Различие между проводниками, полупроводниками и диэлектриками наиболее наглядно можно показать с помощью энергетических диаграмм зонной теории твердых тел.
Исследование спектров излучения различных веществ в газообразном состоянии, когда атомы расположены друг от друга на больших расстояниях, показывает, что для атомов каждого вещества характерны вполне определенные спектральные линии. Это говорит о наличии определенных энергетических состояний (уровней) для разных атомов.
Часть этих уровней заполнена электронами в нормальном, невозбужденном состоянии атома, на других уровнях электроны могут находиться только после того, как атом подвергнется внешнему энергетическому воздействию, при этом он будет находиться в возбуж-денном состоянии. Стремясь прийти к устойчивому состоянию, атом излучает избыток энергии в момент возвращения электронов на те уровни, где энергия атома минимальна.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 |



