Какой-либо универсальной формулы для U(г), пригодной для всех молекул, .не существует. Обычно потенциал межмолекулярного взаимодействия берут в виде:
![]()
где аi, а2, n т подбираются но требования наилучшей аппроксимации реального потенциала. Для неполярных молекул хорошим приближением является n = 12, m = б при uj и а2, уточняемых для конкретных атомов, из которых состоит молекула. Полученный при этом потенциал называется потенциалом Леннарда-Джонса:
![]()
Отметим, что для неполярных молекул это выражение дополняется членом, учитывающим взаимодействие двух точечных диполей, которое зависит не только от расстояния г, но и от температуры. На рис.8 приведены зависимости потенциальных энергий отталкивания (Г/от), притяжения (Uпр) и их суммы U(r) от расстояния между центрами молекул. Как видно из рис.8, потенциальная кривая U(r)t характеризующая межмолекулярное взаимодействие, имеет вид потенциальной ямы с минимумом при r = rо, которая определяется двумя параметрами: € и Sо - Глубина потенциальной ямы е характеризует максимальную энергию притяжения молекул, So - так называемый нулевой диаметр молекулы (фактически, это минимальное расстояние, на которое могут сблизиться две молекулы, когда полная энергия равна нулю).
Анализируя с помощью потенциальных кривых движение молекул, находящихся в поле межмолекулярных сил, нетрудно определить характер этого движения в зависимости от их полной энергии. Так, например, для образования конденсированного состояния необходимо,
чтобы полная энергия была отрицательной. (При этом потенциальная энергия up абсолютной величине должна быть больше кинетической.)
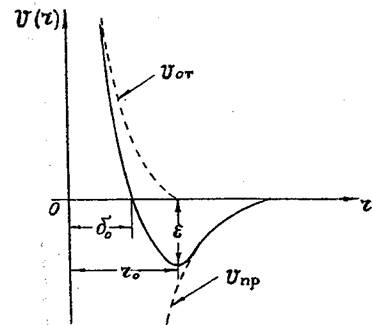
Рис.8. Потенциал межмолекулярного взаимодействия
Силы притяжения действуют при г > tq, силы отталкивания - при г < го - В точке г = го силы притяжения между молекулами компенсируются силами отталкивания (положение равновесия).
Необходимо отметить, что в действительности потенциальные ямы для межмолекулярных взаимодействий узки по сравнению с межмолекулярными расстояниями в газах, что свидетельствует о малости области проявления молекулярных сип.
Наиболее надежные значения для параметров е и sq потенциала Ленварда-Джонса определяются из результатов измерений вязкости разреженных газов, для которых статистическая механика при учете парных столкновении дает строгие выражения. Обычно параметр sq выражают в ангстремах, а вместо величины е используют е* = e/Jb, где k - постоянная Больцмана. Тогда глубина потенциальной ямы измеряется в градусах Кельвина. Ниже приводятся параметры межмо-пекулярвого потенциала для некоторых веществ:
So, (Л) | Э/к, (К) (К) | |
гелии | 2.576 | 10.22 |
£968 | 33.3 | |
3.681 | 91.5 | |
кислород | 3.433 | 113 |
углекислота | 3.897 | 213 |
бензол | 5.27В | 440 |
В заключение отметим, что потенциальная: кривая межмолекуляр-ного взаимодействуя очень напоминает потенциальную кривую, описывающую химическое взаимодействие атомов в молекуле. Однако количественное различие между ними достаточно велико: глубина минимума на кривой ван-дер-ваазьсова взаимодействия очень мала (она измеряется десятыми или даже сотыми электрон-Вольта), в то время как глубина потенциальной ямы на кривой химического взаимодействия порядка нескольких электрон-Водьт.
Другое существенное отличие между обоими видами взаимодействий состоит в томт что межмолекулярные силы притяжения в отличие от химических сил не обладают свойством насыщаемости. Ван-дер-ваальсово взаимодействие существует между всеми молекулами,
находящимися в сфере молекулярного действия. Поэтому силы молекулярного притяжения не приводят к образованию "сверхмолекул", а только содействуют общему стремлению всех молекул сблизиться друг с другом. Это стремление осуществляется при переходе вещества в конденсированное состояние - жидкое или твердое.
ПРИРОДА МЕЖМОЛЕКУЛЯРНОГО ПРИТЯЖЕНИЯ
Межмолекулярное взаимодействие в основном проявляется в виде сил притяжения (так называемых сил Ван-дер-Ваальса). Силы отталкивания между молекулами действуют только на очень малых расстояниях, когда приходят в соприкосновение заполненные электронные оболочки атомов, входящих в состав сближающихся молекул (то есть начинается перекрытие их волновых функций). Понять природу межмолекулярных сил отталкивания можно, только опираясь на представления квантовой механики. 2 Ввиду исключительной сложности этой задачи, обычно используют довольно грубые аппроксимации молекулярного потенциала} описывающего силы отталкивания. При этом, в первую очередь, учитывают короткодействие этих сил. Наиболее распространенным является упомянутый выше потенциал Леннарда-Джонса: U(r) — ai/r12 - a%/r*, где первый член представляет собой
3 При вынужденном сближении двух электронных облаков и их проникновении друг в друга необходимо учитывать так называемые квантовые эффекты обмена. В соответствии с принципом Паули валентно не связанные атомы на малых расстояниях будут испытывать обменное и кулоновское отталкивание. Полное квантовомеханическое рассмотрение этой проблемы очень сложно, т. к. требует учета тонких особенностей волновых функций и их перекрывания.
потенциальную энергию отталкивания Uот = a1/r12. Наряду с этой зависимостью довольно часто используют предположение об экспоненциальном убывании сил отталкивания с расстоянием.
Силы притяжения между молекулами (или атомами) начинают действовать на расстояниях, при которых перекрытие волновых функций еще отсутствует, и квантовыми эффектами можно пренебречь. Можно считать, что ван-дер-ваальсово молекулярное взаимодействие имеет электрическую природу. При этом необходимо помнить, что речь идет об нейтральных атомах и молекулах, поэтому первым вопросом, требующим ответа, является вопрос об электрическом поле нейтральных систем. В принципе, любах нейтральная система с пространственным распределением зарядов создает электрическое (точнее - электромагнитное) поле. Только в случае, если заряды противоположного знака совмещены в одной точке, создаваемые ими поля полностью компенсируют друг друга.
Притяжение между молекулами объясняется на основе так называемого дипольного приближения: взаимодействие между нейтральными молекулами (атомами) сводится к взаимодействию эквивалентных диполей. Вопрос о происхождении собственных дипольных моментов м'о-лекун будет рассмотрен позже. А пока рассмотрим взаимодействие двух молекул, обладающих дипольными моментами![]() соответственно, и найдем их потенциальную энергию.
соответственно, и найдем их потенциальную энергию.
Рассмотрим следующий механизм дипольного взаимодействия двух молекул. Под действием электрического поля, создаваемого молекулой с дипольнъм моментом![]() (потенциал п напряженность этого поля
(потенциал п напряженность этого поля
соответственно:![]() вторая молекула приобретает ди-
вторая молекула приобретает ди-
польный момент![]() (это так называемый индуцированный ди-
(это так называемый индуцированный ди-
коньяый момент). В неоднородном электрическом поле на диполь дей-
ствует сила, направленная в область более сильных полей. В результате между диполями возникает притяжение.
Чтобы получить зависимость для потенциала межмолекулярного притяжения, найдем потенциальную энергию взаимодействия диполей. Потенциальная энергия диполя p=ql в поле, создаваемом диполем
•*
p=ql равна![]() , где
, где![]()
- потенциалы электрического поля в точках нахождения зарядов - q и
+q соответственно,
![]()
Считая V < г, проведем разложение в ряд, ограничиваясь первыми двумя членами разложения:
![]()
Окончательно получаем![]() • Учитывая,
• Учитывая,
что индуцированный дипольный момент пропорционален напряженности электрического поля![]() , получаем /' ~ //г3. Следовательно,
, получаем /' ~ //г3. Следовательно,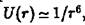 , что соответствует потенциалу сил притяжения
, что соответствует потенциалу сил притяжения
![]() Леннарда-Джонса. В общем случае межмолекулярное притяжение обусловлено взаимодействием трех видов: ориентационным, индукционным и дисперсионным. Полный потенциал сия притяжения имеет соответственно три составляющие: Все три составляющие в первом приближении пропорциональны ~ 1/г и могут быть объяснены в рамках дипольного взаимодействия. Рассмотрим теперь вопрос о дипольных моментах молекул. Отметим, во-
Леннарда-Джонса. В общем случае межмолекулярное притяжение обусловлено взаимодействием трех видов: ориентационным, индукционным и дисперсионным. Полный потенциал сия притяжения имеет соответственно три составляющие: Все три составляющие в первом приближении пропорциональны ~ 1/г и могут быть объяснены в рамках дипольного взаимодействия. Рассмотрим теперь вопрос о дипольных моментах молекул. Отметим, во-
первых, что все молекулы во внешнем электрическом поле приобретают индуцированный дкполъвъш момент благодаря смещению отрицательных и положительных зарядов в противоположные стороны:
![]()
где постоянная B является характеристикой атома или молекулы и называется соответственно атомной или молекулярной поляризуемо-стью. Приведем для сравнения поляризуемости (в единицах 10~24см3) некоторых атомов (Рп} и молекул (Дим):

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



