Министерство общего и профессионального образования РФ
РГУ нефти и газа им.
Кафедра физики
,
Лабораторные работы 162, 163
МОСКВА 2004
Министерство общего и профессионального образования РФ
РГУ нефти и газа им.
Кафедра физики
,
Лабораторные работы 162, 163
Под. ред. доц.
МОСКВА 2004
УДК 53
, / Под. ред. доц.
В пособии описаны краткая теория и порядок выполнения работ. Лабораторные работы предназначены для студентов всех специальностей
Рецензент проф.
КРАТКАЯ ТЕОРИЯ К ЛАБОРАТОРНЫМ РАБОТАМ N 162,163
Жидкости - вещества в конденсированном агрегатном состоянпп, промежуточном между твердым и газообразным. Характерным параметром, определяющим для вещества возможность находиться в газообразном, жидком или твердом состояниях, служит отношение U/К средней потенциальной энергии U молекулы к ее средней кинетической энеркии К. Для твердых тел U/K > 1, для жидкостей U/K ~ 1, для газов U/K < 1. Потенциальная энергия молекул обусловлена взаимодействием между ними, которое в зависимости от расстояния между молекулами может проявляться как в виде сил притяжения, так п в виде сил отталкивания. 1 На рис.1 приведена качественная завпсп-мость сил межмопекулярного взаимодействия от расстояния г между молекулами. При г < t-q преобладают силы отталкивания (F > 0). при г < го - силы притяжения (F < 0). На расстоянии г = го результирующая сила F = 0, т. е. силы притяжения и отталкивания уравновешивают друг друга. Таким образом, расстояние г0 соответствует равновесному расстоянию между молекулами, на котором бы они находились в отсутствие теплового движения. "Межмозекулярные силы взаимодействия являются короткодействующими. Начиная с некоторого расстояния (которое называется радиусом молекулярного действия), взаимодействием между молекулами можно пренебречь
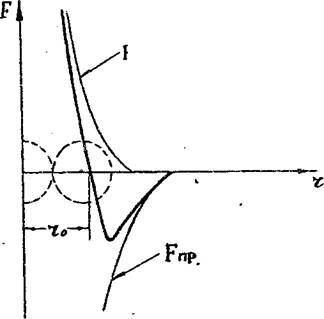
Рис.1. Зависимость сил притяжения, отталкивания п их результирующей от расстояния между молекулами
Радиус молекулярного действия имеет величину порядка 10~э м, (т. е. не превышает нескольких диаметров молекулы). Силы отталкивания меняются, с расстоянием значительно быстрее сик притяжения. Обычно считают, что Р<„ = а/г13, FDP = - Ь/r1 (см. приложение). Именно силы отталкивания не позволяют молекулам сблиолться на сколь угодно малое расстояние.
В газах средние расстояния между молекулами велики и силы взаимодействия практически не проявляются. Молекулы газа та-оа теплового движения стремятся разойтись на бесконечно большие расстояния (стремление гаоа к расширению). В конденсированном состоянии (когда потенциальная энергия притяжения молекул преобладает
над их кинетической энергией) молекулы находятся на расстояниях, сравнимых с их размерами (см. рис.1 и приложение), так что вся система имеет вполне определенный объем (так называемый собственный обьем жидкости). Однако жидкости при сохранении своего объема, в отличие от твердых кристаллических тел, под действием внешних сил могут легко изменять свою форму.
Для всех тез, находящихся в конденсированном состоянии, характерно наличие свободных поверхностей, ограничивающих их объем. Строго говоря, следует говорить не просто о поверхности тел, а о поверхности раздела двух сред. Площадь поверхности, ограничивающей данный объем, зависит от формы поверхности. Наличие у жидких тел свободных поверхностей приводит к существованию особой категории явлений, называемых поверхностными или явлениями капиллярности.
Поверхность раздела между фазами (жидкость/пар) представляет собой переходный слой, в котором плотность меняется от плотности жидкости до плотности пара. При обычных температурах этот слой тонок и его толщина измеряется несколькими молекулярными диаметрами, при повышении температуры толщина переходного слоя увеличивается.
Молекулы в поверхностном слое находятся в условиях, отличных от условий внутри жидкости: равнодействующая сил для молекул внутри жидкости равна нулю, в то время как на молекулы поверхностного слоя действует результирующая сила, направленная внутрь жидкости нормально к поверхности (рис. 2).
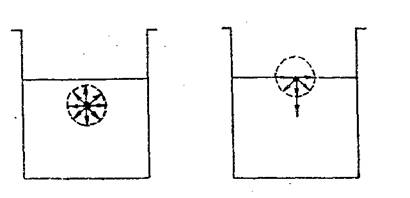
Рис.2. Силы, действующие на молекулы, находящиеся а) внутри жидкости, б) вблизи поверхности жидкости
При увеличении поверхности раздела, т. е. при переводе части молекул из глубины жидкости в пограничный слой, необходимо совершить работу против некомпенсированных у границы раздела межмолеку-,11ярных сия. Таким образом, поверхностный спой обладает избыточной энергией, обусловленной различием межмолекулярных взаимодействий в обеих фазах. Разность между энергией всех молекул (обеих сред) вблизи поверхности раздела и той энергией, которую его молекулы имели бы, если бы они находились внутри жидкости, называется поверхностной энергией Uttw,
Очевидно, что поверхностная энергия пропорциональна площадп S поверхности раздела:
![]() (1)
(1)
Коэффициент о называется коэффициентом поверхностного натяжения (или просто поверхностным натяжением). Поверхностное натяжение зависит от природы соприкасающихся сред и их состояния.
Известно, что люба* система стремится достигнуть состояния с наименьшей потенциальной энергией. Поэтому поверхность жидкости стремится уменьшить свою площадь. Именно с этим связано стремление капелек жидкости (или пузырьков газа) принять сферическую форму. В этом отношении тонкий поверхностный слой действует наподобие резиновой оболочки, которой окружен объем жидкости. Возникающие в этом слое поверхностные силы, действующие вдоль поверхности, всегда стремятся привести к сокращению площади поверхности. Однако, в отличие от упругой пленки, натяжение которой возрастает при ее растяжении, величина поверхностного натяжения не изменяется при изменении площади поверхности.
Наряду с "энергетическим" определением можно ввести "силовое" определение поверхностного натяжения. Физический смысл "силового" определения состоит в том, что когда поверхность ограничена пинией или контуром (периметром смачивания) длины /, то поверхностное натяжение можно представить как отношение силы F, приложенной нормально к линии, ограничивающей поверхность, к длине этой линии (сила действует в плоскости, касательной к поверхности раздела и направлена в сторону уменьшения площади поверхности, т. е. внутрь пленки):
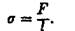 (2) Для иллюстрации вышесказанного можно рассмотреть следующлй
(2) Для иллюстрации вышесказанного можно рассмотреть следующлй
простой пример. Представим себе пленку жидкости, натянутую на проволочную рамку, одна из сторон которой (с длиной /) может перемещаться (рис.3).
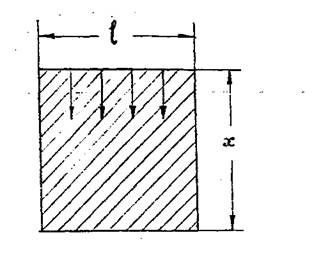
Рис.3. Пленка жидкости, натянутая на рамку
Благодаря стремлению поверхности уменьшиться, на проволочку будет действовать сила, которую на подвижной части рамки можно непосредственно измерить. Эта сила определяется производной от энергии по координате вдоль направления действия силы:
![]()
Так как площадь поверхности одной стороны пленки S = xl, то F = —ol (сравни с формулой 2). Это и есть сила, действующая на отрезок / рати и обусловленная поверхностным натяжением на одной из сто-
рон пленки (так как пленка имеет две стороны, то всего на отрезок действует сила, вдвое большая). Знак минус показывает, что эта сила направлена внутрь поверхности пленки. Для сравнения ниже приведены значения коэффициента поверхностного натяжения раздела жидкость/пар при температуре 20°С для различных веществ.
Жидкость/пар мН/м Ртуть 484 Вода 72,75 ± 0,25 Глицерин 64 Бензол 29 Гексан 18,4 Двуокись углерода 1,16 |
Поверхностное натяжение характеризует различие в межмолеку-кярных взаимодействиях в обеих фазах, образующих поверхность раздела, а в случае границы жидкость/пар вдали от критической тем-прературы - молекулярные силы сцепления в данной фазе (см. при-ложение). Таким образом, необходимым и достаточным условием существования поверхности раздела, а следовательно, и поверхностного натяжения, является, во-первых, наличие сил притяжения между моле-кулами, приводящих к конденсации» и, во-вторых, различие в величине этих сил в граничащих фазах. В связи с этим становится понятным уменьшение поверхностного натяжения с ростом температуры вплоть до обращения его в нуль в критической точке, где исчезает различие между жидкостью и паром.
Величина поверхностного натяжения может сильно меняться при введении в жидкость примесей. Существует целый класс так называемых поверхностно активных веществ (ПАВ), способных адсорбиро-
ваться на поверхности раздела фаз, с соответствующим понижением их поверхностного натяжения. Для воды такими веществами являются, например, различные мыла.
Поверхностное натяжение на границе двух жидкостей (иногда наз. межфазным натяжением) понижается с возрастанием их взаимной растворимости, обращаясь в нуль в случае двух неограниченно растворимых жидкостей. Поверхностное натяжение на границе раздела нефть-вода в среднем порядка (0,025-0,035) Н/м. Для увеличения нефтеотдачи пластов часто требуется снизить межфазное натяжение. Эффективным методом является метод заводнения пластов растворами ПАВ или нагнетание в пласт щелочных вод, которые способствуют образованию натриевых мыл вблизи поверхности раздела вода-нефть и тем самым уменьшению поверхностного натяжения нефти на границе с водой. Введение в пласт углекислого газа СО2 (растворенного в воде или в жидком виде), при котором происходит взаимное растворение углекислоты в нефти и углеводородов в жидком СО%, также приводит к снижению межфазного натяжения.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



