5. По полученным значениям оптической плотности постройте калибровочный график на миллиметровой бумаге в координатах А - C.
6. Получите у преподавателя контрольную задачу с неизвестной концентрацией соли железа (III) (колба № х), добавьте 2 мл разбавленной (1:1) азотной кислоты, 10 мл раствора роданида аммония, доведите дистиллированной водой до метки. Закройте пробкой, хорошо перемешайте.
7. Измерьте оптическую плотность контрольного раствора Аx и по калибровочному графику определите концентрацию железа (III) Сх. Узнайте у преподавателя точной значение концентрации раствора и вычислите погрешность измерения.
ПОТЕНЦИОМЕТРИЯ
Метод потенциометрии основан на зависимости потенциала электрода, погруженного в раствор, от концентрации определенных ионов в данном растворе (уравнение Нернста). Потенциал применяемого в работе стеклянного электрода зависит от концентрации ионов водорода в растворе, что используется при измерении рН. Стеклянный электрод в паре с электродом сравнения, потенциал которого не зависит от рН, опускают в определяемый раствор и измеряют разность их потенциалов. Вольтметр, применяемый для измерений, имеет шкалу, градуированную как в милливольтах, так и в единицах рН, что позволяет снимать показания рН раствора непосредственно со шкалы прибора.
При кислотно-основном титровании добавление каждой порции титранта вызывает изменение рН раствора. На этом основано потенциометрическое титрование. К точному объему определяемого раствора последовательно добавляют небольшие порции стандартного раствора и после каждого добавления измеряется рН. Точку эквивалентности определяют графически (см. рис.1 и 2).
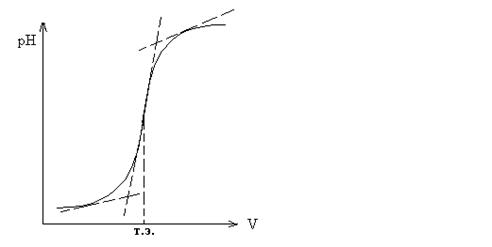
Рис. 1. Интегральная кривая: точка эквивалентности соответствует середине отрезка касательной скачка титрования
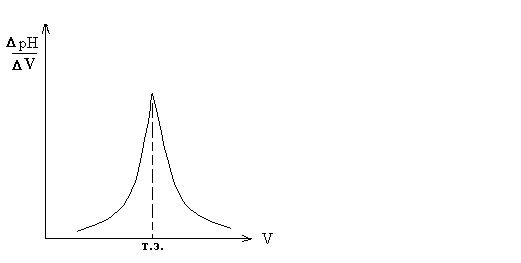
Рис. 2 . Дифференциальная кривая: точка эквивалентности соответствует максимуму кривой.
Лабораторная работа № 12
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ РАСТВОРА NaOH
Ознакомьтесь с установкой для потенциометрического титрования. Электрохимическая ячейка для определений представляет собой стакан с определяемым раствором, в который погружен парный электрод, присоединеный к вольтметру (рН-метру). Раствор HCl добавляют в стакан из бюретки. Раствор в стакане перемешивают с помощью опущенного в стакан магнитного стержня, который приводится в движение магнитной мешалкой. РН-метр измеряет водородный показатель.
Порядок выполнения работы
1. Заполните бюретку раствором HCl до нулевой метки.
2. Промойте электрод: опустите его несколько раз в стакан с дистиллированной водой. Включите рН-метр в сеть.
3. В стакан на 50 мл отмерьте из общей бюретки 10,0 мл титрованного раствора NaOH, положите в него магнитный стержень и опустите электроды (электроды должны быть выше дна стакана на 1,5-2 см). Долейте в стакан дистиллированной воды так, чтобы концы электродов находились в растворе.
4. Включите магнитную мешалку и перемешайте раствор в течение 1 мин.
5. Выключите мешалку и измерьте рН раствора с точностью до 0,01.
6. Добавляйте в стакан из бюретки по 1,0 мл раствора HCl, перемешивайте раствор в течение 1 мин, выключайте мешалку и измеряйте рН с точностью до 0,01. Значения V(HCl) и рН занесите в таблицу 5.
Таблица 5
Значения рН при потенциометрическом титровании
№ измерения | VHCl, мл | рН | DVHCl , мл | DрН | DрН/DVHCl |
7. Повторяйте операции 6 до того момента, когда значение DрН окажется значительно больше, чем предыдущие. После этого продолжайте измерения, уменьшив DV до 0,5 мл: близка точка эквивалентности!
8. После прохождения точки эквивалентности повторите операции 6 еще 5 раз.
9. По полученным данным на миллиметровой бумаге постройте графики интегральной и дифференциальной кривых (рис. 1-2) и определите Vэ (HCl).
10. Рассчитайте молярную концентрацию эквивалента соляной кислоты.
Задачи для самостоятельного решения
Тема 1. Диссоциация слабых электролитов
Сильные и слабые электролиты. Степень электролитической диссоциации. Константа диссоциации. Закон разбавления Оствальда. РН растворов слабых электролитов. Влияние общего иона на диссоциацию слабого электролита. Вычисление константы равновесия реакции по константам реагентов и продуктов. Определение возможности протекания химических реакций.
Вариант 1
1. При какой концентрации фтороводородной кислоты (HF) в растворе степень ее диссоциации будет равна 2%?.
2. Найти концентрацию гидрата аммиака NH3×H2O в растворе, если рН раствора равен 9.
3. В смеси азотной и азотистой кислот концентрация нитрит-иона рана 10-3 М, а рН = 2. Определите концентрацию азотистой кислоты в растворе.
4. Вычислив константу равновесия, определите возможность протекания реакции: CaCrO4 + CH3COOH ® .
Вариант 2
1. Найти степень диссоциации фтороводородной кислоты HF в ее 0,05 М растворе.
2. Вычислите рН 0,2 М раствора гидрата аммиака NH3×H2O.
3. В 0,1 М раствор сернистой кислоты добавили серную кислоту до рН = 1. Пренебрегая изменением объема раствора при этом, определите концентрацию сульфит-иона.
4. Вычислив константу равновесия, определите возможность протекания реакции: BaCrO4 + CH3COOH ® .
Вариант 3
1. Найти степень диссоциации гидрата аммиака NH3×H2O в его 0,1 М растворе.
2. Найти молярную концентрацию уксусной кислоты CH3COOH, если рН ее раствора равен 4.
3. В 0,2 М раствор ортофосфорной кислоты добавили серную кислоту до рН = 1. Пренебрегая изменением объема раствора при этом, определите концентрацию ортофосфат иона.
4. Вычислив константу равновесия, определите возможность протекания реакции: BaCrO4 + HCl ® .
Вариант 4
1. Найти степень диссоциации муравьиной кислоты НСООН в ее 0,2 М растворе.
2. Вычислите рН 0,3 М раствора уксусной кислоты CH3COOH.
3. В 0,6 М раствор циановодородной кислоты добавили серную кислоту до рН = 2. Пренебрегая изменением объема раствора при этом, определите концентрацию цианид иона.
4. Вычислив константу равновесия, определите возможность протекания реакции: NaOH + HCN ® .
Вариант 5
1. Найти степень диссоциации уксусной кислоты CH3COOH в ее 0,4 М растворе.
2. Найти рН 0,2 М раствора фосфорной кислоты H3PO4.
3. В 0,3 М раствор щавелевой кислоты Н2С2О4 добавили серную кислоту до рН = 1. Пренебрегая изменением объема раствора при этом, определите концентрацию оксалат иона.
4. Вычислив константу равновесия, определите возможность протекания реакции: NaOH + H2S ® .
Вариант 6
1. При какой концентрации уксусной кислоты CH3COOH в растворе степень ее диссоциации будет равна 1%?.
2. Найти концентрацию фосфорной кислоты H3PO4, если рН ее раствора равен 3.
3. В смеси фтороводородной и хлороводородной кислот концентрация фторид иона рана 10-3 М, а рН = 1. Определите концентрацию фтороводородной кислоты в растворе.
4. Вычислив константу равновесия, определите возможность протекания реакции: NH3´H2O + HNO2 ® .
Вариант 7
1. При какой концентрации муравьиной кислоты НСООН в растворе степень ее диссоциации будет равна 4%?.
2. Найти рН 0,1 М раствора сернистой кислоты H2SO3.
3. В 0,2 М раствор азотистой кислоты пропускали хлороводород до рН = 1. Пренебрегая изменением объема раствора при этом, определите концентрацию нитрит иона.
4. Вычислив константу равновесия, определите возможность протекания реакции: BaC2O4 + CH3COOH ® .
Вариант 8
1. При какой концентрации гидрата аммиака NH3×H2O в растворе степень его диссоциации будет равна 1,5%?.
2. Найти молярную концентрацию сернистой кислоты H2SO3, если рН ее раствора равен 2.
3. В 0,1 М раствор гидрата аммиака NH3×H2O добавили гидроксид натрия до рН = 13. Пренебрегая изменением объема раствора при этом, определите молярную концентрацию иона аммония.
4. Вычислив константу равновесия, определите возможность протекания реакции: CaC2O4 + CH3COOH ® .
Тема 2. Диссоциация сильных электролитов
Активность ионов. Коэффициент активности ионов. Ионная сила раствора. Зависимость коэффициента активности иона от его заряда и от ионной силы раствора. Формула Дебая – Хюккеля. Водородный показатель. Буферные растворы.
Вариант 1
1. Вычислите ионную силу раствора, содержащего 0,44 г К2SO4 в 250 мл раствора.
2. Вычислите активные концентрации ионов в 0,02 М растворе Al2(SO4)3
3. Найти рН буферного раствора, полученного добавлением 35 г ацетата натрия к 1000 мл 0,5 М раствора уксусной кислоты.
4. Вычислите рН буферной смеси, полученной из 250 мл 0,8 М раствора СН3СООН и 250 мл 0,4 М раствора СН3СООNа. Как изменится рН при добавлении к этому раствору 0,01 моль HCl?
Вариант 2
1. Вычислите ионную силу раствора, содержащего 1,625 г FeCl3 в 125 мл раствора.
2. Вычислите активные концентрации ионов в 0,03 М растворе CaCl2.
3. Найти рН буферного раствора, полученного при смешивании равных объемов 1 М раствора KCN и 0,1 М раствора HCN.
4. Вычислите рН буферной смеси, полученной из 1000 мл 0,2 М раствора HNO2 и 1000 мл 0,4 М раствора NaNO2. Как изменится рН при добавлении к этому раствору 0,01 моль NaOH?
Вариант 3
1. Вычислите ионную силу раствора, содержащего 3,42 г Al2(SO4)3 в 250 мл раствора.
2. Вычислите активные концентрации ионов в 0,04 М растворе FeCl3.
3. Найти рН буферного раствора, полученного добавлением 10,7 г хлорида аммония к 500 мл 0,4 М раствора гидрата аммиака.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 |




