1.1. Реакция с дифениламином, (C6H5)2NH. (Раствор дифениламина приготовлен в концентрированной H2SO4 (будьте осторожны!) Дифениламин в присутствии концентрированной серной кислоты окисляется нитрат ионом NO3- до соединения, имеющего темно-синюю окраску.
Выполнение реакции: внесите в сухую пробирку (по стенке пробирки!) 1-2 капли раствора любого нитрата (NaNO3, или KNO3, или др.) и прибавьте 1-2 капли раствора дифениламина (по стенке пробирки!). На стенке пробирки (в месте соприкосновения растворов) наблюдайте темно-синее окрашивание.
Запишите наблюдение в тетрадь.
2. Аналитические реакции анионов MoO42-, WO42-, VO3-
2.1. Восстановление цинком в концентрированной HCl. Анионы MoO42-, WO42-, VO3- восстанавливаются цинком в концентрированной соляной кислоте до Mo2O5 - зеленый, W2O5 - синий и VOCl2 - фиолетовый:
2 WO42- + Zn + 6 H+ → W2O5 + Zn2+ + 3 H2O
2 VO3- + Zn + 8 H+ + 8 Н2О → 2 [VO(H2O)6]2+ + Zn2+
2 MoO42- + Zn + 6 H+ → Mo2O5 + Zn2+ + 3 H2O
Выполнение реакции: поместите в 3 пробирки по 3-4 капли исследуемых растворов (обычно используется (NH4)2WO4, (NH4)2MoO4 , NH4VO3), прибавьте 3-4 капли концентрированной соляной кислоты и одну гранулу цинка. Окрашивание раствора в синий, зеленый или фиолетовый цвет указывает на присутствие этих анионов.
Запишите наблюдения и уравнения реакций в молекулярном и ионно-молекулярном виде.
2.2. Реакции на анион MoO42- в присутствии WO42-
Действие концентрированной HCl, раствора NH4SCN и раствора SnCl2.
При обнаружении MoO42- в присутствии WO42- последний выделяется в осадок в виде H2WO4 действием концентрированной HCl. Молибденовая кислота H2MoO4 остается в растворе, так как растворима в избытке HCl:
WO42- + 2 H+ → ¯ H2WO4
Затем молибденовую кислоту восстанавливают SnCl2 в кислой среде, а пятивалентный молибден в виде иона MoO3+ связывают NH4SCN в комплексное соединение красного цвета:
2MoO42- + Sn2+ + 12H+ + 10SCN - + 6Cl - → 2[MoO(SCN)5]2- + [SnCl6]2- + 6H2O
После этого восстанавливают вольфрамовую кислоту SnCl2 в концентрированной HCl до оксида W2O5 синего цвета:
¯ 2H2WO4 + Sn2+ + 2 H+ + 6Cl - → W2O5 + [SnCl6]2- + 3H2O
Выполнение реакций. На фильтровальную бумагу нанесите 2 капли концентрированной HCl, 1 каплю раствора NH4SCN и 1 каплю исследуемого раствора ((NH4)2WO4 и (NH4)2MoO4), а затем - 1 каплю раствора SnCl2. Пятно станет красного цвета зе счет образования комплексного иона [MoO(SCN)5]2-. Чтобы открыть ион WO42-, в центр пятна, где есть осадок H2WO4, прибавьте по 1 капле SnCl2 и концентрированной HCl. В присутствии иона WO42- центр пятна синеет за счет образования W2O5, а края остаются красными.
Запишите наблюдения и уравнения реакций в молекулярном и ионно-молекулярном виде.
2.3. Реакции на анион VO3-
2. 3.1. Реакция с пероксидом водорода. Пероксид водорода окисляет ион VO3- до надванадиевой кислоты. Цвет раствора меняется от оранжевого до красно-коричневого в зависимости от рН раствора:
VO3- + H2O2 → VO4- + H2O
Выполнение реакции: поместите в пробирку 3-5 капель раствора серной кислоты (1 М) и 1 каплю раствора H2O2, а через 2 минуты – 5 капель эфира и 3 капли исследуемого раствора (NH4VO3). Хорошо перемешайте. В присутствии иона VO3- органическая фаза окрасится в оранжевый цвет.
Запишите наблюдения и уравнение реакции в молекулярном и ионно-молекулярном виде.
2.3.2. Реакция с лигнином. Лигнин, содержащийся в газетной бумаге, восстанавливает ион VO3- до низших степеней окисления, которые окрашивают газетную бумагу в черно-зеленый цвет.
Выполнение реакции: каплю анализируемого раствора (NH4VO3) нанесите на газетную бумагу, прибавьте 1 каплю концентрированной H3PO4 и наблюдайте появление пятна черно-зеленого цвета.
Запишите наблюдение в тетрадь.
2.4. Реакции на анион СН3СОО-
Действие серной кисоты H2SO4. Серная кислота вытесняет из растворов ацетатов свободную уксусную кислоту, которую можно обнаружить по запаху.
Выполнение реакции:поместите в пробирку 5 капель раствора ацетата натрия и добавьте 2 капли концентрировнной H2SO4.
Обнаружьте уксусную кислоту по запаху.
Запишите наблюдение в тетрадь.
КОЛИЧЕСТВЕННЫЙ АНАЛИЗ
Количественный анализ изучает методы определения количества составных частей (элементов, ионов, молекул, радикалов, функциональных групп и т. д.) в анализируемом образце (веществе, сложном материале, минерале, горной породе).
Методы количественного анализа делятся на химические, физико-химические и физические. Отнесение метода к той или иной группе зависит от того, в какой мере количественное определение основано на использовании химических реакций, физико-химических или физических процессов.
Соответственно трем агрегатным состояниям материи - твердому, жидкому и газообразному - количественные измерения проводят путем определения массы (взвешивание) и путем определения объемов жидких и газообразных веществ.
К химическим методам относятся гравиметрический (весовой), титриметрический (объемный) и газовый анализ.
Физические и физико-химические методы включают оптические, электрохимические, масс-спектральный, хроматографический, радиометрический и др.
ТИТРИМЕТРИЧЕСКИЙ (ОБЪЕМНЫЙ) АНАЛИЗ
Титриметрическим анализом называют метод количественного химического анализа, который основан на точном измерении объема реактива известной концентрации, необходимого для реакции с данным количеством определяемого вещества.
Метод заключается в том, что к раствору определяемого вещества А постепенно прибавляют раствор реактива В известной концентрации. Добавление реактива В продолжается до того момента, пока его количество не станет эквивалентным количеству реагирующего с ним определяемого вещества А.
Количественные определения с помощью этого метода выполняются очень быстро. Момент окончания реакции, когда взаимодействующие вещества полностью прореагируют между собой, называется точкой эквивалентности. В этот момент количества прореагировавших веществ эквивалентны.
Титрование - это процесс постепенного приливания одного раствора к другому для определения концентрации одного из этих растворов.
Титрант (титрованный или рабочий раствор) - это раствор с точно известной концентрацией.
Концентрацию рабочих растворов определяют по стандартному веществу, которое должно удовлетворять следующим требованиям: быть устойчивым при хранении, как в твердом состоянии, так и в растворе, строго соответствовать определенной формуле, хорошо очищаться.
Вычисления в титриметрическом анализе
Для выражения концентрации растворов в этом методе анализа обычно используют молярную концентрацию эквивалента.
Молярная концентрация эквивалента (нормальность) - это количество вещества эквивалента, которое содержится в 1 литре раствора.
Молярная концентрация эквивалента обозначается СЭ (допускается N), и рассчитывается по формуле: СЭ= nэ/V, где nэ - количество вещества эквивалента, моль; V - объем раствора, л единица измерения концентрации - моль/л. Количество вещества эквивалента (nэ) того или иного вещества в заданном объеме равно: nэ = m/Mэ = Сэ·V , где m - масса вещества, г; MЭ - молярная масса эквивалента, г/моль, V - объем раствора, л.
Таким образом, при титровании в точке эквивалентности количество вещества эквивалента титрованного раствора равно количеству вещества эквивалента определяемого вещества - закон эквивалентов: nэ(A) = nэ(B) или
Сэ(А)·V(А) = Сэ(В)·V(В), отсюда 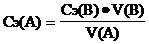
Кроме молярной концентрации эквивалента концентрацию выражают титром (Т). Титр - это количество граммов растворенного вещества, содержащегося в 1 мл раствора.
Титр и молярная концентрация эквивалента раствора связаны формулой:
![]()
Титр по определяемому веществу - это количество граммов определяемого вещества, которое реагирует с 1 мл титранта.
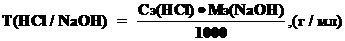
Приемы титрования
Прямое титрование - это простейший прием титрования, заключающийся в том, что к определенному объему раствора определяемого вещества (А) по каплям приливают титрант (рабочий раствор) вещества (В). Зная концентрацию и объем рабочего раствора (В), израсходованного на реакцию с определяемым веществом (А), можно легко вычислить концентрацию последнего:
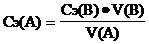
Если основная реакция идет медленно, или нет подходящего индикатора для фиксирования точки эквивалентности, особенно при работе с неустойчивыми веществами, то применяют обратное или заместительное титрование.
Обратное титрование - это процесс титрования, при котором к определенному объему раствора определяемого вещества (А) приливают точно известный объем титранта (В1), взятого в избытке. Избыток, не вошедшего в реакцию вещества (В1), оттитровывают раствором другого титранта (В2) точно известной концентрации. Расчеты производят по формулам:
nэ(A) = nэ(B1) - nэ(B2) ; ![]()

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 |




