Ответ: концентрация диоксида углерода в воздухе составит: 0,034%(об.); 8,67·1015см-3; 1,46·10-5 моль/л; 642 мг/м3; парциальное давление диоксида углерода равно 35 Па.
Пример 2. Масса атмосферы оценивается величиной 5·1014 т. Определите количество кислорода в атмосфере в кг в допущении что атмосфера состоит только из таких «квазипостоянных» компонентов, как азот, кислород и аргон, а их объемная концентрация соответствует значениям, характерным для приземного слоя атмосферы (φ(N2) = 78,11% (об.); φ(O2) = 20,95% (об.); φ(Ar) = 0,94% (об.)).
Решение:
Для решения задачи на первом этапе необходимо определить среднюю молярную массу смеси газов, т. е. среднюю молярную массу воздуха Мвозд:
Мвозд = М(N2) · φ(N2) + М(O2) · φ(O2) + М(Ar) · φ(Ar),
где М(N2), М(O2), М(Ar) − молярная масса азота, кислорода и аргона соответственно;
φ(N2), φ(O2), φ(Ar) − объемные доли соответствующих компонентов смеси в воздухе;
Мвозд = 28,01 · 0,781 + 32,00 · 0,2095 + 39 · 0,0094 = 28,96 г/моль.
Зная общую массу атмосферы Матм(г) среднюю молярную массу воздуха Мвозд(г/моль), определим общее количество воздуха в атмосфере νвозд :
νвозд = Матм/Мвозд
νвозд = 5 · 1015 · 106 /28,96 = 1,7 · 1020 (моль),
где 106 − коэффициент перевода тонн в граммы.
Поскольку мольные и объемные доли газов в смеси равны между собой. Можно найти количество кислорода в атмосфере:
Ν(O2) = νвозд · φ(О2) = 1,7 · 1020 · 0,2095 = 3,6 · 1019(моль).
Теперь легко найти массу кислорода в атмосфере:
М(O2) = ν( O2) · М(O2) = 3,6 · 1019 · 32 = 11,5 · 1020 (г) = 12 · 1017 (кг).
Ответ: масса кислорода в атмосфере равна 12 · 1017 (кг).
Пример 3. Во сколько раз число молекул кислорода в кубическом сантиметре воздуха на высоте вершины Эльбрус (5621 м над уровнем моря) меньше, чем среднее значение у поверхности Земли (на уровне моря) при нормальном атмосферном давлении?
Решение: Число молекул любого газа в 1см3 можно получить, поделив число молекул в 1 моле любого газа NA (число Авогадро) на объем VM, занимаемый этим количеством газа (молярный объем газа), выраженный в см3:
N = NA / VM.
Поскольку молярный объем газа зависит от температуры и давления, то его необходимо привести к условиям задачи:
VM = VM0 · TP0/T0P,
где, VM0 − молярный объем газа при нормальных условиях (22,4 л/моль);
T0, P0, T, P − температура и давление при нормальных и заданных условиях соответственно.
VM = 22,4 · 288 · 101,3/ (273 · 101,3) = 23,63 л/моль = 23,63 · 103 см3/моль.
При 288 К и нормальном атмосферном давлении общее число молекул идеального газа или смеси идеальных газов) в 1см3 составит:
N = 6,02 · 1023 / (23,63 · 103 ) = 2,55 ·1019 см-3 .
Число молекул кислорода в 1см3 воздуха при нормальном давлении при условии, что воздух и кислород ведут себя как идеальные газы, можно определить, зная его объемную долю:
N(O2)З = N · φ (O2) = 2,55 · 1019 · 0,2095 = 5,34 · 1018 см-3 .
Содержание молекул воздуха в атмосфере убывает с увеличением высоты над уровнем моря согласно уравнению:
Nвозд Н = Nвозд З exp[− МвоздgH/(RTH)],
где NH − концентрация молекул в воздухе на высоте H над уровнем моря, см-3; NЗвозд − средняя концентрация молекул в воздухе на уровне моря, см-3;
Мвозд − средняя молярная масса воздуха (28,96 г/моль = 28,96 · 10-3 (кг/моль);
g − ускорение силы тяжести (9,8 м/с2 );
H − высота над уровнем моря, м;
R − универсальная газовая постоянная (8,314Дж/(моль· К));
ТН − средняя температура воздуха на высоте Н, К.
Температуру на заданной высоте в тропосфере можно определить по уравнению:
ТН = ТЗ + ΔТ · Н,
где ТН и ТЗ − температуры на заданной высоте Н и у поверхности Земли соответственно, К;
ΔТ − температурный градиент в стандартной тропосфере ( Δ Т = −б,45 К/км).
Средняя температура атмосферы на высоте вершины Эльбрус составит:
ТН = 288 + (−6,45) · 5,621 = 252 К.
Концентрация молекул воздуха на высоте вершины Эльбрус составит:
NвоздН = 2,55·1019 exp [–28,96 ·10-3 · 9,8 · 5621/(8,314·252)] = 1,19·1019см-3.
Поскольку соотношение числа молекул «квазипостоянных» компонентов воздуха в единице объема практически не меняется в атмосфере до высоты 100 км, можно определить концентрацию молекул кислорода на высоте вершины Эльбрус (N(O2)Н) по уравнению:
N(O2)Н = Nвозд Н · φ (O2) = 1,19 ·1019 · 0,2095 = 2,49 · 1018 см-3.
Отношение частичных концентраций молекул кислорода в воздухе у поверхности Земли и на вершине горы Эльбрус составит:
Х = N(O2)З/ N(O2)Н = 5,34 · 1018 /(2,49 · 1018) = 2,1.
Ответ: концентрация молекул кислорода в воздухе на вершине горы Эльбрус в 2,1 раза меньше, чем у поверхности Земли
Пример 4. Количество метана, поступающего ежегодно с поверхности Земли в атмосферу, составляет 550 млн. т. Среднее содержание метана в слое атмосферы, на который приходится 90% ее массы, составляет 1,7 млн-1. Определите время пребывания метана в этом слое атмосферы, если принять, что в других частях атмосферы он отсутствует.
Решение:
Оцененное ранее (пример 2.3) количество воздуха в атмосфере равно 1,7 · 1020 моль. В слое воздуха, составляющем 90% массы атмосферы, будет содержаться воздуха:
νвозд 90 = 1,1·1020 · 0,9 = 1,53 ·1020 моль.
Количество метана, содержащегося в этом слое атмосферы, составит
ν(CH4) = νвозд · φ (CH4),
где φ (CH4) − объемная доля метана в воздухе, по условию задачи равная
1,7 · 10-6.
ν(CH4) = 1,5 · 1020 · 1,7 · 10-6 = 2,6 ·1014 моль.
Масса метана в рассматриваемом слое атмосферы составит:
М(СН4) = М(СН4)· ν(CH4),
где М(СН4) − молярная масса метана (16 г/моль);
М(СН4) = 2,6 · 1014 · 16 = 41,6 · 1014 г = 41,6 · 108 т.
Время пребывания метана можно определить из уравнения:
τ = М(СН4)/Q(СН4),
где τ − время пребывания вещества в атмосфере, в единицах времени;
М(СН4) − масса вещества в атмосфере, в единицах массы;
Q(СН4) − скорость поступления или вывода вещества из атмосферы, в единицах массы на единицу времени.
Время пребывания метана в слое, содержащем 90% массы атмосферы, составит:
τ = 41,6 · 108 /(550 · 106) = 7,6 года.
Ответ: время пребывания метана в слое, содержащем 90% массы атмосферы, составляет 7,6 года.
Пример 5. Определите градиент потенциальной температуры и дайте характеристику степени устойчивости атмосферы в случае, когда температура у поверхности Земли равна минус 15°С, на высоте 500 м − минус18,5°С, на высоте 1000м − минус 15°С. а на высоте 1500м снижается до минус 21°С.
Решение:
Определим градиент потенциальной температуры для различных слоев тропосферы:
Гпот = 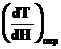 + Г =
+ Г = ![]() + Г.
+ Г.
В слое от поверхности Земли до высоты 500м градиент потенциальной температуры составит:
Г1пот = 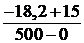 + 6,45 · 10-3 = 5,0 · 10-5 град/м.
+ 6,45 · 10-3 = 5,0 · 10-5 град/м.
В этом случае атмосфера может характеризоваться как слабо устойчивая, или безразличная.
В зоне от 500 до 1000м имеем:
Г2пот = 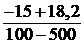 + 6,45 · 10-3 = 1,1 · 10- 2град/м.
+ 6,45 · 10-3 = 1,1 · 10- 2град/м.
Атмосфера – устойчивая.
На высотах от 1000 до 1500м потенциальный градиент температуры составит:
Г3пот = 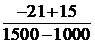 + 6,45 · 10-3 = −5,5 · 10-3 град/м.
+ 6,45 · 10-3 = −5,5 · 10-3 град/м.
В этой зоне атмосфера неустойчива.
Таким образом, по степени устойчивости в атмосфере выделяются три различные слоя. Присутствие зоны устойчивой атмосферы свидетельствует о наличии условий, характерных для приподнятой зоны температурной инверсии.
Ответ: потенциальные градиенты температуры на высотах от 0 до 500, от 500 до 1000 и от 1000 до 1500м составляют 5,0 · 10-5, 1,1 · 10-2 и −5,5 · 10-3 град/м соответственно. Атмосфера в этих зонах характеризуется как безразличная, устойчивая и неустойчивая. В атмосфере наблюдается приподнятая температурная инверсия.
Пример 6. Оцените мольное соотношение и общую массу диоксида серы и оксида азота, поступающих атмосферу в течение суток с выбросами тепловой электростанции, работающей на угле. Содержание серы в угле равно 1,5% (мас.). В сутки на станции сжигается 10 тыс. тонн угля. Концентрация оксида азота в газовых выбросах составляет 150 млн-1. Для сжигания угля используется стехиометрически необходимое количество воздуха. При оценке принять, что уголь состоит из углерода и содержит в качестве примеси только серу.
Решение:
Появление диоксида серы в выбросах отходящих газов связано с процессом окисления соединений серы. Присутствующих в исходном топливе. В рассматриваемом случае процесс можно представить уравнением:
S + O2 = SO2.
Количество серы, сжигаемое на станции в сутки, составит:
m(S) = m(угля ) ·ω(S),
где m(S) и m(угля ) − массы серы и угля, сжигаемого на станции в сутки;
ω(S) − массовая доля серы в угле.
m(S) = 10000 · 0,015 = 150 т/сут.
Количество диоксида серы, образующегося в процессе сжигания угля, равное количеству серы, содержащейся в угле, составит:
ν(SO2) = ν(S) = m(S)/М(S),
где М(S) − молярная масса серы, г/моль;
ν(SO2) = 150 ·106 /32 = 4,69 ·106 моль/сут.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




