Задание №2
Физико-химические превращения в атмосфере:
состав и строение атмосферы, приоритетные загрязнители
1 СОСТАВ И СТРОЕНИЕ АТМОСФЕРЫ
Общая масса газовой оболочки нашей планеты – атмосферы – составляет 5,14*1015т. Это примерно одна миллионная часть массы Земли. Состав атмосферы претерпевал серьезнейшие изменения в различные геологические эпохи. В настоящее время состав атмосферы находится в состоянии динамического равновесия, поддерживаемого в результате действия живых организмов, геохимических явлений и хозяйственной деятельности человека.
Главными компонентами атмосферы являются азот, кислород и аргон: на их долю в приземном слое приходится соответственно 78,11; 20,95 и 0,94% (об.). На долю всех остальных компонентов приходится менее 0,1% (об.), но их роль в общей динамике состояния атмосферы чрезвычайно велика. Объемные концентрации постоянно содержащихся в атмосфере (так называемых «квазипостоянных») компонентов (N2, O2, Ar, He, Xe, Kr, H2) остаются практически неизменными вплоть до высоты 100 км. Содержание других («активных») газов и аэрозолей существенно меняется в зависимости от сезона, географического положения и высоты над уровнем моря. К «активным» компонентам атмосферы относятся водяной пар, углекислый газ, монооксид углерода, оксиды азота, диоксид серы, метан и озон. Антропогенное влияние на состав атмосферы ограничено, в основном, изменениями концентрации «активных» газов и аэрозолей.
Одним из важных показателей, характеризующих поведение примесей в атмосфере, является время их пребывания в рассматриваемом объеме атмосферы. В случае динамического равновесия – равенства скоростей поступления примеси из всех возможных источников и суммарного стока примеси из резервуара – время пребывания примеси и ее общая масса в резервуаре связаны уравнением:
Qисточник = Qсток = A / τ ,
где Qисточник и Qсток – скорости поступления и стока веществ соответственно для произвольного резервуара, атмосферы в целом или ее части;
А – общая масса примеси, содержащейся в произвольном резервуаре, атмосфере в целом или в ее части;
τ – время пребывания примеси в произвольном резервуаре, атмосфере в целом или в ее части.
2 ОСНОВНЫЕ ЗОНЫ АТМОСФЕРЫ
По вертикали атмосфера имеет слоистое строение. Наиболее распространенное деление на слои основано на изменении температуры с высотой. Некоторые характеристики основных слоев атмосферы приведены в таблице 1. Cледует отметить, что границы отдельных слоев, разделяемых узкими переходными зонами, называемыми паузами, строго не фиксируются. Их положение зависит главным образом от внешнего фактора – активности солнца и уровня поступающей от него радиации.
Таблица 1 – Основные зоны атмосферы
Слой атмосферы | Нижняя и верхняя границы над уровнем моря, км | Температура, ºС | Температурный градиент, ºС/км | |
Нижняя граница слоя | Верхняя граница слоя | |||
Тропосфера | 0 – (8-18) | 15 | –56 | –6,45 |
Стратосфера | (8-18) – (50-55) | –56 | –2 | +1,38 |
Мезосфера | (50-55) – (80-85) | –2 | –90 | –2,56 |
Термосфера | (80-85) – 1000 | –90 | 1200 | +3,13 |
3 АТМОСФЕРНОЕ ДАВЛЕНИЕ
При нормальных условиях (р = 1 атм, Т = 273 К) газы, входящие в состав атмосферы, мало отличаются по своему поведению от идеальных газов. Поэтому для реальной атмосферы справедливо уравнение состояния идеального газа:
PV = ν RT,
где Р – давление;
V – объем газа;
ν – количество вещества;
R – универсальная газовая постоянная;
Т – температура.
Распределение давления в атмосфере по высоте Н описывается так называемой «барометрической формулой»:
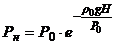 ,
,
где ρ0 и Р0 – плотность и давление при Н = 0 (т. е. на уровне моря), причем Р0=101325 Па;
g – ускорение свободного падения; g = 9,81м∙с-1.
Распределение концентрации составляющих атмосферу компонентов по высоте имеет вид:
![]() ,
,
где M – молярная масса газа;
N0 – концентрация молекул на высоте Н=0 (на уровне моря);
R – универсальная газовая постоянная.
4 УСТОЙЧИВОСТЬ АТМОСФЕРЫ
Химические процессы в атмосфере и, следовательно, ее химический состав как в глобальных и региональных, так и локальных масштабах зависят не только от присутствия тех или иных соединений и их потенциальной способности вступать в определенные химические реакции, но и от многих других параметров атмосферы в данном месте и в данный момент.
Количество (масса) примесей в атмосфере (А) есть функция деятельности всех возможных источников (Qист), стоков (Qсток) и переноса (Qпер.). В неравновесных условиях:
![]() = Qист – Qсток ± Qпер.
= Qист – Qсток ± Qпер.
Стоки – это процессы удаления примеси в ходе химических реакций и соосаждения. Qпер. – скорость процессов переноса и рассеяния. Решающую роль в этих процессах наряду с горизонтальным переносом (адвекцией) играет перемещение вверх от земной поверхности.
Такой перенос воздуха определяется уже одним только фактом наличия температурного градиента, однако в реальной атмосфере он может не реализовываться, поскольку зависит от характеристики, называемой устойчивостью атмосферы. Устойчивость атмосферы проявляется в отсутствии в ней значительных вертикального движения и перемешивания. В этом случае загрязняющие вещества, выброшенные в атмосферу вблизи земной поверхности, будут иметь тенденцию задерживаться там.
Интенсивность теплового перемешивания определяют, сравнивая температурный градиент, реально наблюдаемый в атмосфере, со стандартным адиабатическим вертикальным градиентом.
 ,
,
где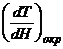 – изменение температуры по высоте, наблюдаемое в окружающей среде.
– изменение температуры по высоте, наблюдаемое в окружающей среде.
Значение Гпот< 0 свидетельствует о сверхадиабатическом характере профиля температуры и неустойчивых условиях в атмосфере. В случаях, когда Гпот> 0, атмосфера устойчива. В случае, если Гпот≈ 0, атмосфера характеризуется как безразличная.
Если температура повышается с ростом высоты, то атмосферные условия определяются как инверсия. В этом случае атмосфера является весьма устойчивой.
Примеры решения задач
Пример 1. В восьмидесятых годах 20-ого века среднегодовая концентрация диоксида углерода в атмосфере, приведенная к температуре 273 К и давлению воздуха 101,3 кПа, достигла 340 млн-1 Определите значения концентрации CO2 в %(об.), см-3, моль/л, мг/м3 и парциальное давление CO2 в Па при средней температуре воздуха вблизи поверхности Земли(288 К).
Решение:
Выразим объемную долю диоксида углерода φ, %(об.):
φ (CO2) = С · 10-4,
где С – концентрация диоксида углерода, выраженная в млн-1,
10-4 − коэффициент перевода млн-1 в % (об.).
φ (CO2) = 340 ∙10-4 = 0,034% (об.).
Число молекул любого газа в 1см3 можно получить, поделив число молекул в 1 моле любого газа NA (число Авогадро) на объем VM, занимаемый этим количеством газа (молярный объем газа), выраженный в см3:
N = NA / VM.
Поскольку молярный объем газа зависит от температуры и давления, то его необходимо привести к условиям задачи:
VM = VM0·TP0/T0P,
где, VM0 − молярный объем газа при нормальных условиях (22,4 л/моль);
T0, P0, T, P − температура и давление при нормальных и заданных условиях соответственно.
VM = 22,4 · 288 · 101,3/ (273 ∙101,3) = 23,63 л/моль = 23,63 · 103 см3/моль.
При 288 К и нормальном атмосферном давлении общее число молекул идеального газа или смеси идеальных газов) в 1см3 составит:
N = 6,02 · 1023 / (23,63 · 103 ) = 2,55 ·1019 см-3 .
Число молекул диоксида углерода в 1см3 воздуха при условии, что воздух и диоксид углерода ведут себя как идеальные газы, можно определить, зная его объемную долю:
N(CO2) = N · φ (CO2) = 2,55 · 1019 · 3,4 · 10-4 = 8,67 · 1015 см-3 .
Определим парциальное давление диоксида углерода в воздухе. Значения объемных концентраций примесей приводятся обычно в пересчете на сухой воздух; при определении парциального давления в реальных условиях следует учитывать парциальное давление паров воды, которые всегда присутствуют в атмосферном воздухе. Поэтому рекомендуется пользоваться следующим уравнением:
P = (Pвозд − Pводы ) C/100,
где P − парциальное давление примеси, кПа;
Pвозд − атмосферное давление, кПа;
Pводы − давление паров воды, кПа;
C − концентрация примеси, %(об.),
100 − коэффициент перевода % в доли.
Однако, поскольку в условиях задачи отсутствуют данные о парциальном давлении паров воды в воздухе, проведем упрощенный расчет:
P = Pвозд C /100;
P = 101,3 · 3,4 · 10-2 /100 = 3,46 · 10-2 кПа = 35 Па.
Молярную концентрацию CM (моль/л) диоксида углерода в воздухе определим, пользуясь уравнением состояния идеального газа:
PV = ν RT ; P = νRT /V = CMRT; CM = P/(RT),
где P, V,ν, T − давление, объем, количество и температура идеального газа соответственно,
R − универсальная газовая постоянная 8,314 Дж/(моль· К).
CM (CO2) = 35/(8,314 · 288) = 1,46 · 10-2 моль/м3 = 1,46 · 10-5 моль/л.
Число мг диоксида углерода в кубическом метре воздуха составит:
С*(CO2) = CM (CO2) · M(CO2) · 106 = 1,46 · 10-5· 44 · 106 = 642 мг/м3.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




