Режимы выщелачивания. По характеру загрузки (во времени) твердого вещества и жидкости различают три режима выщелачивания: периодический, полунепрерывный и непрерывный. При периодическом режиме реагирующие вещества (твердая фаза и жидкость) загружают в аппарат единовременно. После определенного времени контакта при перемешивании, необходимого для достижения требуемой степени превращения, продукты реакции выгружают. Периодическое выщелачивание применяют в случае малых масштабов производства. Полунепрерывный режим выщелачивания характеризуется единовременной загрузкой и выгрузкой твердой фазы и непрерывной подачей и выгрузкой жидкой фазы (перколяция, кучное и подземное выщелачивание). При непрерывном режиме осуществляют непрерывную подачу в аппарат (или систему аппаратов) исходных веществ и непрерывную выгрузку продуктов реакции. При этом большей частью используют каскад из последовательно соединенных аппаратов, в которых осуществляется прямоточное или противоточное выщелачивание. При непрерывном прямоточном выщелачивании исходные твердая и жидкая фазы одновременно поступают (обычно в форме пульпы) в первый аппарат, проходят последовательно все аппараты каскада и выгружаются из последнего аппарата.
В случае непрерывного противоточного выщелачивания твердый выщелачиваемый материал и выщелачивающий раствор движутся навстречу один другому. Таким образом, материал, наиболее обедненный извлекаемым компонентом, контактирует со свежим выщелачивающим раствором. С точки зрения кинетики это наиболее рациональный способ, но его осуществление связано с необходимостью разделять фильтрацией твердую и жидкую фазы после каждого аппарата.
2.1.2 Осаждение компонентов из растворов
Осаждение компонентов из растворов после выщелачивания может осуществляться разными способами: осаждением в виде трудно растворимого соединения, цементацией, электролизом, кристаллизацией.
При осаждении цветных металлов из растворов в виде трудно растворимых соединений чаще всего используют осаждение в виде гидроокисей или в виде сульфидов.
Основной количественной термодинамической характеристикой малорастворимой соли является произведение растворимости L. Для соли МеnAm учитывая, что для малорастворимой соли коэффициенты активности ионов равны 1, L=[Me]n[A]m. Если концентрация ионов в растворе такая, что [Me]n[A]m>L, то будет происходить осаждение твердой соли, если[Me]n[A]m<L, то¾растворение до установления равновесия.
Если растворимость соли МеnAm обозначить S, то концентрации ионов [Me] и [A] будут равны nS и mS. Отсюда
L=[Me]n[A]m=(nS)n (mS)m и S=![]()
Растворимость соли в воде помимо произведения растворимости зависит также от ряда других факторов (ионная сила раствора, рН раствора, гидролиз ионов и др.)
При рассмотрении процесса осаждения гидроокисей металлов необходимо учитывать равновесие двух реакций:
Ме(ОН)n«Men+ + nOH - и
H2O«H+ +OH-
Легко показать, что гидроокиси металлов выделяются при определенном рН, значение которого является функцией произведения растворимости, активности и заряда иона металла в растворе:
PH= - lg[H+]=(1/n)lgL – lgKw – (1/n)lg[Men+]
В таблице 8 даны рН гидратообразования некоторых металлов рассчитанных для активностей равной единице.
Таблица 8
РН гидратообразования металлов при аМе=1
Металл | L | pН выделения | Металл | L | pН выделения |
Tl3+ Sn4+ Co3+ Sb3+ Sn3+ Fe3+ Al3+ Bi3+ | 1,5*10-44 1*10-56 3*10-41 4*10-42 5*10-26 4*10-38 1,9*10-33 4,3*10-33 | - 0,5 0,1 1,0 1,1 1,4 1,6 3,1 3,9 | Cu2+ Zn2+ Co2+ Fe2+ Cd2+ Ni2+ Mg2+ Tl+ | 5,6*10-20 4,5*10-17 2,o*10-16 1,0*10-15 1,2*10-14 1,0*10-15 5,5*10-12 7,2*10-1 | 4,5 5,9 6,4 6,7 7,0 7,1 8,4 13,8 |
При осаждении гидроокисей металлов из растворов прежде всего начнет осаждаться гидроокись того металла, рН гидратообразования которого меньше. Пользуясь приведенным выше выражением, можно вычислить остаточную концентрацию металла в растворе при определенном рН, а также рН начала и конца осаждения при заданных начальной и конечной концентрации металла в растворе.
Например, требуется определить рН начала и конца осаждения гидроокиси железа, если концентрация железа в растворе снижается от 0,1 до 0,01 г-ион/л. Произведение растворимости гидроокиси железа L=4*10-38 (из таб. 8), тогда: рНнач.= -(1/3*37,4)+14+1/3*1=1.87;
РНкон.= -(1/3*37,4)+14+1/3*2=2,2.
Осаждение сульфидов металлов осуществляют сероводородом, сульфидами натрия или аммония. Трудно растворимые сульфиды металлов, подобно гидроокисям, выделяются при определенном значении рН раствора. При упрощенном выводе зависимости рН выделения сульфида от концентрации металла в растворе и величины констант, характеризующих равновесие протекающих реакций, на примере сульфида двухвалентного металла необходимо учитывать:
1. Равновесие диссоциации сульфида
MeSÛMe2+ +S2- L=[Me2+] [S2-]
2.Равновесие диссоциации сероводорода
H2SÛH+ +HS - K1=[H+][S2-]/[H2S]=10-7
HS-Û H+ +S2- K2=[H+][S2-]/[HS-]=10-13
Из этих выражений легко показать, что рН осаждения сульфида будет равно: рН=1/2(lgL - lg [Me2+] - lg[H2S] - lgK H2S),
то есть рН осаждения сульфида определяется природой металла (L), концентрацией металла и сероводорода в растворе. В таблице 9 приведены расчетные значения рН осаждения некоторых металлов.
Таблиц 9
рН осаждения сульфидов при 250С и давлении сероводорода 1 ат.
Сульфид | L | РН выделения сульфида при [Ме2+] | ||
10-1 | 10-3 | 10-5 | ||
MnS FeS NiS CoS ZnS SnS CdS PbS CuS | 2,8*10-13 4,9*10-18 2,8*10-21 1,8*10-22 8,9*10-25 1*10-15 7,1*10-27 9,3*10-28 8,9*10-36 | 4,23 1,65 0,23 -0,32 -1,5 -2,0 -2,7 -3,01 -7,0 | 5,73 3,15 1,72 1,18 -0,02 -0,5 -1,07 -1,5 -6,0 | 7,22 4,65 3,22 2,68 1,5 1,0 0,42 0,0 -4,0 |
Видно, что рН осаждения различных металлов изменяются в широких пределах. Этим обстоятельством часто пользуются для селективного осаждения металлов.
Осаждение металлов цементацией это процесс вытеснения ионов металла из раствора каким либо другим металлом (цементатором). Процесс цементации рассматривается как электрохимический процесс, термодинамическая вероятность которого определяется соотношением величин электрохимических потенциалов вытесняемого и вытесняющего металлов. Цементация:
Ме12+ + Ме2=Ме1 + Ме22+
Может осуществляться только тогда, когда вытесняемый металл имеет потенциал более электроположительный, чем потенциал вытесняющего j1>j2.
Потенциал металла в растворе его соли зависит от концентрации ионов металла в растворе. В течение процесса цементации в растворе будут изменяться ионов металлов (осождаемого убывать, а вытесняющего возрастать), следовательно будут изменяться и потенциалы этих металлов (j1 ¾ в сторону электроотрицательных значений, а j2¾ в электроположительную сторону). Процесс цементации будет происходить до тех пор, пока не установятся равновесия, при котором j1=j2, или
j10 +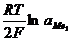 = j20 +
= j20 +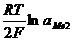 .
.
Пользуясь этим выражением можно оценить глубину осаждения при цементации. В таблице 10 приведены результаты расчета по этому выражению для некоторых двухвалентных металлов.
Таблица 10
Равновесные соотношения активностей для пар металлов
Металл | Стандартный потенциал, в |
| ||
Ме2 | Ме1 | j0Ме2 | j0Ме1 | |
Zn Fe Ni Zn Cu Zn Zn Co | Cu Cu Cu Ni Hg Cd Fe Ni | -0 763 -0,440 -0,230 -0,763 +0,340 -0,763 -0,763 -0,270 | +0,340 +0,340 +0,340 -0,230 +0,798 -0,402 -0,440 -0,230 | 1*10-38 1,3*10-27 2*10-20 5*10-19 1,6*10-16 3,2*10-13 8*10-12 4*10-2 |
Из таблицы видно, что некоторые металлы осаждаются цементацией практически до следов, например, медь цинком.
Процессы осаждения металлов из растворов осуществляются на практике в таких же аппаратах, как и выщелачивание.
2.1.3 Сорбция
С о ρ б ц и я - это процесс, при котором ионы раствора сорбируются поверхностью твердых частиц и извлекаются с ними из раствора. Сорбция основана главным образом на обмене ионов твердой частицы на ионы раствора того же знака. Поэтому применяемые в сорбционном процессе твердые частицы называют ионообменниками (или ионитами). В зависимости от заряда обмениваемых ионов эти вещества делят на катиониты (обмениваются катионами) и аниониты (обмениваются анионами). Существуют также амфотерные иониты — амфолиты, способные одновременно осуществлять катионный и анионный обмен. В качестве сорбентов могут применяться минеральные иониты (различные алюмосиликаты группы цеолитов, монтмориллонит, железоалюмосиликаты - глаукониты), синтетические неорганические иониты (пермутиты и селикагели) и синтетические высокомолекулярные органические полимеры, называемые часто смолами. Выпускаемые в настоящее время ионообменные смолы, обладающие высокой емкостью, химической стойкостью и механической прочностью, вытеснили другие ионообменные материалы. Для сорбции золота и серебра из цианистых растворов применяют иногда активированный уголь. Очистка растворов от мышьяка, сурьмы, коллоидной серы и некоторых других примесей производится за счет сорбции их гидроксидом железа (Ш).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



