DН0Т=DН0298 +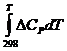 , а
, а
DS0T=DS0298 + 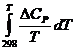 , следовательно:
, следовательно:
DG0Т=DН0298 - ТDS0298+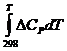 -Т
-Т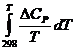 ,
,
или после преобразований:
DG0Т=DН0298 - ТDS0298 - Т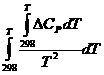 .
.
Последний член этого уравнения представляет собой поправку на отклонение DН0Т и DS0T от стандартных значений, легко определяется с помощью специальных таблиц.
В большинстве гидрометаллургических процессах реакции протекают при условиях мало отличающихся от стандартных, поэтому этой поправкой можно пренебречь и расчеты проводить по приближенному уравнению:
DG0Т==DН0298 - ТDS0298, где
DН0298=åDН0298(кон.) - åDН0298(исх.)
DS0298=åDS0298(кон.)- åDS0298(исх.)
Более того, чтобы оценить термодинамическую вероятность протекания процесса, часто достаточно стандартных значений DG0298.
Проиллюстрируем сказанное примером. Пусть необходимо оценить термодинамическую вероятность протекания реакции растворения металлической меди в растворе серной кислоты в присутствии кислорода воздуха при температуре 920С:
Cu + H21SO4 + 1/2O2=CuSO4 + H2O
Термодинамические величины, взятые из справочников следующие:
Величина | Cu | H2SO4 | O2 | CuSO4 | H2O |
DG0298, ккал/моль DН0298, ккал/моль DS0298, кал/моль. град | 0 0 7,96 | -177,34 -216,9 4,1 | 0 0 49,0 | -158,2 -184,0 27,1 | -56,69 -68,3 16,7 |
Сначала оценим величину изменения энергии Гиббса реакции по упрощенной формуле:
DG0298= - 158,2- 56,69-(-177,34+0+1/2*0)= -37,55ккал/моль (-157,11кДж/моль)
Как видно из большого отрицательного значения изменения энергии Гиббса протекание реакции термодинамически вероятно. Но по условию задачи реакция должна протекать при 920С. Определяем величину DG0Т при этой температуре:
DН0298= - 184 – 68,3 –(0-216,9+1/2*0)= -35,4 ккал/моль,
DS0298=27,1+16,7 –(7,96+4,1=1/2*49)=7,24 кал/моль. град
DG0365= -35,4 –365*7,24*10-3= -38,08 ккал/моль (-159,3кДж/моль)
Не трудно заметить, что изменение энергии Гиббса несколько уменьшилось, однако для оценки термодинамической вероятности протекания данной реакции вполне можно было ограничиться первым вариантом.
Глубину протекания реакции легко оценить по величине константы равновесия этой реакции. Если величина константы большая, значит равновесие сильно сдвинуто вправо и преобладающей является прямая реакция. Значение константы равновесия может быть определено экспериментально или расчетным путем.
Для расчетного определения константы равновесия реакции можно воспользоваться уравнением:
DG0Т= - RTlnKР, где
DG0Т¾изменение энергии Гиббса, ккал/моль; R¾универсальная газовая постоянная,1,987кал/моль. град (8,314дж/моль. град); Т¾температура,0К.
Для стандартной температуры и переходя к десятичным логарифмам получим:
DG0298== - 1,364lgKР
Например, требуется рассчитать константу равновесия для приведенной выше реакции растворения меди. Для этой реакции было определено изменение энергии Гиббса (DG0298), которое составило – 37,55ккал/моль. Следовательно:
lgKР= - 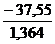 =27,5, отсюда
=27,5, отсюда
КР=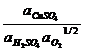 =1027,5=3,1*1027
=1027,5=3,1*1027
Такое высокое значение константы равновесия свидетельствует, что данная реакция практически необратима и целиком сдвинута вправо.
Если в процессе выщелачивания протекает окислительно-восстановительная реакция, то есть реакция сопровождается изменением валентности элементов (наиболее распространенный случай при выщелачивании), то константа равновесия реакции и изменение энергии Гиббса могут быть вычислены по известным значениям электрохимических потенциалов:
DG0298= - nF(j0ок-j0в) и
lgKР=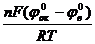 =n(j0ок-j0в)/0,059, где
=n(j0ок-j0в)/0,059, где
n¾число переходящих электронов; F¾число Фарадея (23,06ккал/Вг-экв);
j0ок и j0в¾стандартные потенциалы окислителя и восстановителя, вольт.
В качестве примера рассмотрим реакцию растворения меди в сульфате трехвалентного железа:
Cu+Fe2(SO4)3=CuSO4+2FeSO4.
Эту реакцию можно записать в ионной форме:
Cu+2Fe3+=Cu2++2Fe2+
или состоящей из двух полуреакций¾окисления:
Сu=Cu2+ +2e j0= +0,345в,
и восстановления:
2Fe3+ +2e=2Fe2+ j0= +0,771в.
Зная стандартные потенциалы пределяем:
DG0298= - 2*23,06(0,771-0,345) = -19,7ккал/моль (-82,42кдж/моль) и
lgKР=2(0,771-0,345)/0,059=14,43, КР=2,7*1014
Высокое значение константы равновесия, а также большая убыль энергии Гиббса показывают, что термодинамически реакция вполне вероятна и сильно сдвинута вправо.
Таким образом, зная состав твердого и выщелачивающего раствора, а также параметры процесса ( температуру и давление) можно расчетным путем на основании термодинамических данных оценить вероятность поведения различных компонентов твердого в процессе выщелачивания.
2.1.1.2 Кинетика процесса выщелачивания
Выщелачивание — гетерогенный процесс, в котором участвуют по меньшей мере две фазы: твердое вещество и раствор. Гетерогенные процессы отличаются от гомогенных тем, что они проходят не во всем объеме системы, а на определенных ее участках, например, на границе раздела фаз. Поэтому для непрерывного протекания реакции необходим непрерывный подвод реагирующих веществ к этим участкам и отвод от них продуктов реакции. Этим объясняется сложность гетерогенных процессов, состоящих из нескольких последовательных стадий и помимо собственно химической реакции включающих в себя также стадии диффузии исходных реагентов и конечных продуктов. Совокупность всех стадий, из которых складывается гетерогенный процесс в целом, называется механизмом этого процесса.
Из учения о химической кинетике известно, что скорость наиболее медленной стадии определяет скорость всего процесса. Поэтому выяснение механизма процесса и его самой медленной стадии является хотя и трудной, но весьма важной задачей изучения кинетики любого процесса.
Если самая медленная стадия гетерогенного процесса — собственно химическая реакция, то скорость всего процесса определяется исключительно скоростью этой химической реакции. В этом случае принято говорить, что процесс протекает в кинетической области. К гетерогенным процессам, протекающим в кинетической области, могут быть применены кинетические уравнения гомогенных реакций с тем лишь отличием, что действующей станет не объемная концентрация, а поверхностная.
Если же скорость диффузии значительно меньше скорости химической реакции, то определяющим этапом будет диффузия, и процесс протекает в диффузионной области. Скорость всего процесса при этом определяется законами диффузии. И, наконец, если скорости диффузии и химической реакции соизмеримы, то процесс протекает в смешанной области, и скорость его определяется как законами диффузии, так и законами химической кинетики.
Следует, однако, помнить, что когда мы говорим о различиях в скоростях диффузии и химической реакции, характеризуя одну из них как быструю, а другую как медленную, это не означает реального неравенства скоростей этих стадий во время протекания данного процесса. В действительности по условиям материального баланса в стационарно протекающем процессе скорости диффузии и химической реакции равны, и словами «быстрый» и «медленный» мы характеризуем только потенциальные возможности этих стадий. Так, при быстрой диффузии и медленной химической реакции у поверхности растворяющегося твердого тела устанавливается такое состояние, при котором диффузия могла бы протекать быстрее, но медленная химическая реакция этому препятствует.
При выщелачивании химическая реакция протекает не во всем объеме раствора, а на поверхности твердого тела. Известно, что частицы растворенного в жидкости вещества при ее движении переносятся от точки к точке двояким образом. Во-первых, при разности концентраций возникает молекулярная диффузия и появляется направленный поток вещества из области большей концентрации в область меньшей. Во-вторых, вследствие движения жидкости (конвекции) частицы растворенного вещества увлекаются потоками жидкости и переносятся вместе с ними. Совокупность этих процессов называется конвективной диффузией. Скорость молекулярной диффузии гораздо ниже скорости переноса вещества за счет движения жидкости, поэтому даже при небольшой скорости течения жидкости перенос вещества, обусловленный этим движением, будет преобладать над переносом молекулярной диффузией, и: лишь при очень малой скорости движения жидкости основную роль начинает играть молекулярная диффузия. Из гидродинамики известно, что скорость жидкости, обтекающей твердую поверхность, в непосредственной близости от нее равна нулю, а далее постепенно возрастает и достигает величины, свойственной самому потоку. На рис. 13 показано распределение скоростей движения жидкости вблизи поверхности твердого тела.
За пределами пограничного слоя толщиной d0 скорость потока всюду одинакова и имеет величину V0. На расстоянии, меньшем, чем dо, скорость движения жидкости снижается, но остается все же достаточно большой, и перенос вещества осуществляется так же, как и в объеме раствора, главным образом, за счет движения жидкости. И только в непосредственной близости от твердой поверхности находится тонкий слой толщиной δ, в котором преобладающая доля вещества переносится молекулярной диффузией. Таким образом, основное сопротивление переносу растворенного вещества оказывает не весь пограничный слой, а только его небольшая часть толщиной d, так называемый диффузионный слой. В этом слое происходит основное изменение концентрации диффундирующего вещества. Толщина его тем меньше, чем больше скорость движения жидкости относительно твердого тела и чем меньше коэффициент диффузии и вязкость раствора. В общем случае толщина диффузионного слоя не одинакова в различных точках поверхности, что обусловлено различием в скоростях движения жидкости в различных точках. Так как величина δ зависит от коэффициента диффузии вещества, то при одновременной диффузии нескольких веществ для каждого из них характерна своя толщина диффузионного слоя. С практической точки зрения наиболее важной является зависимость δ от интенсивности перемешивания (скорости движения жидкости относительно твердого тела).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |



 Соединение
Соединение