1. аллостерическая регуляция;
2. кооперативный эффект;
3. химическая модификация фермента;
4. ограниченный протеолиз.
3.102 При аллостерическом ингибировании активности ферментов:
1. уменьшается скорость реакции;
2. изменяется конформация фермента;
3. эффектор присоединяется в активном центре фермента;
4. нарушается комплиментарность активного центра субстрату;
5. эффектор присоединяется в аллостерическом центре;
6. изменяется конформация активного центра.
3.103 Участок фермента, стереохимически комплементарный субстрату - это:
1. аллостерический центр;
2. регуляторный центр;
3. активный центр;
4. адсорбционный центр.
3.104 Оптическая специфичность – это:
1. способность фермента действовать на определенные связи в большом количестве субстратов;
2. способность фермента воздействовать на определенный участок субстрата;
3. способность фермента катализировать превращение одного изомера субстрата;
4. способность фермента катализировать реакции одного типа.
3.105 Трансферазы -это:
1. ферменты, катализирующие перенос групп с субстрата на субстрат;
2. ферменты, катализирующие перенос одноуглеродных фрагментов;
3. ферменты, катализирующие перенос групп внутри субстратов;
4. ферменты, катализирующие перенос альдегидных и кетонных группировок.
3.106 В состав активного центра входят:
1. аминокислоты с функциональными группировками;
2. все аминокислоты;
3. определенные аминокислоты, расположенные в полипептидной цепи вдали друг от друга и приближенные друг к другу;
4. несколько аминокислот, расположенных в полипептидной цепи непосредственно друг около друга.
3.107 К особенностям ферментативного катализа относятся:
1. исходная активность при низкой температуре;
2. высокие кинетические параметры;
3. специфичность действия;
4. высокая скорость реакции;
5. разнообразие реакций при отсутствии специфичности.
3.108 Абсолютная специфичность - это:
1. способность фермента воздействовать на определенную часть молекулы субстрата;
2. способность фермента катализировать только одну реакцию;
3. способность фермента катализировать превращение одного субстрата.
3.109 Групповая специфичность – это:
1. способность фермента воздействовать на определенную часть молекулы субстрата;
2. способность фермента катализировать превращения одного субстрата;
3. способность фермента действовать на определенные связи в большом числе субстратов;
4. способность фермента катализировать реакции одного типа.
3.110
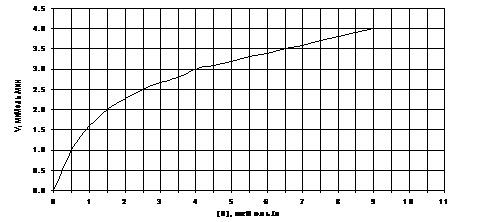 |
По графику зависимости скорости реакции от концентрации субстрата определите Км этого фермента:
1. 0,5
2. 1
3. 1,5
4. 2,5
5. 3
3.111 На рисунке изображен график зависимости скорости реакции от концентрации субстрата.
 |
Определите тип ингибирования:
1. Конкурентное.
2. Неконкурентное.
3. Бесконкурентное.
4. Субстратное.
 |
3.112. На рисунке изображены графики зависимости скорости реакции от концентрации субстрата. А – без действия ингибитора; Б – с добавлением ингибитора.
Определите тип ингибирования:
1. Конкурентное.
2. Неконкурентное.
3. Бесконкурентное.
4. Субстратное.
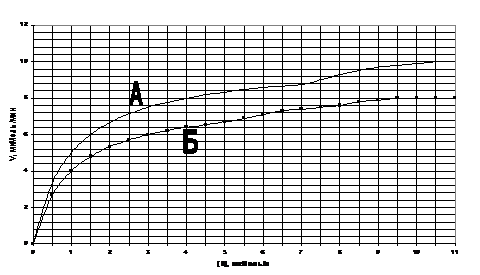 3.113. На рисунке изображены графики зависимости скорости реакции от концентрации субстрата. А – без действия ингибитора; Б – с добавлением ингибитора.
3.113. На рисунке изображены графики зависимости скорости реакции от концентрации субстрата. А – без действия ингибитора; Б – с добавлением ингибитора.
Определите тип ингибирования:
5. Конкурентное.
6. Неконкурентное.
7. Бесконкурентное.
8. Субстратное.
Раздел 4. СИНТЕЗ БЕЛКА.
4.1 Укажите последовательность стадий синтеза белка:
1. инициация рибосомального цикла;
2. посттрансляционный процессинг;
3. транскрипция;
4. элонгация рибосомального цикла;
5. терминация рибосомального цикла;
6. посттранскрипционный процессинг.
4.2 Укажите последовательность процессов, идущих на начальной стадии элонгации рибосомального цикла:
1. образование пептидной связи между метионином и аминокислотным радикалом в А-сайте при участии пептидилтрансферазы;
2. в Р-сайте находится метионил-тРНК;
3. в А-сайт присоединяется первая аминоацил-тРНК, соединенная с фактором элонгации и ГТФ;
4. тРНК покидает Р-сайт;
5. пептидилтранслоказа, фактор элонгации и энергия ГТФ участвуют в перемещении рибосомы на 1 триплет;
6. в А-сайт присоединяется вторая аминоацил-тРНК;
7. А-сайт становится свободным.
4.3 Подберите к каждой группе (А, Б, В) соответствующие им соединения (а, б, в, …):
А. Нуклеозид. | 1. аденин; |
2. цитидин 5’-монофосфат; | |
Б. Азотистое основание. | 3. гуанозин; |
4. цитозин; | |
В. Нуклеотид. | 5. аденозин; |
6. уридин; 7. тимидин 5’-монофосфат. |
4.4 Укажите, какие источники энергии используются на отдельных этапах трансляции:
А Образование пептидных связей. | 1. Энергия АТФ. |
Б. Присоединение мРНК к малой субъединице рибосомы. | 2. Энергия ГТФ. |
В. Присоединение метионил-тРНК к мРНК и субчастице рибосомы. | 3. Энергия субстратов. |
Г. Перемещение рибосомы на мРНК на один кодон. | 4. Без энергии. |
Д. Освобождение белка с рибосомы. | |
Е. Присоединение аминоацил-тРНК к аминоацильному участку рибосомы. |
4.5 Укажите необходимые условия для процесса репликации:
А. Субстраты:
1. азотистые основания;
2. дезоксинуклеозидтрифосфаты;
3. дезоксинуклеозидмонофосфаты.
Б. Матрица:
1. иРНК;
2. ДНК
3. пептид
В. Ферменты:
1. РНК-полимераза;
2. ДНК – полимераза;
3. ДНК-зависимая РНК-полимераза;
4. праймаза;
5. АРС-аза.
Г. Источники энергии:
1. нет;
2. ГТФ;
3. дезоксинуклеозидтрифосфаты;
4. дезоксинуклеозидмонофосфаты.
4.6 Укажите условия, необходимые для процесса транскрипции:
А. Матрица:
1. рРНК;
2. тРНК;
3. иРНК;
4. ДНК;
5. аминокислоты;
6. полипептид.
Б. Субстраты:
1. мононуклеотиды;
2. азотистые основания;
3. нуклеозидтрифосфаты;
4. дезоксинуклеозидтрифосфаты.
В. Источники энергии:
1. энергия гидролиза АТФ;
2. энергия гидролиза ГТФ;
3. энергия субстратов.
Г. Ферменты:
1. ДНК-полимераза;
2. ДНК-праймаза;
3. ДНК-зависимая РНК-полимераза.
Д. Место синтеза:
1. ядро;
2. митохондрии;
3. цитозоль.
4.7 Укажите условия, необходимые для процесса репарации:
А. Матрица:
1. нить неповрежденной иРНК;
2. неповрежденная нить ДНК.
Б. Субстраты:
1. нуклеозидтрифосфаты;
2. дезоксинуклеозидтрифосфаты;
3. азотистые основания.
В. Ферменты:
1. эндонуклеазы, экзонуклеазы;
2. ДНК-полимеразы;
3. ДНК-лигазы;
4. праймаза;
Г. Источники энергии:
1. ГТФ;
2. субстраты - дезоксинуклеотидтрифосфаты;
3. не нужно;
4. АТФ.
Д. Локализация в клетке:
1. ядро;
2. цитоплазма.
4.8 Ген – это:
1. отрезок ДНК, состоящий из экзонов и интронов;
2. отрезок ДНК, где хранится информация о первичной структуре полипептида;
3. отрезок РНК, соответствующий информации об одном белке на ДНК;
4. отрезок ДНК, где хранится информация о первичной структуре полисахаридов.
4.9 Функциями ДНК являются:
1. хранение генетической информации;
2. передача генетической информации по наследству дочерним клеткам;
3. матрица для синтеза РНК;
4. участие в окислительных реакциях.
4.10 Первичный транскрипт – это:
1. соединение РНК с белком в цитоплазме;
2. ДНК, синтезированная полуконсервативным методом;
3. совокупность всех видов РНК, синтезируемых в стадии транскрипции;
4. РНК, полученная в результате модификации концов молекулы.
4.11 В молекуле ДНК не содержится:
1. аденин;
2. тимин;
3. урацил;
4. гуанин;
5. рибоза;
6. цитозин;
7. дезоксирибоза.
4.12 Аминоацил-тРНК-синтетаза (АРС-аза):
1. связывает аминоацил-тРНК с рибосомой;
2. активирует аминокислоту с помощью АТФ;
3. связывает аминокислоту с тРНК;
4. образует пептидные связи между аминокислотами;
5. переносит аминоацил-тРНК в рибосомы.
4.13 Процесс рекогниции – это:
1. включение рибосомы в синтез белка;
2. активация аминокислот;
3. активация т-РНК;
4. узнавание и выбор аминокислот;
5. связывание т-РНК с факторами инициации и ГТФ.
4.14 Посттранскрипционный процессинг включает в себя:
1. модификацию 5- и 3-концов всех видов РНК;
2. модификацию 5- и 3-концов и-РНК;

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 |



