4. Мерные колбы вместимостью 50 мл - 4 шт.
5. Стаканы вместимостью 50 мл.
6. Пипетка на 5 мл.
7. Стандартный раствор ![]() (≈ 1 моль/л).
(≈ 1 моль/л).
8. Раствор 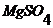 (1 моль/л).
(1 моль/л).
Ход анализа. Последовательным разбавлением исходного стандартного раствора ![]() раствором
раствором 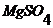 в мерных колбах готовят стандартные растворы для калибровки бромид-селективного электрода, содержащие ≈ 0,1; ≈ 0,01 и ≈ 0,001 моль/л
в мерных колбах готовят стандартные растворы для калибровки бромид-селективного электрода, содержащие ≈ 0,1; ≈ 0,01 и ≈ 0,001 моль/л ![]() .
.
К рН-метру, используемому в качестве высокоомного милливольтметра, подключают бромид-селективный электрод (вместо стеклянного), хлорсеребряный электрод сравнения и поочередно наливают в стакан потенциометрической ячейки указанные растворы. Опустив электроды в раствор каждый раз измеряют устанавливающееся значение э. д.с.
При смене раствора электроды и стакан ячейки обязательно ополаскивают небольшим количеством очередного стандартного раствора. Измерения проводят в порядке возрастания концентрации бромида калия в растворах.
На основании полученных данных строят градуировочный график в координатах ![]() - Для работы с графиком необходимо, чтобы анализируемый раствор имел ту же ионную силу, что и применявшиеся стандартные растворы. Для этого 5 мл исследуемого раствора доводят в мерной колбе до 50 мл раствором
- Для работы с графиком необходимо, чтобы анализируемый раствор имел ту же ионную силу, что и применявшиеся стандартные растворы. Для этого 5 мл исследуемого раствора доводят в мерной колбе до 50 мл раствором 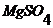 . Измерив э. д.с. ячейки с данным раствором, по градуировочному графику находят искомую концентрацию бромид-ионов, учтя десятикратное разбавление исходного раствора.
. Измерив э. д.с. ячейки с данным раствором, по градуировочному графику находят искомую концентрацию бромид-ионов, учтя десятикратное разбавление исходного раствора.
Работа 5.3.5. Определение содержания хлорид - и иодид-ионов
Сущность метода. Определение ионов ![]() и
и ![]() при их совместном присутствии основано на значительном различии растворимостей
при их совместном присутствии основано на значительном различии растворимостей ![]() и
и ![]()
![]() . При титровании смеси хлорид - и иодид-ионов раствором
. При титровании смеси хлорид - и иодид-ионов раствором ![]() сначала осаждается
сначала осаждается ![]() и лишь после того, как практически все ионы
и лишь после того, как практически все ионы ![]() будут связаны, начинается осаждение
будут связаны, начинается осаждение ![]() :
:
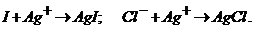
Таким образом, индикаторный электрод, реагирующий на изменение концентрации ионов ![]() в растворе (серебряный электрод), покажет два скачка потенциала: первый - соответствующий осаждению
в растворе (серебряный электрод), покажет два скачка потенциала: первый - соответствующий осаждению ![]() , а второй - осаждению
, а второй - осаждению ![]() .
.
Для предотвращения образования коллоидных растворов галогенидов серебра и уменьшения адсорбции галогенид-ионов образующимся осадком в титруемый раствор добавляют сильный электролит (обычно нитрат бария).
Аппаратура, реактивы и материалы.
1. Потенциометрическая установка для компенсационного титрования.
2. Серебряный электрод.
3. Каломельный или хлорсеребряный электрод.
4. Электролитический ключ, заполненный раствором KNO3 (1 моль/л).
5. Магнитная мешалка.
6. Стакан для титрования вместимостью 50 мл,
7. Микробюретка на 2 мл.
8. Мерная колба вместимостью 50 мл.
9. Пипетка на 10 мл - 2 шт.
10. Стандартный раствор ![]() (»0,1 моль/л).
(»0,1 моль/л).
11. Раствор 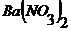 (масс. дол. 5%).
(масс. дол. 5%).
12. Раствор 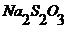 (нас.).
(нас.).
Ход анализа. Раствор, содержащий не более 0,8 ммоль смеси ![]() - и
- и ![]() , переносят в мерную колбу, доводят водой до метки и хорошо перемешивают. В стакан для титрования наливают пипеткой аликвотную часть раствора и добавляют такой же объем раствора
, переносят в мерную колбу, доводят водой до метки и хорошо перемешивают. В стакан для титрования наливают пипеткой аликвотную часть раствора и добавляют такой же объем раствора 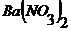 .
.
Перед каждым титрованием серебряный электрод очищают от возможной пленки галогенидов серебра. Для этого его на короткое время погружают в раствор ![]() , после чего тщательно промывают дистиллированной водой.
, после чего тщательно промывают дистиллированной водой.
Подготовив, таким образом, серебряный электрод, погружают его и колено электролитического ключа, соединенного с электродом сравнения, в титруемый раствор. Включив мешалку, приступают к титрованию раствором ![]() , приливая его по 0,2 мл, а в областях обоих скачков потенциала по 0,05 мл, выжидая после каждого прибавления титранта некоторое время установления э. д.с. ячейки.
, приливая его по 0,2 мл, а в областях обоих скачков потенциала по 0,05 мл, выжидая после каждого прибавления титранта некоторое время установления э. д.с. ячейки.
Форма записи результатов титрования
Объем раствора
|
| Э. д.с. ячейки |
|
|
На основании полученных данных строят графики в координатах ![]() и
и ![]() , по которым определяют обе точки эквивалентности.
, по которым определяют обе точки эквивалентности.
Массы ![]() (
(![]() , мг) и
, мг) и ![]() (
(![]() , мг) вычисляют по формулам:
, мг) вычисляют по формулам:
![]()
![]()
где ![]() - объемы стандартного раствора
- объемы стандартного раствора ![]() , израсходованные на титрование
, израсходованные на титрование ![]() (первая точка эквивалентности) и
(первая точка эквивалентности) и ![]() +
+![]() (вторая точка эквивалентности), мл;
(вторая точка эквивалентности), мл; ![]() концентрация раствора
концентрация раствора ![]() , моль/л;
, моль/л; ![]() - молярные массы иода и хлора, г/моль.
- молярные массы иода и хлора, г/моль.
Примечание. После титрования растворы с осадком солей серебра сливают в специальные сосуды для последующего извлечения из них серебра.
Работа 5.3.6. Определение малых количеств карбоната натрия или
соляной кислоты в разбавленных растворах
Сущность метода. Титрование с использованием цветного индикатора оснований и сильных кислот в очень разбавленных растворах часто невозможно или связано с большой ошибкой. Определение точки эквивалентности по интегральной или дифференциальной кривым потенциометрического титрования в этом случае также приводит к ошибочным результатам в основном из-за влияния на рН раствора вблизи точки эквивалентности диссоциации угольной кислоты, обычно присутствующей в растворе.
В отличие от указанных методов, метод Грана, основанный на линеаризации участков кривой титрования, лежащих либо до, либо после точки эквивалентности, позволяет выбрать для определения эквивалентного объема титранта (![]() ) участок кривой титрования в кислой области (при рН<4,3), где диссоциация угольной кислоты практически подавлена. Для этого при определении малых концентраций как оснований, так и сильных кислот в качестве титранта применяют раствор сильной кислоты (
) участок кривой титрования в кислой области (при рН<4,3), где диссоциация угольной кислоты практически подавлена. Для этого при определении малых концентраций как оснований, так и сильных кислот в качестве титранта применяют раствор сильной кислоты (![]() ). В первом случае
). В первом случае ![]() находят по участку кривой титрования, лежащему за точкой эквивалентности, во-втором - точку эквивалентности вообще не проходят, т. е. титруют методом добавок.
находят по участку кривой титрования, лежащему за точкой эквивалентности, во-втором - точку эквивалентности вообще не проходят, т. е. титруют методом добавок.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |



