Затем приступают к отбору проб из нижнего водного слоя гетерогенной системы вода – эфир. (осторожно! Не встряхивать колбу, не нарушать фазового равновесия!) Отбор проб и титрование, как и при определении концентраций исходных растворов кислоты, начинают с самого разбавленного раствора. Микропипетку тщательно споласкивают дистиллированной водой, зажимают пальцем ее верхний конец и погружают в нижний водный слой так, чтобы носик пипетки упирался в дно колбы. Затем слегка дуют в пипетку не вынимать носик из водного слоя!), чтобы удалить приставшие капельки эфира. Отбирают по 1 мл три параллельные пробы водного слоя и титруют с индикатором 0,05Н раствором щелочи, обозначая через ![]() мл количество миллилитров раствора щелочи, пошедшее на титрование. Результаты титрований заносят в таблицу. Таким же образом отбирают и титруют параллельные пробы из каждого водного слоя.
мл количество миллилитров раствора щелочи, пошедшее на титрование. Результаты титрований заносят в таблицу. Таким же образом отбирают и титруют параллельные пробы из каждого водного слоя.
Таблица. Определение коэффициента распределения органической кислоты … между двумя несмешивающимися жидкостями: водой и эфиром
Концентрация кислоты, н. | Количество мл 0,05Н Раствора NaOH, пошедшее на параллельные титрования 1 мл раствора кислоты | Количество кислоты в эфире (в мл 0,05Н раствора NaOH) | Значение К при t°C | |||||
Исходного, | После распределения (водный слой) | |||||||
1 | 2 | среднее | 1 | 2 | среднее | |||
В воде молекулы органических кислот незначительно распадаются на ионы. В данной работе диссоциацией кислот можно пренебречь (![]() ). Вторым растворителем является эфир, в котором молекулы не ассоциированы (
). Вторым растворителем является эфир, в котором молекулы не ассоциированы (![]() ). Следовательно, коэффициент распределения
). Следовательно, коэффициент распределения ![]() , согласно закону Нернста-Шилова, можно вычислить из соотношения двух концентраций в водном и эфирном слоях. В описанном выше опыте концентрация кислоты
, согласно закону Нернста-Шилова, можно вычислить из соотношения двух концентраций в водном и эфирном слоях. В описанном выше опыте концентрация кислоты ![]() пропорциональна количеству миллилитров щелочи, пошедшей на титрование:
пропорциональна количеству миллилитров щелочи, пошедшей на титрование:
![]()
где ![]() - коэффициент пропорциональности;
- коэффициент пропорциональности; ![]() - количество миллилитров раствора щелочи. Так как для опыта были взяты равные объемы растворов кислоты и эфира, то уменьшение концентрации кислоты в воде равно ее увеличению в эфире, т. е.
- количество миллилитров раствора щелочи. Так как для опыта были взяты равные объемы растворов кислоты и эфира, то уменьшение концентрации кислоты в воде равно ее увеличению в эфире, т. е. ![]()
Тогда
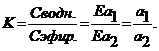
После работы все растворы, содержащие эфир, следует слить в отдельную колбу, находящуюся под тягой, для регенерации, которая осуществляется лаборантом. Категорически запрещается слив эфирных растворов в раковину.
Форма отчета
1. Указать цель работы.
2. Таблица 1.
3. Рассчитать коэффициент распределения по уравнению. И сделать соответствующие выводы.
Работа 6.2.4. Потенциометрическое титрование
Потенциометрическое титрование основано на определении точки эквивалентности по результатам потенциометрических измерений. Вблизи точки эквивалентности происходит резкое изменение (скачок) потенциала индикаторного электрода. При потенциометрическом титровании могут быть использованы следующие типы химических реакций, в ходе которых изменяется концентрация потенциалопределяющих ионов: реакции кислотно-основного взаимодействия, реакции окисления-восстановления, реакции осаждения и комплексообразования.
При кислотно-основном титровании используют, как правило, стеклянный электрод с Н-функцией (измерительный) и хлорсеребряный (вспомогательный).
Потенциал измерительного электрода в процессе титрования изменяется в соответствии с уравнением Нернста. Если графически изобразить зависимость потенциала электрода от количества добавленного титранта, то получится кривая, по которой можно найти конечную точку (или точки) титрования.
Для нахождения точки эквивалентности часто строят дифференциальную кривую в координатах 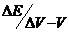 . На точку эквивалентности указывает максимум полученной кривой, а отсчет по оси абсцисс, соответствующий этому максимуму, дает объем титранта, израсходованного на титрование до эквивалентности. Определение точки эквивалентности по дифференциальной кривой значительно точнее, чем по простой зависимости
. На точку эквивалентности указывает максимум полученной кривой, а отсчет по оси абсцисс, соответствующий этому максимуму, дает объем титранта, израсходованного на титрование до эквивалентности. Определение точки эквивалентности по дифференциальной кривой значительно точнее, чем по простой зависимости ![]() .
.
В простом и удобном методе Грана точка эквивалентности определяется по графику в координатах 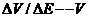 . Перед точкой эквивалентности и после нее кривая Грана линейна, а сама точка эквивалентности находится как точка пересечения этих прямых. Достоинства и удобства метода Грана особенно заметны при анализе разбавленных растворов, позволяя определить точку эквивалентности с достаточной точностью вследствие линейности графика.
. Перед точкой эквивалентности и после нее кривая Грана линейна, а сама точка эквивалентности находится как точка пересечения этих прямых. Достоинства и удобства метода Грана особенно заметны при анализе разбавленных растворов, позволяя определить точку эквивалентности с достаточной точностью вследствие линейности графика.
Потенциометрический метод анализа позволяет провести количественное определение компонентов в смеси кислот, если константы диссоциации различаются не менее чем на три порядка. Например при титровании смеси, содержащей соляную и уксусную кислоты, на кривой титрования обнаруживаются два скачка. Первый свидетельствует об окончании – титрования ![]() , второй скачок наблюдается при оттитровывании
, второй скачок наблюдается при оттитровывании 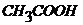 .
.
Главное преимущество потенциометрического метода, по сравнению с другими методами анализа – быстрота и простота проведения измерений. Он позволяет проводить определение в мутных и окрашенных растворах, вязких пастах. В водных и неводных растворителях. Используя микроэлектроды. Можно проводить измерения в пробах при потенциометрическом титровании 0,5-1,0%.
Порядок работы
Цель работы – определение содержания соляной и уксусной кислот в их смеси методом потенциометрического титрования. Титрант – 0,1 н. раствор ![]() .
.
1. Получите в два стаканчика раствор для титрования.
2. В первом стаканчике проведете приближенное титрование. Для этого установите стаканчик с раствором на магнитную мешалку, опустите в него магнит и погрузите в исследуемый раствор стеклянный и хлорсеребряный электроды, соединенные с рН-121. Включите магнитное перемешивание и, убедившись, что магнит не задевает электроды, измерьте первое значение э. д.с. Опустите носик бюретки, заполненной 0,1 Н раствором ![]() в стаканчик (так, чтобы он не касался раствора кислот) и порциями по 1 мл добавляйте щелочь в раствор. После добавления каждой порции титранта производите измерение э. д.с., дав предварительно установиться показаниям прибора. Данные титрования записываются в таблицу 1. По достижении второго скачка потенциала продолжайте титрование до тех пор, пока не убедитесь, что дальнейшее изменение э. д.с. незначительно.
в стаканчик (так, чтобы он не касался раствора кислот) и порциями по 1 мл добавляйте щелочь в раствор. После добавления каждой порции титранта производите измерение э. д.с., дав предварительно установиться показаниям прибора. Данные титрования записываются в таблицу 1. По достижении второго скачка потенциала продолжайте титрование до тех пор, пока не убедитесь, что дальнейшее изменение э. д.с. незначительно.
3. Во втором стаканчике проведите точное титрование. Установив первый скачок при приближенном титровании (например после 4 мл ![]() ) добавьте в стаканчик сразу 3 мл титранта и измерьте э. д.с. После этого титрант добавляйте порциями по 0,5 мл, записывая каждый раз показания прибора в таблицу 2.
) добавьте в стаканчик сразу 3 мл титранта и измерьте э. д.с. После этого титрант добавляйте порциями по 0,5 мл, записывая каждый раз показания прибора в таблицу 2.
Таблица 1. Данные приближенного титрования (наносить на график синими точками)
| 1 | 2 | 3 | 4 | 5 | 6 | …… |
| |||||||
| |||||||
| |||||||
|
Таблица 2. Данные точного титрования (наносят на график красными
точками)
| 1 | 2 | 3 | 4 | 5 | 6 | …… |
| |||||||
| |||||||
| |||||||
|
Форма отчета

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |



