Стабильная работа спектрофотометра обеспечивается через 1 час после его включения.
Выключение спектрофотометра производится в обратном порядке.
Для включения лампы накаливания после дейтериевой лампы переключить тумблер (83) в положение ЛАМПА НАКАЛИВАНИЯ. После двухминутного прогрева нити накала лампы рукоятку (82) поставить в положение ЛАМПА НАКАЛИВАНИЯ.
Для включения после лампы накаливания дейтериевой или ртутной лампы нужно выключить спектрофотометр, а затем включить, как указано выше.
Порядок работы
Поставить рукоятку (71) в одно из положений “1”, “2”, “3”, “4”, а рукоятку (72) – в среднее положение.
Установить требуемую длину волны, вращая рукоятку (21) в сторону увеличения длины волн. Если при этом шкала повернется на большую величину, то следует возвратить её назад на 3-5 нм и снова подвести к требуемому делению.
Поставить рукоятку (69) в положение ВЫКЛ. Скомпенсировать темновой ток фотоэлемента грубой и плавной регулировками темнового тока (рукоятки 70 и 58).
Открыть фотоэлемент, поставив рукоятку (60) шторки- переключателя в положение ОТКР.
Установить стрелку миллиамперметра на центральном штрихе шкалы, вращая рукоятку (24) механизма измерения ширины щели.
Установить в рабочее положение измеряемый образец, перемещая каретку рукояткой (48).
Установить рукоятку (69) в положении “1”.
Установить стрелку миллиамперметра на центральный штрих шкалы, поворачивая движок отчетного потенциометра рукояткой (68), и снять отсчет по шкале оптической плотности “D”.
Вывести измеряемый образец и ввести контрольный образец в поток излучения, установить рукоятку (69) в положение ВЫКЛ, при этом стрелка миллиамперметра должна оставаться на центральном штрихе. (Если стрелка миллиамперметра, заметно отклонилась, проверить измерения). Измерение рекомендуется производить до 3-5 раз. За истинный отсчет принимается среднее из 3-5 измерений.
Практические замечания
Перед началом измерений кюветы должны быть тщательно промыты в щелочном растворе, а затем протерты чистой ватой, намотанной на деревянную палочку и смоченной смесью, состоящей из 85 частей эфира и 15 частей спирта.
При длине волны 635 нм производится смена фотоэлементов.
IY. ПОЛЯРОГРАФИЧЕСКИЙ МЕТОД АНАЛИЗА
Выполнение работ
1. Устройство полярографа ППТ-1. Техническое описание и инструкция по эксплуатации.
2. Работа на установке (согласно инструкции) в переменно-токовом режиме.
3. Задание.
3.1. Запись вольт-амперной характеристики ионов меди и цинка.
Очистка ртути. Ртуть применяемая для капельного электрода должна быть чистой и сухой, не содержать амальгам металлов. Загрязненная и влажная ртуть прилипает к стенкам капилляра и может явиться причиной больших погрешностей в анализах.
Для очистки от механических примесей ртуть фильтруют через бумажный фильтр, в центре которого иглой прокалывают отверстия. После этого ртуть промывают дистиллированной водой в толстенной делительной воронке. Для удаления металлов её пропускают через специальную стеклянную воронку (высотой 85-100 см), наполненную 10-процентной азотной кислотой, и затем 2-3 раза через эту же колонку, которую наполняют 5-процентным раствором нитрата одновалентной ртути в 5-процентной азотной кислоте. Раствор для очистки меняют 3 раза. Затем ртуть промывают дистиллированной водой до нейтральной реакции по лакмусовой бумаге. Промытую ртуть высушивают кусочками фильтровальной бумаги. Затем её протирают ватой смоченной в спирте. Сухую ртуть фильтруют через бумажный фильтр в чистую сухую склянку, которую плотно закрывают чистой сухой резиновой пробкой.
При работе с ртутью необходимо соблюдать меры предосторожности, чтобы предотвратить отравления: не проливать её на лабораторные столы и пол; электролитическая ячейка и склянки с ртутью должны находиться в эмалированной кювете, по окончании анализа надо тщательно осмотреть кювету, стол и при обнаружении капель ртути немедленно собрать их эмалированной медной лопаточкой.
Перед началом работы и по её окончании необходимо, хорошо проветрить помещение.
3.2. Включить полярографу в сеть.
Подготовить капающий ртутный электрод. Дать прогреться полярографу не менее 1 часа.
В электродную ячейку заливают определенное количество фонового электролита (0,1М ![]() ) и производят полярографирование. К фоновому электролиту добавляют 0,1 мл раствора сернокислой меди, снимают полярограмму и отмечают потенциал пика. Потенциал пика является характеристикой анализируемого вещества.
) и производят полярографирование. К фоновому электролиту добавляют 0,1 мл раствора сернокислой меди, снимают полярограмму и отмечают потенциал пика. Потенциал пика является характеристикой анализируемого вещества.
Полярографирование обоих растворов следует производить в одинаковых условиях (с одним и тем же капилляром, с одинаковым периодом копания ртути, при одинаковой концентрации одного и того же фона и при одинаковой чувствительности полярографа). Чувствительность полярографа должна быть такой, чтобы получить пик определяемого компонента в исследуемом растворе высотой 75-100 мм по диаграммной ленте КСП-4. Определение высоты пика необходимо производить с возможно большой точностью.
3.3. Концентрация исследуемого компонента определяется высотой пика на переменнотоковой полярограмме.
Записать калибровочный график меди (цинка). Записать фоновую полярограмму 0,1М ![]() . Затем добавлять 0,03; 0,04; 0,05; 0,06 мл солянокислого раствора исследуемого иона. Определить высоту пиков и построить калибровочный график.
. Затем добавлять 0,03; 0,04; 0,05; 0,06 мл солянокислого раствора исследуемого иона. Определить высоту пиков и построить калибровочный график.
Полярограммы растворов при концентрации определяемых элементов 10-6 моль/л и выше обычно представлены пиками, расшифровка которые не представляет трудности, т. к. пики симметричны. Высотой пика является перпендикуляр, опущенный из его вершины на линию фоновой кривой.
Y. ПОТЕНЦИОМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА
5.1. Сущность метода. Потенциалы электрода
Метод основан на изменении потенциала электрода в зависимости от физико-химических процессов, протекающих в растворе. Величина потенциала зависит от природы электрода, концентрации и природы раствора, в который опущен электрод, от характера химических реакций, температуры и т. п.
В потенциометрии электроды играют роль индикаторов.
В прямой потенциометрии определяют значение электродного потенциала, вычисляя затем концентрацию определяемого иона в растворе. Этот метод часто используется в рН-метрии. В объемном методе анализа при потенциометрическом титровании цветной индикатор заменяют металлическим электродом. Окончание реакции определяется по резкому изменению электродного потенциала в эквивалентной точке - скачок потенциала.
Равновесный потенциал. Равновесный потенциал - величина электродного потенциала, возникшая на границе металл - раствор. Его зависимость от концентрации ионов металла в растворе выражается уравнением Нернста:
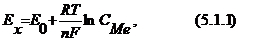
где ![]() - потенциал металлического электрода при данной концентрации ионов металла в растворе;
- потенциал металлического электрода при данной концентрации ионов металла в растворе;
- нормальный потенциал металлического электрода (при концентрации ионов равной единице);
![]() - концентрация ионов металла;
- концентрация ионов металла;
![]() - газовая постоянная,
- газовая постоянная, ![]() = 8,313 Дж;
= 8,313 Дж;
![]() - абсолютная температура;
- абсолютная температура;
![]() - число Фарадея,
- число Фарадея, ![]() =96500 К;
=96500 К;
![]() - заряд ионов металла.
- заряд ионов металла.
При потенциометрическом анализе используют уравнение (5.1.1), принимая температуру равной +25°С и подставляя соответствующие значения ![]() и
и ![]() с учетом коэффициента перехода от натуральных логарифмов к десятичным (2,3026). Тогда уравнение (5.1.1) будет иметь вид
с учетом коэффициента перехода от натуральных логарифмов к десятичным (2,3026). Тогда уравнение (5.1.1) будет иметь вид
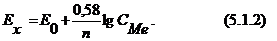
Окислительно-восстановительная система характеризуется определенным значением потенциала, фиксируемым платиновым электродом и зависящим от природы системы, от концентрации окисленной и восстановленной формы вещества:
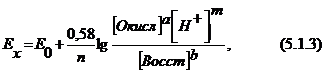
где ![]() и
и ![]() - соответствующие стехиометрические коэффициенты у окислителя, восстановителя и иона водорода из уравнения реакции;
- соответствующие стехиометрические коэффициенты у окислителя, восстановителя и иона водорода из уравнения реакции; ![]() - концентрация ионов водорода в анализируемом растворе.
- концентрация ионов водорода в анализируемом растворе.
Нормальные потенциалы. Для определения значения потенциала используют метод, основанный на сравнении потенциала одного электрода с потенциалом другого. В качестве эталона выбирают нормальный водородный электрод, представляющий собой платиновую пластинку, покрытую платиновой чернью, насыщенной водородом при нормальном атмосферном давлении и погруженной в раствор с активностью водородных ионов, равной 1 г-экв. Водород, адсорбированный платиной, ведет себя по отношению к водородным ионам в растворе так же, как металлический электрод по отношению к своим ионам. Установившееся равновесие соответствует уравнению 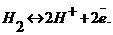 Потенциал водородного электрода условно принимают равным нулю, а любому другому электроду, измеренному по отношению к нему, приписывают потенциал, равный э. д.с. гальванического элемента. Нормальным электродным потенциалом
Потенциал водородного электрода условно принимают равным нулю, а любому другому электроду, измеренному по отношению к нему, приписывают потенциал, равный э. д.с. гальванического элемента. Нормальным электродным потенциалом ![]() называется потенциал электрода, погруженного в раствор соответствующей соли с активностью ионов в 1 г-экв, измеренный относительно нормального водородного электрода.
называется потенциал электрода, погруженного в раствор соответствующей соли с активностью ионов в 1 г-экв, измеренный относительно нормального водородного электрода.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 |



