Из-за вязкости газов у поверхности подложки, а также у стенок и других внутренних поверхностей элементов реактора образуется граничный слой толщиной δ, на котором линейная скорость газового потока изменяется от нуля на поверхности подложки до стационарной скорости свободного ламинарного потока. Реагенты должны диффундировать через граничный слой для того, чтобы достичь поверхности подложки и вступить на ней в химическую реакцию с образованием пленки осаждаемого материала и конечных газообразных побочных продуктов.
Процесс ХОГФ материала М на подложку с помощью термоактивируемой реакции разложения газообразного исходного реагента (ИР) MRa можно представить в виде
МRa(g)![]() M(s) +
M(s) + ![]() R2(g), (4)
R2(g), (4)
где R2 - конечный газообразный побочный продукт (ПП) реакции осаждения; kr1 и kr2 - константы скорости прямой и обратной реакций, см/сек; а - стехиометрический коэффициент реакции осаждения.
Не нарушая общности рассмотрения процесса ХОГФ материала, можно предположить, что молекулы ИР диффундируют из свободного хорошо перемешанного потока в объеме реактора к поверхности раздела газ - подложка через граничный слой толщиной δ. Вследствие сопротивления этого слоя диффузии на нем происходит перепад концентрации ИР от nirv в объеме реактора до пirs на поверхности подложки.
На поверхности подложки молекулы ИР распадаются с образованием атомов осаждаемого материала и конечного газообразного побочного продукта (ПП), молекулы которого диффундируют обратно в объем реактора с изменением концентрации от nbs на поверхности подложки до пbv в объеме реактора.
В случае обратимой химической реакции первого порядка в прямом и обратном направлениях на поверхности подложки скорость осаждения материала определяется как:
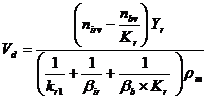 (5)
(5)
где Kr = kr1/kr2 - константа равновесия химической реакции (4), б/р; βir = Dir /δ и βb = Db /δ - коэффициенты массопередачи соответственно для ИР и ПП реакции, см/сек; Dir и Db - коэффициенты диффузии молекул ИР и ПП, см2/сек; Yr- коэффициент образования атомов осаждаемого материала из одной молекулы ИР в химической реакции (4), атом/молекула; ρт = (ρ×NA)/Am - атомная плотность осаждаемого материала, атом/см3; ρ - плотность осаждаемого материала, г/см3; NA - число Авогадро, атом/моль; Ат - атомная масса материала, г/моль.
Если прямая и обратная реакции в (4) термодинамически эквивалентны (krl = kr2, Kr = 1) или обратная реакция термодинамически более выгодна, чем прямая (krl << kr2, Kr << 1), то образующиеся атомы осаждаемого материала и молекулы ПП не стабильны при температуре и давлении процесса осаждения и реагируют друг с другом с образованием молекул ИР. Такие процессы ХОГФ называются лимитируемыми равновесием. Например, если в процессе АР НТ CVD Si (SiCl4 / Н2) осаждения слоев эпитаксиального кремния при атмосферном давлении в результате реакции
SiCl4 (g) + 2Н2 (g) ![]() Si (s) + 4HCl (g) (6)
Si (s) + 4HCl (g) (6)
снизить температуру процесса меньше 1450 °С или повысить ее выше 1920 °С, то будет наблюдаться травление осаждаемого кремния молекулами НCl с образованием ИР.
Для получения высоких скоростей осаждения материалов в процессах ХОГФ необходимо, чтобы прямая реакция в (4) была термодинамически более выгодна, чем обратная, т. е. выполнялись неравенства
( krl >> kr2, Kr >> 1) (7)
при температуре и давлении процесса осаждения. С учетом неравенств (7) выражение (5) можно преобразовать к виду
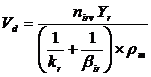 (8)
(8)
где индекс «1» в константе скорости прямой реакции опущен.
Проведем анализ выражения (8). Если βir >> kr то скорость ХОГФ материала будет совпадать с истинной скоростью химической реакции на поверхности подложки (поверхности растущего слоя материала), и концентрация молекул ИР в объеме реактора будет равна концентрации ИР у поверхности подложки, т. е. nirv= nirs= nir. Такие процессы ХОГФ называются лимитируемыми кинетикой (гетерогенной стадией) или протекающими в кинетической области, и для них из выражения (8) следует
![]() . (9)
. (9)
Константа скорости химической реакции kr связана с вероятностью химической реакции εr соотношением:
(10)
где 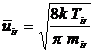 - средняя тепловая скорость молекул ИР; сr - предэкспоненциальный множитель, не зависящий от температуры; mir и Т.ir - соответственно масса и температура молекул ИР; k - постоянная Больцмана; Eact - энергия активации химической реакции осаждения материала; Ts - температура подложки (пластины).
- средняя тепловая скорость молекул ИР; сr - предэкспоненциальный множитель, не зависящий от температуры; mir и Т.ir - соответственно масса и температура молекул ИР; k - постоянная Больцмана; Eact - энергия активации химической реакции осаждения материала; Ts - температура подложки (пластины).
В общем случае для процессов ХОГФ температуры Тir и Ts отличаются друг от друга, хотя и находятся в пропорциональной зависимости: чем выше Ts, тем больше Тir. В частных случаях, например для трубчатого реактора с «горячей стенкой» и протяженной (объемной) реакционной зоной, Тir ≈ Ts. Температура Ts, которая также определяет температуру реакционной зоны, часто называется температурой процесса осаждения (Td).
Из выражений (9) и (10) следует, что в кинетической области скорость и равномерность ХОГФ материала определяются значениями и распределениями энергии активации и температуры по поверхности подложки (пластины). Распределение энергии активации по поверхности исходной подложки или растущего слоя материала связано с тем, что молекулы ИР (или промежуточных продуктов) вступают в реакцию между собой на активных центрах поверхности (центрах адсорбции). Аналогичным образом, образовавшиеся на поверхности структурные единицы осаждаемого материала встраиваются в растущий слой тоже на активных центрах. Активные центры представляют собой поверхностные атомы со свободными валентностями или участки поверхности с минимальной свободной энергией.
Скорость осаждения материала в процессах ХОГФ, протекающих в кинетической области, сильно (экспоненциально) зависит от температуры подложки (см. формулы (9) и (10)).
Если kr >> βir , то скорость осаждения материала будет определяться скоростью диффузии молекул ИР (или промежуточных продуктов) к поверхности подложки (пластины), и nirv>> nirs. Такие процессы ХОГФ материалов называются лимитируемыми диффузией или протекающими в диффузионной области, и для них из (9) с учетом βir = Dir /δ и Dir = (1/3) λir× следует
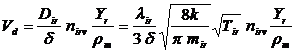 , (11)
, (11)
где λ.ir - средняя длина свободного пробега молекул ИР.
Очевидно, что наблюдаемая в диффузионной области макроскопическая кинетика осаждения материала не имеет ничего общего с истинной химической реакцией на поверхности подложки (или растущего слоя). В этом случае скорость и равномерность процессов ХОГФ материалов определяются значением и распределением концентрации молекул ИР (или промежуточных продуктов) у поверхности подложки. Все химические реакции в диффузионной области имеют первый порядок по концентрации молекул ИР при постоянном давлении в реакторе, не зависят от конкретных особенностей химического механизма осаждения материалов, а их скорости различаются только коэффициентами диффузии молекул используемых ИР.
Практическими критериями диффузионной области процессов ХОГФ являются:
- загрузочный эффект, т. е. наблюдаемое уменьшение скорости осаждения с увеличением площади подложки;
- и слабая зависимость скорости осаждения материала от температуры подложки (пластины) Ts (сравните формулы (9) и (10) с формулой (11)).
На рисунке 7 приведена типичная зависимость скорости термоактивированных процессов ХОГФ материалов от температуры с переходом из диффузионной области в кинетическую область.
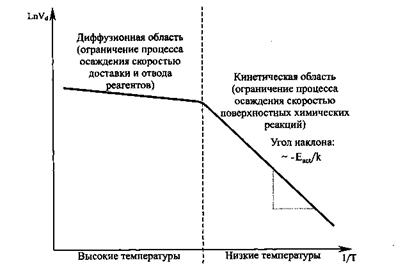
Рисунок 7. Типичная зависимость скорости осаждения Vd термоактивированных процессов ХОГФ материалов от температуры Т с переходом из кинетической области в диффузионную область: Eact - энергия активации химической реакции осаждения; k - постоянная Больцмана.
Теоретическим критерием, определяющим, в какой области протекает процесс ХОГФ материала в планарном реакторе с одинаковыми электродами радиусом rе и межэлектродным расстоянием Неg, является критерий Тилле Ф:
(12)
При Ф ≤ 0,1 процесс ХОГФ протекает в кинетической области, а при Ф ≥ 10 - в диффузионной области. Если 1 < Ф < 10, то процесс ХОГФ протекает в переходной области, для которой скорость осаждения определяется из выражения (8).
На первый взгляд кажется привлекательным проводить процессы ХОГФ материалов в диффузионной области для обеспечения максимальных скоростей осаждения. Однако, с другой стороны, в диффузионной области трудно контролировать равномерность осаждения пленки по толщине по всей подложке, которая зависит от равномерности распределения реагентов в газовой фазе над поверхностью подложки. Распределение реагентов в газовой фазе определяется динамикой газовых потоков в реакторе, а, следовательно, равномерность распределения реагентов трудно контролировать из-за сложной геометрии внутренних частей реактора.
Кроме того, обеспечение диффузионной области процессов ХОГФ межслойной изоляции требует высоких температур осаждения, которые могут превысить допустимые температуры стабильности алюминиевой металлизации микросхем. Поэтому межслойную изоляцию микросхем осаждают обычно в кинетической области с тщательным контролем значения температуры и равномерности ее распределения по поверхности подложки (пластины), особенно в краевых областях. Это накладывает дополнительные требования к конструкциям систем нагревания подложек.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



