Соотношение между размерами столбчатой зоны и равноосной зон в слитке зависит от перегрева расплава, теплопроводности изложницы, содержания примесей и др.
Полиморфные превращения.
Многие металлы в зависимости от тем-ры могут существовать в различных кристаллических формах или в различных модификациях. В результате полиморфного превращения атомы кристаллического тела, имеющие решетку одного типа перестраиваются в другую решетку. Полиморфную модификацию, устойчивую при более низких тем-рах принято обозначать a, затем b и т. д. Примеры полиморфных превращений a-Fe - g-Fe, a-Co - b-Co, a-Ti - b-Ti, a-Sn - b-Sn, a-Mn - b-Mn - g-Mn - d-Mn.
|
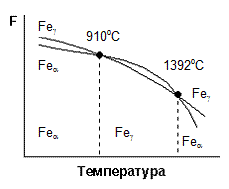
Рассмотрим полиморфизм железа. В интервале температур 910-1392оС устойчивым является g-Fe с кристаллической решеткой, имеющей меньшую свободную энергию, чем a-Fe. При температурах ниже 910оС и выше 1392оС устойчива a-Fe.
Переход чистого металла из одной полиморфной модификации в другую в условиях равновесия происходит при постоянной температуре и сопровождается поглощением тепла при плавлении, и выделением тепла при кристаллизации.
Как и при кристаллизации из жидкой фазы, для полиморфного превращения необходимо переохлаждение или перегрев относительно равновесной температуре, чтобы возникла разность свободных энергий. Полиморфное превращение по своему механизму кристаллизационный процесс и осуществляется путем зарождения и роста центров. В результате полиморфного превращения образуются новые зерна, имеющие другой размер и форму. Поэтому такое превращения также называют перекристаллизацией.
Полиморфное превращение сопровождается скачкообразным изменением свойств металлов и сплавов: удельного объема, теплоемкости, тепло - и электропроводности, магнитных, механических и химических свойств и т. д.
Основы теории сплавов.
Фазы в сплавах. Фазой называется однородная обособленная часть системы (металла и сплава), имеющая одинаковый состав, строение и свойства, отделенная от других частей поверхностью раздела. При переходе поверхности раздела хотя бы одно свойство изменяется на конечную величину.
В зависимости от характера взаимодействия между атомами компонентов в сплавах образуются твердые растворы или промежуточные соединения.
Твердые растворы. Твердые растворы - это фазы, содержание компонентов в которых может изменяться без нарушения типа кристаллической решетки основного компонента. В зависимости от способа размещения атомов в кристаллической решетке твердые растворы делятся на твердые растворы замещения, внедрения и вычитания.
|
Твердые растворы могут быть непрерывными и граничными. Непрерывными могут быть только твердые растворы замещения, гранич-ными - растворы замещения и внедрения.
Условия образования непрерывных твердых растворов:
1) сходство размеров атомов компонентов - различие обычно не больше 10-15% (правило Юм-Розери);
2) сходство решеток компонентов;
3) близкое расположение компонентов в таблице Менделеева и близкое строение валентных оболочек электронов в атомах. Например, системы Ag-Au, Au-Cu, Mo-W, Bi-Sb, - в одной группе, системы Cu-Ni, Ni-Fe, Fe-Cr, Co-Ni - в одном периоде, Au-Ni, Au-Pd, Co-Pd, Fe-Pd - в близких группах и периодах. Если хотя бы одно их указанных условий не выполняется имеет место ограниченная растворимость - граничный твердый раствор.
Твердые растворы внедрения получаются, если соотношение атомных диаметров растворенного элемента и растворителя £0,59. Эти растворы образуются на базе переходных металлов (Fe, Co, Mn, Ti, Mo, W, Zr, V и др.), в которых растворяются неметаллы (C, H, O, N) с малыми атомными диаметрами. Концентрация неметалла обычно незначительная. Образование твердых растворов ведет обычно к заметному росту структурно чувствительных свойств: твердости, прочности, удельного электросопротивления и т. д.
Твердые растворы вычитания образуются на основе некоторых химических соединений и характеризуются дефектной решеткой со свободными узлами, которые должны были принадлежать атомам одного из компонентов.
Промежуточные фазы. Более сильная химическая связь между атомами компонентов в промежуточных фазах приводит к образованию иных кристаллических решеток, чем у атомов компонентов.
1. Химические соединения. Это фазы постоянного состава, образующиеся при взаимодействии металлов с неметаллами или с элементами, обладающих промежуточными свойствами при определенных соотношениях элементов, отвечающих правилу валентности.
Характерные особенности химических соединений, образованных по закону нормальной валентности, следующие:
1. Крист. решетка отличается от решеток компонентов, образующих соединение. Атомы в решетке химического соединения располагаются упорядоченно, т. е. атомы каждого компонента расположены закономерно и по определенным узлам решетки. Большинство химических соединений имеют сложную кристаллическую структуру.
2. В соединении всегда сохраняется простое кратное массовое соотношение элементов. Это позволяет выразить их в состав простои формулой АnВт, где А и В— соответствующие элементы; n и т— простые числа.
3. Свойства соединения резко отличаются от свойств образующих его компонентов.
4. Температура плавления (диссоциации) постоянная.
5. Образование химического соединения сопровождается значительным тепловым эффектом.
В отличие от твердых растворов химические соединения обычно образуются между компонентами, имеющими большое различие в электронном строении атомов.
Типичными примерами химических соединений с нормальной валентностью являются соединения магния с элементами IV— VI групп периодической системы: Mg2Sn, Mg2Pb, Mg2Pb2, Mg3Sb2, Mg3Bi2, MgS, MgSe и др.
Электронные соединения (фазы Юм-Розери) - промежуточные фазы из двух металлов, мало различающихся атомным диаметром. Характеризуются постоянным отношением общего числа валентных электронов (e) к общему числу атомов (n). Различные соединения имеют однотипные решетки, если отношение e:n одинаково. Например, Cu3Sn, Ag5Al3 и CuZn3 имеют гексагональную решетку, несмотря на разное атомное содержание, поскольку отношение e:n постоянно и равно 7:4.
e:n=3:2 - b-фаза - три типа решетки - ОЦК, сложная кубическая типа b-Mn с 20 ат. в ячейке, и ГПУ.
e:n=21:13 - g-фаза - решетка типа a-Mn с 52 ат. в ячейке.
e:n=7:4 - e-фаза - ГПУ
Промежуточные фазы внедрения образуются при взаимодействии элементов, сильно различающихся своими атомными диаметрами: d/D=0,41-0,59. Это - обычно карбиды, нитриды и бориды: TiC, TiN, HfC, TaC, ZrC, NbC, TaN и др.
Фазы Лавеса постоянного состава образуются при большом различии атомных диаметров компонентов (около 20%) и не подчиняются законам валентности. Их компоненты могут принадлежать к любой группе элементов таблицы Менделеева. Соединения такого типа образуют кристаллы кубической (тип MgCu2) и гексагональной (тип MgZn2, MgNi2) симметрии.
Промежуточные фазы постоянного состава называют часто химическими соединениями или интерметаллидами.
Диаграммы состояний сплавов двойных систем, не имеющих превращений в твердом состоянии.
Диаграмма состояния однокомпонентной системы имеет только одно измерение - шкалу температур (давление - постоянное). Точки на этой шкале показывают температуры фазовых превращений.
Для двухкомпонентной системы должна быть еще шкала содержания компонентов и диаграмма строится в двух измерениях. По оси ординат откладывают температуру, по оси абсцисс - содержание компонентов. Каждая точка на оси абсцисс соответствует определенному составу сплава. При этом крайние точки оси абсцисс соответствуют чистым компонентам, промежуточные - двойным сплавам.
Диаграмма равновесия трехкомпонентных сплавов имеет две концентрационные оси и одну температурную.
Состояние сплава данного состава при данной температуре характеризуется на диаграмме точкой, называемой фигуративной точкой. Вертикаль, отвечающая изменению температуры определенного состава, называется линией фигуративных точек. При определенных температурах происходят те или иные изменения фазового состояния сплавов, или фазовые превращения. Линии, соединяющие точки аналогичных превращений, разграничивают на диаграмме области различных фазовых состояний.
Таким образом, диаграмма фазового равновесия - графическое изображение зависимости фазового состояния сплава от температуры и состава сплава. Фазовое состояние характеризуется природой фаз, находящихся в равновесии, их химическим составом и относительным количеством.
Все основные виды диаграмм фазового равновесия могут быть получены из основных законов термодинамики, из рассмотрения кривых изменения термодинамического потенциала в зависимости от состава для твердых и жидких фаз при различных температурах.
Правило фаз. При анализе диаграмм фазового равновесия часто пользуются правилом фаз, или законом Гиббса. Правило фаз дает количественную зависимость между числом степеней свободы и количеством фаз и компонентов системы.
Числом степеней свободы, или вариантностью системы, называется число независимых внутренних и внешних факторов (температура, давление, концентрация и др.), которые можно изменять без изменения числа фаз в системе. В общем случае С= П - У, П - число внутренних (химический состав фаз) и внешних переменных, таких как, температура и давление; У - число уравнений.
Число переменных. Если k - число компонентов, то при одной фазе мы можем менять (k - 1) концентраций (концентрация последней компоненты зависит от изменения концентрации остальных компонентов), а при f фазах - (k-1)f. Если p число внешних переменных, то общее число переменных - (k-1)f+p.
Число уравнений. Для одного компонента находящегося в равновесии в f фазах, мы имеем (f - 1) независимых уравнений. Для k компонентов - (f - 1)k уравнений.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)