Основная литература:
1. Материаловедение. /Под ред. Б. Н.Арзамасова. - М.: Машиностроение, 1986, 384 с.
2. М. и др. Материаловедение. - М.: Металлургия, 1993, 447 с.
3. П. и др. Материаловедение и технология конструкционных материалов, - М.: МИСиС, 1996, 567 с.
4. Лабораторные работы по материаловедению
Введение.
Материаловедение - наука, изучающая зависимость между составом, строением и свойствами металлов и сплавов и закономерности их изменения под воздействием внешних факторов: тепловых, химических, механических и др.
В 60-х годах 18 века русский ученый В.: металлом называется «светлое тело, которое ковать можно». Т. о., Ломоносов отметил высокую отражательную способность металлических тел, или их блеск, и высокую пластичность. Ломоносов сделал и второе важное открытие. Он подметил кристалличность самородных металлов (Cu и Au) и отметил сходство металлических кристаллов и солей.
Основоположниками современного металловедения явились российские заводские инженеры П. П.Аносов (1799-1851) и Д. К.Чернов (1839-1921). Павел Петрович Аносов на Златоустовском заводе впервые (в 1831 г.) применил микроскоп для исследования структуры металлов. При этом он применил химическое травление полированной поверхности металла (шлиф). Аносову принадлежит приоритет в создании легированных сталей и в разработке технологии изготовления клинков из булатной стали. Булатный узор на поверхности стали непосредственно зависит от ее внутренней структуры.
В 1868 г. Д. К.Чернов впервые указал на превращения в твердой стали при определенных температурах, сопровождающиеся тепловыми эффектами. В дальнейшем Д. К.Чернов высказал предположение, что эти превращения аллотропические (т. е. связаны с изменением типа кристаллической решетки), что впоследствии было подтверждено рентгеноструктурным анализом. Изображенная графически зависимость температуры этих превращений и плавления стали от содержания в ней углерода, которая была найдена Д. К. Черновым по цветам каления, явилась прототипом диаграммы равновесия Fе - С. Своим открытием аллотропических превращений в стали Д. К.Чернов заложил прочный фундамент теории термической обработки стали. Критические точки в стали, найденные им, позволили рационально выбирать температуру ее закалки, отпуска и пластической деформации в производственных условиях. Он указал также на значение времени выдерживания стали при той или иной температуре, заложив тем самым основы изучения кинетики фазовых превращений и формирования структуры.
В 1873 - 1876 гг. Гиббс изложил основные законы фазового равновесия и, в частности, правило фаз, основываясь на законах термодинамики. Из законов Гиббса о минимуме термодинамического потенциала можно вывести все типовые диаграммы равновесия, не прибегая дополнительно ни к каким другим допущениям.
В начале 20 века большую роль в развитии металловедения сыграли работы С., применившего для исследования металлов методы физико-химического анализа (электрические, дилатометрические, магнитные и др.).
Определение атомного строения фаз стало возможным после открытия Лауэ (1912 г.), показавшего, что атомы в кристалле регулярно заполняют пространство, образуя пространственную дифракционную решетку, и что рентгеновские лучи имеют волновую природу.
Весьма большое значение в развитии металловедения сыграли работы В., Д., Т. и др.
Основные свойства металлов. Особенности строения атомов простых и переходных металлов.
Среди известных 106 элементов, металлов - подавляющее большинство, 76. Такие элементы как Si, Ge, As, Se, Te являются переходными между металлами и неметаллами.
Металлы в тв-м и отчасти в ж-м состояниях обладают рядом характерных свойств:
- высокой тепло - и электропроводностью
- положительным температурным коэффициентом электросопротивления, т. е. с повышением температуры электросопротивление чистых металлов возрастает (отметить сверхпроводимость).
- термоэлектронной эмиссией, т. е. способностью испускать электроны при нагреве,
- хорошей отражательной способностью, металлы непрозрачны и обладают металлическим блеском,
- повышенной способностью к пластической деформации.
Кристалл металла можно рассматривать как коллектив полож-х ионов, находящихся в среде свободных элек-в. Взаимодействие между полож. ионами и коллективиз. электронами определяет природу металлической связи. Она не направленна.
|
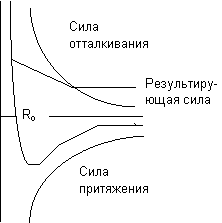
Сила связи в металлах определяется соотношением между силами отталкивания и силами притяжения между ионами и электронами. Атомы (ионы) располагаются на таком расстоянии друг от друга, чтобы энергия взаимодействия была минимальной (Рис.1). Этому положению соответствует равновесное расстояние R0, т. е. состояние с минимальной энергией.
Т. о., при закономерном расположении атомов в металле будет реализовано состояние с минимальной энергией взаимодействия атомов.
Для описания атомно-кристаллической структуры пользуются понятием пространственной или кристаллической решетки.
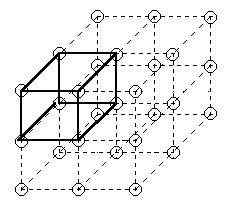
Кристаллическая решетка представляет собой воображаемую пространственную сетку, в узлах которой располагаются атомы (ионы), образующие твердое кристаллическое тело. (Рис.). Наименьший объем кристалла, дающий представление об атомной структуре металла во всем объеме, получил название элементарной кристаллической решетки.
|
Пространственные кристаллические решетки делят на 14 типов кристаллических решеток, которые называются решетками Браве и 7 систем - сингоний, исходя из соотношения между осевыми единицами (параметрами или периодами кристаллической решетки) и углами.
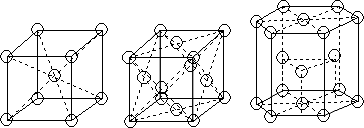
Металлы образуют одну из следующих высокосимметричных решеток с плотной упаковкой атомов (Рис.): кубическую объемноцентрированную (ОЦК), кубическую гранецентрированную (ГЦК) и гексагональную (ГП) (Рис.)
|
ОЦК металлы - W, Mo, Cr, V, Ka, Na, Li, b-Ti, a-Fe, Ta и др.
ГЦК металлы - Al, Cu, Ni, Ag, Au, Pb, g-Fe, Pd, Ir Ce и др.
ГП металлы - Mg, Zn, Cd, Be и др.
Плотность кристаллической решетки (объем занятый атомами) характеризуется координационным числом, т. е. числом ближайших соседних атомов, окружающих данный атом. Чем выше координационное число - тем больше плотность упаковки атомов.
В ОЦК решетке - наименьшее расстояние d = 0,5aÖ3. На этом расстоянии находятся 8 атомов. К=8. Коэффициент заполнения = 0,68. ГЦК - наименьшее расстояние d = 0,5aÖ2. К=12. Коэффициент заполнения = 0,74. ГП - наибольшая плотность при с/ a=1,633, К=12, Коэффициент заполнения = 0,74.
Для определения положения атомных плоскостей в кристаллических решетках пользуются индексами Миллера (hkl), которые являются величинами, обратными длине отрезков, измеряемых в осевых единицах. Например, для ОЦК решетки плоскости куба пересекает отрезки (1 ¥ ¥) (¥ 1 ¥) (¥ ¥ 1). Обратные величины (100) (010) (001). Индексы могут быть и с минусами. Совокупность плоскостей обозначаются фигурными скобками. Например {100}. Для ГП решетки пользуются индексами Миллера-Браве (hkil), где i= - (h+k).
Кристаллографические направления обозначаются индексами [u v w], где u v w - простые числа, пропорциональны координатам выбранного узла вдоль осей X Y Z, который лежит на прямой, проходящей через начало координат, выраженных в осевых единицах.
Плотность расположения атомов по различным плоскостям неодинакова. Наиболее плотноупакованными плоскостями для ОЦК решетки является (110), для ГЦК (111) и для ГП решетки (001). Из-за неодинаковой плотности атомов в различных плоскостях многие физические и механические свойства зависят от направления вырезки образцов. Подобная неодинаковость свойств по различным кристаллографическим направлениям называется анизотропией. Анизотропия является важнейшим свойством кристалла. Например, для монокристалла чистой Сu (ГЦК) предел прочности в направлении [100] составляет 146 МН/м2, а в направлении [110] - 350 МН/м2.
Очень многие металлы используются в поликристаллическом виде, где обычно кристаллы расположены беспорядочно и макроскопические свойства в различных направлениях одинаковы, т. е. квазиизотропны. Однако иногда необходимо получение анизотропных свойств, тогда в материале создают преимущественную ориентировку кристаллографических плоскостей, которая называется текстурой.
Дефекты кристаллического строения реальных металлов.
Дефекты кристаллического строения подразделяются по геометрическим признакам на точечные, линейные, поверхностные и объемные.
Точечные дефекты. Точечные дефекты могут быть собственными (структурными) и примесными. К собственным дефектам относят вакансии и межузельные атомы, к примесным - атомы примеси.
Вакансии представляют собой незаполненный узел кристаллической решетки. Межузельный атом - это собственный атом расположенный в междоузлии. Если происходит выход атома из узла кристаллической решетки в междоузлие, то образуется вакансия и межузельный атом (парный дефект Френкеля). Если же атом выходит на поверхность кристалла, то образуется вакансия (дефект Шоттки).
Вокруг точечных дефектов кристаллическая решетка сильно искажена, следовательно, их образование всегда требует затраты энергии. Однако присутствие точечных дефектов в определенных концентрациях, зависящих от температуры является термодинамически выгодным. Это объясняется тем, что образование точечных дефектов хотя и повышает U в уравнении F = U - ST, одновременно увеличивает энтропию системы S. В результате свободная энергия при наличии дефектов какой-то равновесной концентрации уменьшается. Равновесная концентрация вакансий составляет Сv= exp(-Eвак/kT), где Евак - энергия образования вакансий. Отсюда видно, что равновесная концентрация вакансий сильно зависит от температуры. Вблизи Тплав Сv ~10-4, вблизи комнатной температуры 10-20.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)