С=[(k-1)f+p] - [(f-1)k] С=k+p-f - это и есть правило Гиббса, которое дает математическое выражение фазового равновесия. p - давление и температура. Большая часть работ в металлургической практике проводится при постоянном давлении, равном атмосферному. Поэтому для таких процессов правило фаз принимает вид С=k+1-f.
Примеры. 1) Чистый металл может находиться в двухфазном состоянии и переходить из одного состояния в другое при постоянной и строго определенной температуре, так как вариантность равна нулю (нонвариантное равновесие): С=1+1-2=0 - справедливо для затвердевания и аллотропического превращения - на кривой охлаждения имеется горизонтальный участок.
2) В сплаве двух металлов кристаллизация твердого раствора или аллотропическое превращение происходят в интервале температур, поскольку С=2+1-2=1 (моновариантное равновесие).
Построение реальных диаграмм фазового равновесия осуществляется экспериментально.
|
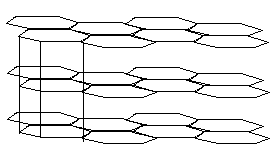
Рассмотрим пример построения диаграммы равновесия с неограниченной растворимостью компонентов в жидком и твердом состояниях с применением термического анализа. Приготовив ряд сплавов разной концентрации, можно для каждого их них получить кривую охлаждения. Сплавы промежуточного состава дают ряд качественно одинаковых кривых охлаждения, на каждой из них видны два перелома: верхний - соответствует началу кристаллизации, а нижний - концу кристаллизации. По полученным данным можно построить диаграмму состояния.
Геометрическое место точек начала затвердевания называется "ликвидусом", а конца затвердевания "солидусом". Между этими кривыми лежит область, в которой сплавы находятся в виде смеси жидкости и кристаллов.
В реальных условиях при затвердевании сплава равновесие не наблюдается. Диффузия идет медленно, особенно в твердой фазе. В результате образуется химически неоднородный твердый раствор. Такая химическая неоднородность в пределах каждого зерна называется внутризеренной или дендритной ликвацией. Оси дендрита, затвердевшие раньше, обогащены тугоплавким и обеднены легкоплавким компонентом, по сравнению с межосным пространством.
Образование эвтектики при полной растворимости в жидком состоянии.
Рассмотрим систему, в которой из жидкости при затвердевании выпадают кристаллы чистых компонентов А и В, не образующие в твердом состоянии растворов и соединений.
Построить эвтектич. диагр. сост. на основе кривых охлаждения.
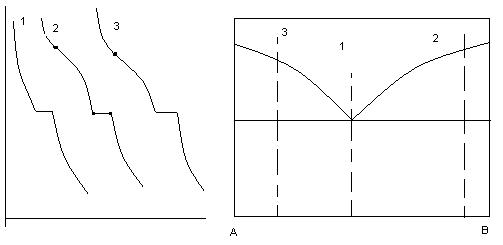
Эта диаграмма характеризуется понижением температуры плавления при введении в каждый из компонентов некоторого количества второго компонента. Кривые ликвидуса пересекаются в точке, соответствующая составу сплава с самой низкой температурой плавления и называемая эвтектической.
Подобную диаграмму состояния имеет система Pb-Sb. Эвтектический сплав в условиях стабильного равновесия плавится и затвердевает при постоянной температуре, которая также называется эвтектической, в соответствии с реакцией
![]()
Микроструктура. Однородная смесь двух фаз, кристаллизующихся одновременно из расплава: в данном случае кристаллы свинца и сурьмы, называется эвтектикой. В доэвтектическом сплаве: эвтектика + первичные кристаллы свинца. В заэвтектическом сплаве: эвтектика + первичные кристаллы сурьмы.
|
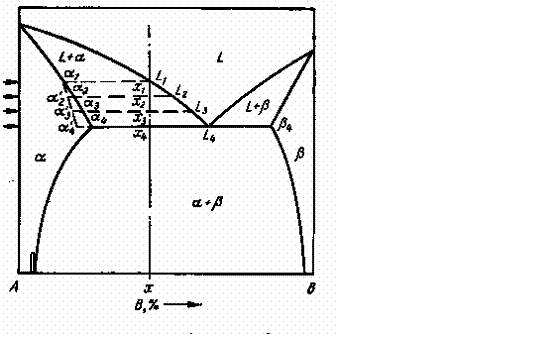
Диаграмму равновесия при наличии ограниченной растворимости в твердом состоянии выглядит следующим образом.
Линия предельной растворимости одного компонента в другом называются "сольвусом".
Перитектическое превращение. Как правило, если температуры плавления компонентов не очень сильно различаются, то получается эвтектическая диаграмма, если же температуры различаются значительно, то получается перитектическая диаграмма.
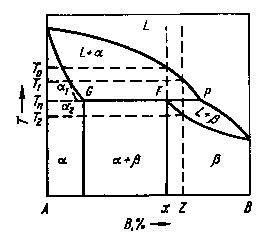
Перитектическое превращение при наличии ограниченной растворимости в твердом состоянии.
|
На диаграмме фазового равновесия при Tп - перитектической температуре в равновесии находятся три фазы. При этой температуре происходит перитектическое превращение![]() .
.
Оно идет при постоянной температуре, поскольку здесь имеет место нонвариантное равновесие и представляет собой реакцию соединения при охлаждении и реакцию распада при нагреве.
Диаграммы состояний и структура сплавов двойных систем, имеющие превращения в твердом состоянии
В некоторых сплавах после их затвердевания, т. е. в твердом состоянии, происходят фазовые превращения. Они вызываются полиморфными превращениями компонентов и распадом твердого раствора, т. к. растворимость в твердых растворах может изменяться с повышением температуры.
|
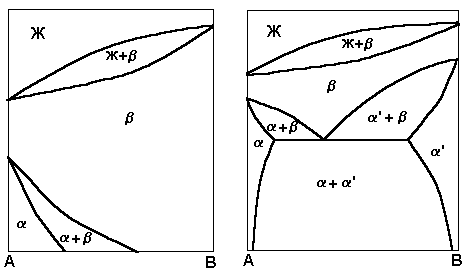
Диаграмма состояния сплавов, компоненты которых имеют полиморфные превращения имеет следующий вид (Рис). Если только один компонент имеет полиморфное превращение рис. слева, если оба, то один из вариантов диаграммы состояния на рис. справа.
Распад b раствора на смесь двух фаз a и a' может быть описан аналогично эвтектической реакции.
b Û a + a'
Превращения, в которых не принимает участие жидкая фаза, называются эвтектоидными и перитектоидными. Эвтектоидное превращение приводит к образованию смеси кристаллов двух фаз, которая носит название эвтектоида. В условиях высокой диффузионной подвижности эвтектоид имеет пластинчатое строение.
Сплавы, расположенные левее эвтектоидного состава называются доэвтектоидными, и правее - заэвтектоидными.
Железо и его сплавы.
Компоненты и фазы в системе железо-углерод.
|
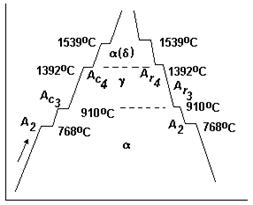
Железо - ат. номер -26. Тпл.=1539оС. Имеет две полиморфные модификации: a-Fe и g-Fe. a-Fe существует при температурах ниже 910оС и выше 1392оС. Для интервала 1392-1539оС a-Fe обозначают как d - Fe.
a-Fe имеет ОЦК решетку. До температуры 768оС a-Fe ферромагнитно, выше этой температуры - парамагнитно. Парамагнитное железо обозначают как b-Fe. Температуру перехода называют точкой Кюри и обозначают А2.
Критическую точку a«g превращения при 910оС обозначают соответственно Ас3 (при нагреве) и Аr3 (при охлаждении). Критическую точку d«g превращения при 1392оС обозначают соответственно Ас4 (при нагреве) и Аr4 (при охлаждении).
g-Fe имеет ГЦК решетку. При a - g превращении происходит сжатие, объемный эффект сжатия составляет ~1% (Рис.).
|
Углерод - неметалл, ат. номер 6, плотность 2,5 г/см3, Тпл. - 3500оС. В обычных условиях - в виде графита (гексагональная решетка), имеет слоистый характер. Силы ковалентной связи внутри каждого слоя велики, между слоями гораздо слабее (типа сил Ван-дер Ваальса), поэтому чешуйки графита легко отделяются друг от друга. Метастабильное состояние - алмаз. Растворяется в Fe в жидком и твердом состоянии. Может образовать химическое соединение с Fe.
В системе Fe-C различают следующие фазы: жидкий сплав, твердые растворы - феррит и аустенит, а также цементит и графит.
Феррит (Ф) - твердый раствор углерода в a-железе. Различают низкотемпературный a-феррит с растворимостью углерода до 0,02% и высокотемпературный d феррит с предельной растворимостью углерода 0,1%. Под микроскопом феррит выявляется в виде однородных полиэдрических зерен. Феррит имеет примерно следующие механически свойств sв = 250 МПа, s0,2 = 120 МПа, d= 50%, y = 80%, НВ= 80-90 (800-900 МПа).
Аустенит (А) - твердый раствор углерода в g-железе. Предельная растворимость углерода в g-железе - 2,14%..
Различные объемы элементарных сфер в о. ц.к, и г. ц.к. решетках предопределяют значительно большую растворимость углерода в g-железе по сравнению с a-железом. Аустенит обладает высокой пластичностью, низкими пределами текучести и прочности. Микроструктура аустенита - полиэдрические зерна.
Цементит - это химическое соединение железа с углеродом - карбид железа Fe3C. В цементите содержится 6,67% углерода. Цементит имеет сложную ромбическую решетку с плотной упаковкой атомов. Температура плавления цементита точно не определена в связи с возможностью его распада и принимается примерно равной 1500°С. К характерным особенностям цементита относятся высокая твердость HV= 1000 (10 000 МПа) и очень малая пластичность. Цементит является метастабильной фазой. В условиях равновесия в сплавах с высоким содержанием углерода образуется графит.
Диаграмма состояния железо-цементит (метастабильное равновесие)
Система Fe-Fe3C метастабильная. Образование цементита вместо графита дает меньший выигрыш свободной энергии, однако кинетически образование карбида железа более вероятно.
На диаграмме Fe-Fe3C точка А (1539°С) - температура плавления железа,
точка D (1500оС) - температуре плавления цементита.
Точки N (1392оС) и G (910оС) полиморфное превращение a Û g.
Концентрация углерода (по массе) для характерных точек диаграммы состояния Fe-Fe3C (см. рис.) :
В - 0,51%С в жидкой фазе, находящейся в равновесии с d-ферритом и аустенитом при перитектической температуре 1499°С;
Н - 0,1%С предельное содержание в d-феррите при 1490оС,
|
J - 0,16%С - в аустените при перитектической температуре 1490°С;
Е - 2,14%С предельное содержание в аустените при эвтектической температуре 1147оС;

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 |
 Основные порталы (построено редакторами)
Основные порталы (построено редакторами)